第七章--逐步聚合
- 格式:doc
- 大小:496.50 KB
- 文档页数:31






总结逐步聚合引言在软件开发过程中,逐步聚合是一种常用的技术,它允许我们逐渐构建复杂的系统。
逐步聚合的核心思想是将大型的问题分解为一系列的子问题,并逐步实现,最后将它们聚合起来形成完整的解决方案。
本文将介绍逐步聚合的概念、原则以及使用该技术时的一些实践经验,并分析它的优缺点。
通过阅读本文,读者将能够更好地理解逐步聚合,并在实际项目中灵活运用该技术。
什么是逐步聚合逐步聚合是一种软件开发技术,它将复杂的问题划分为多个较小的子问题,并逐步解决这些子问题。
通常情况下,逐步聚合的过程可以分为以下几个步骤:1.划分问题:将大型问题分解为若干个独立的子问题。
每个子问题都可以单独解决,而且对其他子问题没有任何依赖关系。
2.逐步实现:从最简单的子问题开始实现,逐步扩展功能。
每个子问题的实现都应该是独立的,可以独立运行和测试。
3.聚合功能:将所有子问题的解决方案整合到一起,形成最终的解决方案。
在聚合过程中,可能需要解决不同子问题之间的交叉依赖或冲突问题。
逐步聚合的最终目标是构建一个完整且可靠的系统,同时也使开发过程更加可控和可维护。
逐步聚合的原则在使用逐步聚合技术时,有一些原则需要遵守,以确保成功实施逐步聚合过程:1. 单一职责原则在划分问题和实现子问题的过程中,每个子问题都应该具有清晰的责任范围。
这意味着每个子问题应该仅实现一种功能,避免功能的耦合和相互依赖。
这样可以提高代码的可维护性和可测试性。
2. 模块化设计原则在实现子问题时,应该使用模块化的设计原则。
将每个子问题看作是一个独立的模块,通过定义清晰的接口和合理的模块之间的依赖关系,可以降低复杂度并提供更好的代码重用性。
3. 渐进式开发原则在逐步实现和聚合功能的过程中,应该遵循渐进式开发原则。
先实现基本功能,然后逐步添加更复杂或高级的功能。
这样可以逐步迭代和测试,并及时发现和解决问题。
4. 自动化测试原则为了确保每个子问题的正确性,应该在开发过程中引入自动化测试。
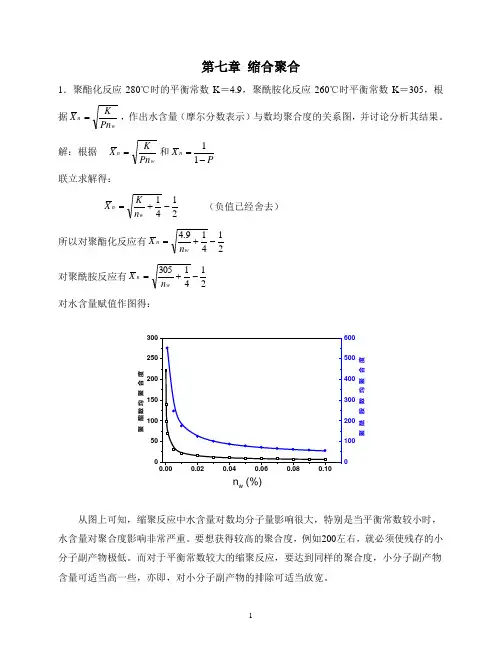
第七章 缩合聚合1.聚酯化反应280℃时的平衡常数K =4.9,聚酰胺化反应260℃时平衡常数K =305,根据wn Pn KX =,作出水含量(摩尔分数表示)与数均聚合度的关系图,并讨论分析其结果。
解:根据 wn Pn KX =和P X n -=11联立求解得:2141-+=w n n K X (负值已经舍去) 所以对聚酯化反应有21419.4-+=w n n X 对聚酰胺反应有2141305-+=w n n X 对水含量赋值作图得:n w (%)聚酯 数均聚合 度100200300400500600聚酰 胺 数 均聚合 度从图上可知,缩聚反应中水含量对数均分子量影响很大,特别是当平衡常数较小时,水含量对聚合度影响非常严重。
要想获得较高的聚合度,例如200左右,就必须使残存的小分子副产物极低。
而对于平衡常数较大的缩聚反应,要达到同样的聚合度,小分子副产物含量可适当高一些,亦即,对小分子副产物的排除可适当放宽。
2.从对苯二甲酸(1mol)和乙二醇(1mol)聚酯化反应体系中,共分出水18克,求产物的平均分子量和反应程度,设平衡常数K =4。
解:设分离出20g 水后,反应达到平衡的反应程度为p ,此时分子量为 。
起始官能团数: N 0 N 0 0 0 t 时刻官能团数:N 0(1-P) N 0(1-P) PN 0 N W 残留水分子数=生成的水分子数-排出的水分子数18W P N N 水0w -=0.5P 21818=P 18N W P N N n 0水0w w -=⨯--==根据:wpn K n X =PX n -=11代入数据:)5.0(4-=P P n XPX n -=11解得:4.4771.0==n X P数均分子量 4.42221924.4=⨯=n M3.生产尼龙-66,想获得数均分子量为13500的产品,采用己二酸过量的办法, 若使反应程度P 达到0.994,试求己二胺和己二酸的配料比。


第七章逐步聚合(stepwise polymerization)7.1 概述7.1.1逐步聚合反应分类1.按反应机理缩合聚合:多次缩合反应,有小分子析出(典型逐步聚合,重点研究)nH2N(CH2)6NH2+nHCOOC(CH2)8COOH H [ NH(CH2)6NHOC(CH2)8CO ]n OH+ (2n-1)H2O逐步加聚: 多次官能团间加成, 无小分子析出nHO-R1-OH+nO=C=N-R2-N=C=O nHO-R1-O- CO-NH-R2-N=C=O ……..HO-R1-O [CO-NH-R2-NH-CO-O-R1-O] CO-NH-R2-NCO(聚氨酯)2. 按反应动力学平衡反应:K<103聚酯(K≈4)不平衡反应: K>103聚碳酸酯3. 按产物链结构线型缩聚: 单体f=2 线型结构,可溶解,可熔融尼龙体型缩聚: 单体f=3 体型(支化或网状)结构,不溶解,不熔融环氧树脂4. 按所含特征官能团: 聚醚化, 聚酯化, 聚酰胺化…..5. 按反应单体种类homopolycondensation:aRb→N(CH2)5COOH→2mixing polycondensation:aRa+bR’b→H2N(CH2)6NH2+HOOC(CH2)4COOH→co-condensation polymerization:7.1.2逐步聚合反应的单体一单体的官能团与官能度官能团:参与反应并表征反应类型的原子(团)官能度:单体分子中反应点的数目叫做单体功能度(f ), 一般就等于单体所含功能基的数目。
二单体种类1两功能基相同并可相互反应:如二元醇聚合生成聚醚2两功能基相同, 但相互不能反应,聚合反应只能在不同单体间进行:如二元胺和二元羧酸聚合生成聚酰胺3两功能基不同并可相互反应:如羟基酸聚合生成聚酯三单体的反应能力1 官能团种类2 官能团位置3 单体设计7.2 线性逐步聚合反应机理aAa+bBb aABb+ab 单体+单体反应速率R1平衡常数K1aABb+ aAa aABAa+ab 单体+二聚体R2K2aABb+ bBb bBABb+ab 单体+二聚体R3K3aABb+ aABb aABABb+ab 二聚体+二聚体R4K4……a(AB)n/2b+ a(AB)n/2b a(AB)n b+ab R n K n7.2.1 官能团的等活性一概念(Flory)官能团等活性概念:反应物的两官能团的反应活性是相等的,它与分子链大小无关,与另一官能团是否反应也无关⇒缩聚反应表示:~a+~b ~~ +ab, R1 =R2=…=R, K1=K2=…= K 二依据1 实验依据(表2-2,2-3)2 理论依据(1)化学效率(2)碰撞频率三成立条件1 真溶液,均相体系2 官能团所处环境在反应中不变3 无扩散控制7.2.2 反应机理一大分子生成反应1 反应的逐步性2 官能团间反应:无活性中心,各基元反应活化能相同3(大多数)为可逆平衡反应4 反应进度描述(1)转化率无意义(2) 反应进程P:参加反应的官能团数/起始官能团数X n = 1/(1-P)二大分子生长终止1 热力学特征:平衡常数,黏度2 动力学限制(1)用单官能团封端(2)副反应①环化反应(聚合初期)羟基酸HO(CH2)n COOH措施: 提高单体浓度,降低反应温度,利于线型聚合②官能团消去反应(聚合中后期)③化学降解反应(聚合中后期)(缩合反应的逆反应)④链交换反应(聚合中后期)(不影响Mn,且利于Mn均匀化)(1)【作业】p50-27.3 线性逐步聚合反应动力学7.3.1 不可逆条件下线性逐步聚合动力学(以聚酯反应为例) 适用情况:1:K 小且不断排除小分子:情况2:K 很大O OH HA2AA C OHOH OH6OHOHAC OH OHOH AO及时移走及时排出水,k 4,k 6=0 另外,k 1,k 2,k 5>k 3⇒聚酯化速率]][)([])([][233OH OH C k dtOH C d dt COOH d R p ++==-=而K k k HA COOH A OH C ==-+212]][[]][)([ 且}[]][[HA A H K HA-+=⇒]][][[]][][[][]][][[0231231++-=∙=∙=H OH COOH kH OH COOH K k k k A HA OH COOH k k k R HAp 即一 自催化聚合(体系中的羧酸单体起自催化作用) 1 方程式R P = k [COOH][OH][酸催化剂]= k [COOH]2[OH] R P =-d[M]/d t = k [M]3 2[M]02kt = 1/(1-P )2 – 1 X n 2 = 1 + 2[M]02kt 2动力学曲线(1)P=0.8-0.93,符合三级动力学关系 (2)P<0.8,偏离 (3) P>0.93,偏离二 外加催化剂(外加催化剂不消耗,其浓度为常量) 1 方程式X n = 1 + [M]0k’t 2动力学曲线三 官能团不等活性体系7.3.2平衡逐步聚合动力学(不排除小分子)CO OH-1OH 2O起始 C 0 C 0 0 0t 时刻,未除水 C C C 0-C C 0-C t 时刻,部分除水 C C C 0-C n w 1.封闭体系(不排出水分子)2.开放体系(部分排出水分子)3 分析7.4 线性逐步聚合反应聚合度的控制7.4.1 影响线性逐步聚合反应聚合度的因素 一 反应程度 X n = 1/(1-P )二 平衡常数 1 封闭体系)1/(+=K K P1+=K X n2 开放体系wn Pn KC X 0=3 K 的影响三 官能团过量程度越大,分子量越小 7.4.2 控制相对分子质量方法一 (max)n X 小✋需增大聚合度✋在开放的环境中及时移走小分子 二 (max)n X 大✋需控制聚合度✋ 1控制反应程度2控制反应官能团的当量比 3加入少量单官能团单体7.4.3 某一官能团过量时的定量关系 一 A-A 与B-B (过量) 1 过量表示参数 (1)当量系数BAN N r =(2)过量分率AAB N N N q -=(3)关系r=1/(1+q) 2 X n 与r,q 的关系数均聚合度 X n=起始单体的A-A 和B-B 分子总数/生成聚合物的分子总数rP r r X n 211-++=)1(22P q q X n -++=3 讨论结论:要获得高聚合度,需同时使r →1,P →1; r 的微妙变化会引起聚合度大幅变化 二A-A 与B-B (等当量)+单官能团单体B 聚合度计算公式同前,但r,q 需调整,2BB AN N N r +=ABN N q ,2= 二A-B+单官能团单体B聚合度计算公式同前,但r,q 需调整,2BA AN N N r +=ABN N q ,2= 四 反应中r 的变化7.5 重要线性逐步聚合物学生自学,要求掌握涤纶、聚酰胺、聚氨酯、聚碳酸酯的合成工艺与反应式7.6 体型逐步聚合7.6.1 基本概念一.体型逐步聚合:由至少一种三官能团(及以上)单体参与缩聚并生成交联网状结构聚合物的逐步聚合反应二.热塑性树脂与热固性树脂三. 热固性树脂的合成线型 可溶可熔 甲阶 P<Pc部分支化 不溶可熔 乙阶 P Pc 交联 不溶不熔 丙阶 P>Pc凝胶化现象:在交联型逐步聚合反应中,随着聚合反应的进行,体系粘度突然增大,失去流动性,反应及搅拌所产生的气泡无法从体系逸出,可看到凝胶或不溶性聚合物的明显生成。

逐步聚合(Stepwise polymerization)和连锁聚合(Chain polymerization)是高分子化学中的两种重要的聚合反应。
以下是这两种聚合反应的定义及详细解释:逐步聚合(Stepwise polymerization):逐步聚合是一种通过逐步增加单体分子数量,从而逐步形成聚合物分子的过程。
这个过程中,每一步的聚合反应都是相对较慢的,因此整个聚合过程可以分成多个步骤进行。
在每个步骤中,一种单体分子与一个或多个预聚合物分子反应,从而增加聚合物的分子量。
这种聚合反应通常发生在相对较低的温度下。
逐步聚合可以分为两种主要类型:缩聚反应和加聚反应。
缩聚反应是指两个或多个单体分子在聚合过程中发生缩合反应,从而减少水分或其它小分子的生成。
这种反应常用于合成高聚物,如尼龙、聚酯等。
加聚反应是指单体分子在聚合过程中不断与预聚物分子反应,从而增加聚合物分子量。
这种反应通常用于合成低聚物,如聚乙烯、聚丙烯等。
逐步聚合的特点是聚合反应速率较慢,但可以得到分子结构明确、分子量分布较窄的聚合物。
此外,逐步聚合可以通过控制反应条件和单体比例,实现定制化的聚合物合成。
连锁聚合(Chain polymerization):连锁聚合是一种通过不断添加单体分子到预聚物或已形成的聚合物链上,从而迅速增加聚合物分子量的过程。
这个过程中,引发剂首先引发单体分子的聚合反应,生成一个活性中心(如自由基)。
这个活性中心会迅速与周围的单体分子反应,生成新的活性中心,并迅速传递下去。
随着聚合反应的进行,新的单体分子不断加入到已形成的聚合物链上,使聚合物分子量迅速增加。
连锁聚合可以分为自由基聚合、离子聚合和配位聚合等类型。
自由基聚合是最常见的一种连锁聚合,它通常发生在高温或引发剂作用下,通过自由基引发和传递实现聚合。
离子聚合则是在低温下通过离子引发和传递实现聚合。
配位聚合则是通过金属催化剂引发和传递实现聚合。
连锁聚合的特点是聚合反应速率快,可以在短时间内生成大量聚合物。
第七章逐步聚合反应引言(Introduction)绝大多数天然高分子都是缩聚物,例如蛋白质是氨基酸通过酶催化的缩聚反应的生成物,淀粉和纤维素是单糖的缩聚物。
作为生命和物种延续物质基础的核糖核酸(RNA)和脱氧核糖核酸(DNA)也是某些蛋白质分子按照空间特定部位和特殊形态的要求通过缩合反应而生成的。
另一方面,目前广泛使用的许多塑料、化纤、涂料、胶粘剂等都是缩聚物,如聚酯、聚酰胺、聚碳酸酯、酚醛树脂等是缩聚物的典型代表。
1)逐步聚合反应最基本特征是单体转变成高分子是逐步进行的,即单体官能团间相互反应而逐步增长2)逐步聚合反应范围广泛,包括绝大多数的缩聚反应,如聚酯合成,以及非缩聚反应型逐步聚合:聚加成:形式上是加成反应,但反应机理是逐步反应,如聚氨酯的合成开环反应:部分开环反应为逐步反应,如水引发的己内酰胺的开环反应氧化-偶合:单体与氧气的缩合反应,如2,6 -二甲基苯酚和氧气形成聚苯撑氧,也称聚苯醚Diels-Aldel反应:如共轭双烯烃与另一个烯类化合物发生 1,4 加成反应形成聚合物的反应本章内容:缩聚反应单体及分类线形缩聚反应机理线型缩聚动力学影响线型缩聚物聚合度的因素和控制方法分子量分布逐步聚合方法体型缩聚与凝胶点的预测7.1 缩聚反应单体及分类缩聚反应(Polycondensation)定义:是由带有两个或两个以上官能团的单体之间连续、重复进行的缩合反应,是缩合聚合反应的简称。
缩聚反应单体常带有各种官能团:如1. 缩聚反应单体体系官能度(Functionality)定义:是指一个单体分子中能够参加反应的官能团的数目单体的官能度一般容易判断,如醋酸与乙醇的官能度都为1;己二酸与邻苯二甲酸酐的官能度均为2;甘油及季戊四醇的官能度分别为3和4个别单体,反应条件不同,官能度不同,如苯酚:官能度体系> 1-n官能度体系一种单体的官能度为1,另一种单体的官能度大于1,即 1-1、1-2、1-3、1-4体系,只能得到低分子化合物,属缩合反应。
第七章--逐步聚合第七章逐步聚合习题参考答案1. 连锁聚合与逐步聚合的单体有何相同与不同?解答:连锁聚合单体的主要反应部位是单体上所含不饱合结构(双键或叁键),在聚合过程中不饱合键打开,相互连接形成大分子链。
需要有活性中心启动聚合反应,为此多需用引发剂,反应活化能低,反应速率快,相对分子质量高。
逐步聚合单体的主要反应部位是单体上所带可相互反应的官能团,在聚合过程中官能团相互反应连接在一起,形成大分子链。
不需活性中心启动反应,但反应活化能高,为此多需用催化剂,反应速率慢,受平衡影响大,相对分子质量低。
2. 在高分子化学中有多处用到了“等活性”理论,请举出三处并给予简要说明。
解答:①推导自由基聚合初期聚合反应速率,自由基活性与链长无关。
②推导共聚合共聚组成方程,活性中心活性与链长无关。
③研究线形缩聚反应速率:在缩聚反应中反应物官能团的反应活性是相等的,与分子链的大小、另一官能团是否已经反应无关。
3.名词解释(1)反应程度与转化率(2)平衡逐步聚合与不平衡逐步聚合(3)线形逐步聚合与体形逐步聚合(4)均缩聚、混缩聚与共缩聚(5)官能团与官能度(6)当量系数与过量分数(7)热塑性树脂与热固性树脂(8)结构预聚物与无规预聚物(9)无规预聚物与无规立构聚合物(10)凝胶点与凝胶效应解答:(1)反应程度:参加反应的官能团的数目与起始官能团的数目的比值。
转化率:参加反应的物质与起始物质的比值。
(2)平衡逐步聚合:或称平衡可逆聚合反应,通常系指平衡常数小于103的逐步聚合反应。
不平衡逐步聚合:或称不可逆聚合反应,通常系指平衡常数大于103的逐步聚合反应,(3)线形逐步聚合:参加聚合反应的单体都只带有两个官能团,聚合过程中,分子链成线形增长,最终获得的聚合物结构是可溶可熔的线形结构。
体形逐步聚合:参加聚合的单体至少有—种含有两个以上官能团,在反应过程中,分子链从多个方向增长,形成支化的或者交联的体形结构聚合物。
(4) 均缩聚:只有一种单体参加的缩聚反应称为均缩聚这种单体本身含有可以发生缩合反应的两种官能团。
混缩聚:混缩聚是指两种单体(a-A-a 和b-B-b)分别含有两个相同的官能团,聚合反应是通过a 和b 的相互反应进行,聚合产物的重复单元含有两种结构单元。
共缩聚:均缩聚的反应体系中加入第二种单体,或混缩聚反应体系中加入第三种甚至第四种单体进行的缩聚反应称共缩聚。
(5) 官能团:逐步聚合单体所带可相互反应的基团。
官能度:一个单体分子中参加反应的官能团的数目。
(6) 对两单体非等当量比,其中B-B 稍过量体系:当量系数:γ=N A /N B (γ≤ 1)过量分率:A 分分子A A 分分子B 分分子数-B q ---= (7) 热塑性树脂:双官能团单体缩聚得到线型聚合物,产物可以在加热时熔融,在溶剂中溶解。
热固性树脂:当一种双官能度单体与一个大于两官能度单体缩聚时,其缩聚反应首先产生支链,然后将自行交联成体型结构或通过外加交联剂交联成体型结构,这类已经交联了的体型聚合物不溶、不熔、尺寸稳定,被称为热固性高分子。
(8)结构预聚物:可进一步反应的官能团的结构、数量、位置可知的预聚物。
无规预聚物:可进一步反应的官能团的结构、数量、位置不可知的预聚物。
(9)无规预聚物:可进一步反应的官能团的结构、数量、位置不可知的预聚物。
(逐步聚合概念)无规立构聚合物:聚合物中没有一种立构可以占到多数,且排列没有规律。
(配位聚合概念)(10)凝胶点:出现凝胶化时的反应程度。
(逐步聚合概念)凝胶化:体形逐步聚合的交联反应到一定程度时,体系粘度变得很大,难以流动,反应及搅拌产生的气泡无法从体系中溢出,出现凝胶或不溶性聚合物明显生成的实验现象。
(逐步聚合概念)凝胶效应:自由基聚合中随反应进行体系粘度加大,妨碍了大分子链自由基的扩散运动,降低了两个链自由基相遇的几率,导致链终止反应速率常数随粘度的不断增加而逐步下降;另一方面,体系粘度的增加对小分子单体扩散的影响并不大,链增长反应速率常数基本不变,因而出现了自动加速现象。
这种因体系粘度增加引起的自动加速又称凝胶效应。
(自由基聚合概念)4. 举例说明下列逐步聚合反应(写出反应式)(1)缩合聚合(缩聚反应)(2)逐步加聚反应(聚加成反应)(3)Diels-Alder 反应(4)氧化偶联反应(5)加成缩合反应(6)分解缩聚(7)自由基缩聚(8)环化缩聚解答:(1) 缩合聚合(缩聚反应),PET 合成:OH 22CH 2OH COOH HOOC OCH 2CH 2OOC CO O CH 2CH 2OH H n ++n (2n-1)(2) 逐步加聚反应(聚加成反应),聚氨酯合成: C N R N C O O R'OHO C N R N H C O OR'O C O N H R N H C O OR'OHn n +n(3) Diels-Alder 反应,可溶性梯形聚合物合成:O O O O OO n +(4) 氧化偶联反应,聚苯醚合成:CH 3O CH 3CH 3O n n(5) 加成缩合反应,酚醛合成:OH CH 2O OHCH 2OH+(加成)OH CH 2OH OH OH CH 2OH+(缩合)(6) 分解缩聚,聚甲撑合成:(7) 自由基缩聚,参上氧化偶联反应,聚苯醚合成,先氧化成自由基,自由基再偶联成聚合物: CH 3O CH 3CH 3O n n(8) 环化缩聚,参上Diels-Alder 反应,反应结果成环:n+5. 用“结构特征命名法”命名大分子链中含有下列特征基团的聚合物,并各写出一例聚合反应式。
(1)-O-(2)-OCO-(3)-NH-CO-(4)-NH-O-CO-n CH =N -[-CH ]n- + n N BF 3(5)-NH-CO-NH-解答:(1) -O- 聚醚,例:聚苯醚: CH 3CH 3OHO CH 3CH 3O n n(2) -OCO- 聚酯,例:PET :O 22CH 2OH COOHHOOC OCH 2CH 2OOC CO O CH 2CH 2H n ++n (2n-1) (3) -NH-CO- 聚酰胺,例:尼龙-6,6:nHOOC(CH 2)4COOH +nH 2N(CH 2)6NH 2 →HO-[-OC(CH 2)4COHN(CH 2)6NH -]n -H + (2n-1)H 2O(4) -NH-O-CO- 聚氨酯: C N R N C O R'OH O C N R N H C O OR'O C O N H R N H C O OR'OH nn +n(5) -NH-CO-NH- 聚脲,例:脲醛树脂 ONH N H 2C O N H CH 2OH N HHOCH 2+N CH 22OH nHCHO+6. 为什么在缩聚反应中不用转化率而用反应程度描述反应过程?解答:在逐步聚合中,带不同官能团的任何两分子都能相互反应,无特定的活性种,因此,在缩聚早期单体很快消失,转变成二聚体、三聚体等低聚物,单体的转化率很高。
而相对分子质量却很低。
因此在逐步聚合反应中,转化率无甚意义。
随着逐步聚合反应的进行,官能团数目不断减少,生成物的相对分子质量逐渐增加。
因此把参加反应的官能团的数目与起始官能团的数目的比值称为反应程度,记做p。
反应程度是描述逐步聚合反应进程的重要参数。
7. 讨论下列缩聚反应成环的可能性(m=3~8),哪些因素决定环化或线形聚合是主要反应?若反应以线形聚合为主,影响聚合物相对分子量的因素有哪些?(1)HN-(CH2)m-COOH(2)HO-(CH2)7-OH+ HOOC-(CH2)m-COOH解答:①当(1)中的m=3,4时,易成较稳定有5,6元环化合物;(2)为混缩聚,主要成线形聚合物。
②从环数与环的稳定性看,存在3,4,8-11<7,12<5,6。
因此当反应可生成稳定的环时,易发生环化反应,反之易线形逐步聚合。
对(1)主要为分子内环化,故提高单体浓度可加大分子间反应,成线形聚合物。
环化反应活化能一般高于逐步聚合,故降低温度利于逐步聚合。
③两单体的配比,小分子浓度,反应程度8. 166℃下乙二醇与己二酸缩聚,测得不同时间下的羧基反应程度如表所示。
时间/m in 12 37 88 170 270 398 596 9001371羧基反应程度0.24700.49750.68650.78940.85000.88370.90840.92730.9406 (1)求对羧基浓度的反应级数,判断属于自催化或酸催化。
(2)已知[OH]0=[COOH],[COOH] 浓度以(mol.kg-1反应物)计,求出速率常数。
解答:(1)设为外加酸催化,则存在:1/(1-P)= k′C 0t+1以1/(1-P )对t 作图(略) 由图可看出,为一曲线,说明两者间不存在线形关系。
设为自催化的三级反应,则存在:1/(1-P )2= 2kC 02t+1以1/(1-P )2对t 作图(略)由图可看出,为一直线, 说明两者间存在线形关系。
图中直线的斜率为2kC 02。
(2) 由:[OH]0 =[COOH]= C 0则:2kC 02= 0.2092k = (0.1014/ C 02) Kg 2/mol 2·s9. 在外加酸条件下进行缩聚,证明P 从0.98到0.99所需的时间与从开始到P=0.98所需的时间相近。
解答:由:011[]'1COOH k t P=+- 则:`0k[COOH]1P 11t --= P = 0.98 t 1 = 49/[COOH]0k ′P = 0.99 t 2 = 99/[COOH]0k ′t 从0.98到0.99 △t =(99-49)/[COOH]0k ′= 50/[COOH]0k ′t 1 /△t ≈ 1 证毕10. 用碱滴定法和红外光谱法均测得21.3g 聚己二酰己二胺试样中含有2.5×10-3mol 的羧基。
计算该聚合物的数均相对分子质量为8520,计算时需做什么假定?如何通过实验来确定其可靠性?如该假定不可靠,如何由实验来测定正确的数均分子量?解答:① 按计算值,21.3g 聚己二酰己二胺为:21.3 /8520 = 2.5×10-3mol ,与所测羧基相当。
由此可假定每一大分子含一个羧基。
分子式为:HO-[-OC(CH 2)4COHN(CH 2)6NH -]n -H② 可用仪器(如GPC 、膜渗透等)测产物实际相对分子质量,如大于计算值,说明有可能部分大分子两端均有羧基。
如全部大分子两端均有羧基,则相对分子质量增加一倍。
分子式为:HO-[-OC(CH 2)4COHN(CH 2)6NH -]n -OC(CH 2)4CO-OH11. 对开放体系的逐步聚合,聚合度公式为o nwK CX P n⋅=⋅数学上讲,反应程度(P )越小,聚合度越大,从高化上讲是否可认为“反应程度越低,聚合度越高”?解答:① 对逐步聚合,K 为平衡常数,K 越大,反应越向右(生成聚合物方向)进行,当K 足够大后,体系由平衡逐步聚合变为不平衡逐步聚合,即反应未到平衡,聚合度己达到要求。