经导管主动脉瓣植入治疗的适应症(完整版)
- 格式:doc
- 大小:36.50 KB
- 文档页数:11


经导管主动脉瓣置换术进展(完整版)主动脉瓣狭窄(AS)是常见的心血管疾病,在西方是发病率仅次于高血压,冠心病的心血管疾病。
我国尚无大规模AS流行病学数据。
AS是进展性心血管疾病,一旦出现症状,预后很差。
若不及时干预,中位生存期为2-3年1。
外科主动脉瓣置换手术(SAVR)是严重主动脉瓣狭窄患者的标准治疗方案。
然而,高龄伴有合并症的患者手术风险高,术后恢复慢。
据统计,至少1/3 严重AS 的患者无法行SAVR2。
经导管主动脉瓣置入术(TAVI)是指将组装好的主动脉瓣经导管送至主动脉根部,替代原有主动脉瓣,在功能上完成主动脉瓣的置换,故也称经导管主动脉瓣置换术(TAVR)1。
1.发展现状自2002 年Cribier 等完成了首例人类TAVR,至今全球超过750 个中心已完成30 万例。
TAVR 技术越发成熟,手术并发症在逐渐下降,围手术期死亡概率已降至1% 左右。
在欧美等技术成熟地区,TAVR 已成为常规治疗手段。
2010年中山医院成功实施国内首例人体TAVR。
目前全国有10 多个省市、40 家医院共完成900余例TAVR 手术3。
2.适应症、禁忌症目前国外指南已将TAVR 推荐为有外科手术禁忌、高危以及中危的主动脉瓣狭窄患者的一线治疗手段3。
2015年我国专家共识指出TAVR 的绝对适应症为老年重度主动脉瓣钙化性狭窄、有相关症状、NYHA心功能II级以上、外科手术高危或禁忌、解剖适合、三叶式主动脉瓣、预期寿命超过1年或外科术后人工生物瓣退化。
相对适应症则为有症状、外科手术禁忌、预期术后寿命超过1年的二叶式主动脉瓣伴重度钙化性狭窄。
但对二叶式主动脉瓣钙化性狭窄进行TAVR,尚无大规模临床试验支持。
外科手术高危、禁忌的单纯性AR未来也可能是TAVR的适应证。
禁忌证包括:左心室内血栓,左心室流出道梗阻,30 d内心肌梗死,左心室射血分数<20%,严重右心室功能不全,主动脉根部解剖形态不适合TAVR1。


(Transcatheter Aortic Valve Implantation) Last review date: 1 April 2019 Document no.: PILIC0242C version1.1 Version 1.1 Page 1 of 4 經導管微創主動脈瓣植入術(TA VI) 治療簡介引言主動脈瓣狹窄是一種常見的心臟瓣膜疾病,並會引致心臟衰竭和死亡。
對開始出現癥狀,特別是氣促的主動脈瓣狹窄患者,臨床上一般會推薦外科瓣膜修補或瓣膜置換手術。
外科治療主動脈瓣狹窄已經被證實是唯一有效減輕病人癥狀和延長病人生命的治療方法。
然而,因您在生理或結構上等問題導致手術風險太高,而不適合接受傳統瓣膜修補或置換手術,另一個治療方法是經導管微創主動脈瓣植入術(TA VI)。
這是一項創傷性極小的新技術,通過經皮導管植入人工生物瓣膜於病變瓣膜處。
這項新技術較以往傳統的開胸手術安全,併發率及死亡率亦相對地較低,年紀較大的長者也適用。
對於不適合接受外科手術的主動脈瓣嚴重狹窄患者,經皮導管植入人工生物瓣膜有望成為替代內科藥物治療的一種有效治療方法。
手術前準備主診醫生將審閱您的醫療記錄、病歷以及目前用藥的情況以確定您是否適合進行是項手術。
•醫生會為您做心臟超聲波檢查(TTE),以確定主動脈瓣狹窄的程度。
我們會特別留意您是否合適進行此項手術。
•此外,手術前,醫護人員會為您進行心電圖、肺部X光、抽血檢驗、電腦斷層掃描或冠狀動脈造影血管攝影,以確保您適合進行此手術。
•醫生會詳細向您和您的親屬解釋是項手術的好處、進行過程及風險,而您需要簽署手術同意書。
•手術前,醫生會處方兩種抗血小板藥物從而防止血液凝結,及在手術當天處方抗生素以減低感染風險。
•若您正服用華法林或二甲双胍(一種糖尿藥,英文名稱metformin),可能需要於手術前數天停藥。
如有敏感病歷,您或需要服用類固醇。
•您需要禁食大約4-6小時;您亦可能需要靜脈輸液;如有需要,我們會在進行針刺的部位剃毛。

TAVI(经皮导管主动脉瓣植入术)的手术
前准备
一、患者评估
1.1 病史采集
详细采集患者的病史,包括基础疾病(如高血压、冠心病、糖尿病等)、既往史、手术史、家族史等。
了解患者目前的症状,如心悸、气促、胸痛等,并评估其严重程度。
1.2 体格检查
对患者进行全面体格检查,重点关注心脏大小、心律、肺部啰音、肝脾肿大等。
1.3 辅助检查
对患者进行心电图、超声心动图、胸部X线片、血液生化等检查,以评估患者的心脏功能、瓣膜病变程度、全身状况等。
二、手术风险评估
根据患者的年龄、性别、体重、基础疾病、手术类型等因素,
对手术风险进行全面评估。
主要包括出血风险、感染风险、心律失
常风险、急性肾衰竭风险等。
三、手术方案制定
根据患者的具体情况,制定个性化的手术方案。
包括手术方式、手术入路、瓣膜选择等。
四、术前药物准备
根据患者的心脏功能、血压、心率等,调整现有的药物治疗方案,并准备手术期间的临时用药,如抗凝药物、抗血小板药物、抗
生素等。
五、术前器械准备
准备手术所需的各类导管、瓣膜、支架等器械,并确保其功能正常。
六、术前患者教育
向患者及家属详细解释手术的目的、过程、风险和可能的并发症,以获得患者的理解和配合。
七、术前准备总结
对患者的病情、手术风险、手术方案、药物准备、器械准备等进行全面总结,确保手术的顺利进行。
以上是TAVI手术前准备的主要内容,希望能对您的手术有所帮助。
如有其他疑问,请随时咨询。

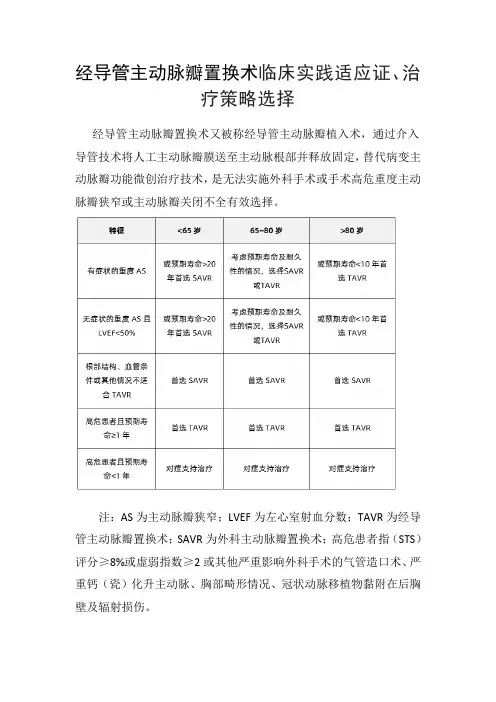
经导管主动脉瓣置换术临床实践适应证、治
疗策略选择
经导管主动脉瓣置换术又被称经导管主动脉瓣植入术,通过介入导管技术将人工主动脉瓣膜送至主动脉根部并释放固定,替代病变主动脉瓣功能微创治疗技术,是无法实施外科手术或手术高危重度主动脉瓣狭窄或主动脉瓣关闭不全有效选择。
注:AS为主动脉瓣狭窄;LVEF为左心室射血分数;TAVR为经导管主动脉瓣置换术;SAVR为外科主动脉瓣置换术;高危患者指(STS)评分≥8%或虚弱指数≥2或其他严重影响外科手术的气管造口术、严重钙(瓷)化升主动脉、胸部畸形情况、冠状动脉移植物黏附在后胸壁及辐射损伤。
推荐,干预措施明显利大于弊;建议,干预措施可能利大于弊。
A,非常确信真实值接近观察值;B,对观察值有中等程度信心:真实值有可能接近观察值,但仍存在两者不同的可能性;C,对观察值的确信程度有限:真实值可能与观察值不同。

经导管主动脉瓣植入治疗的适应症(完整版)主动脉瓣狭窄(Aortic Stenosis,AS)是老年人群中常见的心脏瓣膜病,据国外文献的报道,65岁以上人群中发病率约为2-7%[1]。
当其逐渐进展并产生相应症状(胸痛/呼吸困难/晕厥)后,若不经治疗,约有50%的患者在两年内死亡[2,3]。
长期以来,外科主动脉瓣置换术(Surgical Aortic Valve Replacement,SAVR)为AS的标准治疗方式。
然而,至少1/3的患者因其高龄、合并症、存在手术禁忌等原因无法进行SAVR[4]。
而对于这一类患者来说,内科保守治疗方式仅能暂时改善其症状而不能缓解疾病进展并改善预后。
2002年,法国的Cribier医生及其同事成功在人体首次实施经导管主动脉瓣植入术(Transcatheter Aortic Valve Implantation,TAVI),为这类患者带来了一种新的治疗选择。
在过去的10余年中,随着经验的积累和技术的改进,越来越多的患者可以从该治疗手段中获益。
随着新的临床证据不断涌现,TAVI适用人群还在不断扩展。
本文将结合现存指南以及最新的临床研究证据对TAVI技术的适应症进行探讨。
一、TAVI在不同外科手术风险人群中的应用(一)外科手术极高危(手术禁忌)和高危患者具有里程碑意义的PARTNER I研究证实在外科极高危AS患者中TAVI明显优于保守治疗[5],而在高危AS患者中TAVI不劣于SAVR[6],五年随访结果显示,TAVI在长期效果和耐久性方面同样不劣于SAVR[7]。
随后,美国CoreValve高风险研究进一步显示,在高危AS患者中,TAVI 优于SAVR,1年全因死亡率明显较低(14.2%vs 19.1%; P = 0.04)[8],并且该优越性在2年随访结束时保持不变 [9]。
因此,在最新的2017年美国心脏病学会/美国心脏协会(American College ofCardiology/American Heart Association,ACC/AHA)瓣膜病管理指南中,对于极高危和高危患者,TAVI都是I类推荐(A级证据)[10]。


经导管主动脉瓣置换术中国专家共识经导管主动脉瓣置入术(Transcatheter aortic valve implantation,TAVI)是指将组装好的主动脉瓣经导管置入到主动脉根部,替代原有主动脉瓣,在功能上完成主动脉瓣的置换,故也称经导管主动脉瓣置换术(Transcatheter aortic valve replacement,TAVR)。
主动脉瓣狭窄(aortic valve stenosis)是一种进展性心血管疾病,一旦出现症状,预后很差。
TAVR在欧美国家迅速发展,并相继发布了TAVR的专家共识和指南。
目前我国正逐步开展TAVR,为更加规范、安全地进展,特整理此专家共识。
1 适应证和禁忌证I类适应证: 外科手术禁忌、预期寿命超过1年、症状性钙化性重度AS。
外科手术禁忌是指预期术后30d内发生死亡或不可逆合并症的风险>50%,或存在手术禁忌的合并症,如胸部放射治疗后、肝衰竭主动脉弥漫性严重钙化、极度虚弱等。
外科手术高危主要是指美国胸外科医师协会(society of thoracic surgeons,STS)评分≥8分的患者。
现阶段,对于外科手术高危和禁忌患者,建议由两位或两位以上心胸外科医师评估认定,STS评分作为参考。
1.1 绝对适应症(1)老年重度主动脉瓣钙化性狭窄:超声心动图跨主动脉瓣血流速度≥4.0m/s,或跨主动脉瓣压力差≥40mmHg,或主动脉瓣口面积<0.8cm,或有效主动脉瓣口面积指数<0.5cm²/m²。
(2)患者有症状,如心悸、胸痛、晕厥,纽约心脏病协会心功能分级II级以上(3)外科手术高危或禁忌(4)解剖上适合TAVR。
不同瓣膜系统对TAVR的解剖有不同的要求,包括瓣膜钙化程度、主动脉瓣环内径、主动脉窦内径及高度、冠状动脉开口高度、入路血管内径等。
(5)三叶式主动脉瓣。
(6)纠正AS后的预期寿命超过1年。
同时符合以上所有条件者为TAVR的绝对适应证。

2023经导管主动脉瓣置换术临床实践指南(完整版)经导管主动脉瓣置换术(transcatheter aortic valve replacement, TAVR ),或称经导管主动脉瓣植入术(transcatheter aortic valve implantation z TAVI) z 是通过介入导管技术将人工主动脉瓣膜送至主动脉根部并释放固定,替代病变主动脉瓣功能的微创治疗技术。
自2002年诞生以来,TAVR在国际上得到广泛应用,其安全性和有效性已被多项大型前瞻性随机对照研究所证实[1 ]o因其无需开胸、心脏停跳和体外循环等优点,TAVR成为无法实施外科手术或手术高危的重度主动脉瓣狭窄(aortic stenosis ,AS )和(或)主动脉瓣关闭不全(aortic regurgitation , AR )患者的有效选择[2-3 ]o近年来,随着外科中危和低危AS患者TAVR 循证证据的积累,新的欧美瓣膜性心脏病患者管理指南已经不再按外科危险分层来选择AS患者的手术方式,而将年龄和预期寿命作为是否选择TAVR的主要因素[4-5]。
我国于2017年开始陆续有国产及进口TAVR器械上市,虽然TAVR 技术的开展晚于国际水平,但是临床应用数量快速增长,并已开始在各级医院逐步开展。
在临床普及的过程中,由于缺乏标准化的指南及培训,且我国患者存在一些不同于欧美患者的独有特点,为TAVR技术在中国的推广带来了挑战。
为了规范TAVR技术的应用及提高医疗质量,国家心血管病中心及国家结构性心脏病介入质控中心联合中华医学会心血管病学分会及中华医学会胸心血管外科学分会共同成立TAVR临床实践指南联合专家组,结合国内外新研究结果,在广泛征求意见的基础上制订了TAVR临床实践指南(以下简称〃本指南〃)o本指南适用于所有临床医师,尤其是内科(心内科、神经内科、呼吸与重症医学等)、外科(心外科等)、麻醉科、体外循环科、影像科、超声科及其他与主动脉瓣疾病诊疗和管理相关学科的专业人员。
经导管主动脉瓣置换术术前准备及术后护理(全文)一.概述经导管主动脉瓣植入(Transcatheter Aortic ValveImpiantation, TAVI) ,又称经导管主动脉瓣置换(Transcatheter Aortic ValveReplacement,TAVR),是通过患者的动、静脉系统或左心室心尖,利用介入导管将人工心脏瓣膜输送至主动脉瓣区后打开,替代原有主动脉瓣,实现瓣膜的正常生理功能。
二.评估与观察要点1.一般情况的评估:年龄、职业、文化程度、宗教信仰、住址、家属情况、经济及社会保障情况、病人在家庭中的地位和作用。
2.术前评估要点:生命体征、心脏B超检查、CTA检查、检验结果、用药情况、其它阳性体征、患者心理状况、患者及家属对疾病及治疗效果的预期值,女性患者是否在月经期。
3.术后评估及观察要点:(1)了解手术情况:麻醉方式、手术部位、手术方式、术中有无特殊情况。
(2)观察患者意识、生命体征,有无胸闷、心悸、气紧、呼吸困难、恶心、呕吐、头晕。
(3)伤口及穿刺部位有无渗血、红、肿、热、痛,术侧肢端血液循环情况。
(4)管道情况:临时起搏器起搏信号、导管固定是否良好、尿管引流是否通畅、中心静脉置管深度、输液是否通畅。
三.术前准备1.皮肤准备:给予患者双侧腋下、双侧腹股沟区、会阴部备皮。
2.术前指导患者床上进行大小便练习,练习床上饮水进餐,以免造成窒息,练习床上翻身及踝泵运动。
3.心功能不全患者遵医嘱强心利尿,控制出入量平衡,术前予水化治疗。
4.饮食:术前进食低钠、高蛋白、易消化饮食;术前晚22:00禁食,0:00后禁饮。
5.呼吸训练:术前指导患者有效咳嗽及深呼吸训练,以利于有效排痰。
6.术晨留置尿管、左上肢输液。
7.心理护理:术前向患者及家属详细讲解手术具体过程,及术中、术后注意事项,减轻患者心理不安因素,稳定患者情绪。
术前晚遵医嘱给予适量镇静药物,提供安静、整洁、舒适环境保证患者充分休息。
哪些病人适合接受经导管主动脉瓣置换术?经导管主动脉瓣置换术(TAVR)也称为经导管主动脉瓣置入手术(TAVI),是一种新型心脏介入的微创手术,主要是将经股动脉等外周血管穿刺送入介入导管,将人工心脏瓣膜输送至主动脉瓣区后打开,从而完成人工瓣膜的置换,恢复瓣膜功能。
随着医学和技术水平的不断提升,已广泛应用于临床疾病治疗中,那么,TAVR手术适用于哪些患者?该如何护理呢?一起来看!什么是TAVR手术?TAVR手术是一种微创瓣膜置换手术,患者不开胸,而是通过介入导管技术,仅穿刺股动脉的情况下,逆行将处理好的人工心脏瓣膜输送至主动脉瓣位置,在不处理原瓣膜的情况下进行主动脉瓣置换,恢复瓣膜功能。
传统的外科主动脉瓣置换需要打开胸腔暴露心脏,在体外循环支持心脏停跳的情况下进行手术,创伤较大;TAVR手术与传统的手术相比创伤小,操作时间短,对患者身体的影响相对较小,接受手术的患者第二天便可像正常人一样下地活动。
TAVR手术是当今国际上较先进的外科技术之一,对于高危的患者群体,是更为合适的治疗方案。
TAVR手术适用于哪些患者?该手术主要适用于高龄、高危或存在外科手术禁忌症的患者,主要包括以下疾病患者群体:(1)心功能较差的主动脉瓣疾病患者。
由于经济因素、疾病重视程度等各种因素的影响,患者疾病未接受及时治疗;出现胸闷、胸痛、气短、心慌、晕厥、水肿等症状,存在较为严重的心功能不全表现,并通过检查显示心脏收缩功能明显减低。
此类患者行常规外科的开胸手术风险系数较高,死亡率将增大,可考虑使用TAVR手术。
(2)高龄主动脉瓣疾病患者。
高龄患者的各项身体机能均出现不同程度的下降,应急代偿功能相对较差,常规外科的开胸体外循环术中心脏停跳手术耐受性较差,且术后身体恢复较慢,极大影响生活质量。
此外,据相关的临床数据显示,高龄患者开胸体外循环术后出现并发症及死亡的概率明显增高,因此,高龄重度主动脉瓣狭窄或者关闭不全的患者首选治疗方式是TAVR手术,能极大减少并发症出现的概率,从而提高预后恢复速度。
经导管主动脉瓣植入治疗的适应症(完整版)主动脉瓣狭窄(Aortic Stenosis,AS)是老年人群中常见的心脏瓣膜病,据国外文献的报道,65岁以上人群中发病率约为2-7%[1]。
当其逐渐进展并产生相应症状(胸痛/呼吸困难/晕厥)后,若不经治疗,约有50%的患者在两年内死亡[2,3]。
长期以来,外科主动脉瓣置换术(Surgical Aortic Valve Replacement,SAVR)为AS的标准治疗方式。
然而,至少1/3的患者因其高龄、合并症、存在手术禁忌等原因无法进行SAVR[4]。
而对于这一类患者来说,内科保守治疗方式仅能暂时改善其症状而不能缓解疾病进展并改善预后。
2002年,法国的Cribier医生及其同事成功在人体首次实施经导管主动脉瓣植入术(Transcatheter Aortic Valve Implantation,TAVI),为这类患者带来了一种新的治疗选择。
在过去的10余年中,随着经验的积累和技术的改进,越来越多的患者可以从该治疗手段中获益。
随着新的临床证据不断涌现,TAVI适用人群还在不断扩展。
本文将结合现存指南以及最新的临床研究证据对TAVI技术的适应症进行探讨。
一、TAVI在不同外科手术风险人群中的应用(一)外科手术极高危(手术禁忌)和高危患者具有里程碑意义的PARTNER I研究证实在外科极高危AS患者中TAVI明显优于保守治疗[5],而在高危AS患者中TAVI不劣于SAVR[6],五年随访结果显示,TAVI在长期效果和耐久性方面同样不劣于SAVR[7]。
随后,美国CoreValve高风险研究进一步显示,在高危AS患者中,TAVI 优于SAVR,1年全因死亡率明显较低(14.2%vs 19.1%; P = 0.04)[8],并且该优越性在2年随访结束时保持不变 [9]。
因此,在最新的2017年美国心脏病学会/美国心脏协会(American College ofCardiology/American Heart Association,ACC/AHA)瓣膜病管理指南中,对于极高危和高危患者,TAVI都是I类推荐(A级证据)[10]。
(二)外科手术中危患者随着TAVI技术在手术高危的患者中显示出良好的效果,越来越多的研究开始探索TAVI能否应用于外科手术中危的患者当中。
PARTNER ⅡA研究纳入了2032例手术中危AS患者(平均STS评分5.8%),随机分为两组,分别进行SAVR和TAVI治疗,2年随访结果显示两组之间全因死亡和致残性卒中复合终点发生风险无明显差别(TAVI:HR 0.89, 95%CI 0.73-1.09, P = 0.25)。
而亚组分析更显示经股动脉TAVI在上述终点事件方面优于SAVR(HR 0.79, 95%CI 0.62-1.00, P = 0.05)[11]。
基于上述研究结果,2017年ACC/AHA指南认为对于外科手术中危AS患者,TAVI是SAVR的合理替代治疗方案(Ⅱa类推荐,BR级证据)。
这也是TAVI作为外科中危AS患者的可选治疗方式首次被写入ACC/AHA指南中。
随后公布的另一项重磅研究——SURTAVI同样显示,在中危AS患者中,TAVI组与SAVR组相比,2年死亡和致残性卒中复合终点的发生风险相当,且TAVI组(使用自扩张式CoreValve)血流动力学优于SAVR组(平均跨瓣压差更低,有效瓣口面积更大)[12]。
不过这项研究公布于2017年ACC/AHA指南发布之后,否则TAVI在中危患者中的推荐级别可能会更高。
(三)外科手术低危患者TAVI现已成为外科极高危、高危和中危AS患者的标准治疗方式。
在低危AS患者中,TAVI可能同样不劣于甚至优于SAVR。
NOTION研究是目前唯一一项已经完成的比较TAVI和SAVR在低危AS患者中相对效果的随机对照试验。
该研究纳入了280例手术风险较低的AS患者,患者平均STS评分为3.0%,其中81.8%STS评分<4%。
结果显示TAVI组与SAVR组之间的1年死亡率无明显差别(4.9%vs 7.5%; P = 0.38)[13]。
目前NOTION 2 研究正在进行,预计将纳入992例年龄≤75 岁的低危患者,并按1:1的比例随机分配至TAVI组或SAVR组。
由于纳入了相对年轻的患者,该研究将有助于评估TAVI的长期效果及瓣膜耐久性。
近期公布的一项前瞻性多中心非随机对照研究结果显示,在200例接受TAVI治疗的低危AS患者中,30天死亡率和住院期间脑卒中发生率均为零(同期在参加研究的中心接受SAVR治疗的低危AS患者,30天死亡率和住院期间脑卒中发生率分别为1.7%和0.6%),提示在低危AS患者中,TAVI具有优异的临床效果[14]。
目前,2项大规模的随机对照试验(预计各纳入约1300例外科手术低患者)正在进行,即PARTNER Ⅲ和Medtronic低风险TAVI研究。
这些研究的结果有望为TAVI在外科手术低危的AS患者中的应用提供进一步的证据支持,并促使指南将TAVI的推荐适应证扩大至该类患者。
二、TAVI在特殊人群中的应用(一)外科生物瓣退化近年来,SAVR中生物瓣的使用比例逐年上升。
然而,由于生物瓣的耐久性有限,生物瓣衰败人群有所增加。
再次开胸手术一直以来是这一类患者的标准治疗方式,然而再次开胸手术具有较高的风险,尤其对于高龄患者。
经导管主动脉瓣瓣中瓣治疗有希望成为一种较好的替代治疗方案。
目前有关瓣中瓣最大型的临床研究是Dvir等牵头的全球瓣中瓣注册研究。
该研究纳入了从2007年至2013年共459例行瓣中瓣治疗的患者,结果显示术后30天35例患者(7.6%)死亡,8例发生严重卒中(1.7%),余下存活患者中有313例(92.6%)心功能明显改善。
1年死亡率为16.8%,其危险因素包括较小的外科生物瓣(≤21 mm; HR:2.04; 95%CI, 1.14-3.67; P = 0.02) 以及基线外科生物瓣狭窄(vs 反流,HR:3.07; 95%CI, 1.33-7.08; P = 0.008)[15]。
另一项较大型的研究为2017年Webb及其同事所公布的PARTNER Ⅱ瓣中瓣注册研究。
该研究再次显示出TAVI 用于治疗外科生物瓣衰败的有效性。
该研究纳入365例手术高危外科生物瓣衰败患者,总体平均年龄为78.9岁,平均STS评分为9.1%。
结果显示30天和1年全因死亡率分别为2.7%和12.4%。
术后一年随访结果显示,平均跨瓣压差为17.6 mm Hg,有效瓣口面积1.16 cm2,轻度以上瓣周漏发生率为1.9% [16]。
总体上,经导管瓣中瓣植入治疗人工生物瓣衰败的安全性和临床效果良好,因此美国FDA在2015年即已批准将Medtronic CoreValve系统用于TAVI瓣中瓣(治疗人工生物主动脉瓣衰败),并于2017 年批准Edwards SAPIEN 3 瓣膜用于主动脉瓣瓣中瓣和经导管二尖瓣瓣中瓣(治疗人工生物主动脉瓣和二尖瓣衰败)。
2017年的ACC/AHA指南首次指出,对于症状严重的外科生物瓣衰败的患者,经心脏团队评估后手术风险较高以及不能手术并且治疗后有望改善其症状的情况下,瓣中瓣治疗是合理的选择(Ⅱa类推荐,B-NR级证据)。
(二)二叶式主动脉瓣二叶式主动脉瓣是常见的先天性心脏结构异常,并且因其特殊的瓣叶形态使其承受更大的机械应切力因此更易发生钙化和瓣膜狭窄。
国内TAVR候选患者中二叶式主动脉瓣的比例明显高于国外,达40%[17]。
随着TAVI技术逐渐应用至更年轻和手术风险更低的患者中,术者所面临的二叶式主动脉瓣患者也将越来越多。
一直以来,人们认为二叶瓣是TAVI治疗的禁忌症,因此过去早期的TAVI临床研究常将其列为排除标准。
对于TAVI治疗来说,二叶瓣解剖形态的特殊之处在于其瓣环更倾向于椭圆形、瓣叶钙化分布不对称、各个瓣叶大小不等以及常常合并有升主动脉扩张。
这些因素可能会使植入的瓣膜呈椭圆形进而损害瓣膜耐久性,并且使瓣周漏、冠脉堵塞、瓣环破裂和升主动脉并发症发生率升高。
2016年Yoon等报道的二叶式AS TAVI注册研究纳入了来自欧洲、北美以及亚太地区20个中心的301例患者。
其中199例患者使用了早一代器械(Sapien XT: n=87; CoreValve: n=112),102例患者使用新一代器械(Sapien 3: n=91; Lotus [Boston Scientific]:n=11)。
结果显示使用新一代器械的患者轻度以上瓣周漏发生率更低(0.0 %vs 8.5 %; P = 0.002),手术成功率更高(92.2 %vs 80.9 %; P = 0.01)[18] 。
2017年Yoon等将561例二叶瓣TAVI患者与4546例三叶瓣行TAVI的患者进行倾向性匹配分析,最终形成546组患者。
比较的结果显示,二叶瓣组患者的中转开胸发生率高于三叶瓣组(2.0%vs. 0.2%; p= 0.006) ,手术成功率低于三叶瓣组(85.3%vs 91.4%; p = 0.002)。
2年全因死亡率在两组之间无明显差异(17.2%vs 19.4%; p = 0.28)。
在使用早一代器械的患者当中,经球扩瓣治疗的患者,二叶瓣比三叶瓣更易发生主动脉根部损伤(4.5%vs 0.0%; p = 0.015) ,经自扩张瓣膜治疗的患者,二叶瓣组的中重度瓣周漏发生率高于三叶瓣组(19.4%vs 10.5%; p = 0.02) 。
然而在使用新一代器械患者当中,手术结果在二叶瓣与三叶瓣患者之中无明显差异[19]。
以上研究表明,在二叶瓣患者中行TAVI依然具有挑战性。
从目前有限的数据来看,TAVI应用于二叶瓣患者是安全有效的,但仍需更有针对性的临床研究予以证实。
目前二叶瓣与三叶瓣在生存率与手术成功率方面无明显差异,但二叶瓣患者在主动脉根部评估、人工瓣膜的定位和稳定性以及瓣周漏方面都不同于三叶瓣。
另外在远期预后方面,也存在不确定性。
此外,对于合并升主动脉扩张的二叶瓣狭窄患者,TAVI的应用也应十分慎重。
术前进行仔细的影像学评估,选择合适的患者以及更新改进人工瓣膜的设计有助于进一步提高TAVI在二叶瓣患者中的治疗效果。
(三)单纯主动脉瓣反流与AS相比,单纯主动脉瓣反流的发生率较低(不到前者的1/3)。
不过与AS一样,已有明显临床症状的主动脉瓣反流患者如未经治疗预后较差,年死亡率约为10%-20%[20]。
SAVR是主动脉瓣反流的标准治疗方案。
然而仍有部分临床症状明显的重度主动脉瓣反流的患者因因各种原因无法行手术治疗,这些患者可能从TAVI技术中获益。
在单纯主动脉瓣反流的患者中行TAVI治疗是极具挑战的,因此这类患者常常作为TAVI手术的禁忌症。