定量实验的设计与评价
- 格式:ppt
- 大小:762.00 KB
- 文档页数:14
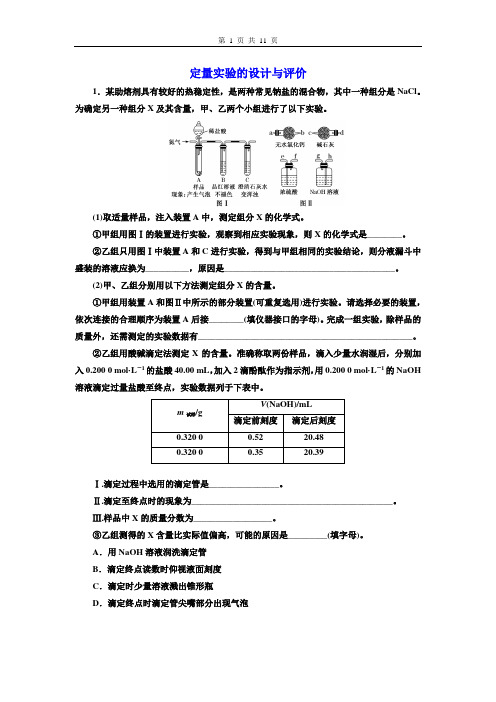
定量实验的设计与评价1.某助熔剂具有较好的热稳定性,是两种常见钠盐的混合物,其中一种组分是NaCl。
为确定另一种组分X及其含量,甲、乙两个小组进行了以下实验。
(1)取适量样品,注入装置A中,测定组分X的化学式。
①甲组用图Ⅰ的装置进行实验,观察到相应实验现象,则X的化学式是________。
②乙组只用图Ⅰ中装置A和C进行实验,得到与甲组相同的实验结论,则分液漏斗中盛装的溶液应换为__________,原因是_______________________________________。
(2)甲、乙组分别用以下方法测定组分X的含量。
①甲组用装置A和图Ⅱ中所示的部分装置(可重复选用)进行实验。
请选择必要的装置,依次连接的合理顺序为装置A后接________(填仪器接口的字母)。
完成一组实验,除样品的质量外,还需测定的实验数据有_________________________________________________。
②乙组用酸碱滴定法测定X的含量。
准确称取两份样品,滴入少量水润湿后,分别加入0.200 0 mol·L-1的盐酸40.00 mL,加入2滴酚酞作为指示剂,用0.200 0 mol·L-1的NaOH 溶液滴定过量盐酸至终点,实验数据列于下表中。
Ⅰ.滴定过程中选用的滴定管是________________。
Ⅱ.滴定至终点时的现象为______________________________________________。
Ⅲ.样品中X的质量分数为__________________。
③乙组测得的X含量比实际值偏高,可能的原因是_________(填字母)。
A.用NaOH溶液润洗滴定管B.滴定终点读数时仰视液面刻度C.滴定时少量溶液溅出锥形瓶D.滴定终点时滴定管尖嘴部分出现气泡解析:(1)①与盐酸反应得到的气体不能使品红溶液褪色,而能使澄清石灰水变浑浊,说明生成的气体为CO 2,则该助熔剂中含有Na 2CO 3或NaHCO 3,由于NaHCO 3受热易分解,热稳定性较差,所以X 是Na 2CO 3。
化学实验第七讲 定量实验设计与评价北京四中:叶长军定量实验定量测量实验设计是为了深入了解物质或自然现象的量的特征, 揭露各因素之间的数量关系,从而确定某些因素的数值。
它能够具体地从量上来测定对象所具有的某种性质或者它们之间的数量关系。
所得到的结果是一定质和量之间的准确函数关系。
因此所有影响此函数关系准确性的因素都被视为干扰因素,设计实验就是确定了某一具体方案后,排除此方案中所有干扰因素。
干扰因素全部排除了,此方案具体的实施程序就清晰且明确了。
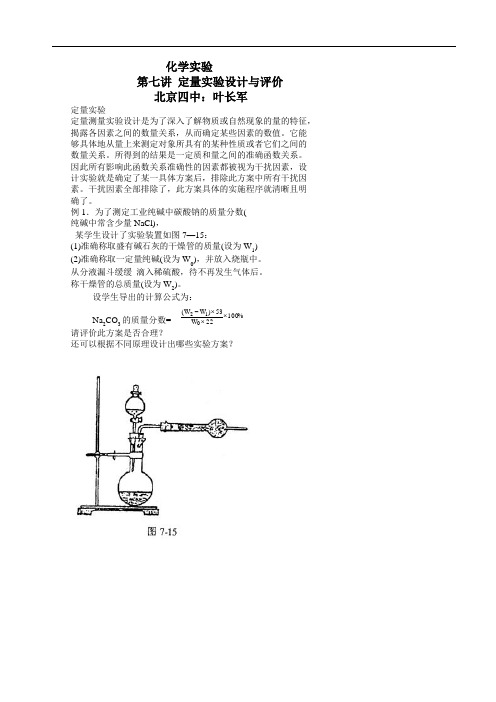
例1.为了测定工业纯碱中碳酸钠的质量分数(纯碱中常含少量NaCl),某学生设计了实验装置如图7—15:(1)准确称取盛有碱石灰的干燥管的质量(设为W 1)(2)准确称取一定量纯碱(设为W 0),并放入烧瓶中。
从分液漏斗缓缓 滴入稀硫酸,待不再发生气体后。
称干燥管的总质量(设为W 2)。
设学生导出的计算公式为:Na 2CO 3的质量分数= 请评价此方案是否合理?还可以根据不同原理设计出哪些实验方案?%10022W 53)W W (012⨯⨯⨯-例2.下列实验方案中,不能测定Na 2CO 3和NaHCO 3, 混合物中 Na 2CO 3质量分数的是A .取a 克混合物充分加热,减重b 克B .取a 克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b 克固体C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克溶液充D.取a克混合物与足量Ba(OH)2分反应,过滤、洗涤、烘干,得b克固体例3.A~G为中学常见的化合物,它们之间有如图所示的转化关系(反应条件及部分产物已略去)。
A为绿色粉末,含H、C、O、Cu四种元素。
常温下D为无色无味气体,B为黑色粉末,E能发生银镜反应。
请回答:(1)D跟G反应的化学方程式为__________________________;(2)F中一定含有的官能团的名称为_______________________;(3)某课外小组同学设计了下列实验装置,通过测定某些装置中试剂的质量变化,探究A中各元素的质量关系。




定量评估的方法简介定量评估是科学研究和实践中常用的一种评估方法。
它基于量化数据的收集与分析,可以更客观地评估一个系统、产品或服务的性能、效果和效能。
本文将介绍几种常用的定量评估的方法,包括实验研究、调查问卷、统计分析等,并探讨它们的优缺点和适用范围。
实验研究实验研究是定量评估中最常用的方法之一。
它通过设定不同的实验组和对照组,并对它们进行相同的操作或处理,然后比较它们的差异来评估一个系统、产品或服务的性能。
实验研究通常包括以下步骤:1.问题定义:明确要研究的问题和目标;2.实验设计:设计实验组和对照组的设置,以及操作或处理的详细步骤;3.数据收集:收集实验过程中产生的各种数据;4.数据分析:基于收集到的数据进行统计分析,比较实验组和对照组之间的差异;5.结果解释:解释分析结果,得出结论。
实验研究的优点是能够更准确地评估因果关系,并可控制其他影响因素的干扰。
然而,实验研究也存在一些缺点,如耗时、昂贵和可能的伦理限制。
调查问卷调查问卷是一种常见的定量评估方法,特别适用于大规模数据收集。
通过设计问题并向受调查者提供选择或自由回答的方式,收集到的数据可以进行统计分析和结果展示。
调查问卷的步骤包括:1.问题设计:设计一系列问题,明确需要收集的信息;2.问卷制作:将问题转换成问卷的形式,并合理组织问题的顺序;3.样本选择:确定调查问卷的受众群体,并进行样本选择;4.数据收集:将问卷发送给受调查者,收集反馈的数据;5.数据分析:对收集到的数据进行统计分析,得出结论。
调查问卷的优点是使用方便、成本较低且适用于大规模数据收集。
然而,调查问卷的缺点在于受调查者可能存在回答偏差,以及有些问题可能无法准确传达受众的真实想法。
统计分析统计分析是定量评估中的重要环节,它可以通过数学和统计方法对收集到的数据进行分析,揭示数据背后的规律和趋势。
常见的统计分析方法包括:1.描述统计:对数据进行概括和描述,包括计算均值、方差、中位数等指标;2.推断统计:根据样本数据对总体进行推断,包括构建置信区间、假设检验等;3.回归分析:通过建立数学模型来分析变量之间的关系,包括线性回归、多元回归等。
定量实验设计与评价编稿:房鑫审稿:于冬梅【高考展望】一、考纲要求1.能根据实验试题要求,做到:〔1〕设计、评价或改良实验方案;〔2〕理解控制实验条件的方法;〔3〕分析或处理实验数据,得出合理结论;〔4〕绘制和识别典型的实验仪器装置图。
2.以上各局部知识与技能的综合应用。
二、高考动向新课程背景下的高考化学实验试题非常重视将定性实验和定量实验进展有机结合,试题中所设计的问题多为实验的根本操作知识及实验原理的分析、实验数据的处理和对实验流程的推理,旨在对学生实验根本素养和分析处理数据才能的考察。
本节主要涉及定量实验设计与评价。
【方法点拨】定量实验方案的设计的一般要求①根据题目要求设计定量实验的测定原理,如混合物组成测定的一般设计思路是使其中一种组分发生化学反响生成气体或沉淀,通过测定气体或固体的量进而求得各组分的含量。
②定量实验的关键是保证数据的准确性,因此确定了某一详细实验方案后,应注意在实验中保证所测数据是准确的:如除杂、数据的重复测定等特征设计,还要排除此方案中所有干扰因素,干扰因素全部排除了,此方案详细的施行程序就明晰且明确了。
因此教学中要尽量创造条件,让学生动手多做实验,让学生自选课题、设计实验、改良或创新实验,并对实验进展评价和分析,培养学生的创新意识的创新精神,训练学生用实验解决化学问题,使学生掌握评价实验方案的常见角度和方法。
总之,新课程理念下的高三化学复习备考应注重近年来高考实验试题考察的动向进展研究,从试题中去领略试题考察的意图和试题命制方向,从而在教学中有目的性地培养学生的实验创新意识和实验探究才能,真正做到有的放矢,进步实验备考复习效率。
【典型例题】类型一、混合物中某物质含量的测定例1.某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用以下图中的装置进展实验。
主要实验步骤如下:①按图组装仪器,并检查装置的气密性②将ag试样放人入锥形瓶中,加适量蒸馏水溶解,得到试样溶液③称量盛有碱石灰的U 型管的质量,得到bg④从分液漏斗滴人6mo1·L -1的硫酸,直到不再产生气体时为止⑤从导管A 处缓缓鼓入一定量的空气⑥再次称量盛有碱石灰的U 型管的质量,得到cg⑦重复步骤⑤和⑥的操作,直到U 型管的质量根本不变,为dg请填空和答复以下问题:(1)在用托盘天平称量样品时,假如天平的指针向左偏转,说明______________________(2)装置中枯燥管B 的作用是___________________________________(3)假如将分液漏斗中的硫酸换成浓度一样的盐酸,测试的结果__________ (填偏高、偏低或不变)(4)步骤⑤的目的是____________________________(5)步骤⑦的目的是________________________________(6)该试样中纯碱的质量分数的计算式为______________________________(7)还可以用其他实验方法测定试样中纯碱的质量分数。