2013年_安徽高考化学
- 格式:doc
- 大小:59.50 KB
- 文档页数:5

2013年高考化学试题分类解析——选择题部分(7.化学键与能量)备注:2013年高考化学或者理科综合(化学)试题统计及顺序(共15套,31地区)1、(1套)大纲版全国卷(广西)2、(1套,9地区)新课标全国卷I(内蒙古、宁夏;黑龙江、吉林、河南、河北、山西、陕西、湖南、江西)3、(1套,7地区)新课标全国卷II(西藏,新疆;青海、甘肃、贵州、云南、辽宁)4、(4套,4地区)4个直辖市各一套:北京、天津、上海、重庆5、(8套,8地区)独立命题省份:安徽,山东,四川,江苏,浙江,福建,广东,海南。
12. 【题文】在1200℃时,天然气脱硫工艺中会发生下列反应H2S(g)+ 32O2(g)=SO2(g)+H2O(g) △H12H2S(g)+SO2(g)=S2(g)+2H2O(g) △H2H2S(g)+O2(g)=S(g)+H2O(g) △H32S(g) =S2(g) △H4则△H4的正确表达式为()A.△H4=32(△H1+△H2-3△H3) B.△H4=32(3△H3-△H1-△H2)C.△H4=32(△H1+△H2+3△H3) D.△H4=32(△H1-△H2-3△H3)【答案】A【解析】考察盖斯定律。
根据S守恒原理,要得到方程式4,可以用(方程式1+方程式2—3×方程式2)×3 2.【试源】2013年高考新课标Ⅱ卷化学试题1.【题文】下列设备工作时,将化学能转化为热能的是()【答案】D【试源】2013北京高考理科综合化学试题11.【题文】下列有关电解质溶液的说法正确的是()A.在蒸馏水中滴加浓H2SO4,K W不变B.CaCO3难溶于稀硫酸,也难溶于醋酸C.在Na2S 稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-)D.NaCl 溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同【答案】C【解析】A稀释的时候放热;C质子守恒;D加了会水解的盐,会促进水的电离。

2013年安徽高考化学卷江苏省丹阳市访仙中学殷传富编辑相对原子质量(原子量):H-1 C-12 N-14 O-16 Al-27 S-32Cl-35.5 Ce-140 Pb-2077.(2013·安徽理综·7)我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO + O2−−−→−催化剂CO2 + H2O。
下列有关说法正确的是()A.该反应为吸热反应B.CO2分子中的化学键为非极性键C.HCHO分子中含δ键又含π键D.每生成1.8gH2O消耗2.24LO2【答案】C【解析】A.燃烧反应均为放热反应,A错误;B.二氧化碳结构为O=C=O,为极性键,由于是直线型对称结构,键的极性抵消,CO2是非极性分子,B错误;。
C.甲醛的结构式为,含有碳氧双键,故其中既含有3个σ键,1个π键,C正确;D.氧气的体积,并没有标明状况,故不一定为2.24L,D错误。
【考点定位】以除甲醛气体为新的情境,考查了化学反应基本理论和基本概念,涉及化学反应中能量变化,分子结构、化学键以及气体的体积等相关知识。
8.(2013·安徽理综·8)实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。
仅用此装置和表中提供的物质完成相关实验,最合理的选项是【解析】该装置分别为固液不加热制气体,向上排空气法收集气体,以及采用防倒吸的方法进行尾气处理。
A.CaO+H2O==Ca(OH)2,反应放热,且促进NH4++OH-NH3·H2O NH3+H2O 平衡移动,产生氨气,氨气不能使用向上排空气法,A错误;B.Na2SO3+ H2SO4== Na2SO4+ H2O+SO2↑,正确;C.3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O,NO不能用排空气法收集,2NO+O2==NO2,C错误;D.4HCl(浓)+MnO2△ MnCl2+Cl2↑+2H2O,制取氯气需要加热,D错误。
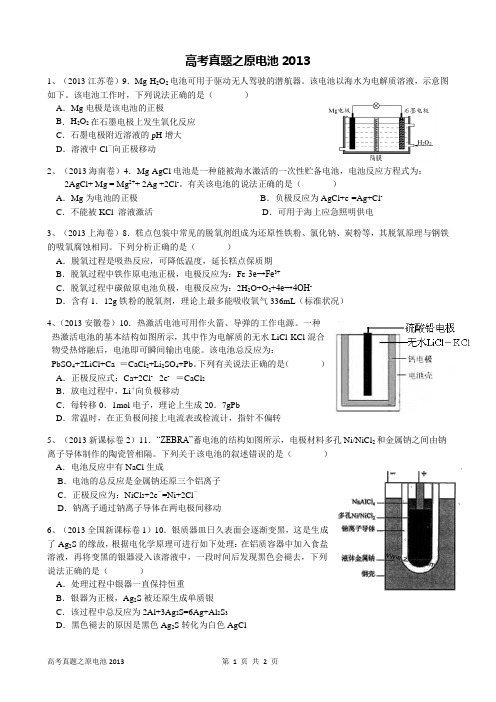
高考真题之原电池20131、(2013江苏卷)9.Mg-H2O2电池可用于驱动无人驾驶的潜航器。
该电池以海水为电解质溶液,示意图如下。
该电池工作时,下列说法正确的是()A.Mg电极是该电池的正极B.H2O2在石墨电极上发生氧化反应C.石墨电极附近溶液的pH增大D.溶液中Cl-向正极移动2、(2013海南卷)4.Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+ Mg = Mg2++ 2Ag +2Cl-。
有关该电池的说法正确的是()A.Mg为电池的正极B.负极反应为AgCl+e-=Ag+Cl-C.不能被KCl 溶液激活D.可用于海上应急照明供电3、(2013上海卷)8.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。
下列分析正确的是()A.脱氧过程是吸热反应,可降低温度,延长糕点保质期B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e→Fe3+C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e→4OH-D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)4、(2013安徽卷)10.热激活电池可用作火箭、导弹的工作电源。
一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。
该电池总反应为:PbSO4+2LiCl+Ca =CaCl2+Li2SO4+Pb。
下列有关说法正确的是()A.正极反应式:Ca+2Cl- - 2e- =CaCl2B.放电过程中,Li+向负极移动C.每转移0.1mol电子,理论上生成20.7gPbD.常温时,在正负极间接上电流表或检流计,指针不偏转5、(2013新课标卷2)11.“ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。
下列关于该电池的叙述错误的是()A.电池反应中有NaCl生成B.电池的总反应是金属钠还原三个铝离子C.正极反应为:NiCl2+2e-=Ni+2Cl-D.钠离子通过钠离子导体在两电极间移动6、(2013全国新课标卷1)10.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,下列说法正确的是()A.处理过程中银器一直保持恒重B.银器为正极,Ag2S被还原生成单质银C.该过程中总反应为2Al+3Ag2S=6Ag+Al2S3D.黑色褪去的原因是黑色Ag2S转化为白色AgCl7、(2013全国新课标卷1)27.锂离子电池的应用很广,其正极材料可再生利用。

绝密★启用前2013年普通高等学校招生全国统一考试(安徽卷)理科综合能力测试本试卷分为第I卷(选择题)和第II卷(非选择题),第I卷第1页至第5页,第II卷第6页至第12页。
全卷满分300分。
考生注意事项:1.答题前,务必在试题卷、答题卡规定的地方填写自己的姓名、座位号,并认真核对答题卡上所粘贴的条形码中的姓名、座位号与本人姓名、座位号是否一致。
务必在答题卡背面规定的地方填写姓名和座位号后两位。
2.答第I卷时,每小题选出答案后,用2B铅笔把答题卡上所对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
3.答第II卷时,必须使用0.5毫米的黑色墨水签字笔在答题卡上....书写,要求字体工整、笔迹清晰。
作图题可先用铅笔在答题卡的规定的位置绘出,确认后再用0.5毫米的黑色墨水签字笔描清楚。
必须在题号所指示的答题区域作答,超出答题区域书写的答案无效,在试题卷、草稿纸上答题无效。
............................4.考试结束后,务必将试题卷和答题卡一并上交。
第I卷(选择题共120分)本卷共20小题,每小题6分,共120分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
以下数据可供解题时参考相对原子质量(原子量):H1 C12 N14 O16 Ai27 S32 Cl35.5 Ce140 Pb2071.生物膜将真核细胞分隔成不同的区室,使得细胞内能够同时进行多种化学反应,而不会相互干扰。
下列叙述正确的是A.细胞核是mRNA合成和加工的场所B.高尔基体是肽链合成和加工的场所C.线粒体将葡萄糖氧化分解成CO2和H2OD.溶酶体合成和分泌多种酸性水解酶2.细胞代谢受酶的调节和控制。
下列叙述正确的是A.激素都是通过影响细胞内酶活性来调节细胞代谢B.代谢的终产物可反馈调节相关酶活性,进而调节代谢速度C.同一个体各种体细胞酶的种类相同、数量不同,代谢不同D.对于一个细胞来说,酶的总类和数量不会发生变化3.右图为第10粒水稻种子在成熟过程中于物质和呼吸速率变化的示意图。

2013年 各地高考《能量及化学平衡》 题目汇编友情提示:江苏、上海、四川题目难度偏大,可根据自己的情况进行选择1. (2013年四川卷)在一定温度下,将气体X 和气体Y 各0.16mol 充入10L 恒容密闭容器中,发生反应△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是A .反应前2min 的平均速率ν(Z)=2.0×10—3mol·L —1·min —1B .其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)C .该温度下此反应的平衡常数K =1.44D . 其他条件不变,再充入0.2molZ ,平衡时X 的体积分数增大2. (2013年安徽卷)一定条件下,通过下列反应可以制备特种陶瓷的原料MgO :MgSO 4(s) + CO(g)MgO(s) + CO 2(g) + SO 2(g); △H>0 该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x 的值,重新达到平衡后,纵坐标y 随x 变化趋势合理的是 3. (2013年 重庆卷)已知:P 4(g)+6Cl 2(g)=4PCl 3(g) △H =a kJ∙mol —1P 4(g)+10Cl 2(g)=4PCl 5(g) △H =b kJ∙mol —1P 4具有正四面体结构,PCl 5中P -Cl 键的键能为c kJ∙mol —1,PCl 3中P -Cl 键的键能为 1.2c kJ∙mol —1。
下列叙述正确的是A .P -P 键的键能大于P -Cl 键的键能B .可求Cl 2(g)+ PCl 3(g)=4PCl 5(s)的反应热△HC .Cl -Cl 键的键能为(b -a+5.6c)/4 kJ∙mol —1D .P -P 键的键能为(5a -3b+12c)/8 kJ∙mol —14. (2013年 重庆卷)将E 和F 加入密闭容器中,在一定条件下发生反应:2G(g)。

2013年安徽省化学高考考试说明及题型示例根据教育部考试中心颁发的《2012年普通高等学校招生全国统一考试大纲(理科·课程标准实验版)》(以下简称《考试大纲》),结合安徽省普通高中化学教学实际,制定《2012年普通高等学校招生全国统一考试安徽卷考试说明(理科·课程标准实验版)》(以下简称《考试说明》)的化学科部分。
一、考试目标与要求化学科考试,为了有利于选拔具有学习潜能和创新精神的考生,以能力测试为主导,将在测试考生进一步学习所必需的知识、技能和方法的基础上,全面检测考生的化学科学素养。
化学科命题注重测量自主学习的能力,重视理论联系实际,关注与化学有关的科学技术、社会经济和生态环境的协调发展,以促进学生在知识和技能、过程和方法、情感、态度和价值观等方面的全面发展。
(一)对化学学习能力要求1.接受、吸收、整合化学信息的能力(1)能够对中学化学基础知识融会贯通,有正确复述、再现、辨认的能力。
(2)能够通过对实际事物、实验现象、实物、模型、图形、图表的观察,以及对自然界、社会、生产、生活中的化学现象的观察,获取有关的感性知识和印象,并进行初步加工、吸收、有序存储的能力。
(3)能够从试题提供的新信息中,准确地提取实质性内容,并经与已有知识块整合,重组为新知识块的能力。
2.分析问题和解决(解答)化学问题的能力(1)能够将实际问题分解,通过运用相关知识,采用分析、综合的方法解决简单化学问题的能力。
(2)能够将分析解决问题的过程和成果用正确的化学术语及文字、图表、模型、图形等表达,并作出解释的能力。
3.化学实验与探究能力(1)了解并初步实践化学实验研究的一般过程,掌握化学实验的基本方法和技能。
(2)在解决简单化学问题的过程中,运用科学的方法,初步了解化学变化规律,并对化学现象提出科学合理的解释。
(二)对知识内容的要求层次为了便于考查,将高考化学命题对各部分知识内容要求的程度,由低到高分为了解、理解(掌握)、综合应用三个层次,高层次的要求包含低层次的要求。
2013年普通高等学校招生全国统一考试安徽卷考试说明·理科综合(化学部分)安徽省教育招生考试院、安徽省教育科学研究院编I.考试性质普通高等学校招生全国统一考试是合格的高中毕业生和具有同等学力的考生参加的选拔性考试.高等学校根据考生成绩,按已确定的招生计划,德、智、体全面衡量,择优录取.因此,高考应具有较高的信度、效度,必要的区分度和适当的难度.II. 考试形式与试卷结构(一)考试形式笔试、闭卷(二)考试时间150分钟(三)科目分值试卷满分300分。
其中物理110分、化学100分、生物90分。
各学科试题原则上不跨学科综合,只涉及本学科内容。
(四)试卷结构试卷分第第I卷和第II卷。
第I卷为物理、化学、生物三个科目的单项选择题组成,共20题,每题6分,合计120分。
其中物理7题、化学7题、生物6题。
第II卷为物理、化学、生物三个科目的非选择题组成,合计180分。
(五)组卷试卷按题型、内容和难度进行排列,选择题在前,非选择题在后;同一题型中同一学科的试题相对集中,同一学科中的不同试题尽量按由易到难的顺序排列。
III.考试内容与题型示例化学根据教育部考试中心颁发的《2013年普通高等学校招生全国统一考试大纲(理科·课程标准实验版)》(以下简称《考试大纲》),结合安徽省普通高中化学教学实际,制定《2013年普通高等学校招生全国统一考试安徽卷考试说明(理科·课程标准实验版)》(以下简称《考试说明》)的化学科部分。
一、考核目标与要求化学科考试,为了有利于选拔具有学习潜能和创新精神的考生,以能力测试为主导,将在测试考生进一步学习所必需的知识、技能和方法的基础上,全面检测考生的化学科学素养。
化学科命题注重测量自主学习的能力,重视理论联系实际,关注与化学有关的科学技术、社会经济和生态环境的协调发展,以促进考生在知识和技能、过程和方法、情感、态度和价值观等方面的全面发展。
(一)对化学学习能力的要求1.接受、吸收、整合化学信息的能力(1)能够对中学化学基础知识融会贯通,有正确复述、再现、辨认的能力。
2013年安徽高考化学卷(真题Word 版)相对原子质量(原子量):H 1 C 12 N 14 O 16 Al 27 S 32 Cl 35.5 Ce 140 Pb 207 一、选择题7.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO + O 2 CO 2 + H 2O 。
下列有关说法正确的是( )A.该反应为吸热反应B.CO 2分子中的化学键为非极性键C.HCHO 分子中含δ键又含π键D.每生成1.8gH 2O 消耗2.24LO 28.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。
仅用此装置和表中提供的物质完成相关实验,最合理的选项是 选项 a 中的物质 b 中的物质 c 中收集的气体 d 中的物质 A 浓氨水 CaO NH 3 H 2O B 浓硫酸 Na 2SO 3 SO 2 NaOH 溶液C 稀硝酸 Cu NO 2 H 2O D浓盐酸MnO 2Cl 2NaOH 溶液9.下列分子或离子在指定的分散系中能大量共存的一组是( ) A.银氨溶液: Na +、K +、NO 3-、NH 3·H 2O B.空气: C 2H 2、CO 2、SO 2、NO C.氢氧化铁胶体:H +、K +、S 2-、Br -D.高锰酸钾溶液:H +、Na +、SO 42-、葡萄糖分子10.热激活电池可用作火箭、导弹的工作电源。
一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl 混合物受热熔融后,电池即可瞬间输出电能。
该电池总反应为:PbSO 4 + 2LiCl + Ca = CaCl 2 + Li 2SO 4 + Pb 。
下列有关说法正确的是( )A.正极反应式:Ca + 2Cl - - 2e - = CaCl 2B.放电过程中,Li +向负极移动C.每转移0.1mol 电子,理论上生成20.7g PbD.常温时,在正负极间接上电流表或检流计,指针不偏转11.一定条件下,通过下列反应可以制备特种陶瓷的原料MgO :MgSO 4(s) + CO(g) ≒MgO(s) + CO 2(g) + SO 2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x 的值,重新达到平衡后,纵坐标y 随x 变化趋势合理的是( )选项 x y A 温度容器内混合气体的密度 B CO 的物质的量 CO 2与CO 的物质的量之比 C SO 2的浓度平衡常数K DMgSO 4的质量(忽略体积)CO 的转化率12.我省盛产矿盐(主要成分是NaCl ,还含有SO 42-等其他可溶性杂质的离子)。
(时间:45分钟 分值:100分) 一、选择题(共7个小题,每小题6分,共42分,每小题给出的四个选项中只有一个是正确的) 1.(改编)一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)2NH3(g) ΔH<0,反应过程如图: 下列说法正确的是( )。
A.t1 min时正、逆反应速率相等 B.X曲线表示NH3的物质的量随时间变化的关系 C.0~8 min,H2的平均反应速率v(H2)= mol·L-1·min-1 D.10~12 min,升高温度使反应速率加快,平衡正向移动 解析 t1 min时,只是X和Y的物质的量相等,没有达到平衡状态,正、逆反应速率不相等;根据图像,Y表示H2的物质的量随时间的变化关系,X表示NH3的物质的量随时间的变化关系,0~8 min,H2的平均反应速率v(H2)=mol·L-1·min-1。
10~12 min,H2的平均反应速率v(H2)=0.007 5 mol· L-1·min-1,由于可逆反应正向是放热的,升高温度平衡将向逆反应方向移动,故D项错误。
答案 B 2.(原创)2SO2(g)+O2(g)2SO3(g) ΔH<0是制备硫酸的重要反应,在固定体积的密闭容器中达到平衡时,下列叙述正确的是( )。
A.缩小反应体系的体积,平衡将向气体化学计量数增大的正反应方向移动 B.降低温度将向吸热反应方向即逆反应方向移动 C.平衡时单位时间内生成n mol O2同时消耗2n mol SO2 D.平衡时容器中气体的密度不再发生变化 解析 缩小反应体系的体积,即增大了压强,平衡将向气体化学计量数减小的正反应方向移动,A项错误;降低温度将向放热反应方向移动,B项错误;生成n mol O2同时消耗2n mol SO2是两个反应方向且速率相等,C项正确;反应混合物全部是气体且反应容器的体积不变,则无论是否是平衡状态,气体的密度均不变,D项错误。
2013年高考化学试题分类解析汇编:有机化学1(2013安徽卷)26.(16分)有机物F 是一种新型涂料固化剂,可由下列路线合成(部分反应条件略去):(1)B 的结构简式是 ;E 中含有的官能团名称是 。
(2)由C 和E 合成F 的化学方程式是 。
(3)同时满足下列条件的苯的同分异构体的结构简式是 。
①含有3个双键 ②核磁共振氢谱只显示1个峰 ③不存在甲基(4)乙烯在实验室可由 (填有机物名称)通过 (填反应类型)制备。
(5)下列说法正确的是 。
a . A 属于饱和烃b . D 与乙醛的分子式相同c .E 不能与盐酸反应d . F 可以发生酯化反应2(2013全国新课标卷2)38.[化学——选修5:有机化学基础](15分)化合物Ⅰ(C 11H 12O 3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。
Ⅰ可以用E 和H 在一定条件下合成:已知以下信息:① A 的核磁共振氢谱表明其只有一种化学环境的氢;② RCH=CH 2 RCH 2CH 2OH①B 2H 6②H 2O 2/OH -③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:(1)A的化学名称为_________。
(2)D的结构简式为_________ 。
(3)E的分子式为___________。
(4)F生成G的化学方程式为,该反应类型为__________。
(5)I的结构简式为___________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基;②既能发生银镜反应,又能和饱和NaHCO3溶液反应放出CO2,共有______种(不考虑立体异构)。
J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式。
3(2013天津卷)8、已知水杨酸酯E为紫外吸收剂,可用于配制防晒霜。
2013年安徽高考化学《考试说明》解读安徽省桐城中学高良启一、《考试说明》解读化学:题型示例数量不变涉及知识变化不大今年的化学《考试说明》修改部分关键词是:“微调”,“拓展”,“删次”。
即对部分内容进行微调,拓展了部分知识点,删去了次要笼统的二个要求。
当然,最值得关注的是其中的拓展部分。
今年化学《考试说明》内容上变化较少,在语言组织上更加规范准确。
从变化的内容来看:第一部分:4.物质结构和元素周期律(2)由原来的“了解原子构成。
了解原子序数,核电荷数,质子数,中子数,核外电子数以及它们之间的相互关系”,改为“了解原子序数,核电荷数,质量数,质子数,中子数,核外电子数以及它们之间的相互关系”,增加了“质量数”。
第二部分:(一)《有机化学基础》模块 1.有机化合物的组成与结构(3)“了解确定有机化合物结构的化学方法和某些物理方法(不包括波普方法)”。
改为(3)“了解确定有机化合物结构的化学方法和某些物理方法(如氢谱法)”2.烃及其衍生物性质与应用中删去了(3)“举例说明烃类物质在有机合成和有机化工中的重要作用”。
将“3.氨基酸”的两点要求删去,把“了解氨基酸的组成、结构特点和主要化学性质,以及氨基酸与人体健康的关系”调整到2.烃及其衍生物性质与应用的(4) “了解氨基酸的组成、结构特点和主要化学性质,以及氨基酸与人体健康的关系”。
删去了3.氨基酸(2)了解化学科学在生命科学发展中所起的重要作用;在(二)《物质结构与性质》模块中将(2)“了解电离能的含义,了解同一周期,同一主族中元素电离能的变化规律”改为“了解电离能的含义,了解同一短周期,同一主族中元素第一电离能的变化规律”。
对《考试说明》中变化的部分,我们的理解是:删去的二大点I :第二部分:(一)《有机化学基础》模块2.烃及其衍生物性质与应用(3)“举例说明烃类物质在有机合成和有机化工中的重要作用”II 将《有机化学基础》模块 3.氨基酸”的两个要点删去了(2)了解化学科学在生命科学发展中所起的重要作用,将(1)“了解氨基酸的组成、结构特点和主要化学性质,以及氨基酸与人体健康的关系”调整到2. 烃及其衍生物性质与应用的(4) “了解氨基酸的组成、结构特点和主要化学性质,以及氨基酸与人体健康的关系”,删去的二点,不影响化学学科的内容,相反在语言组织上更加规范准确,更能体现化学主要知识点。
新增的部分是在原有范围内的拓展,没有涉及大的知识点。
如:增加了“质量数”和“了解电离能的含义,了解同一短周期,同一主族中元素第一电离能的变化规律”。
对于新增的“氢谱等”,我们认为只能狭义理解,千万不要随意联想,推广到与“氢谱”有联系的“红外光谱”“质谱”。
从题型示例看:题型和数量不变,只是对应互换,更换了八道题目,例题涉及的内容基本不变。
考纲无论怎样改变,“双基”的考查总是必要的。
基础知识和基本技能是知识与技能、过程与方法、情感态度与价值观等三维目标的载体。
由于试卷中涉及的学科知识内容远比单科试卷中少,这就为命题内容的选择提供了较大的空间和自由度。
题量少,知识覆盖面低,因此命题就会在注重“双基”的同时,更加突出主干知识的考查。
估计今年会在保持稳定的基础上控制难度,题型不会有大的变动;但会更加注重能力的考查;以“对自然界、社会、生产、生活中的化学现象”和“重视理论联系实际,关注与化学相关的科学技术,社会经济和生态环境的协调发展”为背景的试题,更受青睐;以“能够通过对实际事物,实验现象,实物,模型,图形,图表的观察”为依托的试题应该值得关注。
我们应该清楚地看到,26个选择题中更换了6题,27——40大题只更换了2题,这充分说明,去年的高考后面的主观题是经得住高考的检验,是很成功的模式,40题示例中有24处出现了图形和图表,特别是更换的二大题中都有图表。
我们猜测,新增的“氢谱”可能在有机化学大题中的一个小问,值得关注的是今年是“Grignard试剂”获得诺贝尔奖100周年,有机化学可以以信息的形式出现。
二近三年安徽理综卷对比分析2. .2010、2011、2012年安徽化学卷考点在教材中分布统计对比三、2014届高三化学复习建议1.加强集体备课这是各地成功的经验,更是我校历年高考制胜的做法。
我校高三备课组老师有八人,传统的桐城中学教风让我们养成了集体备课的习惯。
每年高三一开学,备考组长就要带领老师研究考纲,考纲是权威、准确的信息源,在宏观上指引复习的方向。
因此,在以后的复习中我们要经常研究考纲,准确的把握考纲。
在上课时必须以考纲为基本框架,以课本为基础,对课本知识进行再认识,力争让学生形成对知识理解上的升华。
结合课本梳理考纲中的知识点,把握复习的重点和方向,注重夯实学生的基础。
我们集体备课的时间和形式都比较多,也比较灵活。
除了按时做好规定的集体备课之外,平时遇到什么问题,随时研讨解决,绝不拖拉,我们坚持,“吃透教材,吃透考纲,吃透热点,吃透高考试题,吃透学情,吃透学生,”在研究近几年高考试题的基础上,充分把握教材,了解学生,在集体备课时,先把教材的地位和考点以及新热点,由主背人先介绍一下,然后研究本节的重点、难点,确定讲课的内容和训练的题目。
最后,在根据自己班级的情况,进行二次备课。
2. 立足学科基础、打造高效课堂课堂学习,是学生获得知识和培养能力的主渠道,我们要想让学生取得理想的成绩,而且不加重学生学习的负担,提高课堂效率,是我们最重要也是我们唯一的途径,我们深知效率出在课堂上,功夫下在备课上,在做好备课的基础上,鉴于我校的实际,我们对于课堂教学的要求是:“一高、二多、三精”,一高就是起点要稍高,我校的学生基础相对较高,自学能力比较强,绝大多数都能考上二本,要求我们在备课和教学中,要适当提高起点;二多就是让学生多动脑,多动手,把学生的主动性调动起来,让他们积极的参与到学习中来,提高学习效率;三精就是精选、精讲、精练,也就是精选一道例题,带会一类题目,精讲一堂课,带动一节课,精练一套题,带会一章内容。
通过这样的工作,打造高效课堂,提高课堂效率,减轻学生负担,推动学生向大学一步步的迈进。
对基础知识、基本技能和基本方法的考查,是高考永恒的主题。
突出主干知识的复习显得尤为必要。
化学第一轮复习是对学科基础知识的全面复习和整理,一轮复习应当注重夯实基础,滚动提高。
引导学生把握学科基本知识的内在联系,建立学科知识网络,并通过知识的回顾、整理、应用、拓宽,进行知识之间的相互渗透。
如在复习元素及其化合物时,要把其纳入基础理论的框架内。
使零散的知识系统化,同时也为基础理论、基本概念部分的复习注入了丰富的内容,使二者有机地结合起来。
一轮复习内容要细致全面,即要达到在知识上不留死角的目的。
同时要加强变知识点复习为考点复习的研究,高考化学总复习知识点有一百多个,而化学考试热点只有近30个,其中有近二十个考点重现率特别高。
在综合考试中,化学试题题量较小,所考的必然侧重于考试的重点和热点,根据考点来组织化学高考复习,可以缩短复习周期,提高针对性和实效性。
复习中要舍得在难点、重点问题上花时间、下功夫。
复习中穿插进行专题训练和滚动综合训练,针对高考的重点和热点,主要以知识点和以解题方法为线索,注重知识和方法的综合运用。
第二轮复习需要注重提高思维能力,关注过程与方法。
建构化学学科系统,深刻把握“化学平衡”“物质结构决定性质”等学科思想以及元素观、微粒观、转化观、分类观等基本观点。
同时根据理科综合能力测试试卷特点,建立科学、合理的训练方案。
理科综合能力测试卷的题量适中,阅读量较大。
我们应在二轮复习中穿插进行针对性的训练,练做题的速度、练表达的准确性、练解答技巧和取舍决断。
3 .注重思维能力和科学素养培养和提高高三复习要注意学生的思维能力培养和提高。
引导培养学生观察、比较、分析、归纳等能力,适度进行较高要求的思维训练。
可以将工业品的制备、化学反应中的热效应、生产中使用某些化学物质的目的等内容为背景融合在一起。
培养学生通过分析处理题给信息,并综合运用所学化学知识解决相关生产实际问题的能力。
可以参照今年高考理综化学试题的命题特点,编写的训练题要求学生真正理解基础知识,对已有知识具有创新和迁移能力,并且拥有灵活开放的解题思路。
建立起基本的科学观念,这些观念的形成又离不开对核心知识的正确理解。
通过化学学科的学习,能有效地解决日常生活中所遇到的与化学相关的问题,知道如何获取信息,并且在需要时能进行科学的决策。
在复习教学中,注意引导学生关心自然、社会、科技以及生产、生活中的化学问题,了解化学学科研究的最新成果,帮助学生学会运用已有知识对现实问题进行初步研究,使他们逐步形成对社会、对自然的正确的情感、态度和价值观,注重培养学生科学素养、创新精神和运用所学知识综合解决实际问题的能力。
化学实验是化学学习的重要方面,对训练学生的科学素养也十分重要。
从2011安徽高考理综化学题来看,探究实验的考查在高考化学卷中所占比例也相当大。
探究学习是新课改理念下倡导的最重要学习方式之一,复习教学中,用心设计引发学生思考与探究是非常关键的,是提高学生学科能力的核心。
可以通过对一些典型问题的探究,配以拓展训练,提高学生思维的灵活性、变通性、整体性,帮助学生将知识转化为能力,将解法提炼为技巧,从而真正提高学生整合信息、分析问题和解决问题的能力。
4、关注化学用语,减少低级失误元素的名称或符号、化学式、电子式、原子结构示意图、结构式、结构简式、反应方程式(主要有化学方程式,热化学方程式、电极反应方程式、离子方程式等)等化学用语是学习化学的工具,它们的含义及规范书写是化学学科素养的重要组成部分,也是高考重点考查的内容之一。
2011年高考理综卷化学试题最为抢眼的一点仍是高度关注化学用语的考查,特别突出语言文字表达能力的考查,多处出现要求直接书写化学式、电子排布式、结构简式。
第二卷中要求书写反应方程式多处,特别是实验探究题考查了学生用语言文字对实验结论进行分析和评价。
但往往存在考生在考试中解决问题的过程和方法正确,但化学用语使用错误或文字表达错误而失分,十分痛心,这就要求后期老师和学生引起高度重视。
要求学生基础扎实、知识全面、文字表达能力强,化学用语规范,做题思维严谨、准确、切中要害。
2013-6-14。