铜绿假单胞菌检验原始记录Microsoft Word 文档
- 格式:doc
- 大小:54.00 KB
- 文档页数:1
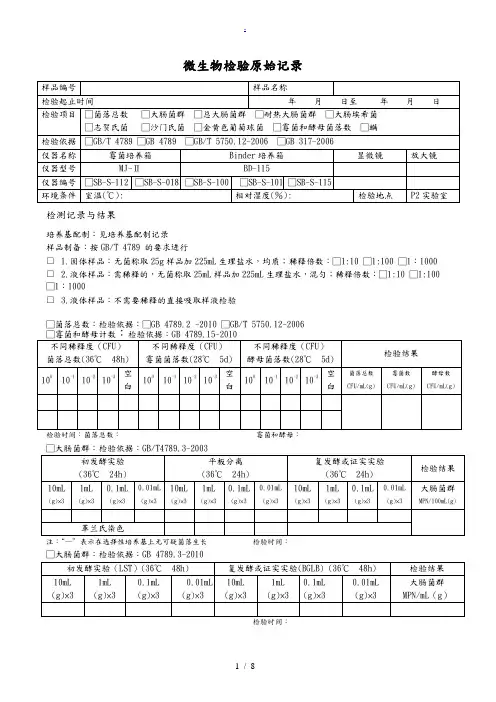
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。




铜绿假单胞菌的菌种鉴定全文共四篇示例,供读者参考第一篇示例:铜绿假单胞菌(Pseudomonas aeruginosa)是一种常见的革兰氏阴性细菌,属于假单胞菌属(Pseudomonas),广泛存在于自然界中,是一种耐受力很强的细菌。
铜绿假单胞菌在人类和动植物体内都有可能成为病原菌,引起多种感染疾病,如呼吸道感染、尿路感染、皮肤感染等。
对铜绿假单胞菌的菌种鉴定十分重要。
铜绿假单胞菌的菌种鉴定主要包括形态学观察、生理生化特性检测、分子生物学方法等。
形态学观察是最为简单直观的方法,通过观察细菌在琼脂培养基上的形态特征来初步鉴定。
铜绿假单胞菌在琼脂培养基上形成典型的青绿色凝块状菌落,通常呈金黄色至淡黄色,具有辛辣气味。
除了形态学观察外,生理生化特性检测也是菌种鉴定的重要方法之一。
铜绿假单胞菌具有一系列特殊的生理生化特性,如利用氧化物作为唯一氧化剂和膜脂组成特殊等。
铜绿假单胞菌产生溶血素、胞外聚合物酶、脂肪酶等多种外源酶,可以降解寡糖、脂质等物质。
分子生物学方法也成为现代菌种鉴定的重要手段。
通过PCR扩增和测序技术,可以对靶基因进行测序分析,比如16S rRNA基因序列分析。
铜绿假单胞菌16S rRNA序列具有较高的保守性,同时又有足够的变异性,能够帮助界定种和属的分类关系。
在进行铜绿假单胞菌菌种鉴定的过程中,需特别注意以下几点:1. 选择合适的菌落:铜绿假单胞菌菌落为青绿色,有金黄色至淡黄色的边缘。
需避免选择其他青绿假单胞菌属菌种带来的干扰。
2. 确认生理生化特性:对于一些特殊的生理生化特性,如氧化物利用情况、酶产生等,可以通过专门的生化试验进行验证。
3. 结合分子生物学方法:如果需要进一步确定菌种的归属,可结合分子生物学方法进行16S rRNA序列分析,加深对菌种的认识。
铜绿假单胞菌的菌种鉴定是一项重要且复杂的工作,需要结合形态学观察、生理生化特性检测和分子生物学方法等多种手段进行综合分析。
只有准确鉴定出铜绿假单胞菌的菌种,才能更好地开展相关的医学、环境等研究工作,为防治相关感染病害提供科学依据。

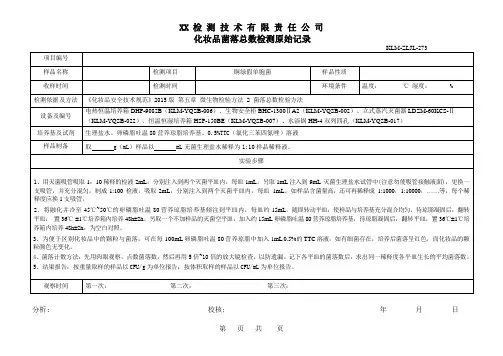

微生物限度检验记录一、检验目的:确认产品是否满足微生物限度要求,保证产品的安全性和质量。
二、检验项目:1.总大肠菌群:用于评估产品是否受到粪便污染。
2.霉菌和酵母菌:用于评估产品是否受到霉菌和酵母菌的污染。
3.沙门氏菌:用于评估产品是否受到沙门氏菌的污染,沙门氏菌是一种常见的食源性病原菌。
4.铜绿假单胞菌:用于评估产品是否受到铜绿假单胞菌的污染,铜绿假单胞菌是一种常见的致病菌。
5.谷氨酰胺酶阳性菌:用于评估产品是否受到谷氨酰胺酶阳性菌的污染,谷氨酰胺酶阳性菌是一种常见的致病菌。
三、检验步骤:1.样品准备:从产品中取得一定量的样品,确保样品的代表性。
2.样品处理:根据产品的不同特性,选择适当的方法进行样品处理,如水解、稀释等。
3.培养基制备:根据所需的检验项目,制备相应的培养基。
4.培养基接种:将处理后的样品接种到相应的培养基中,利用无菌技术确保操作的无菌。
5.培养:将接种过的培养基培养在适宜的温度和湿度条件下,培养一定的时间,一般为24-72小时。
6.检查结果:观察培养基上是否有菌落形成,记录菌落的数量和形态特征。
7.鉴定:对培养出的菌落进行进一步的鉴定,如形态学观察、生理生化特性测试等。
8.统计和分析:根据检查结果,统计并分析微生物的数量,计算出产品的微生物限度。
四、检验结果:1.总大肠菌群:每克不超过100个。
2.霉菌和酵母菌:每克不超过10个。
3.沙门氏菌:每克不得检出。
4.铜绿假单胞菌:每克不得检出。
5.谷氨酰胺酶阳性菌:每克不得检出。
五、检验记录样例:日期:2024年4月1日样品名称:XXX产品检验员:XXX检验项目:1.总大肠菌群结果:每克10个,符合微生物限度要求。
2.霉菌和酵母菌结果:每克2个,符合微生物限度要求。
3.沙门氏菌结果:未检出,符合微生物限度要求。
4.铜绿假单胞菌结果:未检出,符合微生物限度要求。
5.谷氨酰胺酶阳性菌结果:未检出,符合微生物限度要求。
六、结论:根据检验结果,XXX产品符合微生物限度要求,产品安全可靠。

菌落总数与大肠菌群检验原始记录
共页第页
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
共页第页
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
培养温度:28±1℃培养时间:年月日时 --- 年月日时:
菌落计数:
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。

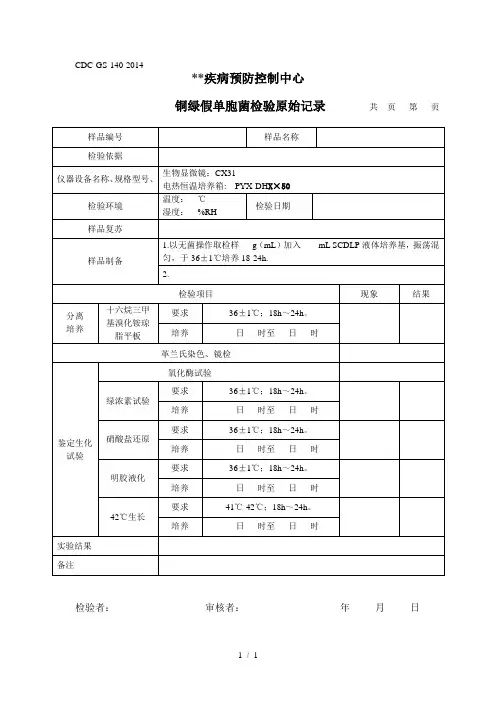
南昌市疾病预防控制中心NCCDC(原)-010-03
矿泉水微生物检验原始记录
共页第页样品编号样品名称
收样日期年月日检测环境温度℃;湿度%RH
检验日期年月日样品状态□正常□异常
检验项目□大肠菌群□粪链球菌□铜绿假单胞菌□产气荚膜梭菌
检测方法□GB/T8538—2008
检验仪器□GNP-9270A型隔水式电热恒温培养箱(NCCDC-SB-644)□BUGBOX厌氧培养箱(NCCDC-SB-515)
培养基
(批号)
□KF()□CN()□SPS()□BGB()
结果记录
大肠菌群(多管发酵法)
接种量(ml)10ml×5 1ml×5 0.1ml×5
检验结果
(MPN/100ml) 乳糖胆盐发酵阳性管数
(36±1℃,24h)
BGB培养
(36±1℃,48h)
粪链球菌250ml水样用孔径为0.45um
滤膜过滤,将滤膜贴于KF平板,
培养36±1℃,48h
生长情况:G染色: BHIM斜面: H2O2试验:CFU/250ml
铜绿假单
胞菌250ml水样用孔径为0.45um
滤膜过滤,将滤膜贴于CN平
板,培养36±1℃,48h
生长情况:乙酰胺: 氧化酶:金氏B培养
基上产生荧
光:
CFU/250ml
产气荚膜
梭菌50ml水样用孔径为0.22um
滤膜过滤,将滤膜贴于SPS平
板,厌氧培养36±1℃,24h
生长情况:FT:
G染色:
动力-硝酸盐
含铁牛奶:
卵黄琼脂:CFU/50ml
检验者:复核者:检毕日期:年月日。
保健用品微生物检验方法 第3部分:铜绿假单胞菌测定警示——使用本标准的人员应有正规实验室工作的实践经验。
本标准并未指出所有可能的安全问题。
使用者有责任采取适当的安全和健康措施,并保证符合国家有关法规规定的条件。
1 范围本标准规定了保健用品中微生物中铜绿假单胞菌的测定方法。
本标准适用于生产和经营的保健用品中的铜绿假单胞菌测定。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 6682 分析实验室用水规格和试验方法GB 19489 实验室生物安全通用要求3 术语和定义下列术语和定义适用于本文件。
3.1铜绿假单胞菌 Pseudomonas aeruginosa属于假单胞菌属,为革兰氏阴性杆菌,氧化酶阳性,能产生绿脓菌素。
此外还能液化明胶,还原硝酸盐为亚硝酸盐,在42 ℃±1 ℃条件下能生长。
4 试剂和材料除另有规定外,所有试剂均为分析纯 。
实验用水符合GB/T 6682中二级水的要求。
4.1 灭菌生理盐水:详见附录A.1。
4.2 灭菌液体石蜡:详见附录A.2。
4.3 灭菌吐温-80:详见附录A.3。
4.4 SCDLP:详见附录A.4。
4.5 十六烷基三甲基溴化铵:详见附录A.5。
4.6 乙酰胺:详见附录A.6。
4.7 革兰氏染液:详见附录A.7。
4.8 绿脓菌素测定培养基:详见附录A.8。
4.9 硝酸盐蛋白胨水:详见附录A.9。
4.10 明胶液化培养基:详见附录A.10。
5 仪器和设备5.1 天平:感量0.1 g。
5.2 灭菌刻度吸管:10 mL、5 mL、1 mL。
5.3 高压灭菌器。
5.4 量筒:100 mL、200 mL、2000 mL。
5.5 恒温水浴箱或隔水式恒温箱:44.5 ℃±0.5 ℃。
5.6 无菌锥形瓶:100 mL、200 mL、250 mL、2000 mL。
GB 8538—2016铜绿假单胞菌方法学验证报告一、验证目的验证《食品安全国家标准饮用天然矿泉水检验法GB 8538-2016》-铜绿假单胞菌检验在本实验室的适用性。
二、验证方法样品采样方案依据GB4789.1-2016 《食品微生物学检验总则》的要求进行,本实验样品取三个不同品牌的饮用天然矿泉水的典型样品进行实验,严格按照GB8538-2016进行。
除上述实验程序外,为保证本次验证的科学性和准确性,本次实验添加阳性对照组,对照组由标准菌株铜绿假单胞菌(CMCC(B)10104)接种培养而成,与样品实验程序同时进行。
三、验证设备和试剂1.冰箱:SC-322 青岛海尔电器2.生化培养箱:SPX-150B-Z 上海博迅实业3.电位pH计:PHS-3C+(精确度0.01)成都世纪方舟科技有限公司4.恒温振荡器:SHA-A 江苏金坛环宇科学仪器厂5.菌落计数仪:Scan-500 北京五洲东方科技发展有限公司6.天平:JE-502 上海浦春计量仪器有限公司7.六联不锈钢过滤器北京中兴伟业仪器有限公司8.三用紫外分析仪:ZF-2 上海安亭电子仪器厂培养基和试剂:1.假单胞菌琼脂基础培养基北京陆桥技术股份有限公司2.绿脓菌素测定用培养基北京陆桥技术股份有限公司3.金氏B培养基北京陆桥技术股份有限公司4.营养琼脂北京陆桥技术股份有限公司5.氧化酶试剂北京陆桥技术股份有限公司6.乙酰胺肉汤北京陆桥技术股份有限公司7.三氯甲烷国药集团有限公司8.纳氏试剂北京陆桥技术股份有限公司四、验证环境1.依据《消毒与灭菌效果的评价方法与标准GB15981-1995》定期对高压蒸汽灭菌锅的灭菌效果进行检测评价并记录;2.依据《无菌室消毒灭菌操作规程》定期对对无菌室、生物安全柜进行清洁消毒灭菌并记录;3.依据《实验室质量控制规范食品微生物检测GB/T27405-2008》定期对对无菌室及生物安全柜进行沉降菌检测并记录;4.无菌室检验:详见《XXXX》;五、验证步骤1.操作步骤1. 1水样过滤在100级的洁净工作台进行过滤操作。
表面微生物检测原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:□菌落总数□金黄色葡萄球菌检测依据:□β型溶血性链球菌□铜绿假单胞菌采样方法:用5cm×5cm的标准规格板,放在被检物体表面,将浸有无菌生理盐水采样液的棉拭子1支于规格板内往返各涂抹5次,并随之转动棉拭子,根据物体表面大小,采平行样1~4个,剪去手接触部分,将棉拭子放入装有10ml采样液的试管中,待检。
人员手采样:被检人五指并拢,将浸有无菌生理盐水采样液的棉拭子一支在右手指曲面,从指跟到指端来回涂擦2次,并随之转动棉拭子,剪去手接触部分,将棉拭子放入装有10ml 采样液的试管中送检。
一、菌落总数检查:将装有10ml棉拭子的采样液振摇后,然后取样液2ml注入2个平皿,每皿1ml。
用营养琼脂倾注平皿,每皿约15ml。
待凝固后置37℃培养48小时。
结果:表面微生物菌落总数(CFU/cm2)=平均菌数×稀释倍数/采样面积人员手菌落总数(CFU/手)=平均菌数×稀释倍数电子天平编号:使用状况试验前:试验后:培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:二、β型溶血性链球菌:注:+生长或有可疑菌落;-未生长或无可疑菌落。
电子天平编号:使用状况试验前:试验后:培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:注:+生长或有可疑菌落;-未生长或无可疑菌落;G-b革兰氏阴性杆菌;G+b革兰氏阳性杆菌;G+c革兰氏阳性球菌电子天平编号:使用状况试验前:试验后:培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:四、金黄色葡萄球菌注:+生长或有可疑菌落;-未生长或无可疑菌落;G-b革兰氏阴性杆菌;G+b革兰氏阳性杆菌;G+c革兰氏阳性球菌电子天平编号:使用状况试验前:试验后:培养箱编号:使用状况试验前:试验后:检测人:校核人:审核人:。
铜绿假单胞菌的临床分离和药敏情况分析目的分析铜绿假单胞菌的临床分离和药敏情况,指导临床合理使用抗生素。
方法对本院2016年1月~2017年10月临床分离的524株铜绿假单胞菌采用统一的方法、设备和判断标准进行耐药性检测,使用WHONET5.6进行数据分析。
结果铜绿假单胞菌耐药率在50%以上的抗生素包括复方新诺明、阿莫西林/克拉维酸、氯霉素、头孢噻肟、四环素、氨苄西林、呋喃妥因和头孢唑啉,敏感性高于70%的抗生素包括头孢他啶、哌拉西林、左旋氧氟沙星、头孢吡肟、美洛培南、环丙沙星、亚胺培南、哌拉西林/他唑巴坦、庆大霉素、阿米卡星和多粘菌素B。
结论铜绿假单胞菌的耐药机制复杂,应加强对铜绿假单胞菌的临床分布及耐药性监测,指导临床合理使用抗生素,采取有效的防范措施控制医院感染,采取多种治疗策略最大限度减少铜绿假单胞菌耐药性发展。
[Abstract] Objective To analyze the clinical isolation and drug susceptibility of Pseudomonas aeruginosa and to guide the rational use of antibiotics in clinic. Methods A total of 524 strains of pseudomonas aeruginosa clinically isolated from January 2016 to October 2017 in our hospital were tested for drug resistance using a uniform method,equipment and judgment criteria. And data analysis was performed using WHONET 5.6. Results Antibiotics with pseudomonas aeruginosa drug resistance rate above 50% included cotrimoxazole,amoxicillin/clavulanic acid,chloramphenicol,cefotaxime,tetracycline,ampicillin,nitrofurantoin and cefazolin. Antibiotics with sensitivity greater than 70% included ceftazidime,piperacillin,levofloxacin,cefepime,meropenem,ciprofloxacin,imipenem,piperacillin/tazobactam,gentamicin,amikacin and polymyxin B. Conclusion The mechanisms of drug resistance monitoring of pseudomonas aeruginosa are complicated. The clinical distribution and drug resistance of Pseudomonas aeruginosa should be strengthened to guide the rational use of antibiotics in clinic. Effective preventive measures should be taken to control nosocomial infections and various treatment strategies should be taken to minimize the development of pseudomonas aeruginosa drug resistance.[Key words] Pseudomonas aeruginosa;Drug-resistance;Antibiotics;Meropenem銅绿假单胞菌在自然界分布广泛,是土壤中存在的最常见的细菌之一,在水、空气、正常人的皮肤、呼吸道和肠道等都有本菌存在,该菌存在的重要条件是潮湿的环境,本菌为条件致病菌,是医院内感染的主要病原菌之一。