抗血小板药物的作用机理及临床应用
- 格式:ppt
- 大小:3.48 MB
- 文档页数:71

抗血小板药物在肿瘤临床治疗中的作用及其研究进展
抗血小板药物可通过干扰肿瘤相关的血小板活化、聚集等生理过程,从而起到肿瘤防治作用。
目前,已有不少研究发现,抗血小板药物的应用可延缓癌症患者术后复发的时间,同时也能帮助肿瘤患者减轻疾病相关的症状。
一些研究发现,抗血小板药物还能通过抑制血小板相关的血管生成因子的释放,从而参与肿瘤的血管生成和生长途径的调控。
此外,同样有研究发现,抗血小板药物的应用并不能显著地提高肿瘤患者的生存率,这一结论与其他研究结果存在差异,其原因目前还需进一步探究。
首先,抗血小板药物在肿瘤治疗中的作用机制仍有待进一步深化理解,这一问题的解决将有助于制定更加有效的治疗方案。
其次,由于抗血小板药物的应用与肿瘤的种类、临床阶段等因素关系密切,故而药物的选择和使用需要精确判断。
随着基因检测技术的进步,抗血小板药物也可以实现个体化精准治疗。

抗⾎⼩板药的临床应⽤抗⾎⼩板药的临床应⽤⼀、动脉⾎栓形成的危害性动脉⾎栓形成主要发⽣在动脉粥样硬化的基础上,动脉⾎管⾎栓形成在临床上可导致⼼绞痛、⼼肌梗死、缺⾎性脑卒中和周围⾎管闭塞症等常见多发病。
⼼脑⾎管栓塞是常见的病死原因,在我国⼈⼝的死因中约占半数。
⼆、⾎⼩板激活和动脉⾎栓形成⾎⼩板是由巨核细胞⽣成的⾎液中3种有形成分之⼀。
⾎⼩板在初期⽌⾎作⽤中占有重要地位。
正常⾎管内⽪细胞有抗⾎栓形成作⽤,⾎管受损破裂后⾎⼩板可黏附聚集于⾎管裂⼝处,形成⽌⾎栓⼦⽽达到初期⽌⾎。
在动脉粥样硬化时,由于斑块破溃从⽽激活⾎⼩板,⾎⼩板在破溃处黏附、聚集,并可黏附⽩细胞形成⽩⾊⾎栓。
因此,⽩⾊⾎栓和⽌⾎栓⼦的形成机制是相似的,不同之处是⽩⾊⾎栓发⽣于内⽪受损但⾎管未破裂,⽽⽌⾎栓⼦是形成于⾎管裂⼝处。
⾎⼩板黏附是通过其膜糖蛋⽩Ⅰb与⾎管性⾎友病因⼦(vWF)结合,进⽽与内⽪下组织结合⽽发⽣的。
激活的⾎⼩板膜糖蛋⽩IIb和IIIa形成复合体,通过纤维蛋⽩原与另⼀⾎⼩板的膜糖蛋⽩IIb/IIIa 复合体结合⽽出现⾎⼩板聚集体。
激活的⾎⼩板还释放多种活性物质,如ADP,TXA2,PF3等,可促进聚集体进⼀步发展,增⼤并且为凝⾎过程提供反应平台。
粥样硬化斑块和⽩⾊⾎栓使⾎管腔狭窄并影响⾎流,从⽽在局部可使⽣成的凝⾎酶积蓄达到有效浓度,使纤维蛋⽩原转变为纤维蛋⽩,并⽹络红细胞等形成红⾊⾎栓。
因此,动脉⾎栓的结构特点是⽩⾊⾎栓的头部和红⾊⾎栓的尾部。
从动脉⾎栓的形成过程可见,⾎⼩板的激活是动脉⾎栓形成的始动物,若能控制⾎⼩板不被激活即可阻⽌或延缓动脉⾎栓的形成。
三、抗⾎⼩板药的作⽤机制60年代初发现⼆磷酸腺苷(ADP)可以引起⾎⼩板聚集,因此建⽴了⽐浊法测定⾎⼩板聚集性,为体外分析⾎⼩板功能开辟了新途径。
当时,发现了不少可以促进⾎⼩板聚集的物质,如肾上腺素、凝⾎酶、⾎清素(5羟⾊胺)和胶原等。
随后,由于分⼦⽣物学、分⼦免疫学的发展,对⾎⼩板黏附聚集机制有了深⼊的了解。


抗血小板药物在肿瘤临床治疗中的作用及其研究进展
随着肿瘤治疗技术的不断发展,抗血小板药物在肿瘤临床治疗中的作用受到了越来越多的关注。
血小板在肿瘤发生和发展过程中扮演着重要角色,因此影响血小板功能的药物成为了肿瘤治疗领域的研究热点之一。
本文将就抗血小板药物在肿瘤临床治疗中的作用及其研究进展进行介绍。
一、抗血小板药物在肿瘤临床治疗中的作用
1. 抑制肿瘤转移和侵袭:肿瘤细胞转移和侵袭是肿瘤发展的重要环节,而血小板对肿瘤细胞的转移和侵袭起着重要作用。
抗血小板药物的使用可以有效的抑制肿瘤细胞的转移和侵袭,从而延缓肿瘤的发展。
2. 增强肿瘤放疗和化疗效果:研究表明,抗血小板药物可以增强肿瘤放疗和化疗的疗效。
由于肿瘤组织内血管的异常增生和血小板的异常聚集,使得肿瘤组织的血液灌注不足,从而导致放疗和化疗药物难以有效的到达肿瘤组织。
而抗血小板药物可以通过抑制血小板的聚集和血管生成,从而增加肿瘤组织的血液供应,增强放疗和化疗的疗效。
3. 减轻肿瘤相关的血栓并发症:肿瘤患者常常伴有血栓形成的并发症,而血小板在血栓形成过程中起着重要作用。
抗血小板药物可以有效的减轻肿瘤患者的血栓并发症,改善患者的生存质量。
二、抗血小板药物在肿瘤临床治疗中的研究进展
1. 抗血小板药物与肿瘤微环境的关系:近年来的研究发现,血小板在肿瘤微环境的形成和发展中起着关键作用。
抗血小板药物可以通过影响肿瘤微环境的形成,从而抑制肿瘤的发展。
研究抗血小板药物与肿瘤微环境的关系对于肿瘤治疗具有重要的意义。
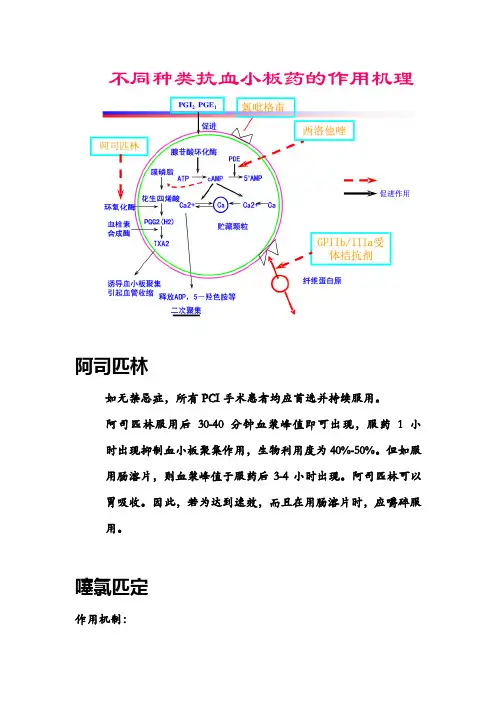
阿司匹林如无禁忌症,所有PCI手术患者均应首选并持续服用。
阿司匹林服用后30-40分钟血浆峰值即可出现,服药1小时出现抑制血小板聚集作用,生物利用度为40%-50%。
但如服用肠溶片,则血浆峰值于服药后3-4小时出现。
阿司匹林可以胃吸收。
因此,若为达到速效,而且在用肠溶片时,应嚼碎服用。
噻氯匹定作用机制:1、选择性地与血小板表面ADP受体P2Y12结合,而不可逆地抑制由胶原和凝血酶诱导的血小板聚集。
2、抑制由胶原和凝血酶诱导的血小板聚集。
临床评价:A 抗血小板作用等于或略大于阿司匹林;B 起效慢, 偶可引起粒细胞减少和血栓性血小板减少性紫癜(TIP)等严重不良反应。
其适应证和阿司匹林相似。
噻氯匹啶剂量为250mg,每日1次或2次。
由于它可抑制骨髓,引起中性粒细胞减少等,因此逐渐被氯吡格雷代替。
后者一般先采用300-600mg负荷剂量,然后每日75mg。
氯吡格雷的抗血小板作用呈现量效关系,在不同个体中有明显差异。
氯吡格雷300mg vs 600mg vs 900mg氯吡格雷对ADP诱导的最大血小板聚集率的影响:600mg优于300mg,但900mg与600mg相似。
目前不支持对稳定型心绞痛患者联合应用氯吡格雷和阿司匹林,通常在冠状动脉支架术后或急性冠脉综合征初期内联合应用。
血小板GPⅡb/Ⅲa受体拮抗剂单克隆抗体:ReoPro (abciximab 阿昔单抗)肽类:KGD环肽Integrelin(eptifibatide,依替非巴肽)非肽类衍生物:Tirofiban(替罗非班)作用机制阻断或妨碍血小板GPⅡb/Ⅲa受体与纤维蛋白原等配体的特异性结合,有效的抑制各种血小板激活剂诱导的血小板聚集,防止血栓形成,从而达到抗血栓的目的。
临床评价:直接抑制血栓形成的关键和唯一通路,作用最强,最直接[糖蛋白Ⅱb /Ⅲa是血小板聚集的最后的共同途径,因此糖蛋白Ⅱb / Ⅲa拮抗剂是最强的抗血小板药]。
GPⅡb/Ⅲa受体拮抗剂共识1.能使PCI术后急性缺血事件的发生率下降15%-50%,急性事件包括急性心梗,死亡,紧急血管重建术等。




抗血小板药适应症及使用说明抗血小板药物是一类常用于预防和治疗血液循环系统疾病的药物,其主要作用是抑制血小板的聚集和凝集,进而减少血栓形成的风险。
在临床上,抗血小板药物广泛应用于心脑血管疾病的治疗和预防,如冠心病、脑血栓等疾病。
在本文中,我们将介绍抗血小板药物的适应症及使用说明,以帮助读者更好地了解和正确使用这类药物。
一、抗血小板药物的适应症1. 预防心肌梗死和心血管死亡:抗血小板药物如阿司匹林广泛用于冠心病患者,可减少心肌梗死和心血管死亡的风险。
2. 预防脑血栓形成:对于有缺血性脑卒中病史的患者,抗血小板药物的使用能够减少脑血栓形成的风险。
3. 预防血栓性静脉炎和静脉血栓栓塞:抗血小板药物可用于减少手术后和长期卧床患者出现血栓形成的可能性。
4. 预防带原者心绞痛:某些患者在运动或其他诱发因素下出现心绞痛,使用抗血小板药物可减轻症状并预防心肌梗死。
5. 防治外周动脉疾病:使用抗血小板药物可预防外周动脉疾病患者下肢缺血和静脉炎症的发生。
二、抗血小板药物的使用说明1. 用药方法:抗血小板药物通常以口服形式使用,可根据医嘱每日一次或两次。
有些药物需特殊剂型如咀嚼片或肠溶片,须根据药品说明书正确使用。
2. 用量选择:具体用量应根据患者的病情、年龄、体重和合并症等因素进行调整。
一般而言,常用的阿司匹林剂量为75-300毫克/日。
3. 注意禁忌症:抗血小板药物存在一些禁忌症,如严重肝肾功能不全、溃疡病或出血性疾病、妊娠和哺乳期等,患者应谨慎使用或避免使用。
4. 注意副作用:使用抗血小板药物可能会引起一些不良反应,如胃肠道不适、出血倾向、头痛等。
患者在用药期间应密切关注自身反应,如出现异常情况应及时就医。
5. 贯彻医嘱:患者在使用抗血小板药物时必须严格按照医嘱进行用药,不可随意增减用药剂量或停药。
如有要求更改用药方案,应及时咨询医生并遵循专业建议。
6. 药物相互作用:抗血小板药物与其他药物可能存在相互作用,如华法林、非甾体抗炎药等。


抗血小板药物在肿瘤临床治疗中的作用及其研究进展肿瘤是威胁全球人类健康的严重疾病之一,然而在肿瘤的治疗中,除了化疗、放疗和手术等传统治疗手段外,抗血小板药物也在肿瘤治疗中发挥着重要作用。
近年来,随着肿瘤治疗领域的不断深入研究,抗血小板药物在肿瘤治疗中的作用逐渐被重视。
本文将就抗血小板药物在肿瘤临床治疗中的作用及其研究进展进行探讨。
一、抗血小板药物在肿瘤治疗中的作用抗血小板药物主要通过抑制血小板功能,阻止血小板粘附和凝聚,从而起到抗凝血、抗血栓作用。
而在肿瘤治疗中,抗血小板药物也展现出了一些独特的作用。
1. 抑制肿瘤生长和扩散研究表明,血小板与肿瘤细胞具有密切的关联,血小板释放的生长因子和细胞因子可以促进肿瘤细胞的增殖和扩散。
而抗血小板药物的使用可以抑制血小板的功能,从而减少这些促进因子的释放,抑制肿瘤细胞的生长和扩散。
2. 增强放疗和化疗的疗效研究发现,抗血小板药物可以增加放疗和化疗对肿瘤的疗效。
一方面,抗血小板药物可以减少肿瘤细胞的血供,使肿瘤细胞更加容易受到放化疗的影响;抗血小板药物还可以通过调节肿瘤微环境,增强肿瘤对放化疗的敏感性。
3. 减少肿瘤转移和复发血小板在肿瘤的转移和复发过程中也发挥着重要作用,抗血小板药物的使用可以减少血小板对肿瘤细胞的促进作用,从而减少肿瘤的转移和复发。
二、抗血小板药物在肿瘤治疗中的研究进展随着对抗血小板药物在肿瘤治疗中作用的深入研究,相关领域的研究也在不断取得进展。
1. 抗血小板药物在肿瘤治疗中的临床应用目前,抗血小板药物已经在一些肿瘤的临床治疗中得到应用,例如在结直肠癌、胃癌和乳腺癌等肿瘤的治疗中,抗血小板药物的使用已经得到了一定的认可。
而随着对抗血小板药物作用机制的不断深入与了解,相信在未来会有更多的肿瘤可以受益于抗血小板药物的治疗。
2. 抗血小板药物与肿瘤免疫治疗的结合应用近年来,肿瘤免疫治疗成为了肿瘤治疗的新希望,而抗血小板药物与肿瘤免疫治疗的结合应用也成为了研究的热点之一。
抗血小板药物在肿瘤临床治疗中的作用及其研究进展一、抗血小板药物的作用机制抗血小板药物主要通过抑制血小板的功能和数量,从而影响凝血系统,发挥其治疗作用。
目前常用的抗血小板药物主要包括阿司匹林、氯吡格雷、替格瑞洛等。
这些药物通过不同的机制干预血小板的凝血功能,从而抑制肿瘤的生长和转移。
二、抗血小板药物在肿瘤治疗中的作用1. 抗血小板药物对肿瘤生长的抑制作用研究表明,血小板在肿瘤的生长和转移过程中起着重要的作用。
抗血小板药物可以通过抑制血小板的凝血功能,干扰肿瘤的血液供应,从而阻断肿瘤的生长和扩散。
抗血小板药物还可以影响肿瘤细胞的黏附和迁移,进而抑制肿瘤的转移和浸润。
3. 抗血小板药物对肿瘤治疗的辅助作用除了直接抑制肿瘤的生长和转移外,抗血小板药物还可以作为其他肿瘤治疗手段的辅助药物。
研究发现,抗血小板药物可以增强放疗和化疗的疗效,提高肿瘤对治疗的敏感性,有助于提高肿瘤治疗的成功率。
三、抗血小板药物在肿瘤治疗中的研究进展1. 抗血小板药物的联合应用目前的研究表明,抗血小板药物与其他肿瘤治疗手段的联合应用具有很大的潜力。
抗血小板药物与免疫治疗、靶向治疗的联合应用,可以有效提高肿瘤治疗的效果,降低肿瘤对治疗的耐药性。
2. 抗血小板药物的个体化治疗随着肿瘤治疗的个体化趋势,抗血小板药物的个体化治疗也备受关注。
研究发现,不同患者对抗血小板药物的反应存在差异,因此个体化的用药方案可以更好地发挥抗血小板药物在肿瘤治疗中的作用。
3. 抗血小板药物的新型研究进展除了已有的抗血小板药物外,目前还有许多新型的抗血小板药物正在不断研究和开发中。
这些新型抗血小板药物可能具有更好的抗肿瘤效果,同时减少了不良反应和耐药性等问题,有望成为未来肿瘤治疗的重要手段。
四、结语随着对肿瘤治疗机制的不断深入研究,抗血小板药物在肿瘤治疗中的作用逐渐受到关注。
目前的研究表明,抗血小板药物通过影响肿瘤生长、转移和治疗的辅助作用,具有重要的临床应用前景。
阿司匹林、氯吡格雷、替罗非班等抗血小板药物机制、作用特点、药代动力学及出血风险处理等并发症处理血小板聚集药物是脑梗死急性期、二级预防的主要治疗药物,它们通过作用于血栓形成的不同阶段,达到抗血小板聚集的作用。
血小板聚集形成血栓的过程在细胞外基质,血小板表面的糖蛋白受体及GPIb-IX-V 与血管内皮细胞释放的血管性血友病因子等相互作用,导致血小板附着在胶原蛋白上形成活化后的血小板。
在整合素αIIbβ3介导下,纤维蛋白原通过桥联的方式,两端与不同的αIIbβ3 结合,最终导致血小板的聚集。
激活的血小板还会释放内源性二磷酸腺苷和血栓素A2,最终导致更多血小板的活化与聚集。
不同抗血小板聚集药物作用机制抗血小板聚集药物作用特点阿司匹林1)机制:作为最经典的抗血小板药物,阿司匹林可以不可逆的抑制血小板环氧化酶(COX-1),导致TXA2 生成减少,从而抑制血小板的聚集。
2)起效时间:阿司匹林的达峰时间约为 0.3~2 小时,清除半衰期与剂量相关;肠溶片较普通片吸收时间可延长3~6 小时。
因此,快速起效时可选择嚼服。
3)功能恢复时间:由于阿司匹林不可逆的抑制环氧化酶活性,因此,血小板功能的恢复需要等待血小板的再生,即完全停药后 7~10 天。
4)代谢途径:阿司匹林经由肾脏代谢,因此,使用时需考虑肾功能情况。
禁用于合并氨甲蝶呤时,可能会减少其肾清除。
5)合并用药:同样作用于水杨酸的NSAID,如布洛芬等,合并时也需要谨慎。
此外,促进尿酸排泄的药物,如苯磺唑酮等,也可能需要谨慎。
6)注意事项:阿司匹林还可能导致支气管痉挛并引起哮喘发作,因此,也需要考虑患者是否合并哮喘。
7)服用时间:普通剂型的阿司匹林通常用于退热止痛,肠溶型的阿司匹林不会在酸性的胃肠道环境下溶解,而会进入碱性的环境,以尽量减少对胃肠道的刺激,建议餐前服用。
同时由于阿司匹林可以直接破坏消化道黏膜,应用时需注意其消化道出血并发症。
氯吡格雷1)机制:氯吡格雷经过CYP450 酶代谢后,生成的活性代谢产物可以不可逆抑制ADP 与血小板P2Y12 受体的结合,从而抑制血小板的聚集。