同分异构现象和同分异构体
- 格式:ppt
- 大小:506.00 KB
- 文档页数:14

7.1.1 同分异构现象与同分异构体
一、同分异构现象与同分异构体
(1)同分异构现象:化合物具有相同的分子式,但具有不同的结构的现象
(2)同分异构体:具有同分异构现象的化合物互称为同分异构体
(3)同分异构体特点:
①分子式相同,即:化学组成和相对分子质量相同
同分异构体要求分子式相同,但结构不同,二者缺一不可;分子式相同,则相对分子质量相等,但相对分子质量相等的物质,分子式不一定相同,如:CO和C2H4②可以是同类物质,也可以是不同类物质
结构不同意味着同分异构体不一定是同类物质,如:CH3CH2CH=CH2和
③结构不同,性质可能相似也可能不同
同分异构体的结构一定不同,因此它们的物理性质存在差异;如果同分异构体的结构相似,属于同类物质,则它们的化学性质相似;如果同分异构体是不同类别的物质,则它们的化学性质不同
④同分异构体之间的转化是化学变化
烷烃中,甲烷、乙烷、丙烷不存在同分异构体,其他烷烃均存在同分异构体,且同分异构体的数目随碳原子数的增加而增多,如:丁烷有2种同分异构体、己烷有5种同分异构体、癸烷有75种同分异构体。
同分异构现象是有机物种类繁多的原因之一
二、化学“四同”的比较
同位素同素异形体同系物同分异构体
概念质子数相同而
中子数不同的
同一种元素的
不同原子
由同种元素
形成的不同
单质
结构相似,在分
子组成上相差
一个或若干个
CH2原子团的
化合物
分子式相同,但结
构不同的化合物。
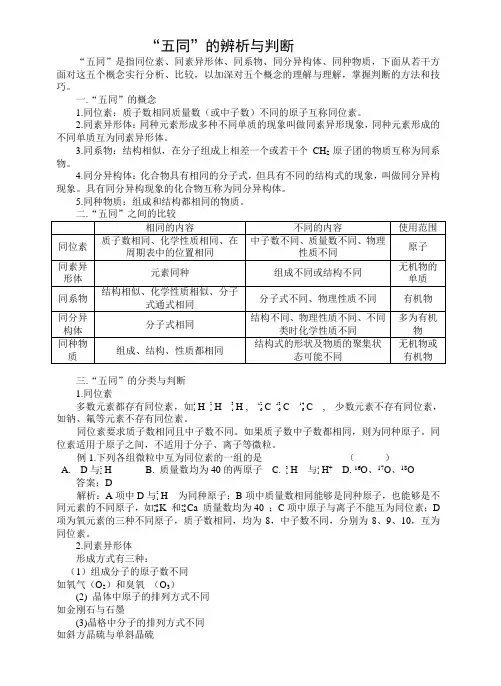
“五同”的辨析与判断“五同”是指同位素、同素异形体、同系物、同分异构体、同种物质,下面从若干方面对这五个概念实行分析、比较,以加深对五个概念的理解与理解,掌握判断的方法和技巧。
一.“五同”的概念1.同位素:质子数相同质量数(或中子数)不同的原子互称同位素。
2.同素异形体:同种元素形成多种不同单质的现象叫做同素异形现象,同种元素形成的不同单质互为同素异形体。
3.同系物:结构相似,在分子组成上相差一个或若干个CH 2原子团的物质互称为同系物。
4.同分异构体:化合物具有相同的分子式,但具有不同的结构式的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
5.同种物质:组成和结构都相同的物质。
三.“五同”的分类与判断 1.同位素多数元素都存有同位素,如1 1H 2 1H 3 1H , 12 6C 13 6C 146C , 少数元素不存有同位素,如钠、氟等元素不存有同位素。
同位素要求质子数相同且中子数不同。
如果质子数中子数都相同,则为同种原子。
同位素适用于原子之间,不适用于分子、离子等微粒。
例1.下列各组微粒中互为同位素的一组的是 ( )A. D 与2 1HB. 质量数均为40的两原子C. 3 1H 与1 1H +D. 16O 、17O 、18O答案:D解析:A 项中D 与2 1H 为同种原子;B 项中质量数相同能够是同种原子,也能够是不同元素的不同原子,如4019K 和40 20Ca 质量数均为40 ;C 项中原子与离子不能互为同位素;D 项为氧元素的三种不同原子,质子数相同,均为8,中子数不同,分别为8、9、10,互为同位素。
2.同素异形体形成方式有三种:(1)组成分子的原子数不同 如氧气(O 2)和臭氧 (O 3)(2) 晶体中原子的排列方式不同 如金刚石与石墨(3)晶格中分子的排列方式不同 如斜方晶硫与单斜晶硫红磷和白磷的形成方式复杂,分子中原子的数目不同,而原子的排列方式也不同。
同素异形体适用于单质,元素相同且性质不同。
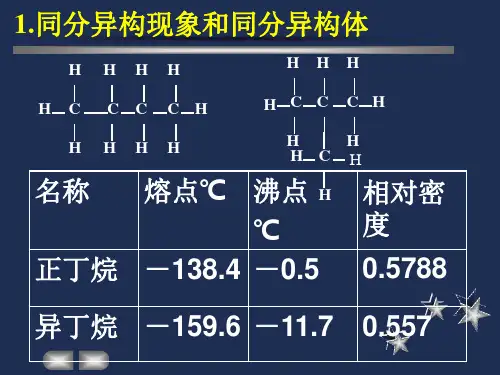





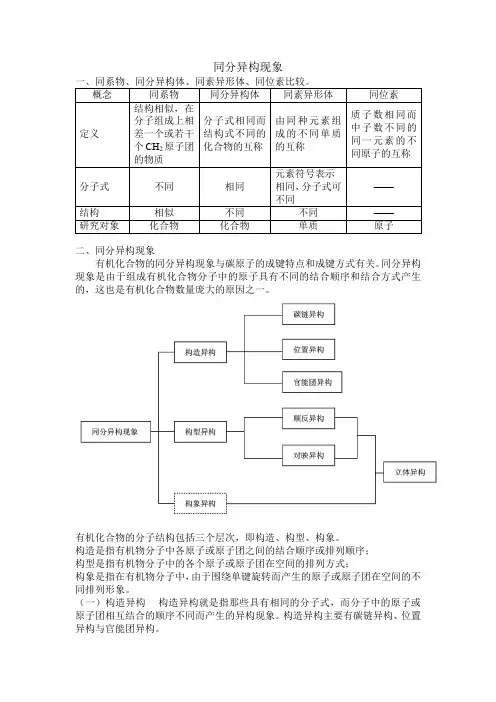
同分异构现象二、同分异构现象有机化合物的同分异构现象与碳原子的成键特点和成键方式有关。
同分异构现象是由于组成有机化合物分子中的原子具有不同的结合顺序和结合方式产生的,这也是有机化合物数量庞大的原因之一。
有机化合物的分子结构包括三个层次,即构造、构型、构象。
构造是指有机物分子中各原子或原子团之间的结合顺序或排列顺序;构型是指有机物分子中的各个原子或原子团在空间的排列方式;构象是指在有机物分子中,由于围绕单键旋转而产生的原子或原子团在空间的不同排列形象。
(一)构造异构构造异构就是指那些具有相同的分子式,而分子中的原子或原子团相互结合的顺序不同而产生的异构现象。
构造异构主要有碳链异构、位置异构与官能团异构。
①碳链异构由于碳链骨架不同而产生的异构现象。
例如:与环己烷甲基环戊烷②位置异构由于取代基或官能团在碳链或碳环上的位置不同而产生的异构现象。
例如:CH3CH2CH2CH2OH 与CH3CH2CHCH3OH1-丁醇 2-丁醇邻溴甲苯间溴甲苯对溴甲苯或2-溴甲苯或3-溴甲苯或4-溴甲苯③官能团异构具有相同的分子组成,由于官能团不同而产生的异构现象,例如:具有相同分子式的烯烃与环烷烃之间也存在异构现象:CH3CH=CH2 (丙烯)与环丙烷(二)构型异构构型异构是指分子中的原子或原子团在空间的排列方式不同而产生的异构现象,有顺反异构和对映异构两类。
1、顺反异构烯烃的同分异构现象比烷烃的要复杂,除碳链异构外,还有由于双键的位置不同引起的位置异构、分子式相同化合类别不同引起的官能团异构和双键两侧的基团在空间的位置不同引起的顺反异构。
例如:丁烷只有正丁烷和异丁烷两个异构体,而丁烯就有三个异构体:CH 3CH 2CH=CH 2 CH 3CH=CHCH 3 CH 3C=CH 2CH 31-丁烯 2-丁烯 2-甲基丙烯 双键位置异构 碳架异构由于双键不能自由旋转又产生了另一个异构现象--顺反异构,如:2-丁烯有两个:CCCCHHHHCH 3CH 3CH 3CH 3顺-2-丁烯 反-2-丁烯 单烯烃的分子通式为C n H 2n ,它与环烷烃(通式为C n H 2n )互为同分异构体,如丁烯和环丁烷(甲基环丙烷)互为同分异构体。
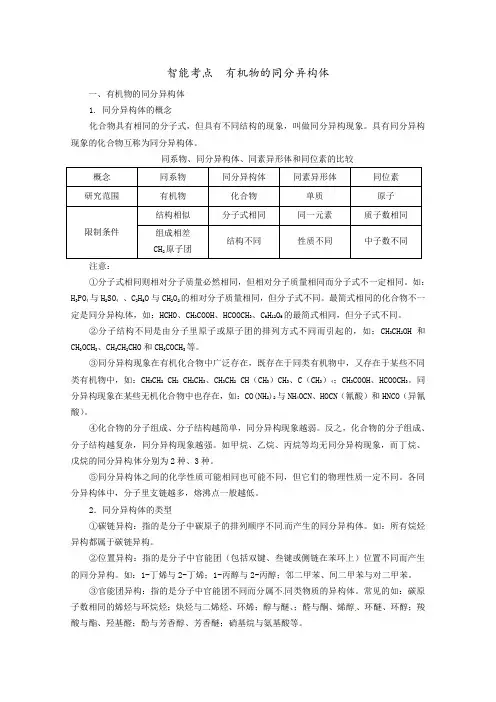
智能考点有机物的同分异构体一、有机物的同分异构体1. 同分异构体的概念化合物具有相同的分子式,但具有不同结构的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
同系物、同分异构体、同素异形体和同位素的比较概念同系物同分异构体同素异形体同位素研究范围有机物化合物单质原子限制条件结构相似分子式相同同一元素质子数相同组成相差CH2原子团结构不同性质不同中子数不同注意:①分子式相同则相对分子质量必然相同,但相对分子质量相同而分子式不一定相同。
如:H3PO4与H2SO4、C2H6O与CH2O2的相对分子质量相同,但分子式不同。
最简式相同的化合物不一定是同分异构体,如:HCHO、CH3COOH、HCOOCH3、C6H12O6的最简式相同,但分子式不同。
②分子结构不同是由分子里原子或原子团的排列方式不同而引起的,如:CH3CH2OH和CH3OCH3、CH3CH2CHO和CH3COCH3等。
③同分异构现象在有机化合物中广泛存在,既存在于同类有机物中,又存在于某些不同类有机物中,如:CH3CH2 CH2 CH2CH3、CH3CH2 CH(CH3)CH3、C(CH3)4;CH3COOH、HCOOCH3。
同分异构现象在某些无机化合物中也存在,如:CO(NH2)2与NH4OCN、HOCN(氰酸)和HNCO(异氰酸)。
④化合物的分子组成、分子结构越简单,同分异构现象越弱。
反之,化合物的分子组成、分子结构越复杂,同分异构现象越强。
如甲烷、乙烷、丙烷等均无同分异构现象,而丁烷、戊烷的同分异构体分别为2种、3种。
⑤同分异构体之间的化学性质可能相同也可能不同,但它们的物理性质一定不同。
各同分异构体中,分子里支链越多,熔沸点一般越低。
2.同分异构体的类型①碳链异构:指的是分子中碳原子的排列顺序不同而产生的同分异构体。
如:所有烷烃异构都属于碳链异构。
②位置异构:指的是分子中官能团(包括双键、叁键或侧链在苯环上)位置不同而产生的同分异构。
第2课时同分异构体1.同分异构体化合物具有相同的分子式,但具有不同结构式的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
同分异构现象普遍存在于有机化合物中,它是有机物种类繁多的重要原因之一。
同分异构体之间的转化是化学变化。
在有机化合物中,当碳原子数目增多时,同分异构体的数目也就越多。
2.同分异构现象的类别(1)碳链异构,是由于碳原子的排列方式不同产生的异构现象。
烷烃中的同分异构体均为碳链异构,如C5H12有三种同分异构体,即正戊烷、异戊烷、新戊烷。
(2)位置异构,是由于官能团位置不同产生的异构现象,如CH3CH===CHCH3和CH2===CH—CH2—CH3。
(3)官能团异构,是由于具有不同的官能团而产生的异构现象。
如CH≡C—CH2—CH3与CH2===CH—CH===CH2、丙烯与环丙烷、乙醇与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、葡萄糖与果糖、蔗糖与麦芽糖、硝基乙烷与甘氨酸等。
(4)立体异构,有机化合物具有相同的组成和相同的结构,而原子在分子中的空间排列情况不同,这种异构称为立体异构。
立体异构又分为顺反异构和对映异构。
CH3—CH===CH—CH3存在顺反异构,甲基在双键同一侧的,称为顺-2-丁烯;甲基在双键两侧的,称为反-2-丁烯。
乳酸存在对映异构,两种分子互为镜像。
立体异构现象广泛存在于自然界中,立体异构和生命现象有着紧密的联系。
如某些昆虫的信息素具有一个或多个碳碳双键,它们通常存在顺反异构。
同样,生命体对手性分子也有着神奇的识别能力。
探究点一同分异构现象和同分异构体一、同分异构现象产生的原因同分异构现象产生的原因是有机化合物分子内部通常含有较多的原子,分子内部原子结合的顺序和成键方式不同。
但并不是所有分子都有同分异构体,例如CH4、C2H6等就没有同分异构体。
同分异构体的性质有较大差异,这是因为结构不同所导致的结果。
二、对同分异构体的理解(1)分子结构式的写法与分子真实结构的差别。
专题03 同分异构现象与同分异构体1.同分异构现象化合物具有相同的分子式,但结构不同,因而产生了性质上的差异的现象。
2.同分异构体(1)概念:具有同分异构现象的化合物互为同分异构体。
(2)实例:戊烷的同分异构体如下表所示3.同分异构体的类型CH3CH2CH2CH3与【例1】下列各组物质不属于同分异构体的是()同分异构体书写方法1.烷烃同分异构体的书写技巧——减碳对称法下面以C5H12为例说明:第一步:所有碳,一条链:C—C—C—C—C(先写碳链,后用H原子饱和,下同)第二步:缩一碳,作支链:第三步:再缩碳,组合连:以上写法也可记为“成直链,一条线;摘一碳,挂中间,往边排,不到端;摘两碳,乙基先,两甲基,同邻间,不重复,要写全”。
2.烯烃、炔烃同分异构体的书写技巧(1)写出相同碳原子数烷烃的同分异构体结构简式。
(2)从相应烷烃的结构简式出发,变动不饱和键的位置。
烯烃、炔烃同分异构体类型包括位置异构(或—C≡C—的位置)、碳链异构、官能团异构。
3.同分异构体数目的判断方法(1)基元法如丁基有四种结构,则丁醇有四种同分异构体。
(2)换元法如二氯苯C6H4Cl2有三种同分异构体,四氯苯也有三种同分异构体(将H替代Cl、Cl替代H)。
(3)对称法(又称等效氢法)等效氢法的判断可按下列三点进行:①同一甲基上的氢原子是等效的;②同一碳原子上所连甲基上的氢原子是等效的;③处于对称位置上的氢原子是等效的。
(4)定一移二法对于二元取代物的同分异构体的判定,可固定一个取代基位置,再移动另一取代基,以确定同分异构体数目。
【例2】某化合物的分子式为C5H11Cl,结构分析表明,该分子中有两个—CH3、两个—CH2—、一个和一个—Cl,它的可能结构有四种,请写出这四种可能的化合物的结构简式:____________________、_________________、_________________、_______________________。