第4章 滴定分析法概述
- 格式:pdf
- 大小:382.61 KB
- 文档页数:31

第四章 滴定分析概论§4.1概述定量分析的任务是测定物质中组分的含量。
定量分析的分析方法有滴定分析法、重量分析法和仪器分析法等。
一、定量分析的一般要求根据定量分析的任务和特点,定量分析的一般要求是: 1、测定结果的准确度准确度高是定量分析的最基本要求。
对于常量组分(≥10%)一般要求测定误差不超过0.2% 对于半微量组分(1%~10%) 对于微量组分(0.01%~1%)2、测定结果应具有代表性测定所用试样只是待测物质中的很小部分,这些少量物质称为分析试样或样品。
3、分析方法应可靠和可行4、分析结果应正确计算和合理报告(1)、被测组分的化学表示形式 a 以被测组分实际存在形式表示。
如测得食盐试样中Cl 含量后,以NaCl%表示分析结果。
b 以氧化物或元素形式表示(实际存在形式不清楚)如硅酸盐水泥Fe Al Ca Mg 、、、含量常以2323Fe O Al O CaO MgO 、、、的含量表示。
分析铁矿石以23%%Fe Fe O 或表示。
c 金属材料和有机分析中,常以元素形式(如Fe 、Zn 、N 、P )的含量表示。
d 电解质溶液的分析,以所存在的离子形式表示含量。
(2)、被测组分含量的表示方法 a 固体试样常量组分常以质量分数表示BB sm W m =微量组分以1g g μ-⋅或6(10)-,1ng g -⋅9(10)-,1pg g -⋅12(10)-表示。
b 液体试样 ①物质的量浓度:Bn V⋅-1单位mol L②质量摩尔浓度:⋅-1单位mol kg (kg 溶剂的质量)③质量分数:待测组分的质量除以试样的质量,即B m m 试样。
④体积分数:B V V 试液表示。
⑤摩尔分数:待测组分的物质的量除以试液的物质的量,量钢为1即B n n 试液 ⑥质量浓度:常以11111mg L g L g mL ng mL pg mL μμ-----⋅⋅⋅⋅⋅、或、、等表示。
对于极稀的水溶液,视其密度为1,此时1mg L -⋅(或1g mL μ-⋅),与11()mg kg g g μ--⋅⋅在数值上相等,但概念不同。



第四章 滴定分析概论思考题与习题1. 什么是滴定分析?它的主要分析方法有哪些?答:滴定分析法又称容量分析法,是经典的化学分析法。
将一种已知准确浓度的试剂溶液滴加到被测物质溶液中,直到所加的试剂溶液与被测组分按化学反应式计量关系恰好反应完全为止,根据试剂溶液的浓度和体积,计算被测组分含量的一类方法称为滴定分析法。
滴定分析法主要的分析方法有:酸碱滴定法,配位滴定法,沉淀滴定法及氧化还原滴定法等。
2. 能用于滴定分析的化学反应应具备什么条件?答:(1)反应必须定量完成;(2)反应速度要快;(3)有简便可靠的方法确定滴定终点。
3. 什么是基准物质?基准物质应具备哪些条件?答:用来直接配制标准溶液或标定标准溶液的物质称为基准物质。
基准物质必须具备下列条件:(1)应具有足够的纯度;(2)物质的组成要与化学式完全符合;(3)性质稳定;(4)具有较大的摩尔质量。
4. 下列物质中哪些可以直接法配制标准溶液?哪些只能用间接法配制?NaOH 、H 2SO 4、HCl 、KMnO 4、NaCO 3、AgNO 3、NaCl 、K 2Cr 2O 7。
答:直接法配制:NaCO 3、NaCl 、K 2Cr 2O 7;间接法配制:NaOH 、H 2SO 4、HCl 、KMnO 4、AgNO 3。
5. 以HCl 溶液为滴定剂测定样品中K 2CO 3的含量,若其中含有少量Na 2CO 3,测定结果将偏高还是偏低?答:偏高。
6. 已知浓硫酸的相对密度为1.84,其中含H 2SO 4约为96%,求其量浓度为多少?如欲配制1L 0.1mol/L 的H 2SO 4溶液,应取这种浓硫酸多少毫升?解:浓硫酸的物质的量的浓度为242424H SO H SO H SO 1.8496%1000mol /L 18mol /L 98.01c M ρω⨯==⨯= 配制浓度为0.10mol/L 溶液1L 需要浓硫酸体积为ml 6.5mol/L18mol/L 10.0ml 100042SO H =⨯==浓稀c Vc V 7. 中和下列酸溶液,需要多少毫升0.2150mol/L NaOH 溶液?①22.53ml 0.1250mol/L 的H 2SO 4溶液;②20.52ml 0.2040mol/L 的HCl 溶液。


滴定分析法(容量分析法)概述滴定分析法(容量分析法)概述一、滴定分析法的原理与种类1.原理滴定分析法是将一种已知精准浓度的试剂溶液,滴加到被测物质的溶液中,直到所加的试剂与被测物质按化学计量定量反应为止,依据试剂溶液的浓度和消耗的体积,计算被测物质的含量。
这种已知精准浓度的试剂溶液称为滴定液。
将滴定液从滴定管中加到被测物质溶液中的过程叫做滴定。
当加入滴定液中物质的量与被测物质的量按化学计量定量反应完成时,反应达到了计量点。
在滴定过程中,指示剂发生颜色变化的变化点称为滴定尽头。
滴定尽头与计量点不肯定恰恰符合,由此所造成分析的误差叫做滴定误差。
适合滴定分析的化学反应应当具备以下几个条件:(1)反应必需按方程式定量地完成,通常要求在99.9%以上,这是定量计算的基础。
(2)反应能够快速地完成(有时可加热或用催化剂以加速反应)。
(3)共存物质不干扰重要反应,或用适当的方法除去其干扰。
(4)有比较简便的方法确定计量点(指示滴定尽头)。
2.滴定分析的种类(1)直接滴定法用滴定液直接滴定待测物质,以达尽头。
(2)间接滴定法直接滴定有困难时常采纳以下两种间接滴定法来测定:a 置换法利用适当的试剂与被测物反应产生被测物的置换物,然后用滴定液滴定这个置换物。
铜盐测定:Cu2++2KI→Cu+2K++I2│用Na2S2O3滴定液滴定、以淀粉指示液指示尽头┗————————————————————→b 回滴定法(剩余滴定法)用定量过量的滴定液和被测物反应完全后,再用另一种滴定液来滴定剩余的前一种滴定液。
二、滴定液滴定液系指已知精准浓度的溶液,它是用来滴定被测物质的。
滴定液的浓度用“XXX滴定液(YYYmol/L)”表示。
(一)配制1.直接法依据所需滴定液的浓度,计算出基准物质的重量。
精准称取并溶解后,置于量瓶中稀释至肯定的体积。
如配制滴定液的物质很纯(基准物质),且有恒定的分子式,称取时及配制后性质稳定等,可直接配制,依据基准物质的重量和溶液体积,计算溶液的浓度,但在多数情况是不可能的。
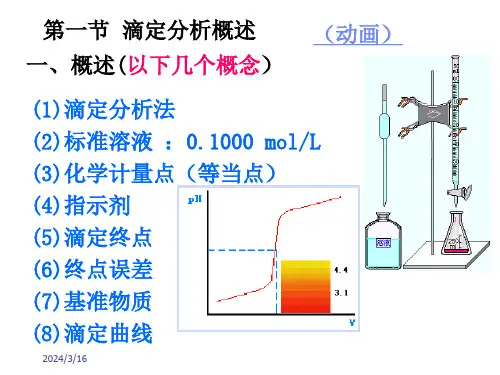



第四章滴定分析法概述第一节概述滴定分析法是化学分析法中的重要分析方法之一。
将一种已知其准确浓度的试剂溶液 (称为标准溶被)滴加到被测物质的溶液中, 直到化学反应完全时为止, 然后根据所用试剂溶液的浓度和体积可以求得被测组分的含量, 这种方法称为滴定分析法(或容量分析法)。
方法特点:1. 加入标准溶液物质的量与被测物质的量恰好是化学计量关系;2. 此法适于常量分析,即组分含量在1%以上各种物质的测定;3. 该法快速、准确、仪器设备简单、操作简便;4.用途广泛。
一、基本术语1、滴定液(标准溶液)2、滴定3、化学计量点4、指示剂5、滴定终点6、终点误差二. 滴定分析法分类根据标准溶液和待测组分间的反应类型的不同,分为四类:1. 酸碱滴定法——以质子传递反应为基础的一种滴定分析方法反应实质: H+ + OH- ⇌ H2O2. 沉淀滴定法——以沉淀反应为基础的一种滴定分析方法Ag+ + Cl- ⇌ AgCl (白色)3. 配位滴定法——以配位反应为基础的一种滴定分析方法Mg2+ +Y4- ⇌ MgY2- (产物为配合物)Ag+ + 2CN-⇌ [Ag(CN)2]- (产物为配合离子)4. 氧化还原滴定法——以氧化还原反应为基础的一种滴定分析方法Cr2O72- + 6 Fe2++ 14H+ ⇌ 2Cr3++ 6 Fe3++7H2OI2 + 2S2O32-⇌ 2I- + S4O62-三、滴定分析法的基本条件1. 反应要按一定的化学方程式进行,即有确定的化学计量关系;2. 反应必须定量进行——反应接近完全(>99.9%);3. 反应速度要快——有时可通过加热或加催化剂来加快反应速度;4.须有适当方法确定滴定终点——简便可靠的方法:合适的指示剂。
四. 滴定方式1. 直接滴定法:一种标准溶液。
完全符合滴定反应要求的滴定反应:如: HCl 标液→ NaOH溶液(最常用、最基本的方式)2. 返滴定法:二种标准溶液。
分析化学第四章《滴定分析法概论》思考问题1、什么是滴定分析法?答:滴定分析法,又叫容量分析法,将已知准确浓度的标准溶液,滴加到被测溶液中(或者将被测溶液滴加到标准溶液中),直到所加的标准溶液与被测物质按化学计量关系定量反应为止,然后测量标准溶液消耗的体积,根据标准溶液的浓度和所消耗的体积,算出待测物质的含量。
这种定量分析的方法称为滴定分析法,它是一种简便、快速和应用广泛的定量分析方法,在常量分析中有较高的准确度。
1.1、滴定分析的特点:1. 加入标准溶液物质的量与被测物质的量恰好是化学计量关系;2. 此法适于组分含量在1%以上各种物质的测定;3. 该法快速、准确、仪器设备简单、操作简便;4.用途广泛。
1.2、什么时候进行一滴半滴操作:加入半滴的操作是将酸式滴定管的旋塞稍稍转动或碱式滴定管的乳胶管稍微松动,使半滴悬于管口,将锥形瓶内壁与管口接触,使液滴流出,并用洗瓶以纯水冲下。
1.3、分析实验中仪器的注意事项:移液管(一直二靠三斜四停)、酸(碱)式滴定管1、使用时先检查是否漏液。
2、用滴定管取滴液体时必须洗涤、润洗。
3、读数前要将管内的气泡赶尽、尖嘴内充满液体4、读数需有两次,第一次读数时必须先调整液面在0刻度或0刻度以下。
5、读数时,视线、刻度、液面的凹面最低点在同一水平线上。
6、量取或滴定液体的体积==第二次的读数-第一次读数。
2、什么是标准溶液、滴定剂?答:标准溶液是指含有某一特定浓度的参数的溶液,比如Cl或Fe的标准溶液。
当用标准溶液代替样品进行测试时,得到的结果应该与已知标准溶液的浓度相符。
如果得到相符的结果,则说明测试操作正确。
2.1、标准溶液的用途:标准溶液还可用来校准仪器,比如色度计和分光光度计,以及pH计和pH/ISE 计等电化学仪器。
不同浓度的标准溶液可以用来绘制校准曲线,从而可以用得到的校准曲线反查测试样品的浓度,这个在学校学习的时候,经常会用到用标准溶液校准仪器,并和样品溶液一起进行测试物性2.2、容量瓶操作有哪些步骤:计算、称量(量取)、溶解、冷却、转移、洗涤、定容、摇匀\装瓶3、滴定分析法是根据什么进行分类的?分类结果怎样?答:根据标准溶液和待测组分间的反应类型的不同,分为四类1. 酸碱滴定法——以质子传递反应为基础的一种滴定分析方法,可用于测定酸、碱和两性物质。