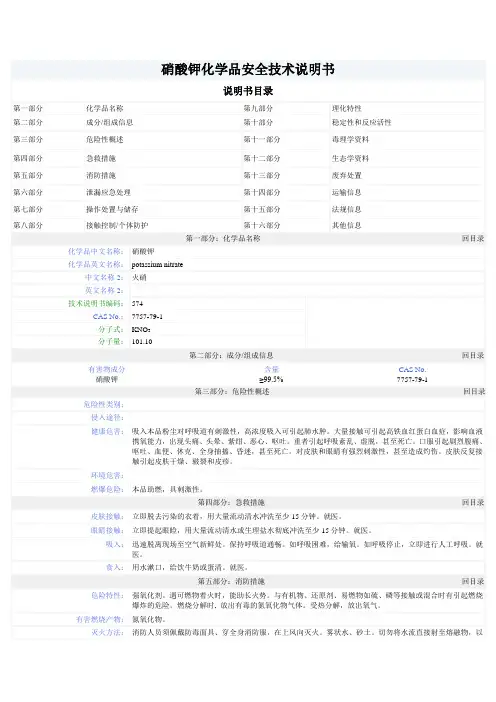
硝酸钾的理化性质及危险特性(表-)
- 格式:doc
- 大小:32.50 KB
- 文档页数:2

目录5.1类氧化剂过氧化氢的理化性质及危险特性(表-) (1)过氧化钠的理化性质及危险特性(表-) (2)高氯酸[含酸50%~72%]的理化性质和危险特性(表-) (3)高氯酸钠的理化性质和危险特性(表-) (4)氯酸钠的理化性质和危险特性(表-) (5)氯酸钾的理化性质和危险特性(表-) (6)亚氯酸钠的理化性质及危险特性(表-) (7)高锰酸钠的理化性质及危险特性(表-) (8)高锰酸钾的理化性质及危险特性(表-) (9)硝酸钠的理化性质及危险特性(表-) (10)硝酸钾的理化性质和危险特性(表-)............. 错误!未定义书签。
硝酸钙的理化性质和危险特性(表-) . (12)硝酸锶的理化性质和危险特性(表-) (13)硝酸钡的理化性质及危险特性(表-) (14)硝酸锌的理化性质和危险特性(表-) (15)硝酸银的理化性质及危险特性(表-) (17)硝酸铅的理化性质及危险特性(表-) (18)亚硝酸钾的理化性质及危险特性(表-) (19)过(二)碳酸钠的理化性质及危险特性(表-) (20)过硫酸铵的理化性质及危险特性(表-) (21)过硫酸钾的理化性质及危险特性(表-) (23)过硼酸钠的理化性质及危险特性(表-) (24)漂白粉的理化性质及危险特性(表-) (25)溴酸钠的理化性质和危险特性(表-) (26)溴酸钾的理化性质和危险特性(表-) (27)高碘酸的理化性质和危险特性(表-) (28)高碘酸钠的理化性质和危险特性(表-) (29)高碘酸钾的理化性质和危险特性(表-) (30)碘酸钠的理化性质和危险特性(表-) (31)碘酸钾的理化性质和危险特性(表-) (32)三氧化铬[无水]的理化性质及危险特性(表-) (33)重铬酸钾的理化性质及危险特性(表-) (34)硝酸镁的理化性质和危险特性(表-) (35)硝酸铁的理化性质和危险特性(表-) (36)硝酸镍的理化性质和危险特性(表-) (37)硝酸钴的理化性质及危险特性(表-) (38)硝酸铝的理化性质和危险特性(表-) (39)硝酸锰的理化性质和危险特性(表-) (40)硝酸铜的理化性质和危险特性(表-) (41)硝酸铋的理化性质和危险特性(表-) (42)硝酸镧的理化性质和危险特性(表-) (43)硝酸铈铵的理化性质和危险特性(表-) (45)亚硝酸钠的理化性质及危险特性(表-) (46)氧化银的理化性质及危险特性(表-) (47)5.2类有机过氧化物过氧化二异丙苯[含量>42%,带有惰性固体]的理化性质和危险特性(表-)48 过氧化(二)苯甲酰[77%<含量<95%,含水]的理化性质和危险特性(表-) 49 过氧化乙酸的理化性质及危险特性(表-) (50)高氯酸[含酸50%~72%]的理化性质和危险特性(表-)高氯酸钠的理化性质和危险特性(表-)氯酸钠的理化性质和危险特性(表-)亚氯酸钠的理化性质及危险特性(表-)硝酸钠的理化性质及危险特性(表-)硝酸银的理化性质及危险特性(表-)过硼酸钠的理化性质及危险特性(表-)溴酸钠的理化性质和危险特性(表-)重铬酸钾的理化性质及危险特性(表-)硝酸钴的理化性质及危险特性(表-)氧化银的理化性质及危险特性(表-)。

硝酸钾1. 化学品及企业标识化学品中文名称:硝酸钾化学品英文名称:potassium nitrate中文名称2:火硝;硝石英文名称2:saltpeter主要用途:用于制造烟火、火药、火柴、医药,以及玻璃工业。
2. 危险性概述2.1 危险性类别:氧化剂、易制爆。
2.2侵入途径:吸入、食入。
2.3健康危害:吸入本品粉尘对呼吸道有刺激性,高浓度吸入可引起肺水肿。
大量接触可引起高铁血红蛋白血症,影响血液携氧能力,出现头痛、头晕、紫绀、恶心、呕吐。
重者引起呼吸紊乱、虚脱,甚至死亡。
口服引起剧烈腹痛、呕吐、血便、休克、全身抽搐、昏迷,甚至死亡。
对皮肤和眼睛有强烈刺激性,甚至造成灼伤。
皮肤反复接触引起皮肤干燥、皲裂和皮疹。
2.4环境危害:对环境有害。
2.5燃爆危险:助燃。
与可燃物混合能形成爆炸性混合物。
3. 成分/组成信息纯品■混合物□主要成分CAS RN 含量(%)硝酸钾7757-79-1 99.04. 急救措施4.1 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗20~30 分钟。
如有不适感,就医。
4.2眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗10~15 分钟。
如有不适感,就医。
4.3吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
4.4食入:饮足量温水,催吐。
就医。
5. 消防措施5.1 危险特性:强氧化剂。
遇可燃物着火时,能助长火势。
与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。
燃烧分解时, 放出有毒的氮氧化物气体。
受热分解,放出氧气。
5.2有害燃烧产物:无意义。
5.3灭火方法:本品不燃。
根据着火原因选择适当灭火剂灭火。
5.4灭火注意事项及措施:消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
切勿将水流直接射至熔融物,以免引起严重的流淌火灾或引起剧烈的沸溅。

硝酸钾(1)化学品及企业标识化学品中文名:硝酸钾;火硝;硝石化学品英文名:potassium nitrate;saltpeter分子式:KNO3相对分子量:140.21(2)成分/组成信息成分:纯品CAS No:7752-79-1(3)危险性概述危险性类别:第5.1类氧化剂侵入途径:吸入、食入健康危害:吸入本品粉尘对呼吸道有刺激性,高浓度吸入可引起肺水肿。
大量接触可引起高铁血红蛋白血症,影响血液携氧能力,出现头痛、头晕、紫绀、恶心、呕吐。
重者引起呼吸紊乱、虚脱,甚至死亡。
口服引起剧烈腹痛、呕吐、血便、休克、全身抽搐、昏迷,甚至死亡。
对皮肤和眼睛有强烈刺激性,甚至造成灼伤。
皮肤反复接触引起皮肤干燥、皲裂和皮疹环境危害:对水生生物是有毒的燃爆危险:助燃。
与可燃物混合能形成爆炸性混合物(4)急救措施皮肤接触:脱去污染的衣着,用大量流动清水冲洗20~30min。
如有不适感,就医眼睛接触:提起眼睑,用流动清水或生理盐水冲洗10~15min。
如有不适感,就医吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸、心跳停止,立即进行心肺复苏术。
就医。
食入:漱口。
就医(5)消防措施危险特性:强氧化剂。
遇可燃物着火时,能助长火势。
与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。
燃烧分解时, 放出有毒的氮氧化物气体。
受热分解,放出氧气有害燃烧产物:无意义灭火方法:本品不燃。
根据着火原因选择适当灭火剂灭火灭火注意事项及措施:消防人员须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
切勿将水流直接射至熔融物,以免引起严重的流淌火灾或引起剧烈的沸溅(6)泄漏应急处理应急行动:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防毒服,戴氯丁橡胶手套。
勿使泄漏物与可燃物质(如木材、纸、油等)接触。
穿上适当的防护服前严禁接触破裂的容器和泄漏物。


农业硝酸钾简介一、性质介绍硝酸钾(俗名火硝或土硝;英文名称potassium nitrate; nitre; saltpetre)1、物理性质分子式:KNO3;分子量:101.10;密度:2.109(16℃) , 1. 145 g/cm3相对密度(水=1) 2.11 ;熔点(℃)334性状无色透明斜方或三方晶系颗粒或白色粉末;气味:无味。
溶解情况:溶于水、稀乙醇、甘油,不溶于无水乙醇和乙醚(稍溶于乙醇),潮解性比硝酸钠低。
在水中的溶解度随水温上升而剧烈增大:0℃:13.3g 20℃:31.6g 100℃:246g2、化学性质1、在400℃分解并放出氧,转变成亚硝酸钾,继续加热分解生成氧化钾和氧化氮,在空气中不潮解。
2、危险特性:强氧化剂,遇可燃物着火时,能助长火势。
与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。
燃烧分解时, 放出有毒的氮氧化物气体。
受热分解,放出氧气。
有害燃烧产物:氮氧化物。
二、工艺简介1、生产原理:KOH+HNO3=KNO3+H20+Q2、工艺特点:本生产方法利用酸碱中和法生产硝酸钾,生产过程无三废排放,并无副产物生成,整个工艺流程简单易于操作,具有转化率高、热能利用率高和产品质量高等优点。
3、工艺流程简述:32%氢氧化钾溶液自化工分公司由管道输送至车间氢氧化钾储槽,再经液碱泵送至中和反应槽;硝酸硝铵车间自产45%稀硝酸由罐区泵送至中和反应槽,按一定配比与氢氧化钾溶液发生中和反应,反应后浓度为30%左右硝酸钾溶液经泵送至料液储槽,再经泵送至四效错流蒸发系统蒸发浓缩成65-70%硝酸钾料浆,在内返料式喷浆造粒干燥机进行喷浆造粒和干燥,所得物料经滚筒筛筛分,大于4mm物料经破碎后与小于2mm物料一并返回喷浆造粒机内重新进行喷浆造粒,2-4mm合格物料进入自动包装机进行包装,生产成品码垛后入库。
四、农业硝酸钾用途农业硝酸钾是一种含钾和氮的高效复合肥料,对各种土壤和农作物施用,均能取得良好效果,特别适用于忌氯作物,如:烟草、西红柿、柑桔、葡萄糖等。

硝酸钾的理化性质及危险特性表-一、硝酸钾的基本信息硝酸钾,又称钾硝酸,化学式为KNO3,分子量为101.1032 g/mol。
它是一种白色粉末,无臭无味,易水解,在水中溶解性较大。
硝酸钾是一种重要的化工原料和农业肥料,在医药、食品和火药等领域也有广泛应用。
二、硝酸钾的理化性质1. 密度:硝酸钾的密度为2.109 g/cm3;2. 熔点:硝酸钾的熔点为334℃,熔化时会产生强烈的白烟;3. 沸点:硝酸钾在常压下不会沸腾,只有在高温高压下才会产生气态;4. 溶解性:硝酸钾在水中的溶解度随温度升高而增大,20℃时每100克水中可以溶解13.3克硝酸钾,100℃时每100克水中可以溶解246克硝酸钾;5. 毒性:硝酸钾的口服半数致死剂量(LD50)为3750毫克/公斤,属于低毒物质;6. 火性:硝酸钾属于氧化剂,可以加速燃烧过程,易与可燃物质发生反应,可能导致燃烧或爆炸;7. 化学反应:硝酸钾可以和硫、硫化氢、亚硫酸盐、硫酸亚铁等还原剂发生化学反应,产生氮氧化物和硫酸盐等物质,具有一定的危险性。
三、硝酸钾的危险特性1. 火灾爆炸危险:硝酸钾属于氧化剂,容易跟可燃物质结合发生燃烧或爆炸,因此必须避免接触火源、高温和摩擦。
2. 刺激性和腐蚀性:硝酸钾对眼睛、皮肤和呼吸道具有刺激性和腐蚀性,接触后会引起眼睛疼痛、红肿、流泪、视力模糊、皮肤灼烧、溶解、皮疹和过敏反应等不适症状。
3. 毒性:硝酸钾的LD50为3750毫克/公斤,虽然属于低毒物质,但长期接触或大量摄入会对人体造成伤害,如头痛、头晕、恶心、呕吐、腹泻、胃肠道出血、肝肾损伤等。
4. 氧化性:硝酸钾属于氧化剂,与还原剂一起存放会产生危险,容易引起燃烧或爆炸,因此必须严格控制储存条件。
综上所述,硝酸钾是一种具有火灾和爆炸危险的氧化剂,在储存、运输、使用过程中必须加强安全防范措施,防止与可燃物质、还原剂等发生反应,避免接触火源、高温和摩擦,注意保护眼睛和皮肤,避免长时间接触,以免引起损害。


目录5.1类氧化剂过氧化氢的理化性质及危险特性(表-) (1)过氧化钠的理化性质及危险特性(表-) (2)高氯酸[含酸50%~72%]的理化性质和危险特性(表-) (3)高氯酸钠的理化性质和危险特性(表-) (4)氯酸钠的理化性质和危险特性(表-) (5)氯酸钾的理化性质和危险特性(表-) (6)亚氯酸钠的理化性质及危险特性(表-) (7)高锰酸钠的理化性质及危险特性(表-) (8)高锰酸钾的理化性质及危险特性(表-) (9)硝酸钠的理化性质及危险特性(表-) (10)硝酸钾的理化性质和危险特性(表-)............. 错误!未定义书签。
硝酸钙的理化性质和危险特性(表-) . (12)硝酸锶的理化性质和危险特性(表-) (13)硝酸钡的理化性质及危险特性(表-) (14)硝酸锌的理化性质和危险特性(表-) (15)硝酸银的理化性质及危险特性(表-) (17)硝酸铅的理化性质及危险特性(表-) (18)亚硝酸钾的理化性质及危险特性(表-) (19)过(二)碳酸钠的理化性质及危险特性(表-) (20)过硫酸铵的理化性质及危险特性(表-) (21)过硫酸钾的理化性质及危险特性(表-) (23)过硼酸钠的理化性质及危险特性(表-) (24)漂白粉的理化性质及危险特性(表-) (25)溴酸钠的理化性质和危险特性(表-) (26)溴酸钾的理化性质和危险特性(表-) (27)高碘酸的理化性质和危险特性(表-) (28)高碘酸钠的理化性质和危险特性(表-) (29)高碘酸钾的理化性质和危险特性(表-) (30)碘酸钠的理化性质和危险特性(表-) (31)碘酸钾的理化性质和危险特性(表-) (32)三氧化铬[无水]的理化性质及危险特性(表-) (33)重铬酸钾的理化性质及危险特性(表-) (34)硝酸镁的理化性质和危险特性(表-) (35)硝酸铁的理化性质和危险特性(表-) (36)硝酸镍的理化性质和危险特性(表-) (37)硝酸钴的理化性质及危险特性(表-) (38)硝酸铝的理化性质和危险特性(表-) (39)硝酸锰的理化性质和危险特性(表-) (40)硝酸铜的理化性质和危险特性(表-) (41)硝酸铋的理化性质和危险特性(表-) (42)硝酸镧的理化性质和危险特性(表-) (43)硝酸铈铵的理化性质和危险特性(表-) (45)亚硝酸钠的理化性质及危险特性(表-) (46)氧化银的理化性质及危险特性(表-) (47)5.2类有机过氧化物过氧化二异丙苯[含量>42%,带有惰性固体]的理化性质和危险特性(表-)48 过氧化(二)苯甲酰[77%<含量<95%,含水]的理化性质和危险特性(表-) 49 过氧化乙酸的理化性质及危险特性(表-) (50)高氯酸[含酸50%~72%]的理化性质和危险特性(表-)高氯酸钠的理化性质和危险特性(表-)氯酸钠的理化性质和危险特性(表-)亚氯酸钠的理化性质及危险特性(表-)硝酸钠的理化性质及危险特性(表-)硝酸银的理化性质及危险特性(表-)过硼酸钠的理化性质及危险特性(表-)溴酸钠的理化性质和危险特性(表-)重铬酸钾的理化性质及危险特性(表-)硝酸钴的理化性质及危险特性(表-)氧化银的理化性质及危险特性(表-)。

硝酸钾的理化性质及危险特性表-硝酸钾是一种常见的化学物质,它由氮、氧和钾元素组成,化学式为KNO3。
在工业和日常生活中,它被广泛使用。
在本文中,我将介绍硝酸钾的理化性质以及其与健康和环境的危险特性。
硝酸钾是一种无色结晶体,具有较高的相对分子质量。
它是可溶于水的化合物,其溶解度随温度的变化而变化。
在常温下,硝酸钾可以溶解在水中,形成无色透明的溶液。
它在空气中相对稳定,不易被氧化或还原。
然而,在高温下,硝酸钾可以分解生成氧气和氮氧化物。
硝酸钾具有一些重要的物理性质。
它的熔点较高,约为334摄氏度。
这意味着在常温下,硝酸钾是固态的。
当加热到熔点以上时,它会熔化成为液体。
在高温下,它可以蒸发成为气体。
硝酸钾的密度约为2.1克/立方厘米,比水的密度大。
硝酸钾在化学反应中具有一些特殊的性质。
它是一种强氧化剂,在某些条件下可以和其他物质发生剧烈的反应。
硝酸钾可以与可燃物质如纸张、木材和织物发生反应,产生火灾的危险。
此外,硝酸钾还可以与其他氧化剂如硫、磷等物质反应,产生易爆的混合物。
因此,在存储和使用硝酸钾时,必须小心,并遵循安全操作规程。
除了对健康的潜在威胁外,硝酸钾还可能对环境造成危害。
当硝酸钾溶液进入水体时,可能导致水体污染。
硝酸钾中的氮元素可以促进水中藻类和植物的生长,这可能导致水体富营养化和水质恶化。
此外,硝酸钾的排放还可能影响土壤的质量,并对植物造成伤害。
为减少硝酸钾对健康和环境的危害,必须严格控制其生产和使用过程中的安全措施。
在工业生产中,应遵循严格的操作规范,并设立相关的防护设施。
在日常生活中,使用硝酸钾时要小心,避免与可燃物质接触,并妥善处理废弃物。
总结起来,硝酸钾是一种常见的化学物质,具有一系列的理化性质。
它是可溶的结晶体,在高温下能分解成氧气和氮氧化物。
硝酸钾是一种强氧化剂,对可燃物质具有危险性。
此外,硝酸钾还可能对健康和环境造成危害。
因此,我们在使用和处理硝酸钾时必须小心谨慎,确保安全操作,并严格遵守相关的规定。
硝酸钾化学品安全技术说明书第一部分:化学品名称化学品中文名称:硝酸钾化学品英文名称:potassium nitrate中文名称2:火硝英文名称2:技术说明书编码:574CAS No.:7757-79-1分子式:KNO3分子量:101.10第二部分:成分/组成信息有害物成分含量CAS No.硝酸钾≥99.5% 7757-79-1第三部分:危险性概述危险性类别:侵入途径:健康危害:吸入本品粉尘对呼吸道有刺激性,高浓度吸入可引起肺水肿。
大量接触可引起高铁血红蛋白血症,影响血液携氧能力,出现头痛、头晕、紫绀、恶心、呕吐。
重者引起呼吸紊乱、虚脱,甚至死亡。
口服引起剧烈腹痛、呕吐、血便、休克、全身抽搐、昏迷,甚至死亡。
对皮肤和眼睛有强烈刺激性,甚至造成灼伤。
皮肤反复接触引起皮肤干燥、皲裂和皮疹。
环境危害:燃爆危险:本品助燃,具刺激性。
第四部分:急救措施皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟。
就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:用水漱口,给饮牛奶或蛋清。
就医。
第五部分:消防措施危险特性:强氧化剂。
遇可燃物着火时,能助长火势。
与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。
燃烧分解时, 放出有毒的氮氧化物气体。
受热分解,放出氧气。
有害燃烧产物:氮氧化物。
灭火方法:消防人员须佩戴防毒面具、穿全身消防服,在上风向灭火。
雾状水、砂土。
切勿将水流直接射至熔融物,以免引起严重的流淌火灾或引起剧烈的沸溅。
第六部分:泄漏应急处理应急处理:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘面具(全面罩),穿防毒服。
不要直接接触泄漏物。
勿使泄漏物与有机物、还原剂、易燃物接触。
小量泄漏:用大量水冲洗,洗水稀释后放入废水系统。
大量泄漏:用塑料布、帆布覆盖。
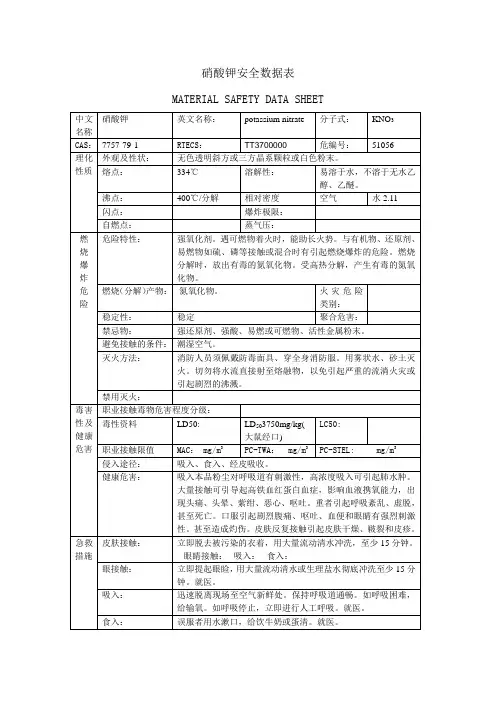
标识中文名:硫酸钾分子式:K2SO4分子量:174.24 CAS号:7778-80-5理化性质外观与性状无色或白色结晶、颗粒或粉末熔点(℃)1069 相对密度(水=1) 2.660 相对密度(空气=1) / 沸点(℃)1689 饱和蒸气压(kPa)/溶解性易溶于水。
临界温度(℃)/健康危害吸入、摄入或经皮吸收有害,具刺激作用。
长期吸入该品粉尘,可引起慢性中毒,早期以神经衰弱综合征和神经功能障碍为主,晚期出现震颤麻痹综合征。
急救方法①皮肤接触:脱去污染的衣着,用流动清水冲洗。
②眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
③吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
④食入:用水漱口,给饮牛奶或蛋清。
就医。
环境危害对环境有危害,对水体可造成污染燃烧爆炸危险性燃烧性不燃燃烧分解物氧化硫闪点(℃) 1689 爆炸上限(v%)/引燃温度(℃)/ 爆炸下限(v%)/危险特性本身不能燃烧。
受高热分解放出有毒的气体.禁忌物强氧化剂。
储运条件与泄漏处理储存条件:储存于阴凉、通风的库房。
远离火种、热源。
防止阳光直射。
包装密封。
应与酸类分开存放,切忌混储。
储区应备有合适的材料收容泄漏物。
泄漏处理:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿一般作业工作服。
不要直接接触泄漏物。
小量泄漏:避免扬尘,小心扫起,收集运至废物处理场所处置。
大量泄漏:收集回收或运至废物处理场所处置。
灭火方法消防人员必须穿全身防火防毒服,在上风向灭火。
灭火时尽可能将容器从火场移至空旷处。
然后根据着火原因选择适当灭火剂灭火。
危险化学品安全周知卡
危险性类别化学品标识危险性标志
助燃!
硝酸钾potassium nitrate
KNO3
CAS号:7757-79-1
危险性理化数据危险特性外观与性状:无色至白色晶体或粉末;
pH值:5.0~7.5(20℃,50g/L);
熔点/凝固点(℃):333~334;
初沸点和沸程(℃):400(分解);爆炸上限/下限[%(v/v)]:无资料;相对密度(水=1):2.1;
溶解性(mg/L):与水混溶;
分解温度(℃):400。
固体。
跟可燃物质接触可能会引起火灾。
短期暴露有严重损伤健康的危险。
长期暴露有严重损伤健康的危险。
与活泼金属粉末的混合物,在加热时剧烈爆炸。
健康危害现场急救措施
咳嗽,咽喉痛。
腹部疼痛,嘴唇发青或指甲发青,皮肤发青,头晕,呼吸困难,意识模糊,惊厥,腹泻,头痛,恶心,神志不清。
发红。
发红,疼痛。
皮肤接触:脱去污染的衣服。
冲洗,然后用水和肥皂清洗皮肤。
眼睛接触:先用大量水冲洗几分钟,就医。
吸入:新鲜空气,休息,给予医疗护理。
食入:漱口,给予医疗护理。
身体防护措施消防灭火介质
可用:使用适合火灾类型的合适的灭火剂。
禁用:无特别说明。
泄漏处理措施
浓度(mg/m3)当地应急救援单位名称当地应急救援单位电话
MAC:未制定PC-TWA:未制定PC-STEL:未制定消防中心
人民医院
火警:119
匪警:110
急救:120。