
一、反应物和产物的电子结构
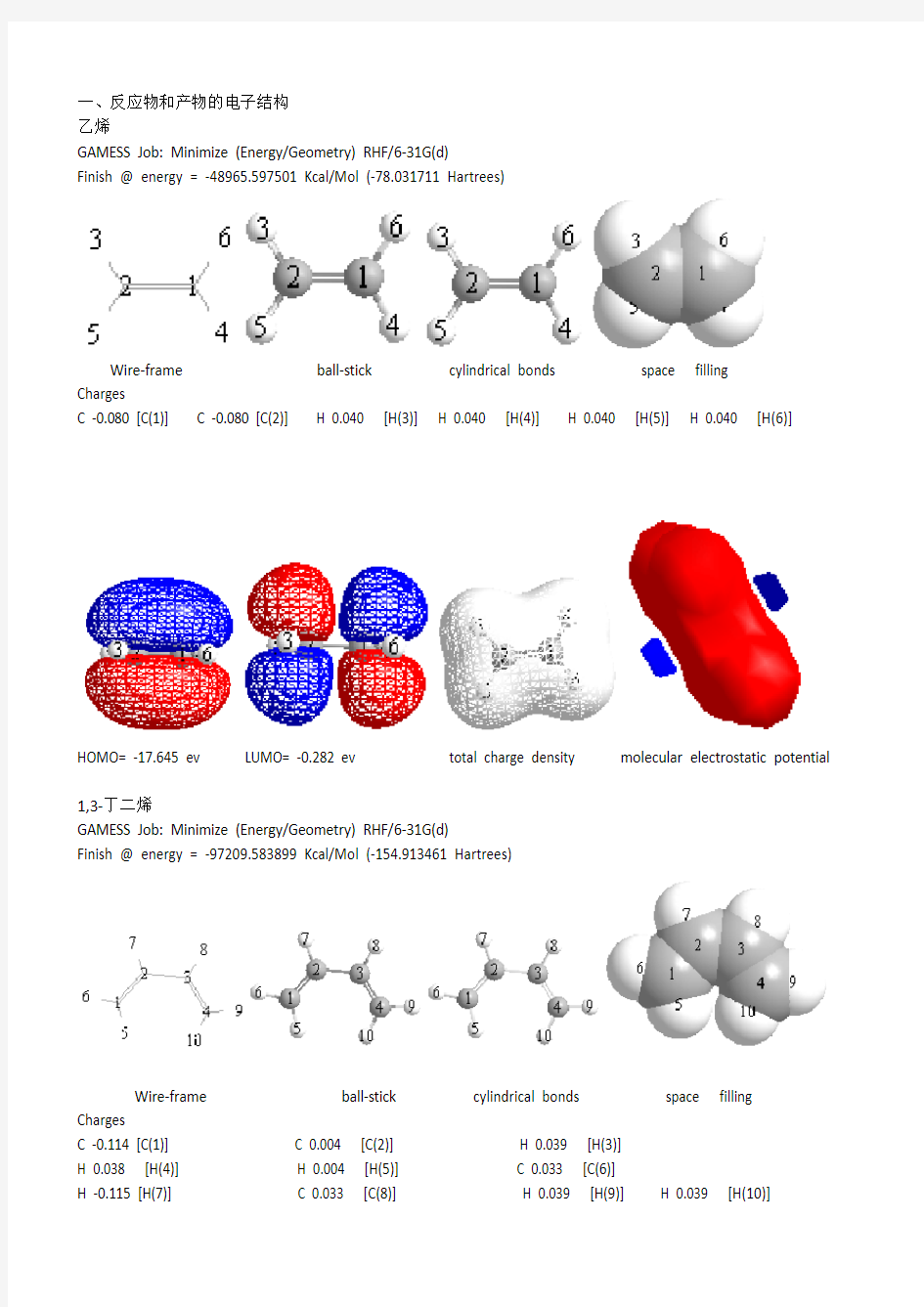
乙烯
GAMESS Job: Minimize (Energy/Geometry) RHF/6-31G(d)
Finish @ energy = -48965.597501 Kcal/Mol (-78.031711 Hartrees)
Wire-frame ball-stick cylindrical bonds space filling
Charges
C -0.080 [C(1)] C -0.080 [C(2)] H 0.040 [H(3)] H 0.040 [H(4)] H 0.040 [H(5)] H 0.040 [H(6)]
HOMO= -17.645 ev LUMO= -0.282 ev total charge density molecular electrostatic potential
1,3-丁二烯
GAMESS Job: Minimize (Energy/Geometry) RHF/6-31G(d)
Finish @ energy = -97209.583899 Kcal/Mol (-154.913461 Hartrees)
Wire-frame ball-stick cylindrical bonds space filling
Charges
C -0.114 [C(1)] C 0.004 [C(2)] H 0.039 [H(3)]
H 0.038 [H(4)] H 0.004 [H(5)] C 0.033 [C(6)]
H -0.115 [H(7)] C 0.033 [C(8)] H 0.039 [H(9)] H 0.039 [H(10)]
HOMO= -15.068 ev LUMO= -3.719ev total charge density molecular electrostatic potential
环己烯
GAMESS Job: Minimize (Energy/Geometry) RHF/6-31G(d)
Finish @ energy = -146221.8807 Kcal/Mol (-233.019592 Hartrees)
Wire-frame ball-stick cylindrical bonds space filling
Charges
C -0.059 [C(1)] C -0.059 [C(2)] H -0.073 [H(3)] C -0.073 [C(4)]
C -0.082 [C(5)] H 0.030 [H(6)] H -0.082 [H(7)] C 0.030 [C(8)]
H 0.052 [H(9)] H 0.052 [H(10)] H 0.052 [H(11)] H 0.052 [H(12)]
H 0.040 [H(13)] C 0.040 [C(14)] H 0.040 [H(15)] H 0.040 [H(16)]
HOMO= -14.895 ev LUMO= 1.618 ev total charge density molecular electrostatic potential
从分子轨道的对称性来看,乙烯的HOMO轨道关于镜面呈对称,LUMO反对称,丁二烯的HOMO反对称,LUMO 对称,环己烯HOMO对称,LUMO反对称。如果乙烯提供LUMO,丁二烯提供HOMO分子轨道对称性是匹配若乙烯提供HOMO丁二烯提供LUMO对称性也是匹配的。因此将他们的轨道能量按能级次序排列为:
-17.645 ev
-15.068 ev
从能级图可以看出乙烯提供LUMO ,丁二烯提供HOMO 是能极差更小,所以更有利于加成反应。理论上环己烯HOMO 的能量应该比1,3-丁二烯的HOMO 低但系由于计算误差的存在使得环己烯能级能量稍高,这是由于环己烯并不是共轭体系,因此在计算π电子轨道时,并不完全准确,误差很大。
从电性上分析,两个反应物分子在相互靠近时电性相同,互相排斥,因此不利于加成反应。
综上,乙烯与丁二烯在轨道匹配性上是有利于反应的,但在电学性质上对反应不利。两者综合起来造成了乙烯与丁二烯间的D-A 反应条件比较苛刻。
二、构想搜索与分子间长程相互作用
为了研究乙烯分子与丁二烯分子靠近时的能量变化我首先进行了建模,再采用Chem3D 中的Dihedral driver 模块探究了能量与接触面以及接触面间距离的关系。结果及分析如下。
ethylene
cyclohexene
butadiene
HOMO LUMO
-0.282 ev
-3.719ev
-14.895 ev
1.618 ev
(1)丁二烯分子绕CCCC二面角转动的构象
稳定构型为
能垒一:{E(-180°) } - 11.27 kcal/mol + 52.17 kcal/mol {E(-90°)} = 40.90 kcal/mol 能垒二:{E(0°)} - 12.80 kcal/mol+52.17 kcal/mol {E(90°) } = 39.37 kcal/mol
(2)扫描3D势能面
初始模型
势能面图及表格
有势能面图可得最低能量作用点为:
当乙烯与丁二烯以如图所示方式相互作用时能量最低。
由势能面图以及势能曲线图可得平衡距离为0.446?,势能垒高度203495.2+(-48965.600362 - 97209.526939)=57320kcal/mol
这个结果显然是不合理的,这与计算软件的精确度有极大关系,与Lennard Joness 函数匹配度低,使得拟合数据出现严重偏差,解决问题的最好办法是提高软件的模拟精度。断面的存在也使得拟合难度增大。
三、反应途径计算:为了研究反应途径我采取了多种计算能量的方法,主要有GAMESS中
的HF/6-31G(d)和Mopac中的PM3,同时还研究了溶剂对反映的影响。
(1)反应热计算
乙烯:
ZPF= 34.369513 KCAL/MOL H= 36.829 KCAL/MOL S= 54.843 cal/(mol K) E= -48965.600362 Kcal/Mol H298K-H0K=36.829 KCAL/MOL - 34.369513 KCAL/MOL = 2.46 KCAL/MOL
E(C)= -23645.077286 Kcal/Mol
E (H) = -312.645612 Kcal/Mol
ΔHΘf,0k(C2H4)=2x169.98+4x51.63-2x(-23645.077286 Kcal/Mol)-4x(-312.645612 Kcal/Mol)+(-48965.600362 Kcal/Mol) +34.369513 KCAL/MOL =155.97KCAL/MOL
ΔHΘf,298 k(C2H4)=155.97KCAL/MOL + 2.46 KCAL/MOL-(2x0.25+4x1.01) KCAL/MOL=153.92KCAL/MOL
ΔGΘf,298 k(C2H4)=153.92KCAL/MOL-298.15x(54.829-2x1.36-4x15.6)/100Kcal/mol=156.89kcal/mol
1,3-丁二烯
ZPF= 57.272926 KCAL/MOL H= 60.264 Kcal/Mol S= 64.626 cal/(mol K) E= -97209.526939 Kcal/Mol
H298K-H0K=60.264 Kcal/Mol - 57.272926 KCAL/MOL =2.99 KCAL/MOL
E(C)= -23645.077286 Kcal/Mol
E (H) = -312.645612 Kcal/Mol
ΔHΘf,0k(C4H6)=4x169.98+6x51.63-4x(-23645.077286 Kcal/Mol)-6x(-312.645612 Kcal/Mol)+(-97209.526939 Kcal/Mol
)+57.272926 KCAL/MOL =293.56KCAL/MOL
ΔHΘf,298 k(C4H6)=293.56KCAL/MOL + 2.99 KCAL/MOL-(4x0.25+6x1.01) KCAL/MOL=289.49KCAL/MOL
ΔGΘf,298 k(C4H6)=289.49KCAL/MOL-298.15x(64.626 -4x1.36-6x15.6)/100Kcal/mol=299.75kcal/mol
环己烯
ZPF= 98.595069 KCAL/MOL H=102.418 KCAL/MOL S= 72.608 cal/(mol K) E= -146221.885759 Kcal/Mol
H298K-H0K=102.418 KCAL/MOL -98.595069KCAL/MOL = 3.823 KCAL/MOL
E(C)= -23645.077286 Kcal/Mol
E (H) = -312.645612 Kcal/Mol
ΔHΘf,0k(C6H10)=6x169.98+10x51.63-6x(-23645.077286Kcal/Mol)-10x(-312.645612Kcal/Mol)+(-146221.88575 Kcal/Mol) + 98.595069 KCAL/MOL =409.77KCAL/MOL
ΔHΘf,298 k(C6H10)=409.77KCAL/MOL + 3.823 KCAL/MOL-(6x0.25+10x1.01) KCAL/MOL=402.003KCAL/MOL
ΔGΘf,298 k(C6H10)=402.003KCAL/MOL-298.15x(72.608 -6x1.36-10x15.6)/100Kcal/mol=429.299kcal/mol
反应的焓变为:ΔHΘr,298 k=402.003KCAL/MOL-289.49KCAL/MOL-153.92KCAL/MOL= -41.4Kcal/mol
焓变是负值,与实验测量值(-39.6±1) kcal/mol相比十分相近,说明模拟计算的能量精度比较高。
反应的吉布斯自由能为ΔG Θ
r,298 k =429.299kcal/mol-299.75kcal/mol-156.89kcal/mol= -27.34Kcal/mol 说明反应是可以自发进行的。
(2)反应途经计算:1、HF 方法
过渡态(HF/6-31G(d))虚频901.46 I
GAMESS Job: Optimize to Transition State RHF/6-31G (d )
Finish @ energy = -146134.028877 Kcal/Mol (-232.879591 Hartrees)
势垒高度41.1 kcal/mol 比测量值高了接近8 kcal/mol 差距相当大,这说明我们的计算方法误差很大。
2、Mopac-PM3方法
丁二烯
Mopac Job: PM3 CHARGE=0 EF GNORM=0.100 SHIFT=80
Finished @ RMS Gradient = 0.07554 (< 0.10000) Heat of Formation = 31.71404 Kcal/Mol
乙烯(-48965.600362 Kcal/Mol) 丁二烯(-97209.526939 Kcal/Mol )
过渡态 -146134.028877 Kcal/Mol
环己烯-146221.885759 Kcal/Mol
COSMO溶剂化
Mopac Job: EPS=78.39 PM3 CHARGE=0 SHIFT=80
Mopac Interface: Heat of Formation = 31.05474 Kcal/Mol
乙烯
Mopac Job: PM3 CHARGE=0 EF GNORM=0.100 SHIFT=80
Finished @ RMS Gradient = 0.08875 (< 0.10000) Heat of Formation = 16.60853 Kcal/Mol 溶剂化
Mopac Job: EPS=78.39 PM3 CHARGE=0 SHIFT=80
Mopac Interface: Heat of Formation = 16.36709 Kcal/Mol
虚频Frequency = -911.03
Mopac过渡态优化
Mopac Job: PM3 CHARGE=0 GNORM=0.100 SHIFT=80 TS
Finished @ RMS Gradient = 0.06084 (< 0.10000) Heat of Formation = 74.63470 Kcal/Mol 溶剂化
Mopac Job: EPS=78.39 PM3 CHARGE=0 SHIFT=80
Mopac Interface: Heat of Formation = 47.69557 Kcal/Mol
环己烯
Mopac Job: PM3 CHARGE=0 EF GNORM=0.100 SHIFT=80
Finished @ RMS Gradient = 0.08605 (< 0.10000) Heat of Formation = -4.95460 Kcal/Mol 溶剂化
Mopac Job: EPS=78.39 PM3 COSMO CHARGE=0 SHIFT=80
Mopac Interface: Heat of Formation = -5.47587 Kcal/Mol
过渡态74.63470
Kcal/Mol
乙烯31.05474 Kcal/Mol
丁二烯16.36709 Kcal/Mol
环己烯-4.95460
Kcal/Mol
势垒高度:26.3kcal/mol
与HF/6-31G(d)结果相比偏小。原因在于他们用的方法不同,PM3用的是半经验方法,HF/6-31G(d)用的是HF自洽场方法,按理论来说没有一定谁的计算结果更准确。但由于处理方法的不同使得给体系带来的误差存在差异。
PM3方法偏低,而HF方法偏高。
2.1 PM3加溶剂化
加入溶剂化后,过渡态能量与反应物能量十分相近,所以反应几乎不经过过渡态直接就生成了产物。所以引进水作溶剂有利于反应的进行,这与水能提供质子有关,质子氢可以催化Diels-Alder反应。
过渡态74.63470
Kcal/Mol
乙烯31.71404 Kcal/Mol
丁二烯16.60853 Kcal/Mol
环己烯-5.47587Kcal/Mol
四、乙烯分子光谱模拟
(1)为了研究乙烯的反应活性,我用GAMESS程序中的【CIS HF/6-31G(d)】对乙烯作了紫外可见光普模拟。分析了光照对实验的影响。
C(1)
C(2) C(1) 1.3163
H(3) C(2) 1.1000 C(1) 120.4998
H(5) C(2) 1.1000 C(1) 120.4986 H(3) 118.9992 Pro-R
H(4) C(1) 1.1000 C(2) 120.4998 H(3) 179.9560 Dihedral
H(6) C(1) 1.1000 C(2) 120.4986 H(4) 118.9992 Pro-R
GAMESS Job: Minimize (Energy/Geometry) RHF/6-31G(d)
Finish @ energy = -48965.601568 Kcal/Mol (-78.031718 Hartrees)
单重激发态:
---------------------------------------------------------------------
CI-SINGLES EXCITATION ENERGIES
STATE HARTREE EV KCAL/MOL CM-1 ---------------------------------------------------------------------
1A 0.3227493151 8.7825 202.5283 70835.29 1A 0.3578344452 9.7372 224.5445 78535.58 1A 0.3786428779 10.3034 237.6020 83102.51 1A 0.3802464419 10.3470 238.6083 83454.45 1A 0.3925945588 10.6830 246.3568 86164.55 单重激发太态能
GAMESS Job: Compute Properties CIS/6-31G(d)
GAMESS Interface: Total Energy = -48763.0735 Kcal/Mol单重激发太态能
单重激发波长:
ΔE=-48763.0735 Kcal/Mol-(-48965.601568 Kcal/Mol)=202.5 kcal/mol=
λ=141 nm
三重激发态:
---------------------------------------------------------------------
CI-SINGLES EXCITATION ENERGIES
STATE HARTREE EV KCAL/MOL CM-1 ---------------------------------------------------------------------
3A 0.1385838847 3.7711 86.9627 30415.65
3A 0.3344942853 9.1021 209.8984 73413.01
3A 0.3614885249 9.8366 226.8375 79337.56
3A 0.3635509739 9.8927 228.1317 79790.22
3A 0.3661781521 9.9642 229.7803 80366.81
三重激发态能
GAMESS Job: Compute Properties CIS/6-31G(d)
GAMESS Interface: Total Energy = -48878.6389 Kcal/Mol
三重激发波长
ΔE= -48878.6389 Kcal/Mol -(-48965.601568 Kcal/Mol)=87 kcal/mol
λ=328 nm
C(1)
C(2) C(1) 1.3163
H(3) C(2) 1.1000 C(1) 120.4998
H(5) C(2) 1.1000 C(1) 120.4986 H(3) 118.9992 Pro-R
H(4) C(1) 1.1000 C(2) 120.4998 H(3) 179.9560 Dihedral
H(6) C(1) 1.1000 C(2) 120.4986 H(4) 118.9992 Pro-R
GAMESS Job: Minimize (Energy/Geometry) CIS/6-31G(d)
Finish @ energy = 0 Kcal/Mol (0 Hartrees)
由于三重态的乙烯分子能量优化不出来,所以三重态的乙烯分子不能稳定存在。因此确定不了绝热激发波长。
光照会使得乙烯的LUMO轨道变为乙烯的HOMO光照后轨道,非光照时,乙烯与丁二烯的轨道对称性是匹配的,光照后轨道对称性改变使得反应更加困难,从而使得不利于反应的进行。
(2)接着用GAMESS程序中的B3LYP/6-31G(d)对乙烯分子的红外光谱以及拉曼光谱作了模拟GAMESS Job: Minimize (Energy/Geometry) B3LYP/6-31G(d)
Finish @ energy = -49277.81857 Kcal/Mol (-78.529267 Hartrees)
6 7 8 9 10
FREQUENCY: 72.48 832.94 957.27 978.84 1069.70 REDUCED MASS: 1.00784 1.04365 1.52010 1.16076 1.00783
IR INTENSITY: 0.00025 0.01749 0.00057 1.97372 0.00001
11 12 13 14 15
FREQUENCY: 1235.83 1406.28 1511.94 1734.98 3147.59 REDUCED MASS: 1.53001 1.25775 1.11164 2.91838 1.05083 IR INTENSITY: 0.00006 0.00047 0.12637 0.00003 0.42801
16 17 18
FREQUENCY: 3164.85 3219.79 3245.78
REDUCED MASS: 1.07607 1.11049 1.11532
IR INTENSITY: 0.02496 0.02008 0.76561
红外光谱模拟
拉曼光谱模拟:
五、分子动力学模拟
我用MM2的方法对1,3-丁二烯作了动力学模拟。观测了分子能量随时间的变化。并用Origin作了能量关系图:
初始MM2优化结构:
Total Energy: -1.3194 kcal/mol
动力学模拟后结构:
取最后的2Ps作为能量平均值得:总能量为16.9 Kcal/mol,势能为8.0kcal/mol
说明动力学模拟之后能量升高了。
总能量
势能
总能量与势能随时间变化图
升温过程
能量 Kca l/m ol
分子模拟 编辑 分子模拟,是指利用理论方法与计算技术,模拟或仿真分子运动的微观行为,广泛的应用于计算化学,计算生物学,材料科学领域,小至单个化学分子,大至复杂生物体系或材料体系都可以是它用来研究的对象。 计算机分子模拟技术Computer Molecular Simulation,CMS 目录 1分类 2计算机分子模拟技术 3应用 1分类编辑 分子模拟的工作可分为两类:预测型和解释型。 预测型工作是对材料进行性能预测、对过程进行优化筛选,进而为实验提供可行性方案设计。解释型工作即通过模拟解释现象、建立理论、探讨机理,从而为实验奠定理论基础。 2计算机分子模拟技术编辑 这是随着计算机在科研中的应用而发展起来的一门新的科学,是计算机科学与基础科学相结合的产物。在药物研究方面通过分析和计算一系列活性药物分子的三维构象并将其叠合,可以了解某一类药物分子所应具有的药物构象,这一信息给予新药研究很大帮助,药效构象的计算为今后的药效基团方法以及数据库虚拟筛选的方法打下了基础。 3应用编辑 近年来分子模拟技术发展迅速并在多个学科领域得到了广泛的应用。在药物设计领域,可用于研究病毒、药物的作用机理等;在生物科学领域,可用于表征蛋白质的多级结构与性质;在材料学领域,可用于研究结构与力学性能、材料的优化设计等;在化学领域,可用于研究表面催化及机理等;在石油化工领域,可用于分子筛催化剂结构表征、合成设计、吸附扩散,可构建和表征高分子链以及晶态或非晶态本体聚合物的结构,预测包括共混行为、机械性质、扩散、内聚与润湿以及表面粘接等在内的重要性质。 生物化学与分子生物学总论 ?生物化学?生物无机化学?原始生物化学?古生物化学?前生命化学 ?地球生物化学?放射生物化学?低温生物化学?制备生物化学?反向生物化学 ?生命科学?分子生物学?结构分子生物学?分子遗传学?生物信息学 ?反向生物学?结构生物学?生物能学?生物物理化学?生物物理学 ?酶学?糖生物学?基因组学?结构基因组学?功能基因组学 ?比较基因组学?药物基因组学?转基因学?蛋白质组学?RNA组学 ?糖组学?相互作用物组学?代谢物组学?代谢组学?表型组学 其他科技名词 ?转录物组学?基因组?功能基因组?蛋白质组?转基因组 ?转录物组?表型组?代谢物组?RNA组?糖组 ?相互作用物组?生物大分子?生物多聚体?单体?多体 ?寡聚体?多聚体?残基?一级结构?二级结构
实验一本体聚合——有机玻璃的制造 1. 实验目的 了解本体聚合的特点,掌握本体聚合的实施方法,并观察整个聚合过程中体系粘度的变化过程。 2. 实验原理 本体聚合是不加其它介质,只有单体本身在引发剂或光、热等作用下进行的聚合,又称块状聚合。本体聚合的产物纯度高、工序及后处理简单,但随着聚合的进行,转化率提高,体系粘度增加,聚合热难以散发,系统的散热是关键。同时由于粘度增加,长链游离基末端被包埋,扩散困难使游离基双基终止速率大大降低,致使聚合速率急剧增加而出现所谓自动加速现象或凝胶效应,这些轻则造成体系局部过热,使聚合物分子量分布变宽,从而影响产品的机械强度;重则体系温度失控,引起爆聚。为克服这一缺点,现一般采用两段聚合:第一阶段保持较低转化率,这一阶段体系粘度较低,散热尚无困难,可在较大的反应器中进行;第二阶段转化率和粘度较大,可进行薄层聚合或在特殊设计的反应器内聚合。 本实验是以甲基丙烯酯甲酯(MMA)进行本体聚合,生产有机玻璃平板。聚甲基丙烯酸甲酯(PMMA)由于有庞大的侧基存在,为无定形固体,具有高度透明性,比重小,有一定的耐冲击强度与良好的低温性能,是航空工业与光学仪器制造工业的重要原料。以 MMA 进行本体聚合时为了解决散热,避免自动加速作用而引起的爆聚现象,以及单体转化为聚合物时由于比重不同而引起的体积收缩问题,工业上采用高温预聚合,预聚至约 10% 转化率的粘稠浆液,然后浇模,分段升温聚合,在低温下进一步聚合,安全渡过危险期,最后脱模制得有机玻璃平板。 3. 实验仪器及药品
三角瓶50ml 1 只 烧杯1000ml 1 只 电炉1KW 1 只 变压器1KV 1 只 温度计100 ℃ 1 支 量筒50、100ml 各1 只 试管10mm×70mm 1 支 烧杯400 ml 1 只 制模玻璃100mm×100mm 2 块 橡皮条3mm×15mm×80mm 3 根 另备玻璃纸、描图纸、胶水、试管夹、玻璃棒若干 2) 药品: 甲基丙烯酸甲酯(MMA)新鲜蒸馏30ml,BP=100.5℃ 过氧化二苯甲酰(BPO)重结晶0.05g 邻苯二甲酸二丁酯(DBP)分析纯(CP)2ml 4. 实验步骤 1) 制模 将一定规格的两块普通玻璃板洗净烘干。用透明玻璃纸将橡皮条包好,使之不外露。将包好的橡皮条放在两块玻璃板之间的三边,用沾有胶水的描图纸把玻璃板三边封严,留出一边作灌浆用。制好的模放入烘箱内,于50℃烘干。
分子动力学的模拟过程 分子动力学模拟作为一种应用广泛的模拟计算方法有其自身特定的模拟步骤,程序流程也相对固定。本节主要就分子动力学的模拟步骤和计算程序流程做一些简单介绍。 1. 分子动力学模拟步驟 分子动力学模拟是一种在微观尺度上进行的数值模拟方法。这种方法既可以得到一些使用传统方法,热力学分析法等无法获得的微观信息,又能够将实际实验研究中遇到的不利影响因素回避掉,从而达到实验研宄难以实现的控制条件。 分子动力学模拟的步骤为: (1)选取所要研究的系统并建立适当的模拟模型。 (2)设定模拟区域的边界条件,选取粒子间作用势模型。 (3)设定系统所有粒子的初始位置和初始速度。 (4)计算粒子间的相互作用力和势能,以及各个粒子的位置和速度。 (5)待体系达到平衡,统计获得体系的宏观特性。 分子动力学模拟的主要对象就是将实际物理模型抽象后的物理系统模型。因此,物理建模也是分子动力学模拟的一个重要的环节。而对于分子动力学模拟,主要还是势函数的选取,势函数是分子动力学模拟计算的核心。这是因为分子动力学模拟主要是计算分子间作用力,计算粒子的势能、位置及速度都离不开势函数的作用。系统中粒子初始位置的设定最好与实际模拟模型相符,这样可以使系统尽快达到平衡。另外,粒子的初始速度也最好与实际系统中分子的速度相当,这样可以减少计算机的模拟时间。 要想求解粒子的运动状态就必须把运动方程离散化,离散化的方法有经典Verlet算法、蛙跳算法(Leap-frog)、速度Veriet算法、Gear预估-校正法等。这些算法有其各自的优势,选取时可按照计算要求选择最合适的算法。 统计系统各物理量时,便又涉及到系统是选取了什么系综。只有知道了模拟系统采用的系综才能釆用相对应的统计方法更加准确,有效地进行统计计算,减少信息损失。 2. 分子动力学模拟程序流程 具体到分子动力学模拟程序的具体流程,主要包括: (1)设定和模拟相关的参数。 (2)模拟体系初始化。 (3)计算粒子间的作用力。 (4)求解运动方程。 (5)循环计算,待稳定后输出结果。 分子动力学模拟程序流程图如2.3所示。
中国海洋大学本科生课程大纲 课程属性:公共基础/通识教育/学科基础/专业知识/工作技能,课程性质:必修、选修 一、课程介绍 1.课程描述: 《高分子物理实验》是高分子科学体系的重要组成部分,是从事高分子科学与材料研究的最基础的实验技术,是研究和表征聚合物结构和性能关系的一门实验科学,是高分子材料与工程专业的一门专业必修课。本实验课的主要内容是使学生掌握研究和表征聚合物的结构、力学性能、电性能、热性能及溶液性质的基本方法和手段,掌握基础的相关实验技能与数据分析处理方法。通过实验使学生能够理论结合实践,进一步加深高分子物理专业知识的理解,使学生基本掌握高分子物理实验的基本原理、操作过程、数据采集、数据分析与处理,实验知识和技能,提高学生的动手能力与实验技能,培养学生严谨的科学态度与思维方法,为后续的高分子材料与科学的相关实践和毕业设计打下基础。 2.设计思路: 本课程实验内容主要包括以下几个方面:高聚物结构的表征与分析(包括实验一、五、六、七、九、十),力学性能的表征与分析(包括实验二、三、四),电性能(实验十一、十二)及热性能(实验七与实验九涉及到了材料的热性能)。实验中既有基本实验技能的操作,又有实验报告、数据处理分析及相应的思考题,使学生通过实验原理学习、实验操作、数据分析与讨论,掌握高分子物理结构与性能研究的基本方法与过程、操作技能、数据分析处理能力,分析解决问题能力,加深对实际科研实践的认识,提高理论知识的综合运用能力和实践能力,为后续的实验、实践和毕业设计打下基础。 - 6 -
3. 课程与其他课程的关系 先修课程:高分子化学、高分子物理。本课程需要学习材料与化学的相关基础课程,这些课程是学习高分子化学与高分子物理的基础,因此在此不再列出。 二、课程目标 本实验课的目的是使学生掌握测定和研究聚合物的结构、力学性能、电性能、热性能及溶液性质的方法和手段,对聚合物结构与性能之间关系获得初步认识。通过本课程的学习使学生增加感性认识,加深理论知识的理解,提高学生的动手能力和实验技能,培养学生的科学态度和工作作风。使学生逐步具备一定的从事科学研究的思维方法和实验能力。 基本要求: 1、使学生进一步理解高分子物理学中的一些基本概念与相关理论知识。 2、使学生掌握测定和表征聚合物结构与性能的基本方法的原理、正确进行仪器操作与使用。 3、能够互相配合完成实验过程,处理实验过程中遇到的简单问题。 4、能够独立进行数据处理分析,并完成实验报告。 三、学习要求 高分子物理实验是理论基础上的实验操作技能课,有利于学生加深对基础理论的理解与实际运用,对提高学生的实验动手能力与实践能力非常重要。另外,课程在实验室进行,因此必须严格遵守实验室的相关规章制度,保障实验过程中的实验安全与人身安全。具体要求如下: 1、学生必须严格遵守实验室的相关规章制度,严禁违反实验室安全要求的任何行为。 2、实验前认真阅读讲义,实验前进行预习,就实验目的、原理、实验注意事项等书写预习报告。实验必须准时,不能擅自更换实验时间。 3、实验时要认真操作,认真观察现象,做好记录。必须准备实验记录本,所有原始记录(实验数据及现象)均记录在记录本上,不允许记在他处。不允许篡改,编造实验数据与记录。 4、实验时,遵守操作规程,注意安全。有与实验相关问题,及时与老师交流,未 - 6 -
分子模拟实验作业——分子光谱模拟 一、 实验部分 1. 红 外 光 谱 : 分 别 用 PM3 , HF/6-31G(d),B3LYP/6-31G(d),MP2/6-31G(d)四种理论方法计算H 2O 分子的红外光谱,并比较结果的优劣。实验上测得的水分子的振动频-1-1 由图像可得四种理论方法得到的振动频率分别为
B3LYP/6-31G(d) 1634 cm-1、3566 cm-1、3662 cm-1 MP2/6-31G(d) 1644 cm-1、3544 cm-1、3684 cm-1 与标准值1594cm-1,3657cm-1,3756cm-1比较,HF/6-31G(d)最为接近标准值; PM3三个频率都偏大,与标准值符合情况不好;B3LYP/6-31G(d)除1634 cm-1与标准值较接近外,其余两个频率均偏小;MP2/6-31G(d) 1644 cm-1与标准值接近,其余两个频率均偏小。 2.拉曼光谱的模拟 HF/6-31G(d)计算的CH4分子的拉曼谱图 图中特征波数为3290 cm-1、3189 cm-1、1705 cm-1 3.紫外可见光谱的模拟 计算甲酸分子5个垂直激发的单重态和三重态,2个绝热激发的单重态和三重态,并确定垂直激发和绝热激发波长。 (1)垂直激发 --------------------------------------------------------------------- CI-SINGLES EXCITATION ENERGIES STATE HARTREE EV KCAL/MOL CM-1 --------------------------------------------------------------------- 1A 0.2550545872 6.9404 160.0492 55978.01
复习提纲: 1、市售的单体一般需要蒸馏精制后才能参与聚合反应,为什么? 答:对于一个化学反应必须接触才能进行反应,而市售试剂单体为了防止其聚合变质,必须降低其浓度来阻止反应,所以要加入稀释剂使其不能接触。从而使该单体长时间保存,当然用的时候要把稀释剂除去(一般采用蒸馏法)后才能发生反应。 2、在悬浮聚合中如何控制悬浮聚合产物颗粒的大小。 答:悬浮聚合产物的颗粒尺寸大小与搅拌速度、分散剂用量及油水比(单体与水的体积比)成反比,主要通过控制反应温度,搅拌速度,以及调节分散剂用量来加以控制悬浮聚合粒径。 3、聚合物的分子量与其熔体流动速率有什么关系?为什么熔体流动速率不能在结构不同的聚合物之间进行比较? 答:熔体流动速率(MFR)是指在一定的温度和压力下,聚合物在单位时间内通过规定孔径的量,用g/min来表示熔体流动速率。一般来说,同一类的聚合物如聚乙烯,聚合度越大即分子量越大,分子链之间作用力越大,链缠结越严重,导致聚合物熔体流动阻力增大,它的熔体流动速率越小;同样分子量的聚合物,由于它们的化学结构不同,它的熔体流动速率也不一样,这主要跟它们分子间的滑动系数有关。 由于不同聚合物测定时的标准条件不同,因此不具有可比性。 4、本体聚合的工业生产分两个阶段,先与预聚合到一定转化率,再进入第二阶段聚合。试解释采取上述步骤的原因。 答:如何排散聚合热,维持聚合温度恒定是实施本体聚合时必须考虑和解决的主要问题。本体聚合的生产分段进行,是为了先在较低温度下使单体以较低聚合速率转化,有利于聚合热的排散;同时由于转化率不高,聚合体系的粘度低,也有利于排散自动加速效应带来的集中放热,以避免由局部过热导致产物分子量分布较宽以及由温度失控而引起爆聚。在聚合塔中逐渐升温聚合是为了逐渐提高单体转化率,尽量使单体完全转化,减少残余单体。 5、与其他聚合方法相比较,乳液聚合的特点是什么?有何缺点?在乳液聚合中如何控制乳胶颗粒的大小和数目? 答:优点:(1)易散热。与本体聚合不同;乳液聚合体系的连续相是水,聚合反应发生在分散于水相中的乳胶粒内荨,尽管乳胶粒内黏度很高,但整个反应体系的黏度并不高,基本上接近于连续相水的黏度,并且在聚合过程中体系黏度也不会发生大幅度的变化,因为同本体聚合相比,乳液聚合体系易散姜,不会出现局部过热,更不易发生爆聚。 同乳液聚合体系中的介质水类似,在溶液聚合中要加入溶剂,介质和溶剂的稀释作用均可降妓热强度[kJ/(min·m3)]。但是乳液聚合体系的散热要比溶液聚合容易得多。这一方面是由于乳液聚合体系要比溶液聚合体系黏度低,前者黏度一般小于100mPa·s,而后者可达几万毫啦·秒;另一方面是由于水的比热容要比溶剂大,水的比热容为4.18kJ/(kg·℃),而有机溶蔫的比热容一般在1.05~2.51kJ/(kg·℃)范围内,故放热量相同时,乳液聚合体系要比溶液爱合体系温升幅度小。 尽管悬浮聚合和乳液聚合有相似之处,即它们的反应中心都是分散在介质水中的粒子中,但是芤液聚合要比悬浮聚合更易散热。对悬浮聚合来说,聚合反应发生在分散于水中的单体珠滴中,单体珠滴的直径一般在100~1000gm范围之内。而在乳液聚合体系中,反应中心乳胶粒直弪一般在O.05~O.1ktm之间。若把悬浮聚合体系中的珠滴比作一个10m直径的大球,那么,乳爱粒则仅相当于一颗绿豆粒。所以从乳胶粒内部向水相传热要比从悬浮聚合的珠滴内部向水相传姜容易得多。故乳胶粒中的温度分布要比悬浮聚合的珠滴中均匀得多。如果说在悬浮聚合中常常因为珠滴向外传热不良而导致“鱼眼”、黑点、红点及烧芯现象出现的话,那么可以认为在乳液藿合体系的乳胶粒中不存在因温度不均而导致的产品质量问题。 综上所述,乳液聚合不仅比本体聚合容易散热,而且也比溶液聚合和悬浮聚合更容易散热。
学号姓名学院(专业)成绩 评卷人得分 一、单选(本题总分:80分每小题:2分) 1.GPC仪器走基线和测样时,流动相流经 A. 样品池 B. 参比池 C. 参比池和样品池 参考答案:A 2.要是合成的聚合物样品是粘稠的胶状物,是否能测GPC?以下是两种对策,你认为哪一种更合理? A. 先把制得的胶状样放入烘箱干燥120度左右,至胶状样干透,成为固体,然后溶样检测 B. 直接溶样检测,先测测看再说 参考答案:B 3.GPC在Purge状态时,流动相流过 A. 参比池和样品池 B. 参比池 C. 样品池 参考答案:A 4.溶剂峰的组成是比较复杂的,峰型也可能比较复杂,有的是一个倒峰,有的是两个倒峰加一个正峰的。用THF做流动相时,利用从废液管接流出的干净THF来溶样,如果还有溶剂峰,那么它一般来自: A. 样品杂质(例如单体等小分子) B. 流动相溶剂的杂质 C. 仪器问题 参考答案:A 5.GPC测试仪中的示差折光检测器是根据聚合物溶液与参比(溶剂)间折光指数的差别来进行测量的,这个差值别再转换成: A. 浓度大小 B. 电压信号 C. 电流信号 参考答案:B 6.确切描述一种聚合物的分子量需要的参数是 A. 仅需平均分子量数值 B. 仅需分子量分布系数
C. 同时需要平均分子量数值和分子量分布系数 参考答案:C 7.通常GPC的标准曲线在10个点以上为好,并要涵盖样品的分子量范围,以下说法哪一种比较准确? A. 样品位置只要在曲线范围内都一样。 B. 样品位置必须在曲线正中间。 C. 样品位置在曲线两头较好。 D. 样品位置最好在曲线中间部位附近。 参考答案:D 8.Waters GPC测试系统用THF溶剂体系适用的“Styragel GPC”柱,通过柱子的流速不能高于2ml/min,正常流量为: A. 1.2ml/min B. 1.6 ml/min C. 1.8 ml/min D. 1.0ml/min 参考答案:D 9.同样分子量的两个聚合物样品,一个是支化分子的和另一个是线性的分子,那个先流出GPC色谱柱? A. 线性均聚样品 B. 支化聚合物样品 C. 线性嵌段共聚样品 D. 线性嵌段共聚物样品 参考答案:B 10.聚合物的分子量分散程度用多分散指数(多分散系数、分布系数)表示,缩写为“PDI”,符号为D或d,高分子文献里面一般是给出Mn、Mw、多分散系数。请问以下表述是否正确? A. D=Mw/Mn<1 B. D=Mn /Mw<1 C. D=Mn /Mw>1 D. D=Mw/Mn>1 参考答案:D 11.GPC图谱哪个轴表示保留时间(Minutes)或淋出体积(ml)。 A. 横轴 B. 纵轴 参考答案:A 12.GPC测试得到的分子量与用乌氏粘度计测得的分子量有较大的差别,后者所得的分子量称为: A. 数均分子量Mn
实验报告 实验课程:DSP原理及应用 学生姓名: 学号: 专业班级: 2012年 5月 25日
目录 实验一定点除法运算 实验二FIR滤波器 实验三FFT算法 实验四卷积计算 实验五数码管显示 实验六语音录放
实验一定点除法运算 一、实验目的 1、熟悉C54指令系统,掌握常用汇编指令,学会设计程序和算法的技巧。 2、学习用指令实现除法运算。 二、实验设备 计算机;DSP 硬件仿真器;DSP 实验开发平台。 三、实验原理 由内置的硬件模块支持,数字信号处理器可以高速的完成加法和乘法运算。但TMS320 系列DSP不提供除法指令,为实现除法运算,需要编写除法子程序来实现。二进制除法是乘法的逆运算。乘法包括一系列的移位和加法,而除法可分解为一系列的减法和移位。本实验要求编写一个16 位的定点除法子程序。 1.除法运算的过程设累加器为8 位,且除法运算为10 除以3,除的过程包括与除数有关的除数逐步移位,然后进行减法运算,若所得商为正,则在商中置1,否则该位商为0 例如:4 位除法示例:(1)数的最低有效位对齐被除数的最高有效位00001010 - 00011000 11110010 (2)由于减法结果为负,丢弃减法结果,将被除数左移一位再减00010100 - 00011000 11111000 (3)结果仍为负,丢弃减法结果,将被除数左移一位再减00101000 - 00011000 00010000 (4)结果为正,将减法结果左移一位后把商置1,做最后一次减00100001 - 00011000 00001001 (5)结果为正,将减法结果左移一位加1 得最后结果,高4 位是余数,低4 位商:00010011 2.除法运算的实现为了尽量提高除法运算的效率,’C54x 系列提供了条件减指令SUBC 来完成除法操作。 四、实验步骤 1.用Simulator 方式启动Code Composer。 2 .执行Project New 建立新的项目,输入chuf作为项目的名称,将程序定位在D:\ti\myprojects\chuf目录。 3.执行File New Source File 建立新的程序文件,为创建新的程序文件命名为chuf.asm 并保存;执行Project Add Files to Project,把chuf.asm 加入项目中。4.执行File New Source File 建立新的文件并保存为chuf.cmd;执行Project Add Files to Project,把chuf.cmd 加入项目中。 5.编辑chuf.asm 加入如下内容: ;*** 编制计算除法运算的程序段。其中|被除数|<|除数|,商为小数*** .title "chuf.asm" .mmregs .def start,_c_int00
实验1 平衡溶胀法测定交联聚合物的溶度参数与交联度 溶度参数是与物质的内聚能密度有关的热力学参数,实际上也是表征分子间作用力的物理量。在高分子溶液性质的研究中以及生产实际中,常常凭借溶度参数来判断非极性体系的互溶性。例如,溶度参数对聚合物的溶解、油漆和涂料的稀释、胶黏剂的配制、塑料的增塑、聚合物的相容性、纤维的溶液纺丝等等,都有一定的参考价值。 对于交联聚合物,与交联度直接相关的有效链平均分子量 C M 是一个重要的结构参数,C M 的大小对交联聚合物的物理机械性能具有很大的影响。 因此,测定和研究聚合物的溶度参数与交联度十分重要,平衡溶胀法是间接测定交联聚合物的溶度参数与有效链平均分子量 C M 的一种简单易行的方法。另外还可间接测得高分子-溶剂的相互作用参数1x 。 一、实验目的: (1)了解溶胀法测聚合物溶度参数及 C M 的基本原理。 (2)掌握重量法测交联聚合物溶胀度的实验技术。 (3)粗略地测出交联聚合物的溶度参数、C M 及1x 。 二、实验原理: 聚合物的溶度参数不像低分子化合物可直接从汽化热测出,因为聚合物分子间的相互作用能很大,欲使其汽化,势必裂解为小分子,所以只能用间接的方法测定,平衡溶胀法是其中的一种方法。交联结构的聚合物不能为溶剂所溶解,但能吸收大量的溶剂而溶胀。溶胀过程中,溶剂分子渗入聚合物内使体积膨胀,以致引起三维分子网的伸展,而分子网受到应力产生了弹性收缩力,阻止溶剂进入网状链。当这两种相反的倾向相互抵消时,即溶剂分子进入交联网的速度与被排出的速度相等,就达到了溶胀平衡态。 溶胀的凝胶实际上是聚合物的溶解液,能溶胀的条件与线性聚合物形成溶液相同。根据热力学原理,聚合物能够在液体中溶胀的必要调节是混合自由能 m F <0 ,而
高分子材料成型加工及性能测试 一、实验目的 应用《高分子物理》、《高分子材料工艺学》、《高分子材料成型与加工》所学的理论知识,进行高分子材料压制成型和注射成型实验,制得的高分子材料试样进行性能测试与分析。通过本实验,掌握常用塑料的压制成型和注射成型工艺流程,了解影响塑料制品性能的因素,初步锻炼学生对高分子材料成型加工方法的实践能力以及对实验数据的综合分析能力。 二、实验内容 1、塑料压制成型: (1)熟练操作开炼机、高速混合机、平板硫化仪成型设备,操作步骤见附录1; (2)制备出塑料试样。 2、塑料注射成型: (1)了解实验设备的基本结构,工作原理和操作要点,操作步骤见附录2; (2)了解注射成型设备对制品性质的影响; (3)掌握如何根据聚合物的性质,确定注射成型机料筒温度和模具温度; (4)制备出塑料试样。 3、塑料制品拉伸性能测试: (1)掌握电子拉力机测定塑料拉伸试样的基本操作,操作步骤见附录3; (2)依据应力-应变曲线,计算出各种力学参数(拉伸强度、断裂伸长率、断裂强度)。 4、塑料制品硬度测试:利用邵氏A型硬度计测定试样的硬度,操作步骤见附录4; 5、塑料制品导电性测试:利用高阻仪测定试样的表面电阻。测试时,将充分放电后的试样,接入仪器测量端,调整仪器,加上实验电压一分钟,读取电阻的指示值。 三、实验原理 大多数高分子材料(尤其是热塑性塑料)可以通过压制和注射成型。 压制是板材成型的重要方法,其工艺过程包括下列工序:(1)混合:按照一定配方称量各组分,按照一定的加料顺序,将各组分加入到高速分散机中进行几何分散;(2)双辊塑炼拉片:用双辊开炼机使混合物料熔融混合塑化,得到片材;(3)压制:把片材放入恒温压制模具中预热、加温、加压,使片材熔融塑化,然后冷却定型成板材。正确选择和调节压制温度、压力、时间以及制品的冷却程度是控制板材性能的工艺措施。通常在不影响制品性能的前提下,适当提高压制温度,降低成型压力,缩短成型周期对提高生产效率是行之有效的;但过高的温度、过长的加热时间会加剧树脂降解和熔料外溢,致使制品的各方面性能变劣。 注射成型亦称注射模塑或注塑,是热塑性塑料的一种重要成型方法。注射成型是将塑料(一般为粒料)在注射成型机的料筒内加热溶化,当呈流动状态时,熔融塑料在柱塞或螺杆的加压下被压缩并向前移动,进而通过塑料筒前端的喷嘴以很快的速度注入温度较低的闭合
目录 实验装置介绍 (1) 实验一一、二阶系统阶跃响应 (2) 实验二控制系统稳定性分析 (5) 实验三系统频率特性分析 (7) 实验四线性系统串联校正 (9) 实验五 MATLAB及仿真实验 (12)
实验装置介绍 自动控制原理实验是自动控制理论课程的一部分,它的任务是:一方面,通过实验使学生进一步了解和掌握自动控制理论的基本概念、控制系统的分析方法和设计方法;另一方面,帮助学生学习和提高系统模拟电路的构成和测试技术。 TAP-2型自动控制原理实验系统的基本结构 TAP-2型控制理论模拟实验装置是一个控制理论的计算机辅助实验系统。如上图所示,TAP-2型控制理论模拟实验由计算机、A/D/A 接口板、模拟实验台和打印机组成。计算机负责实验的控制、实验数据的采集、分析、显示、储存和恢复功能,还可以根据不同的实验产生各种输出信号;模拟实验台是被控对象,台上共有运算放大器12个,与台上的其他电阻电容等元器件配合,可组成各种具有不同系统特性的实验对象,台上还有正弦、三角、方波等信号源作为备用信号发生器用;A/D/A 板安装在模拟实验台下面的实验箱底板上,它起着模拟与数字信号之间的转换作用,是计算机与实验台之间必不可少的桥梁;打印机可根据需要进行连接,对实验数据、图形作硬拷贝。 实验台由12个运算放大器和一些电阻、电容元件组成,可完成自动控制原理的典型环节阶跃响应、二阶系统阶跃响应、控制系统稳定性分析、系统频率特性测量、连续系统串联校正、数字PID 、状态反馈与状态观测器等相应实验。 显示器 计算机 打印机 模拟实验台 AD/DA 卡
实验一一、二阶系统阶跃响应 一、实验目的 1.学习构成一、二阶系统的模拟电路,了解电路参数对系统特性的影响;研究二阶系统的两个重要参数:阻尼比ζ和无阻尼自然频率ωn对动态性能的影响。 2.学习一、二阶系统阶跃响应的测量方法,并学会由阶跃响应曲线计算一、二阶系统的传递函数。 二、实验仪器 1.自动控制系统实验箱一台 2.计算机一台 三、实验原理 模拟实验的基本原理: 控制系统模拟实验采用复合网络法来模拟一、二阶系统,即利用运算放大器不同的输入网络和反馈网络模拟一、二阶系统,然后按照给定系统的结构图将这些模拟环节连接起来,便得到了相应的模拟系统。再将输入信号加到模拟系统的输入端,并利用计算机等测量仪器,测量系统的输出,便可得到系统的动态响应曲线及性能指标。 若改变系统的参数,还可进一步分析研究参数对系统性能的影响。 四、实验内容 构成下述系统的模拟电路,并测量其阶跃响应: 1.一阶系统的模拟电路如图
第二章高分子合成实验 (2) 实验一聚乙烯醇缩甲醛的制备 (2) 实验二苯乙烯的聚合方法综合实验 (4) 实验三甲基丙烯酸甲酯的本体聚合 (9) 实验四水溶性酚醛树脂制备及性能测定 (10) 实验五酚醛树脂的合成 (15) 实验六水性丙烯酸树脂的合成 (17) 实验七醋酸乙烯酯的乳液聚合 (18) 实验八膨胀计法测定苯乙烯聚合反应速率 (21) 实验九甲基丙烯酸甲酯、苯乙烯悬浮共聚合 (26) 实验十乙酸乙烯酯的溶液聚合 (28) 实验十一丙烯酰胺水溶液聚合 (30) 实验十二低分子量聚丙烯酸(钠盐)的合成和分析 (32) 实验十三熔融缩聚反应制备尼龙-66 (34) 实验十四ε-己内酰胺缩聚制备尼龙6 (37) 实验十五强酸型阳离子交换树脂的制备及其交换量的测定 (39) 实验十六苯丙乳液的制备 (43)
第二章高分子合成实验 实验一聚乙烯醇缩甲醛的制备 一、实验目的 1、加深对高分子化学反应基本原理的理解。 2、了解缩醛化反应的主要影响因素。 3、掌握聚乙烯醇缩甲醛的制备方法. 二、实验原理 早在1931年,人们已经研制出聚乙烯醇的纤维,但由于PVA的水溶性而无法实际应用。利用“缩醛化”减少水溶性,使PVA 有了较大的实际应用价值。目前,聚乙烯醇缩醛树脂在工业上被广泛用于生产黏合剂、涂料、化学纤维。品种主要有聚乙烯醇缩甲醛、聚乙烯醇缩乙醛、聚乙烯醇缩甲乙醛、聚乙烯醇缩丁醛等。其中以聚乙烯醇缩甲醛和聚乙烯醇缩丁醛最为重要。前者是化学纤维“维尼纶”和“107”建筑胶水的主要原料,后者可用于制造“安全玻璃”。 聚乙烯醇缩甲醛随缩醛度的不同,性质和用途有所不同,缩醛度在35%左右,就得到人们所称为“维尼纶”的纤维,纤维的强度是棉花的1.5∽2.0倍,吸湿性5%,接近天然纤维,故又称为“合成棉花”,如果控制强度在较低水平,由于聚乙烯醇缩甲醛分子中含有羟基、乙酰和醛基,因此有较强的黏结性能,可用作胶水,用来黏结金属、木材、玻璃、陶瓷、橡胶等。 聚乙烯醇缩甲醛是由聚乙烯醇在酸性条件下与甲醛缩合而成的。其反应方程式如下:
1.红外光谱:分别用 PM3 ,HF/6-31G(d),B3LYP/6-31G(d),MP2/6-31G(d) 四种理论方法计算 H 2O 分子的红外光谱,并比较结果的优劣。实验 上测得的水分子的振动频率为:1594cm 1, 3657cm -1, 3756cm 1。 k(Lore ntz) B3LYP/6-31G(d) 由图像可得四种理论方法得到的振动频率分别为 PM3 1698 cm -1、3770 cm -1、3880 cm -1 HF/6-31G(d) 1634 cm -1、3662 cm -1、3770 cm -1 B3LYP/6-31G(d) 1634 cm -1、3566 cm -1、3662 cm -1 MP2/6-31G(d) 1644 cm -1、3544 cm -1、 3684 cm -1 与标准值1594cm -1, 3657cm'1,3756cm'1比较,HF/6-31G(d)最为接近标准值; PM3三个频率都偏大,与标准值符合情况不好; B3LYP/6-31G(d)除1634 cm -1与 分子模拟实验作业 一、实验部分 分子光谱模拟 k(Lore ntz) -DrnelPL (. 4000 3000 2000 -1 /cm 1000 '! 0.00 0.01 0.02 0.03 0.04 0.05 0.06 4000 3000 2000 1000 /cm -1 PM3 HF/6-31G(d) ------ k(Lore ntz) k(Lore ntz) 0.00 0.01 r 0.04 0.05 J _______ ! ______ ______ J ______ ______ !_ 4000 3000 2000 -1 /cm 1000 MP2/6-31G(d) 0.000 0.002 _ 0.004 0.006 0.008 0.010 0.012 - 0.014 0.02 0.03 - e /cm
高分子科学实验讲义 (内部教材) 高分子教研室
目录 实验一常见塑料和纤维的简易鉴别 (1) 实验二甲基丙烯酸甲酯的本体聚合 (4) 实验三丙烯酰胺的溶液聚合 (6) 实验四苯乙烯的悬浮聚合 (9) 实验五熔融缩聚反应制备尼龙-66 (12) 实验六聚氨酯泡沫塑料的制备 (16) 实验七热固性脲醛树脂的制备 (19) 实验八膨胀计法测定高聚物的玻璃化转变温度 (22) 实验九用偏光显微镜研究聚合物结晶形态 (25) 实验十粘度法测定聚合物的分子量 (28) 实验十一差示扫描量热法(DSC)测定聚合物热性能 (33) 实验十二、热失重法(TGA)测定聚合物的热稳定性 (41) 实验十三DMA测定高聚物的动态力学性能 (44) 实验十四用扫描电子显微镜观察聚合物形态 (48) 实验十五高聚物熔融指数的测定 (51) 实验十六高聚物熔体流变特性的测定 (54)
综合性、设计性实验 (61) 实验十七改性苯丙乳液的合成与性能分析 (63) 实验十八丙烯酸脂类压敏胶的制备与性能测试 (68)
实验一常见塑料和纤维的简易鉴别 一、实验目的 1.了解聚合物燃烧试验和气味试验的特殊现象,借以初步辨认各种聚合物。 2.利用聚合物溶解的规律及溶剂选择的原则,了解并掌握溶解法对常见聚合物的定性分析。 二、基本原理 聚合物的鉴别,特别对未知聚合物试样的鉴别颇为复杂,即使经纯化处理的聚合物也很难用单一的方法进行鉴别。常见聚合物通常可用红外、质谱、X 光衍射、气相色谱等仪器进行不同程度的定性和定量分析。而基于聚合物的特性简单地通过外观、在水中的浮沉、燃烧、溶解性和元素分析的方法进行实验室的鉴别则方便易行。 1.根据试样的表观鉴别 HDPE、PP、PA 66、PA 6、PA1010质硬,表面光滑。LDPE、PVF、PA11质较软,表面光滑,有蜡状感觉。硬PVC、PMMA表面光滑,无蜡状感觉。PS质硬,敲打会发出清脆的“打铃声”。 2.根据试样的透明程度鉴别 透明的聚合物:聚丙烯酸酯类,聚甲基丙烯酸酯类,再生纤维素,纤维素酯类和醚类,聚甲基戊烯类,PC、PS,PVC及其共聚物。半透明的聚合物:尼龙类,PE,PP,缩醛树脂类。透明性往往与样品的厚薄,结晶性,共聚物某些成分的含量等有关。如:EV A中VC的含量大于15%可以从半透明变为透明。半透明的聚合物在薄时变为透明。加入填料共混后,透明聚合物变为不透明。结晶可使透明聚合物变为半透明。 3.根据聚合物燃烧试验的火焰及气味鉴别
高分子成型加工实验讲义 材料科学与工程学院 2010年3月
实验一塑料板材挤出实验 一、实验目的 1.了解塑料板材挤出成型工艺过程; 2.认识狭缝挤出机头的结构和工作原理; 3.理解并掌握板材挤出及压光工艺控制方法; 4.掌握塑料板材的性能测试方法。 二、实验原理 挤出压延成型是生产塑料板材的主要方法之一。塑料板材的成型是用狭缝机头直接挤出板坯后,即经过三辊压光机压光,经冷却、牵引装置而得到塑料板材。 图1-1为聚乙烯(PE)板材挤出工艺流程图。本实验是挤出2.0mm的LDPE板材。 图1-1 PE 板材挤出生产工艺流程图 1-电动机2-料斗3-螺杆4-挤出机料筒5-机头6-三辊压光机7-橡胶牵引辊8-剪切1.PE 原料 PE板材具有无毒、表面光滑平整、耐腐蚀、电绝缘性能优异、低温性能好的优点,广泛应用在包装、化工、电子等领域。PE 挤出板材一般选用适当牌号的树脂直接生产,如果生产特殊用途的片材需添加相关必要的助剂。挤出生产LDPE 板材应选用熔体流动速率(MFR)为0.3~1.0(g/10min)的挤出级PE 树脂。 2.机头 板材挤出的狭缝机头的出料口既宽又簿,塑料熔体由料筒挤入机头,流道由圆形变成狭缝形,这种机头(包括支管型、衣架型、鱼尾型)在料流挤出过程中存在中间流程短、阻力小、流速快,两边流程长、阻力大、流速慢的现象,必须采取措施使熔体沿口模宽度方向有均匀的速度分布,即要使熔体在口模宽度方向上以相同的流速挤出,保证挤出的板材厚度均匀和表面平整。本实验采用支管型机头,可以贮存一定量的物料,起分配物料稳定作用,使料流稳定。 3.三辊压光机 作用是将挤出的板材压光和降温,并准确地调整板材的厚度,故它与压延机的构造原理有点相同,对辊筒的尺寸精度和光洁度要求较高,并能在一定范围内可调速,能与板材挤出相适应。辊筒间距可以调整,以适应挤出板材厚度的控制,压光机与机头的距离应尽量靠近,否则板坯易下垂发皱,光洁度不好,同时在进入压光机前容易散热降温,对制品光洁度不利。 4.温度 挤出机各段温度的设定因原料品种而异,对LDPE,从挤出机加料段至均化段各区(一般为四个区)的温度分别为:150℃~160℃,160℃~170℃,170℃~180℃,180℃~190℃。机头温度原则上高于挤出机均化段5℃~10℃,机头温度过低,板材表面无光泽,甚至导致板材开裂,机头温度过高,物料易分解。机头温度通常采用两边高中间低的温度控制方法,以便和机头阻力调节棒相配合,保证当熔体通过机头的时候,沿板材宽度方向上流动速率与温度相平衡,板材的挤出均匀、稳定。对LDPE,从机头左至右温度分别为:190℃~200℃,180℃~190℃,170℃~180℃,180℃~190℃,190℃~200℃。从机头出来的板坯温度较高,为防止板材产生内应力而翘曲,应使板材缓慢冷却,要求压光机的辊筒有一定的温度。三辊压光机的温度为:上辊85℃~95℃,中辊75℃~85℃,下辊65℃~75℃。经压光机定型为一定厚度的板材温度仍较高,故用冷却导辊输送板材,让其进一步冷却,最后成为接近室温的板材。
脲醛树脂的制备 一、实验目的 加深理解缩合聚合的反应机理,了解脲醛树脂的合成方法。 二、实验原理 脲醛树脂是由尿素和甲醛经缩聚反应制得的热固性树脂。 加成反应:生成多种羟甲基脲的混合物。 H2NCH2NC+H C H HOCH2NH C NH 2 O 缩合反应:或HOCH 2 NH C O NH CH2OH HOCH2NH + HOCH2NH2-H2O HOCH 2 N CH2 NH C O C O C O C O NH2NH2NH 2NH2 也可以在羟甲基与羟甲基间脱水缩合: NH CH 3 OH+ HOCH2NH2NH CH2 O CH2NH2NH CH2 NH C O C O C O C O C O C O NH2NHCH 2 OH NH2NHCH2OH NH2NHCH2OH 此外,还有甲醛与亚氨基间的缩合均可生成低相对分子质量的线型和低交联度的脲醛树脂: NH 2 NH CH 2+HCHO2 N CH2 CH2 N CH2
脲醛树脂的结构尚未完全确定,可认为其分子主链上还有以下结构: NH CH2 C O CH2OH N CH2 C O NH2 N CH2 C O NH2 N C O NHCH2OH 上述中间产物中含有易溶于水的羟甲基,可作胶黏剂使用,当进一步加热,或者在固化剂作用下,羟甲基与氨基进一步缩合交联成复杂的网状体型结构。 CH2 N CH 2 CO N CH2 N CH 2 CO N CH2 N CH 2N CH2 O N CO CO N CH2OH 三、实验仪器和试剂 实验仪器:电动搅拌器、水浴、三口瓶(250mL)、球形冷凝器(30cm)、温度计、量筒(100mL)、pH试纸。实验试剂:新鲜的甲醛水溶液(37%)、尿素、10%氢氧化钠水溶液、氨水、10%甲酸水溶液。 四、实验步骤 在250mL三口瓶上分别安装搅拌器、温度计、球形冷凝器; 用100mL量筒量取甲醛水溶液60mL,加入三口瓶中,开动搅拌器同时用水浴缓慢加热,然后用10%NaOH水溶液调节甲醛水溶液,使甲醛水溶液的pH值介于8~8.5之间; 分别称取尿素三份,质量分别是11.2g,5.6g,5.6g,先将11.2g尿素加入三口瓶中,搅拌至溶解,温度升高到60℃,开始计时,不断调整反应体系的pH值,使之保持8.5左右,保温反应2~3小时; 升温至80℃,加入5.6g尿素,用10%甲酸水溶液小心调节反应体系的pH值,使之介于5.4~6.0之间,继续反应1~1.5h,在此过程中不断的用胶头滴管吸取少量脲醛胶液滴入冷水中,观察胶液在冷水中是否出现雾化现象; 出现雾化现象后,加入剩余的5.6g尿素,用氨水调节反应体系的pH值,使之介于7.0~ 7.5之间,在80℃下继续反应直至在温水中出现雾化现象,即在此过程中不断用胶头滴管吸取少量脲醛胶液滴入约40℃的温水中,观察胶液在温水中是否还会出现雾化现象; 温水中出现雾化现象后,立即降温到40℃左右,终止反应,并用氨水调节脲醛胶的pH =7,再用10%NaOH调节pH=8.5~9,正常情况下得到澄清透明脲醛胶。 五、注意事项 (1)用甲酸溶液调节反应体系pH 值时要十分小心,切忌酸度过大。因为缩合反应速度在pH=3~5之间几乎正比于[H+];
高分子科学实验 材料科学与工程学院 高分子教研室 2015-01-01
(一)高分子化学实验目录实验一甲基丙烯酸甲酯的本体聚合 实验二界面聚合 实验三乙酸乙烯酯的乳液聚合 实验四乙酸乙烯酯的溶液聚合 实验五聚乙酸乙烯酯的碱解 实验六聚乙烯醇的缩甲醛反应 实验七苯乙烯悬浮聚合 实验八强酸离子交换树脂的合成及性能测定实验九 -氰基丙烯酸酯的阴离子聚合 实验十植物废弃物中提取果胶 实验十一丙烯酰胺溶液聚合
实验一甲基丙烯酸甲酯的本体聚合 一、目的要求 1.认识并了解本体聚合及其反应原理 2.了解反应速度与引发剂用量及反应温度的关系 二、基本原理 本体聚合又称为块状聚合,它是在没有任何介质的情况下,单体本身在微量引发剂的引发下聚合,或者直接在热、光、辐射线的照射下引发聚合。本体聚合的优点是: 生产过程比较简单,聚合物不需要后处理,可直接聚合成各种规格的板、棒、管制品,所需的辅助材料少,产品比较纯净。但是,由于聚合反应是一个链锁反应,反应速度较快,在反应某一阶段出现自动加速现象,反应放热比较集中;又因为体系粘度较大,传热效率很低,所以大量热不易排出,因而易造成局部过热,使产品变黄,出现气泡,而影响产品质量和性能,甚至会引起单体沸腾爆聚,使聚合失败。因此,本体聚合中严格控制不同阶段的反应温度,及时排出聚合热,乃是聚合成功的关键问题。 当本体聚合至一定阶段后,体系粘度大大增加,这时大分子活性链移动困难,但单体分子的扩散并不受多大的影响,因此,链引发、链增长仍然照样进行,而链终止反应则因为粘度大而受到很大的抑制。这样,在聚合体系中活性链总浓度就不断增加,结果必然使聚合反应速度加快。又因为链终止速度减慢,活性链寿命延长,所以产物的相对分子质量也随之增加。这种反应速度加快,产物相对分子质量增加的现象称为自动加速现象(或称凝胶效应)。反应后期,单体浓度降低,体系粘度进一步增加,单体和大分子活性链的移动都很困难,因而反应速度减慢,产物的相对分子质量也降低。由于这种原因,聚合产物的相对分子质量不均一性(相对分子质量分布宽)就更为突出,这是本体聚合本身的特点所造成的。 对于不同的单体来讲,由于其聚合热不同、大分子活性链在聚合体系中的状态(伸展或卷曲)的不同;凝胶效应出现的早晚不同、其程度也不同。并不是所有单体都能选用本体聚合的实施方法,对于聚合热值过大的单体,由于热量排出更为困难,就不易采用本体聚合,一般选用聚合热适中的单体,以便于生产操作的控制。甲基丙烯酸甲酯和苯乙烯的聚合热分别为56.5 kJ/mol和69.9 kJ/mol,它们的聚合热是比较适中的,工业上已有大规模的生产。大分子活性链在聚合体系中的状态,是影响自动加速现象出现早晚的重要因素,比如,在聚合温度50 ℃时,甲基丙烯酸甲酯聚合出现自动加速现象时的转化率为10%~15%,而苯乙烯在转化率为30%以上时,才出现自动加速现象。这是因为甲基丙烯酸甲酯对它的聚合物或