大肠埃希氏菌检验原始记录
- 格式:doc
- 大小:38.00 KB
- 文档页数:1

文件编号:************
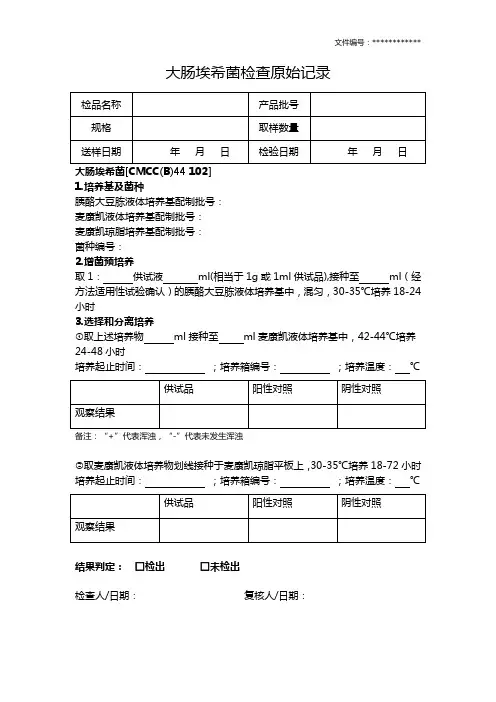
大肠埃希菌检查原始记录
1.培养基及菌种
胰酪大豆胨液体培养基配制批号: 麦康凯液体培养基配制批号: 麦康凯琼脂培养基配制批号: 菌种编号: 2.增菌预培养
取1: 供试液 ml(相当于1g 或1ml 供试品),接种至 ml (经方法适用性试验确认)的胰酪大豆胨液体培养基中,混匀,30-35℃培养18-24小时
3.选择和分离培养
①取上述培养物 ml 接种至
ml 麦康凯液体培养基中,42-44℃培养24-48小时
培养起止时间: ;培养箱编号: ;培养温度: ℃ 备注:“+”代表浑浊,“
-”代表未发生浑浊
②取麦康凯液体培养物划线接种于麦康凯琼脂平板上,30-35℃培养18-72小时 培养起止时间: ;培养箱编号: ;培养温度: ℃ 结果判定: □检出 □未检出
检查人/日期: 复核人/日期:。

大肠埃希氏菌生化鉴定结果大肠埃希氏菌(Escherichia coli)是一种常见的细菌,可以引起多种感染性疾病,包括腹泻、尿路感染和食物中毒等。
鉴定大肠埃希氏菌的生化特征可以帮助确定病原菌的身份以及其潜在的耐药性和毒力因子。
本次实验目的是对一株致病性大肠埃希氏菌样本进行生化鉴定,以确认其菌株的性质和特征。
首先,我们进行了气体产生实验。
在Triple Sugar Iron Agar(TSI)培养基中,观察到菌落周围发生了气体产生,此结果表明该菌株具有产气性。
产气性通常意味着大肠杆菌等需要葡萄糖产生酸,进而分解产生气体的细菌。
其次,我们进行了甲烷发酵试验。
在Methyl Red(MR)试剂中,当菌液发酵产酸时,溶液颜色由黄色变成红色。
然而,该菌株在MR试剂中没有产生红色反应,这表明它无法通过甲烷发酵产酸。
这一结果与典型的大肠杆菌不同,因为大肠杆菌通常可以通过此途径产酸。
进一步,我们进行了亮氨酸脱氨酶试验。
使用亮氨酸脱氨酶(LDC)培养基,如果菌株具有亮氨酸脱氨酶活性,菌液会变色。
然而,我们观察到该菌株在培养基中没有出现任何颜色变化,这表明它不具备亮氨酸脱氨酶活性。
亮氨酸脱氨酶活性通常是大肠杆菌的典型特征之一。
此外,我们还进行了尿素酶试验。
使用尿素平板培养基,如果菌株具有尿素酶活性,培养基颜色将由黄色变为粉红色。
然而,我们观察到该菌株在培养基上未显示出任何颜色变化。
这暗示着该菌株可能缺乏尿素酶活性,与大肠杆菌的典型特征不同。
最后,我们进行了青霉素酶试验。
使用青霉素酶试纸进行反应检测,在试纸上出现蓝色点状斑点表示菌株具有青霉素酶活性。
而对于这个菌株,我们观察到在试纸上没有出现蓝色斑点。
这意味着该菌株可能对青霉素类药物敏感,这对于抗生素选择治疗提供了重要信息。
综上所述,通过对致病性大肠埃希氏菌样本进行生化鉴定,我们发现该菌株具有产气性,但与典型的大肠杆菌不同,它不表现出甲烷发酵、亮氨酸脱氨酶和尿素酶活性。

品名: 批号: 检验日期:
二、大肠埃希菌检查按ZLSOP 微生物限度检查操作规程检查
供试液制备和增菌培养
取本品加无菌氯化钠-蛋白胨缓冲液(配制批号: )至100 ml,
用匀浆仪混匀,即得1:10供试液;取相当于1g或1ml供试品的供试液接种至
ml的胰酪大豆胨液体培养基(配制批号: )中,混匀,培养温度℃,
培养24小时,培养箱型号: 培养箱编号wxzl 。
选择和分离培养
取上述培养物1ml接种至100 ml麦康凯液体培养基(配制批号: )中,
培养温度℃,培养小时,培养箱型号: 培养箱编号
wxzl ;取麦康凯液体培养物划线接种于麦康凯琼脂培养基(配制批
号: )平板上,培养温度℃,培养72小时,培养箱编号wxzl 。
阳性对照试验
同供试品的大肠埃希菌检查,对照菌的加量不大于100cfu,(大肠埃希菌菌
种来源:,大肠埃希菌菌种编号:)
阴性对照试验
以pH 无菌氯化钠-蛋白胨缓冲液代替供试液按大肠埃希菌检查法检查,结
果见下表:
注: +代表麦康凯琼脂平板上有菌落生长,—代表麦康凯琼脂平板
上无菌落生长。
结论 :
检验人: 日期: 复核人: 日期:。
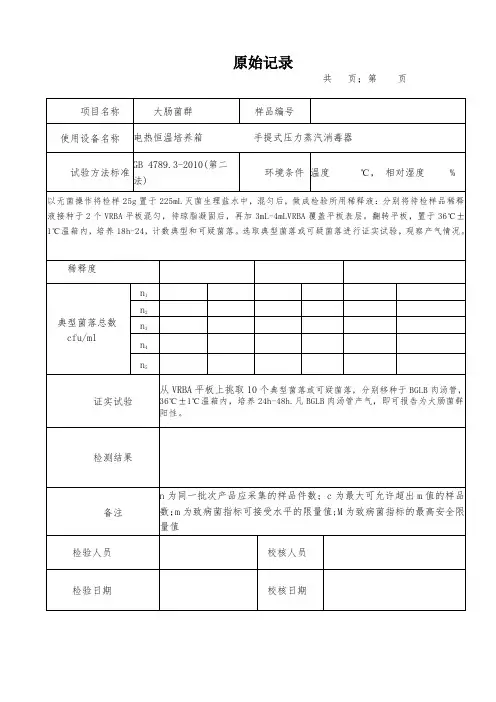
原始记录
共页;第页项目名称大肠菌群样品编号
使用设备名称电热恒温培养箱手提式压力蒸汽消毒器
试验方法标准GB 4789.3-2010(第二
法)
环境条件温度℃,相对湿度 %
以无菌操作将检样25g置于225mL灭菌生理盐水中,混匀后,做成检验所用稀释液:分别将待检样品稀释液接种于2个VRBA平板混匀,待琼脂凝固后,再加3mL-4mLVRBA覆盖平板表层。
翻转平板,置于36℃±1℃温箱内,培养18h-24,计数典型和可疑菌落。
选取典型菌落或可疑菌落进行证实试验,观察产气情况。
稀释度
典型菌落总数cfu/ml n 1
n 2
n 3
n 4
n 5
证实试验从VRBA平板上挑取10个典型菌落或可疑菌落,分别移种于BGLB肉汤管,36℃±1℃温箱内,培养24h-48h.凡BGLB肉汤管产气,即可报告为大肠菌群阳性。
检测结果
备注n为同一批次产品应采集的样品件数;c为最大可允许超出m值的样品数;m为致病菌指标可接受水平的限量值;M为致病菌指标的最高安全限量值
检验人员校核人员检验日期校核日期。
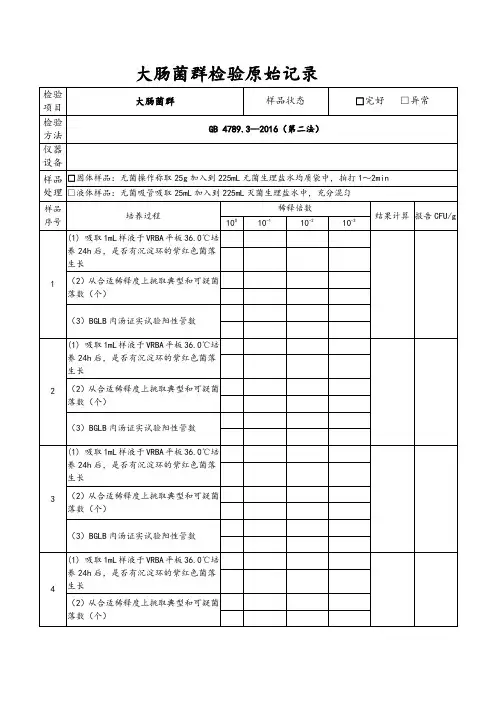
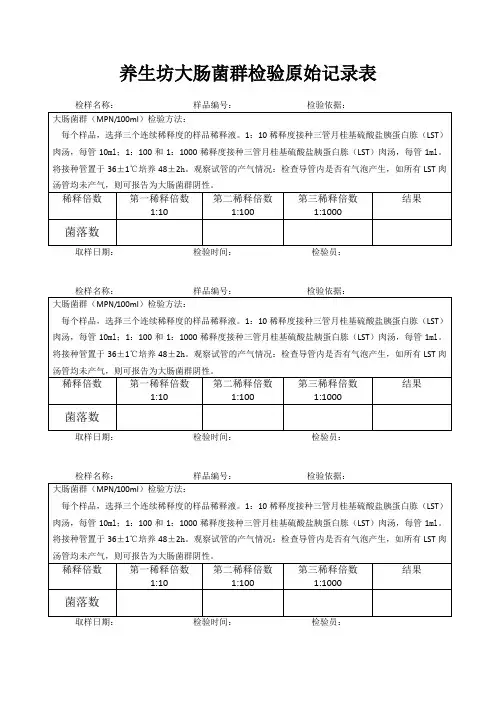
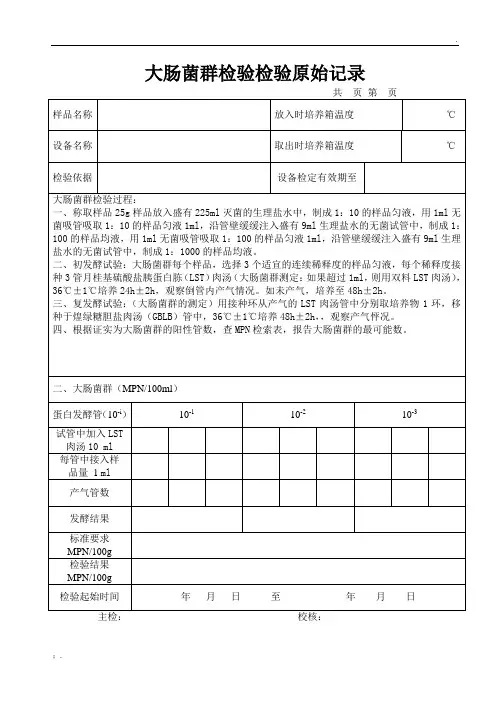
养生坊大肠菌群检验原始记录表检样名称:样品编号:检验依据:大肠菌群(MPN/100ml)检验方法:每个样品,选择三个连续稀释度的样品稀释液。
1:10稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管10ml;1:100和1:1000稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管1ml。
将接种管置于36±1℃培养48±2h。
观察试管的产气情况:检查导管内是否有气泡产生,如所有LST肉汤管均未产气,则可报告为大肠菌群阴性。
稀释倍数第一稀释倍数1:10 第二稀释倍数1:100第三稀释倍数1:1000结果菌落数取样日期:检验时间:检验员:检样名称:样品编号:检验依据:大肠菌群(MPN/100ml)检验方法:每个样品,选择三个连续稀释度的样品稀释液。
1:10稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管10ml;1:100和1:1000稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管1ml。
将接种管置于36±1℃培养48±2h。
观察试管的产气情况:检查导管内是否有气泡产生,如所有LST肉汤管均未产气,则可报告为大肠菌群阴性。
稀释倍数第一稀释倍数1:10 第二稀释倍数1:100第三稀释倍数1:1000结果菌落数取样日期:检验时间:检验员:检样名称:样品编号:检验依据:大肠菌群(MPN/100ml)检验方法:每个样品,选择三个连续稀释度的样品稀释液。
1:10稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管10ml;1:100和1:1000稀释度接种三管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管1ml。
将接种管置于36±1℃培养48±2h。
观察试管的产气情况:检查导管内是否有气泡产生,如所有LST肉汤管均未产气,则可报告为大肠菌群阴性。
稀释倍数第一稀释倍数1:10 第二稀释倍数1:100第三稀释倍数1:1000结果菌落数取样日期:检验时间:检验员:。

XX公司
食品微生物检验记录
检品编号:检品名称:
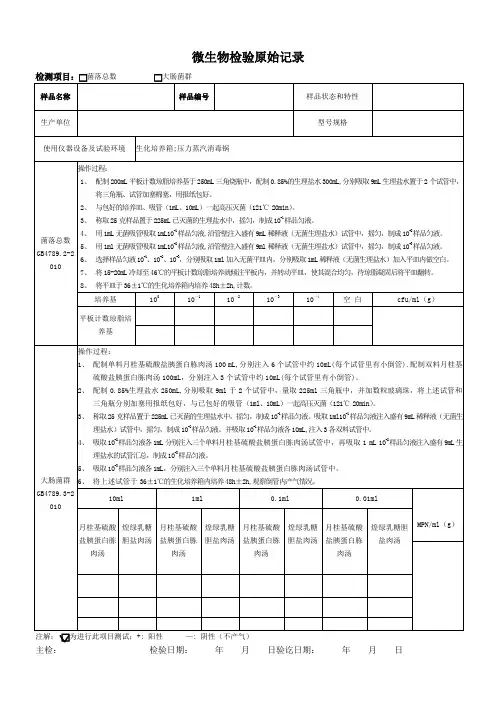
【大肠菌群】按GB 4789.3-2010第二法平板计数法进行检验
环境条件:温度:湿度:
仪器设备:超净工作台编号:;培养箱(36℃±1℃)编号:
电子天平编号:
培养基与试剂:(配制日期:年月日)
①结晶紫中性红胆盐琼脂(VRBA);②无菌生理盐水;③煌绿乳糖胆盐(BGLB)肉汤
样品操作
取 5 份独立包装的样品,分别取()、、、、做为测试样品,按如下述操作,测得结果;
每份测试样品加入225 mL无菌生理盐水,均质,制成1:10样品均液(调节pH值为6.5~7.5),吸取 1 mL(1:10)样品均液至9 mL灭菌生理盐水中做10倍递增稀释。
选、和稀释液检测,培养基为结晶紫中性红胆盐琼脂(VRBA),℃,培养h(从月日: 到月日: ),
挑选10个不同类型典型和可疑菌落,接种煌绿乳糖胆盐(BGLB)肉汤管,℃培养h(从月日: 到月日: )。
标准规定:(标准号:)
n=5 c= m= CFU/g(mL)M= CFU/g(mL)结论:□符合规定□不符合规定
检验者:复核者:检验日期:。
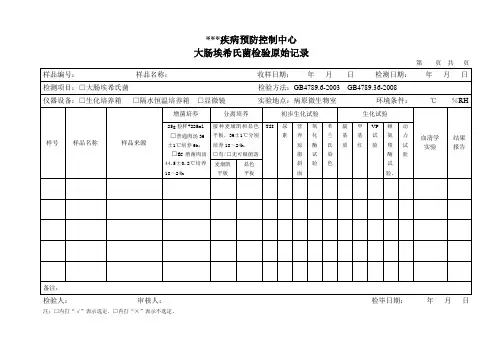
食品中大肠埃希氏菌检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:大肠埃希氏菌检测依据:GB4789.38-2012一、MPN计数法(第一法):1.样品稀释:无菌操作称(量)取样品25g加入盛有225ml的无菌磷酸盐缓冲液的无菌均质杯中,8000r/min~10000r/min均质2分钟,做成1∶10样品液;若样品为液态,吸取25ml 样品至盛有225ml无菌磷酸盐缓冲液的锥形瓶(预置适当数量的无菌玻璃珠)中,震荡混匀,作为1:10的样品匀液。
调样品匀液pH至6.5~7.5。
取1∶10样品匀液1ml加入到盛有9ml磷酸盐缓冲液稀释管中,混匀,做成1∶100样品均液。
根据对样品污染状况的估计,按上述操作,依次制成十倍递增系列稀释样品匀液。
每递增一次,换用1支1ml无菌吸头。
2.初发酵:每个样品,选取3个适宜的连续稀释度的样品匀液(液体样品可选择原液),每个稀释度接种3管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管接种1ml(接种量超过1ml,则用双料LST肉汤),36±1∶培养24±2h,观察倒管内是否有气泡产生,对于24±2h产气者进行复发酵。
对于未产气者,则继续培养48±2h,观察,产气者进行复发酵实验。
如所有LST肉汤管均未产气,即可报告大肠埃希氏菌结果。
3.复发酵:用接种环从产气的LST肉汤管中分别取培养物1环,移种于提前预温至45∶EC 肉汤管中,放入带盖的44.5±0.2∶水浴箱中。
水浴的水面应高于肉汤培养基页面,培养24±2h,检查小导管是否有气泡产生,如未有气泡产生则继续培养至48±2h。
记录24h和48h内产气的EC肉汤产气管数,如所有EC肉汤管均为产气,即可报告大肠埃希氏菌MPN结果;如有产气,则进行EMB平板分离。
4.EMB平板分离:用接种环取培养物分别划线接种于EMB平板,36±1∶培养18~24h,观察平板上有无具有黑色中心光泽或无光泽的典型菌落。
XXXX检测有限公司
菌落总数与大肠菌群检验原始记录共页第页
主检:年月日校核:年月日
XXXX检测有限公司
菌落总数和大肠菌群检测原始记录
共页
第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
致病菌检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
共页第页
培养温度:28±1℃培养时间:年月日时 ---年月日时:
菌落计数:
培养温度:28±1℃培养时间:年月日时 --- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
菌落总数与大肠菌群检验原始记录
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
水质微生物检验原始记录
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。