高中化学有机合成路线设计
- 格式:pptx
- 大小:713.60 KB
- 文档页数:36

第2课时 有机合成路线的设计及有机合成的应用1.了解有机合成路线的设计。
2.掌握有机合成的分析方法——逆推法。
(重点) 3.掌握简单有机物的合成。
(重难点)有机合成路线的设计及有机合成的应用1.有机合成路线的设计 (1)正推法①路线:某种原料分子――→碳链的连接官能团的安装目标分子。
②过程:首先比较原料分子和目标化合物分子在结构上的异同,包括官能团和碳骨架两个方面的异同;然后,设计由原料分子转向目标化合物分子的合成路线。
(2)逆推法①路线:目标分子――→逆推原料分子。
②过程:在逆推过程中,需要逆向寻找能顺利合成目标化合物的中间有机化合物,直至选出合适的起始原料。
(3)优选合成路线依据①合成路线是否符合化学原理。
②合成操作是否安全可靠。
③绿色合成绿色合成主要出发点是:有机合成中的原子经济性;原料的绿色化;试剂与催化剂的无公害性。
(4)逆推法设计有机合成路线的一般程序(5)利用逆推法设计苯甲酸苯甲酯的合成路线①合成路线的设计②以甲苯为原料合成苯甲酸苯甲酯的4条路线:a.b.c.d.③评价优选合成路线a路线中由甲苯制取苯甲酸和苯甲醇,较合理。
b、d路线中制备苯甲酸步骤多、成本高,且Cl2的使用不利于环境保护。
c的步骤虽然少,但使用了价格昂贵的催化剂LiAlH4和要求无水操作,成本较高。
2.有机合成的应用(1)有机合成是化学学科中最活跃、最具有创造性的领域之一。
(2)在化学基础研究方面,有机合成也是一个重要的工具。
请设计以乙烯为原料制备乙二酸乙二酯的合成路线。
【提示】[核心·突破]1.有机合成题的解题思路(1)分析碳链的变化:有无碳链的增长或缩短,有无成环或开环。
(2)分析官能团的改变:引入了什么官能团,是否要注意官能团的保护。
(3)读懂信息:题中的信息可能会成为物质转化中的重要一环,因而要认真分析信息中牵涉的官能团(或碳链的结构)与原料、产品或中间产物之间的联系。
(4)可以由原料正向推导产物,也可以从产物逆向推导出原料,也可以从中间产物出发向两侧推导,还可以由原料和产物推导中间产物。

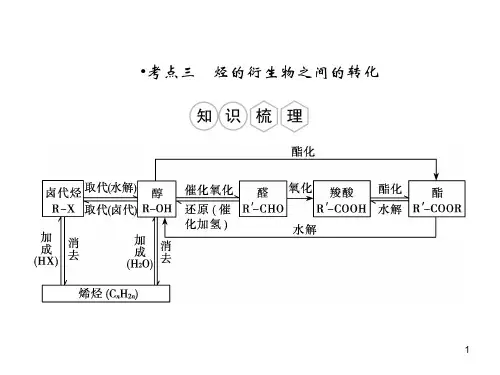
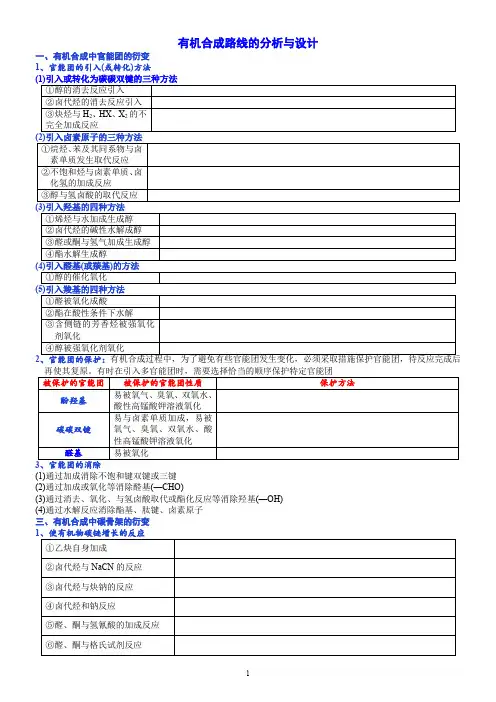
有机合成路线的分析与设计一、有机合成中官能团的衍变1、官能团的引入(或转化)方法(1)引入或转化为碳碳双键的三种方法①醇的消去反应引入②卤代烃的消去反应引入③炔烃与H2、HX、X2的不完全加成反应(2)引入卤素原子的三种方法①烷烃、苯及其同系物与卤素单质发生取代反应②不饱和烃与卤素单质、卤化氢的加成反应③醇与氢卤酸的取代反应(3)引入羟基的四种方法①烯烃与水加成生成醇②卤代烃的碱性水解成醇③醛或酮与氢气加成生成醇④酯水解生成醇(4)引入醛基(或羰基)的方法①醇的催化氧化(5)引入羧基的四种方法①醛被氧化成酸②酯在酸性条件下水解③含侧链的芳香烃被强氧化剂氧化④醇被强氧化剂氧化2、官能团的保护:有机合成过程中,为了避免有些官能团发生变化,必须采取措施保护官能团,待反应完成后再使其复原。
有时在引入多官能团时,需要选择恰当的顺序保护特定官能团被保护的官能团被保护的官能团性质保护方法酚羟基易被氧气、臭氧、双氧水、酸性高锰酸钾溶液氧化碳碳双键易与卤素单质加成,易被氧气、臭氧、双氧水、酸性高锰酸钾溶液氧化醛基易被氧化3、官能团的消除(1)通过加成消除不饱和键双键或三键(2)通过加成或氧化等消除醛基(—CHO)(3)通过消去、氧化、与氢卤酸取代或酯化反应等消除羟基(—OH)(4)通过水解反应消除酯基、肽键、卤素原子三、有机合成中碳骨架的衍变1、使有机物碳链增长的反应①乙炔自身加成②卤代烃与NaCN的反应③卤代烃与炔钠的反应④卤代烃和钠反应⑤醛、酮与氢氰酸的加成反应⑥醛、酮与格氏试剂反应⑦羟醛缩合反应⑧烯烃、炔烃加聚反应⑨苯环与卤代烃反应(傅克反应)⑩苯环与酰卤反应⑪缩聚反应2、使有机物碳链缩短的反应①脱羧反应②氧化反应③水解反应④烃的裂化或裂解反应3、使有机物碳链的成环的反应①二烯烃成环反应(双烯合成)②羟基酸酸的酯化成环③多元羧酸与多元醇的酯化成环④氨基酸的成环⑤二元羧酸与二氨基化合物成环⑥形成环醚4、使有机物碳链的开环的反应①环酯水解开环②环烯烃氧化开环四、有机合成路线的设计与分析1、常见有机物的转化关系2、有机合成路线设计思路3、常见的有机合成路线 (1)一元化合物合成路线:R —CH===CH 2−→−HX R —CH 2—CH 2X ∆−−−→−溶液NaOH R —CH 2—CH 2OH []−→−O R —CH 2—CHO []−→−OR —CH 2—COOH −−−−→−∆醇、浓硫酸、酯 (2)二元化合物合成路线CH 2===CH 2−→−2X CH 2X —CH 2X ∆−−−→−溶液NaOH HOH 2C —CH 2OH []−→−O OHC —CHO []−→−O HOOC —COOH −−−→−一定条件链酯、环酯、聚酯(3)芳香化合物合成路线 ①∆−−−→−溶液NaOH②光照−→−2Cl ∆−−−→−溶液NaOH −−−−→−∆醇、浓硫酸、芳香酯4、有机合成的分析方法(1)正向合成分析法: (2)逆向合成分析法: (3)正、逆合成分析:(4)逆合成分析法设计有机合成路线的思维程序(5)逆向合成分析法应用例析:利用“逆合成分析法”分析由乙烯合成草酸二乙酯的过程逆合成分析思路,概括如下 具体步骤如下5、解决有机合成题的基本步骤第一步:要正确判断合成的有机物属于何种有机物,它带有什么官能团,它和哪些知识、信息有关,它所在的位置的特点等第二步:根据现有原料、信息和有关反应规律,尽可能合理地把目标有机物解剖成若干片段,或寻找官能团的引入、转换、保护方法,或设法将各片段(小分子化合物)拼接衍变,尽快找出合成目标有机物的关键和突破点。


第2课时 有机合成路线的设计与实施题组一 有机合成路线的设计1.(2023·昆明高二检测)由1-氯环己烷()制备1,2-环己二醇()时,需要经过下列哪几步反应( ) A .加成→消去→取代 B .消去→加成→取代 C .取代→消去→加成D .取代→加成→消去2.根据下面合成路线判断烃A 为( )A(烃类)――→Br 2B ――――――→NaOH 的水溶液△C ―――――→浓H 2SO 4△,-H 2OA .1-丁烯B .1,3-丁二烯C .乙炔D .乙烯3.以1-丙醇制取,最简便的流程需要下列反应的顺序是( )a .氧化b .还原c .取代d .加成e .消去f .中和g .加聚h .酯化 A .b 、d 、f 、g 、h B .e 、d 、c 、a 、h C .a 、e 、d 、c 、h D .b 、a 、e 、c 、f题组二 有机合成路线的选择4.绿色化学提倡化工生产应提高原子利用率。
原子利用率表示目标产物的质量与生成物总质量之比。
在下列制备环氧乙烷()的反应中,原子利用率最高的是( )A .CH 2==CH 2+(过氧乙酸)―→+CH 3COOHB .CH 2==CH 2+Cl 2+Ca(OH)2―→+CaCl 2+H 2OC .2CH 2==CH 2+O 2――→催化剂△D .――→催化剂+2H 2O +HOCH 2CH 2—O —CH 2CH 2OH5.以溴乙烷为原料制备乙二醇,下列方案最合理的是( )A .CH 3CH 2Br ――――――→NaOH 的水溶液△CH 3CH 2OH ――→浓硫酸170 ℃CH 2==CH 2――→Br 2CH 2BrCH 2Br ――→水解乙二醇 B .CH 3CH 2Br ――→Br 2CH 2BrCH 2Br ――→水解乙二醇C .CH 3CH 2Br ――――――――→NaOH 的乙醇溶液△CH 2==CH 2――→HBrCH 3CH 2Br ――→Br 2CH 2BrCH 2Br ――→水解乙二醇 D .CH 3CH 2Br ――――――――→NaOH 的乙醇溶液△CH 2==CH 2――→Br 2CH 2BrCH 2Br ――→水解乙二醇 6.(2022·安徽芜湖高二检测)以为基本原料合成,下列合成路线最合理的是( ) A .――→O 2/Cu△K ――→O 2,△催化剂B .――→Br 2X ――――→NaOH/H 2O△Y ――→O 2/Cu△Z ――→O 2,△催化剂M ――→浓硫酸△C .――→H 2O 催化剂N ――→O 2/Cu △P ――→O 2,△催化剂Q ――→浓硫酸△D .――→HCl催化剂L ――→O 2/Cu△J ――――→O 2,△催化剂H ――――――――→①NaOH/乙醇,②H+△7.在有机合成中,若制得的有机化合物较纯净且易分离,在工业生产上才有实用价值。
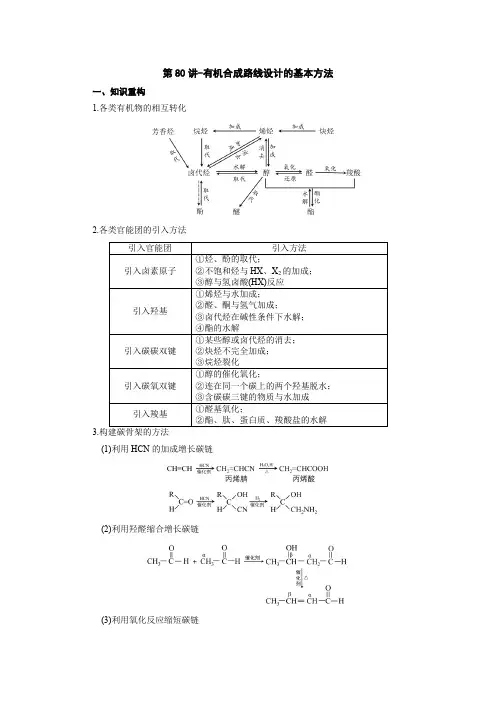
第80讲-有机合成路线设计的基本方法一、知识重构1.各类有机物的相互转化2.各类官能团的引入方法3.(1)利用HCN的加成增长碳链(2)利用羟醛缩合增长碳链(3)利用氧化反应缩短碳链(4)利用周环反应成环4.官能团的保护与恢复(1)碳碳双键:在氧化其他基团前可以利用其与HCl 等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。
HOCH 2CH=CHCH 2OH ――→HCl HOCH 2CH 2CHClCH 2OH ――――→KMnO 4/H+――――→1NaOH/醇2酸化HOOC—CH=CH—COOH 。
(2)酚羟基:在氧化其他基团前可以用NaOH 溶液或CH 3I 保护。
(3)醛基:在氧化其他基团前可以用乙醇(或乙二醇)加成保护。
①――→C 2H 5OHHCl――→H +/H 2O②――――――――→HO—CH 2CH 2—OH H+――→H +/H 2O(4)氨基:在氧化其他基团前可以用醋酸酐将氨基转化为酰胺,然后再水解转化为氨基。
――――→CH 3CO 2O ――――→H 2O H +或OH-(5)醇羟基、羧基可以成酯保护。
二、重温经典1.(2022年全国甲卷36题)用 N -杂环卡宾碱(NHC base)作为催化剂,可合成多环化合物。
下面是一种多环化合物 H 的合成路线(无需考虑部分中间体的立体化学)。
(6)如果要合成H 的类似物H'(),参照上述合成路线,写出相应的D'和G'的结构简式、。
【答案】、【解析】对比H()与H'()的结构可知,将合成H的原料D中的苯环换为,即得到D',将G中的苯环去掉即得到G',所以D'、G'分别为、。
2.(2022湖南19)物质J 是一种具有生物活性的化合物。
该化合物的合成路线如下:已知:①②参照上述合成路线,以和为原料,设计合成的路线(无机试剂任选)【答案】【解析】结合题给信息①、②,及由G到I的转化过程可知,可先将转化为,再使和反应生成,并最终转化为,即合成路线见答案。


《有机合成路线的设计与实施2》教学设计一、课标解读《有机合成路线的设计与实施》是普通高中化学课程标准选择性必修课程模块三有机化学基础主题1(有机化合物的组成与结构)部分的内容。
1、内容要求:认识有机合成的关键是碳骨架的构建和官能团的转化,了解设计有机合成路线的一般方法。
体会有机合成在创造新物质、提高人类生活质量及促进社会发展方面的重要贡献。
2、学业要求:能综合应用有关知识完成推断有机化合物、检验官能团、设计有机合成路线等任务。
二、教材分析有机化学路线的设计与实施是新人教版选择性必修3有机化学基础第3章烃的衍生物第5节的内容。
从章节整体来看,本章分类介绍了烃的衍生物的结构特点、物理性质、化学性质和用途;在本章的最后第5节,教材以有机合成为载体,对此前介绍的官能团的性质与转化、有机反应类型等内容进行系统化梳理和总结,并进行综合应用。
通过本章的学习,引导学生从碳骨架和官能团的视角认识有机化合物结构和性质,建立正向和逆向设计合成路线的方法模型。
在教学过程中落实化学学科核心素养,认识化学的应用价值,培养社会责任感。
本章的第5节有机合成,是对高中阶段学习的烃、卤代烃、醇、酚、醛、羧酸、酯等各类有机化合物性质的综合应用。
需要学生在熟练掌握上述有机化合物的结构特点和典型性质的基础上,能够利用其相互衍生关系及重要官能团的引入和消除方法,通过综合性问题的分析和解决,初步学会有机合成的方法,掌握有机合成过程的表示方法。
本节课为第5节有机合成第3课时,第一课时从碳骨架和官能团视角认识有机化合物结构和性质,并引入官能团保护的概念;第二课时构建了烃的衍生物转化模型,建立了正向和逆向设计合成路线的方法模型;本节课则立足于生活中的复杂有机化合物,巩固正向合成和逆向合成分析法,进一步锻炼在陌生情境中分析问题、解决问题的能力。
通过生活中常见的重要药物的合成路线设计,体会有机合成在创造新物质方面的重要贡献。
三、学情分析学生已经学习了烃、卤代烃、醇、酚、醛、羧酸、酯等各类有机化合物结构特点、物理性质、化学性质和用途,具备一定的有机化学知识基础;在烃的含氧衍生物的学习中,学生已经掌握了从结构(官能团)出发分析化学性质的思维方法;但是仍然缺乏对有机化合物知识的综合性、系统性的应用分析能力。

有机合成路线的设计和应用[核心素养发展目标] 1.宏观辨识与微观探析:结合碳骨架的构建及官能团衍变过程中的反应规律,能利用反应规律进行有机物的推断与合成。
2.证据推理与模型认知:落实有机物分子结构分析的思路和方法,建立对有机反应多角度认识模型、并利用模型进一步掌握有机合成的思路和方法。
一、有机合成路线的设计(正向合成分析法)1.正向合成分析法(1)方法:从确定的某种原料分子开始,逐步经过碳链的连接和官能团的安装来完成。
(2)步骤:首先要比较原料分子和目标化合物分子在结构上的异同,包括官能团和碳骨架两个方面的异同;然后,设计由原料分子转向产物的合成路线。
2.优选合成路线依据(1)合成路线是否符合化学原理。
(2)合成操作是否安全可靠。
(3)绿色合成:主要考虑有机合成中的原子经济性;原料的绿色化;试剂与催化剂的无公害性。
3.有机合成中常用的“四条路线”(1)一元合成路线HXNaOH水溶液[O][O]醇、浓硫酸,△R—CH===CH――→卤代烃――→一元醇――→一元醛――→一元羧酸――→酯。
2△(2)二元合成路线XNaOH水溶液[O][O]2CH===CH――→CHX—CHX――→CH―→OHCCHO――→ OH—CHOH―222222△HOOC —COOH―→链酯、环酯、聚酯。
(3)芳香化合物合成路线水溶液ClNaOH2――――①―――→―→△FeCl3NaOHCl水溶液2――――②――→―→△光照.醇、浓HSO[O][O]42――→―――→芳香酯――→――△h[O]Cl/NaOH/ν水2――→③―――→―→△hνNaOH/水/Cl2―――④――→→△[O] ―→―(4)改变官能团位置加成消去―→CH===CH―Br―→CH―CHCHCH23322HBr—+HBr 相关链接 1.常见有机物的转化关系若以乙醇为原料合成乙二酸(HOOC—COOH),则依次发生反应的类型是消去反应、加成反应、水解(或取代)反应、氧化反应、氧化反应。
(完美版)高中有机化学合成路线总结
1. 引言
有机合成是化学中最重要的分支之一,在高中有机化学研究中,了解一些常用的有机合成路线对于掌握有机化学的基本原理和应用
非常重要。
本文将总结一些常见的高中有机化学合成路线,帮助学
生更好地理解和应用有机合成的方法。
2. 简单醇的制备路线
2.1 醇的氢化制备
醇可以通过对应的醛或酮进行氢化反应得到。
一般而言,醛或
酮物质与氢气在催化剂存在下,在适宜的温度和压力条件下进行反应,生成相应的醇。
2.2 利用饱和碳酸饮料制备醇
某些饱和碳酸饮料中含有醇类物质,可以通过蒸馏和纯化等步骤,从饮料中提取醇。
3. 乙炔的制备路线
3.1 烃类脱氢制备乙炔
某些烃类物质可以通过高温下的脱氢反应得到乙炔。
脱氢反应是指在适当的温度和压力条件下,烃类物质中的氢原子脱离,生成乙炔。
3.2 碳酸盐的醋酸酯的加热分解
碳酸盐的醋酸酯在加热条件下分解,产生乙炔气体。
4. 醛的氧化制备羧酸
醛可以通过氧化反应生成相应的羧酸。
通常,醛物质与氧气在适宜的温度和催化剂存在下进行反应,生成相应的羧酸。
5. 醇的脱水制备烯烃
醇可以通过脱水反应生成相应的烯烃。
一般而言,醇物质在适宜的温度和催化剂存在下进行反应,生成相应的烯烃。
6. 结论
本文总结了高中有机化学中一些常见的合成路线,包括醇的制备、乙炔的制备、醛的氧化和醇的脱水。
通过了解这些合成路线,学生可以更好地理解有机化学的基本原理和应用,提高实验操作的能力和解决问题的能力。
第2课时有机合成路线的设计夯实基础轻松达标1。
乌洛托品在合成、医药、染料等工业中有广泛用途,其结构简式如图所示。
将甲醛水溶液与氨水混合蒸发可制得乌洛托品。
若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为()A.1∶1 B。
2∶3 C.3∶2 D。
2∶11mol乌洛托品含4molN、6molC,因此需要甲醛与氨的物质的量之比为6∶4=3∶2,C正确。
2。
以氯乙烷为原料制取乙二酸(HOOC—COOH)的过程中,要依次经过下列步骤中的()①与NaOH的水溶液共热②与NaOH的醇溶液共热③与浓硫酸共热到170 ℃④在催化剂存在情况下与氯气反应⑤在Cu或Ag存在的情况下与氧气共热⑥与新制的Cu (OH)2悬浊液共热A.①③④②⑥B。
①③④②⑤C.②④①⑤⑥D.②④①⑥⑤,乙二酸→乙二醛→乙二醇→1,2-二氯乙烷→乙烯→氯乙烷。
然后再逐一分析反应发生的条件,可知C 项设计合理。
3.(2020广东第二师范学院番禺附属中学高二期末)用糖类物质制备乙酸乙酯的合成路线之一如图所示:下列说法正确的是()A.淀粉和纤维素互为同分异构体B。
M是麦芽糖C。
反应③:乙醇生成乙酸所需反应条件可为酸性重铬酸钾溶液D.反应④:将产物通入滴有酚酞的饱和碳酸钠溶液中振荡,无明显现象,聚合度n值不同,所以不能互称同分异构体,A项错误;淀粉和纤维素完全水解生成的产物是葡萄糖,B项错误;乙醇转化为乙酸发生氧化反应,所以可以用酸性重铬酸钾溶液做氧化剂,C项正确;制乙酸乙酯时通常用饱和Na2CO3溶液来除杂,同时与乙酸乙酯分层,酯的密度比水小,下层主要是饱和碳酸钠溶液和醋酸钠溶液,溶液呈碱性,所以下层酚酞呈红色,D项错误。
4.(2020广西南宁高二检测)是一种有机烯醚,可由链烃A通过下列合成过程制得,下列说法正确的是()A B CA。
A分子中所有原子不可能共面B.B中含有的官能团有溴原子、碳碳双键C。
①②③的反应类型分别为加成反应、取代反应、消去反应D。
高中化学之有机合成方法归纳.有机合成【知识构建】一、有机合成的关键是、碳链的减短、成:一()、碳骨架的构建碳链的增长环或开环1、碳链增长的途径: Br + NaCN → CHCH23CHO + HCN →CH 3CHCHCHCHO + CHCHO →2323烯烃、炔烃的加聚、加成反应、碳链缩短的途径:2由醋酸钠制备甲烷:3、成环与开环的途径:)成环:如羟基酸分子内酯化1( HOCHCH COOH →22 (2)开环:如环酯的水解反应O → +2H COOCH 22COOCH2结合已学知识,小结以下(二)官能团的引入与转化官能团引入的方法。
的方法:C=C、至少列出三种引入1页 11 共页 2 第有机合成.;如(1)(2) ;如(3) ;如2、至少列出四种引入卤素原子的方法:(1) ;如;如(2);如(3);如 (4) (—OH)的方法:3、至少列出四种引入羟基(1) ;如(2) ;如(3) ;如;如(4)、在碳链上引入羰基(醛基、酮羰基)的方法:4 5、在碳链上引入羧基的方法:(1) ;如;如(2)(3) ;如二、中学常用的合成路线 1.烃、卤代烃、烃的含氧衍生物之间的转化关系页 11 共页 3 第有机合成.2.一元合成路线HX――→CH—CH=一元卤代烃―→一元醇―→R一定条件2一元羧酸―→酯醛―→ 3.二元合成路线X二元→→二元醇―→二元醛――→CH=CH222)羧酸―→酯(链酯、环酯、聚酯 4.芳香族化合物合成路线:应特别注意条件的Cl的反应,特别提醒和2做催化剂取代苯环邻、Fe变化;光照只取代甲基上的氢,对位上的氢。
三、有机合成题的解题思路典型例题:等其他试剂制取为原料,并以Br1例.以2页 11 共页 4 第有机合成.,用反应流程图表示合成路线,并注明反应条件。
1练习.用苯作原料,不能经一步化学反应制得1)(的是苯C..A硝基苯B.环己烷.溴苯 D 酚.在有机物分子中,不能引入羟基的反2) (应是.消 C B.水解反应 A.氧化反应.加成反应 D去反应年诺贝尔化概括了2005”3.“绿色、高效()学奖成就的特点。