高考化学二轮复习课件【12】常见非金属元素
- 格式:ppt
- 大小:3.27 MB
- 文档页数:74



年级高三学科化学版本苏教版内容标题无机非金属元素及其化合物【本讲教化信息】一. 教学内容:无机非金属元素及其化合物二. 教学目标驾驭氯、氧、硫、氮、磷、碳、硅所在主族元素性质的相像性、递变规律和特别性;重点驾驭几种常见典型物质的物理性质和化学性质;驾驭硫酸、硝酸的化学性质;驾驭氯气、二氧化硫、一氧化氮、二氧化氮、二氧化碳、氨气、氢气的试验室制法和气体的收集与尾气的汲取。
三. 教学重点、难点常见非金属元素的性质及相互关系四. 教学过程:元素化合物是中学化学的主体,这部分内容与基本概念、基本理论相互渗透,与化学试验、化学计算联系紧密。
复习元素化合物,要运用规律、把握关键、抓住重点、联系实际、编织元素化合物的科学体系。
元素化合物学问复习中要留意相像、相近内容的总结归纳。
如SO2、CO2、SO3、P2O5、SiO2等都是酸性氧化物,它们的性质有相像之处也有相异点。
高考命题时常会把这种关系编入试题中。
近几年的高考试题中这种趋向比较明显,值得大家重视。
说明:1. 氯元素的学问网络2. 次氯酸、漂白粉的性质HClO分子的结构式为H-O-Cl(氧处于中心),所以电子式为。
次氯酸、次氯酸钙等有多方面的性质,常常用到以下几方面性质:(1)HClO是一种弱酸,与碳酸比较电离实力有如下关系:H2CO3>HClO>HCO3-,请分析下列反应:少量二氧化碳通入NaClO溶液中:NaClO + CO2+H2O=NaHCO3+HClO氯气通入碳酸氢钠溶液中:Cl2+NaHCO3=NaCl+CO2↑+HClO(2)ClO-是一种弱酸的酸根离子,能发生水解反应:ClO-+H2O HClO+OH-,所以次氯酸钙溶液显碱性。
若遇到铁盐、铝盐易发生双水解:3ClO-+Fe3++3H2O=Fe(OH)3↓+3HClO(3)HClO和ClO-都具有强氧化性,无论酸性、碱性条件下都可以跟亚铁盐、碘化物、硫化物等发生氧化还原反应,但不能使品红溶液褪色。

第四讲、非金属元素及其化合物【知识要点】一、元素非金属性的强弱规律1.常见非金属元素的非金属性由强到弱的顺序: F、O、Cl、N、Br、I、S、P、C、Si 、H:2.元素的非金属性与非金属单质活泼性是并不完全一致的:如元素的非金属性O>Cl, N >Br;而单质的活泼性:O2< Cl2,N2<Br2。
3.比较非金属性强弱的依据(1)元素在周期表中的相对位置(2)非金属单质与氢气化合的越容易,非金属性越强。
如F2、Cl2、Br2、I2与H2化合由易到难,所以,非金属性F>Cl>Br>I。
(3)气态氢化物的越稳定,非金属性越强,如稳定性HF>H2O>HCl>NH3>HBr>HI>H2S >PH3,所以非金属性F>O>Cl>N>Br>I>S>P。
(4)最高价氧化物对应的水化物的酸性越强,非金属性越强,如酸性HClO4>H2SO4>H3PO4>H2CO3>H4SiO4,则非金属性Cl>S>P>C>Si。
(5)非金属性强的元素的单质能置换出非金属性弱的元素的单质。
如2F2+2H2O=4HF+O2↑;O2+4HCl=2H2O+2Cl2(地康法制Cl2);Cl2+2NaBr=2NaCl+Br2;3Cl2+2NH3=N2+6HCl;Cl2+H2S=S+2HCl。
(6)非金属单质对应阴离子的还原性越强,该非金属元素的非金属性越弱。
常见阴离子的还原性由强到弱的顺序是S2->I->Br->Cl->F-,则非金属性S<I<Br<Cl<F。
(7)与变价金属反应时,金属所呈价态越高,非金属性越强,如Cu+Cl2CuCl2;2Cu+S Cu2S,说明非金属性Cl>S。
二、非金属元素的化学性质(注意反应条件、现象、生成物的聚集状态)三、常见非全属单质的制取方法1.电解法①电解水溶液:如2NaCl +2H 2O 电解2NaOH +Cl 2↑+H 2↑②电解熔融物:如2KHF 2 电解F 2↑+H 2↑+2KF2.分解法:如2KClO 3 MnO 22KCl +3O 2↑ CH 4C +2H 2 2H 2O 2MnO 22H 2O +O 2↑ 3.置换法:如Cl 2+2NaBr =2NaCl +Br 2 2H 2S +O 2(不足) 点燃2H 2O +2S4.氧化法:如MnO 2+4HCl MnCl 2+Cl 2↑+2H 2O4NaBr +3H 2SO 4+MnO 2=2Na 2SO 4+MnSO 4+2Br 2+3H 2O5.还原法:C +H 2O CO +H 2,Zn +2HCl =ZnCl 2+H 2↑ 2C + SiO 2Si +2CO ↑【例题分析】[例题1]氯化碘(ICl )的化学性质跟氯气相似,预计它跟水反应的最初生成物是 ( )A 、HI 和HClOB 、HCl 和HIOC、HClO3和HIOD、HClO和HIO【拓展】从某些方面看,NH3和H2O相当,NH4+和H3O+(简写为H+)相当,NH2-和OH-相当,NH2-(有时还包括N3-)和O2-相当(1) 已知在液氨中下列2个反应能发生,完成并配平方程式:NH4Cl + KNH2→ , NH4I + PbNH →(2) 已知M为正二价金属,完成下列反应式:M+NH3→,MO+NH4Cl →M(NH2)2→[例题2]可以验证硫元素的非金属性比氯元素弱的事实是()①硫和氢气在加热条件下能形成H2S、H2S受热300℃左右分解。
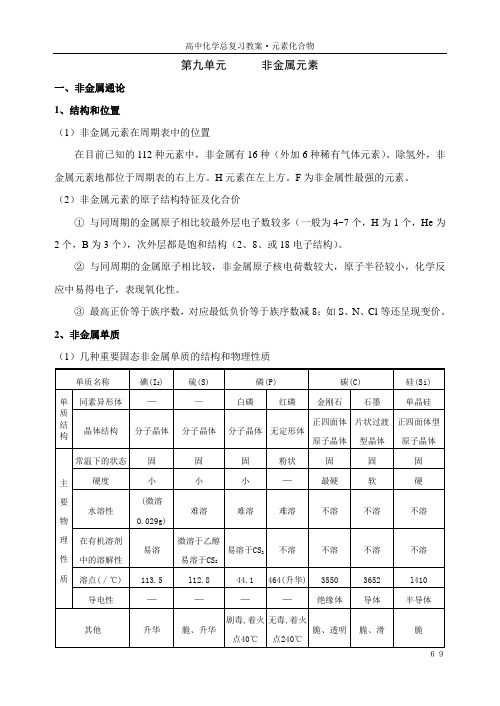
第九单元非金属元素一、非金属通论1、结构和位置(1)非金属元素在周期表中的位置在目前已知的112种元素中,非金属有16种(外加6种稀有气体元素)。
除氢外,非金属元素地都位于周期表的右上方。
H元素在左上方。
F为非金属性最强的元素。
(2)非金属元素的原子结构特征及化合价①与同周期的金属原子相比较最外层电子数较多(一般为4~7个,H为1个,He为2个,B为3个),次外层都是饱和结构(2、8、或18电子结构)。
②与同周期的金属原子相比较,非金属原子核电荷数较大,原子半径较小,化学反应中易得电子,表现氧化性。
③最高正价等于族序数,对应最低负价等于族序数减8;如S、N、Cl等还呈现变价。
2、非金属单质(1)几种重要固态非金属单质的结构和物理性质(2)重要气、液态非金属单质的结构和物理性质(3)结构与单质的化学性质3、非金属单质的制备(1)原理:化合态的非金属有正价态或负价态。
0R R nen−−→−-++,0R R nen−−→−---(2)方法: ① 氧化剂法,如: MnO 2+4HCl (浓)==MnCl 2+Cl 2↑+2H 2O222Br BrCl −→−-,22)(Cl g HCl O−→−(地康法制氯气) ② 还原剂法,如:Si SiO C −→−2,242H SO H Zn−→−③ 热分解法,如:23O KClO−−→−加热,24H C CH+−−→−高温④ 电解法,如:电解水制H 2、O 2,氯碱工业制Cl 2等。
⑤ 物理法,如:工业上分离液态空气得N 2(先)、O 2(后)4、非金属气态氢化物 (1)分子构型与物理性质ⅣA ——RH 4 正四面体结构,非极性分子; ⅤA ——RH 3 三角锥形,极性分子;ⅥA ——H 2R 角型(或“V “型)分子,极性分子; ⅦA ——HR 直线型,极性分子。
固态时均为分子晶体,熔沸点较低,常温下H 2O 是液体,其余都是气体。
(2)化学性质① 稳定性及水溶液的酸碱性非金属元素原子跟氢原子通过共价键形成气态氢化物,一般元素的非金属性越强,跟氢化合能力越强,生成的气态氢化物越稳定,因此气态氢化物的稳定性是非金属性强弱的重要标志之一。

[考纲要求 ] 1.了解常见非金属元素单质及其重要化合物的主要性质及应用。
2.了解常见非金属元素单质及其重要化合物对环境质量的影响。
考点一碳、硅及其重要化合物1.理清知识主线-40+2+4CH4C ―→ CO―→ CO2-40+4+4SiH 4Si ―→ SiO2(H 2S i O3)2.注意网络构建3.扫除知识盲点(1)工业上制备粗硅,是用过量的 C 和 SiO 2高温下反应,由于 C 过量,生成的是 CO 而不是CO2,该反应必须在隔绝空气的条件下进行。
(2)氢氟酸不能用玻璃容器盛放;NaOH 溶液能用玻璃试剂瓶,但不能用玻璃塞。
(3)酸性氧化物一般能与水反应生成酸,但SiO2不溶于水;酸性氧化物一般不与酸作用,但SiO 2能与 HF 反应。
(4)硅酸盐大多难溶于水,常见可溶性硅酸盐是硅酸钠,其水溶液称为泡花碱或水玻璃,但却是盐溶液。
(5)H 2CO3的酸性大于H 2SiO3的,所以有Na2SiO 3+ CO2(少量 )+ H2O===H2SiO3↓+ Na2CO3,高温但高温下Na2CO3+ SiO2=====Na2 SiO3+ CO2↑也能发生,原因可以从两方面解释:①硅酸盐比碳酸盐稳定;②从化学平衡角度,由高沸点难挥发固体SiO2制得低沸点易挥发的CO2。
(6)SiO 2不导电,是制作光导纤维的材料;Si 是半导体,是制作光电池的材料。
(7)水泥、玻璃与陶瓷是三大传统无机非金属材料;碳化硅、氮化硅等是新型无机非金属材料。
题组一重要反应必练1.按要求书写反应方程式。
(1)制水煤气高温C+H 2O(g)=====CO+ H2。
(2)制备粗硅高温2C+ SiO2=====2CO↑+ Si。
(3)Mg 在 CO2中燃烧点燃2Mg +CO2=====2MgO +C。
(4)“水滴石穿”的反应原理(用离子方程式表示)CaCO3+CO2+ H2O===Ca2++ 2HCO -3。
(5)“钟乳石”的形成过程(用化学方程式表示)CaCO3+CO2+ H2O===Ca(HCO 3)2,△Ca(HCO 3) 2=====CaCO3↓+ CO2↑+ H 2O。
目夺市安危阳光实验学校包集中学高考化学第二轮复习教案:非金属元素概论教学目标知识技能:了解元素核外电子排布的周期性与元素性质递变关系,掌握典型非金属在周期表中的位置及其性质的关系。
了解常见非金属元素(Cl、Br、I、F、H、O、S、N、P、C、Si)的单质及其化合物。
能力培养:通过对本节内容的分析讨论,使学生在掌握元素化合物知识的基础上培养学生对知识进行分析综合、归纳演绎的逻辑思维能力和直觉思维能力以及灵活运用所学知识解决问题的能力。
科学思想:培养学生建立“一切客观事物本来是互相联系和具有内部规律的”辩证唯物主义的观点。
科学品质:认识本质,进行知识整理、综合、提高与拓展的方法培养。
科学方法:培养学生科学抽象、概括整理、归纳总结、准确系统地掌握知识规律的方法。
重点、难点非金属元素的结构、性质及应用。
元素化合物知识的综合应用及物质推断。
教学过程设计教师活动【引入】一、元素化合物的复习方法落实存在、性质、制备、用途四要点。
学生活动体会“位、构、性”三者关系。
【举例】(1)从位置出发,以Cs为例。
位置:第六周期,IA族。
→结构特点:最外层只有一个电子,原子半径大。
→比Na、K更活泼的金属元素,具强的金属性。
→应隔绝空气保存;与水反应剧烈,可能发生爆炸;与氧气迅速反应,主要产物肯定不是Cs2O。
(2)从结构出发:已知某元素原子有六个电子层,最外层2个电子→最外层电子数少,电子层数多,应是活泼金属,金属性大于钙→与水剧烈反应;氢氧化物是可溶性强碱;碳酸盐、硫酸盐均不溶于水。
与教师共同分析。
(3)从性质出发:某单质能从水中置换出O2。
→非金属性大于氧,应为最活泼的非金属元素F→在周期表的右上角,第二周期ⅦA族→可与绝大多数金属、非金属甚至某些稀有气体直接反应;化合价只有-1价;几乎无法用氧化剂将F-氧化成F2。
分析:归纳:【投影】例1 BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验,它是锗酸铋的简称,若知:①在BGO中,锗处于其最高价态。