第二章热力学第一定律演示文稿
- 格式:ppt
- 大小:1.98 MB
- 文档页数:74


热力学第一定律ppt引言热力学第一定律是热力学中的基本定律之一。
它表明了能量的守恒原理,也被称为能量守恒定律。
热力学第一定律对于理解能量转化和能量守恒的过程至关重要,应用广泛。
热力学第一定律的表述热力学第一定律可以用如下方式表述:在孤立系统中,能量的增量等于对外界做功和系统热量的和。
这个表述可以用以下数学公式表示:ΔE = Q - W其中,ΔE表示能量的增量,Q表示系统吸收的热量,W表示系统对外做功。
能量转化示意图为了更好地理解热力学第一定律,我们可以通过一个能量转化示意图来说明。
能量转化示意图能量转化示意图在这个示意图中,输入的能量被系统吸收,一部分能量被转化为系统内能的增加(热量),一部分能量被系统用于对外做功。
根据热力学第一定律,系统吸收的热量和对外做的功加起来等于能量的增量。
热力学第一定律的应用热力学第一定律在工程和科学研究中有着广泛的应用。
以下是一些具体的应用:热力学循环分析热力学第一定律用于分析各种热力学循环,如卡诺循环和热力学循环。
通过应用热力学第一定律,我们可以确定循环中的能量转化效率、功率输出等参数。
能量守恒分析热力学第一定律可以应用于能量守恒的分析,例如分析能源系统中的能量损失和能量转化过程。
通过分析系统的能量转化过程,我们可以找出能量损失的原因,并采取措施来提高能源利用效率。
温度变化分析热力学第一定律可以用来分析物质的温度变化。
根据热力学第一定律,物质的内能增加会导致温度升高,而内能减少则会导致温度降低。
因此,可以通过热力学第一定律来研究物质的显热效应和隐热效应。
结论热力学第一定律是热力学中的基本定律之一,它表明了能量的守恒原理。
通过应用热力学第一定律,我们可以分析能量的转化过程,研究能源系统的能量损失和能量转化效率,并进一步提高能源利用效率。
热力学第一定律在工程和科学研究中有着广泛的应用,对于理解能量转化和能量守恒的过程起到了重要的作用。



第二章 热力学第一定律第一节 第一定律的实质及热力学能和总能能量守恒与转换定律是自然界的基本规律之一,它指出:自然界中的一切物质都具有能量,能量不可能被创造,也不能被消灭;但能量可以从一种形态转变为另一种形态,且在能量的转化过程中能量总量不变。
热力学第一定律是能量守恒与转换定律在热现象中的应用。
它确定了热力过程中热力系统与外界进行能量交换时,各种形态能量数量上的守恒关系。
一、热力学能热力学能是与物质内部粒子的微观运动和粒子的空间位置有关的能量。
它包括分子移动、转动、粒子震动运动的内动能和分子间由于相互作用力的存在而具有的内位能,故又称内能。
内动能取决于分子热运动,是温度的函数,而内位能取决于分子间的距离,是比体积的函数,即u = f ( T, v )二、总能除热力学能外,工质的总能量还包括工质在参考坐标系中作为一个整体,因有宏观运动速度而具有动能、因有不同高度而具有位能。
前一种能量称之为内部储存能,后两种能量则称之为外部储存能。
我们把内部储存能和外部储存能的总和,即热力学能与宏观运动动能和位能的总和,叫做工质的总储存能,简称总能。
即p k E U E E =++ (2-1)E---总能; U---热力学能; E k ---宏观动能; E p ---宏观位能。
第二节 第一定律的基本能量方程及工质的焓一、焓在有关热力计算总时常有U+pV 出现,为了简化公式和计算,把它定义为焓,用符号H 表示,即H=U+pV (2-2)1kg工质的焓值称为比焓,用h表示,即h=u+pv (2-3)焓的单位是J,比焓的单位是J/kg。
焓是一个状态参数,在任一平衡状态下,u、p和v都有一定得值,因而焓h也有一定的值,而与达到这一状态的路径无关。
当1kg工质通过一定的界面流入热力系统时,储存于它内部的热力学能当然随着也进入到系统中,同时还把从外部功源获得的推动功pv带进了系统。
因此系统中因引进1kg工质而获得的总能量是热力学能与推动功之和(u+pv),即比焓。



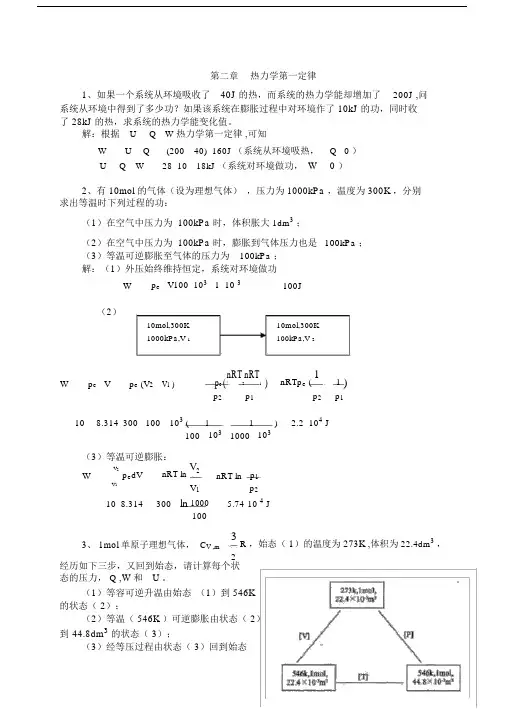
第二章热力学第一定律1、如果一个系统从环境吸收了40J 的热,而系统的热力学能却增加了200J ,问系统从环境中得到了多少功?如果该系统在膨胀过程中对环境作了 10kJ 的功,同时收了 28kJ 的热,求系统的热力学能变化值。
解:根据U Q W 热力学第一定律,可知W U Q (200 40) 160J (系统从环境吸热,Q 0 )U Q W 28 10 18kJ (系统对环境做功,W 0 )2、有 10mol 的气体(设为理想气体),压力为 1000kPa ,温度为 300K ,分别求出等温时下列过程的功:(1)在空气中压力为 100kPa 时,体积胀大1dm3;(2)在空气中压力为 100kPa 时,膨胀到气体压力也是100kPa ;(3)等温可逆膨胀至气体的压力为100kPa ;解:(1)外压始终维持恒定,系统对环境做功W p e V100 103 1 10 3 100J(2)10mol,300K10mol,300K1000kPa,V 1100kPa,V 2W p e V p e (V2 V1 ) p e(nRT2nRT1) nRTp e (11 )p2 p1 p2 p110 8.314 300 100 103 ( 1 1103 ) 2.2 104 J100 103 1000(3)等温可逆膨胀:V2p e dV nRT ln V2 nRT ln p1WV1 V1 p210 8.314 300 ln 1000 5.74 10 4 J1003、 1mol 单原子理想气体,C V ,m 3R ,始态(1)的温度为273K ,体积为 22.4dm3,2经历如下三步,又回到始态,请计算每个状态的压力, Q ,W和U 。
(1)等容可逆升温由始态(1)到 546K 的状态( 2);(2)等温( 546K )可逆膨胀由状态( 2)到44.8dm3的状态( 3);(3)经等压过程由状态( 3)回到始态( 1);解:(1)等容可逆升温过程:W P e V 0UQ WQ VT 2 nC V ,m dT 138.314 546 273 3404.58 JT 12(2)等温可逆膨胀过程:U 0WnRT lnV 21 8.314 546ln 44.83146.50JV 122.4Q W 3146.50J(3)等压过程 :WP e VnRT V 1 V 2 1 8.314 273 22.4 44.8 10 3 2269.72 JV 1 22.4 10 3Q pH T 2nC P ,m dT n 3 R 273 546 5 8.314 273 5674.31J T 1 R 12 2UQ W 5674.31 2269.72 3404.59 J4、在 291K 和 100kPa 下, 1molZn (s) 溶于足量稀盐酸中, 置换出 1molH 2 ( g) ,并放热 152kJ 。

