铁极化曲线
- 格式:docx
- 大小:383.47 KB
- 文档页数:4
实验13 铁的极化和钝化曲线的测定一、极化曲线1. 详细的实验步骤(1) 将电解液倒入三电极电解池指定的刻度,将工作电极(铁电极)、辅助电极(铂电极)以及参比电极(饱和甘汞电极)置于三电极电解池相应的玻璃管中并与电化学工作站相连(三个电极一一对应)。
(2) 打开电化学工作站开关,双击电脑桌面的文件夹” set660c”,双击应用程序“chi660c”进入电化学工作站专用软件。
(3) 单击工具栏中“T”按钮,选择” Tafel Plot”,点击”ok”进入极化曲线参数设置对话框,手动输入参数如下图所示:点击“ok”,再单击工具栏中“►”按钮即开始测定极化曲线。
测试完毕后要存盘,“File”-“Save as”,选择要存盘的地址并输入文件名如“04110711-2-Na”即可,文件格式为系统定义的格式(BIN文件),为了能用于撰写实验报告要先转化为txt格式并导入到origin7.5中作图。
在文件打开的情况下运行“File”-“Convert to text”,并使用相同的文件名存在相同的目录下即可。
(4) 先测定铁电极在中性水溶液中的极化曲线,数据存盘后用直尺测量铁电极没入电解液的高度(其宽度为1cm),从而求得其面积(用于计算自腐蚀电流密度)。
将铁电极用金相砂纸打磨备用。
将溶液换为1mol/LH2SO4溶液,重复上述步骤得到铁电极在1mol/LH2SO4溶液中的极化曲线,文件名可命名为“04110711-2-H”。
2.数据处理及报告撰写2.1 在origin 7.5中将铁电极在两个不同电解液中的极化曲线放在同一坐标内具体操作如下:先运行origin 7.5,执行如下命令:“File”-“Import”-“Simple Single ACSII”,在弹出的对话框中定位到已经换化好的文本文件(如04110711-2-Na),在显示器上你将看到:然后运行“File”-“Save Project as (或在汉化版中选择“保存工程为”)”,选择相应的目录,将文件名命名为“04110711-2-Na”备用,按上述方法建立另外一个文件“04110711-2-H”,备用。
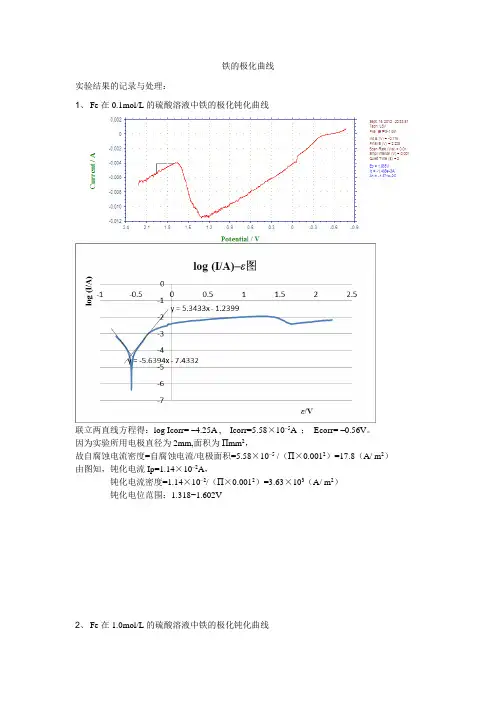
铁的极化曲线实验结果的记录与处理:1、Fe在0.1mol/L的硫酸溶液中铁的极化钝化曲线联立两直线方程得:log Icorr= ‒4.25A , Icorr=5.58×10‒5A ;Ecorr= ‒0.56V。
因为实验所用电极直径为2mm,面积为Πmm2,故自腐蚀电流密度=自腐蚀电流/电极面积=5.58×10‒5 /(Π×0.0012)=17.8(A/ m2)由图知,钝化电流Ip=1.14×10‒2A,钝化电流密度=1.14×10‒2/(Π×0.0012)=3.63×103(A/ m2)钝化电位范围:1.318−1.602V2、Fe在1.0mol/L的硫酸溶液中铁的极化钝化曲线联立两直线方程得:log Icorr= ‒4.25A , Icorr=5.58×10‒5A ;Ecorr= ‒0.56V。
因为实验所用电极直径为2mm,面积为Πmm2,故自腐蚀电流密度=自腐蚀电流/电极面积=5.58×10‒5 /(Π×0.0012)=17.8(A/ m2)由图知,钝化电流Ip=1.14×10‒2A,钝化电流密度=1.14×10‒2/(Π×0.0012)=3.63×103(A/ m2)钝化电位范围:1.318−1.602V3、Fe在1.0mol/L的HCl溶液中铁的极化钝化曲线联立两直线方程得:log Icorr= ‒4.25A , Icorr=5.58×10‒5A ;Ecorr= ‒0.56V。
因为实验所用电极直径为2mm,面积为Πmm2,故自腐蚀电流密度=自腐蚀电流/电极面积=5.58×10‒5 /(Π×0.0012)=17.8(A/ m2)由图知,钝化电流Ip=1.14×10‒2A,钝化电流密度=1.14×10‒2/(Π×0.0012)=3.63×103(A/ m2)钝化电位范围:1.318−1.602V4、Fe在含1%的乌洛托品的1.0mol/L的HCl溶液中铁的极化钝化曲线联立两直线方程得:log Icorr= ‒4.25A , Icorr=5.58×10‒5A ;Ecorr= ‒0.56V。
电化学曲线极化曲线阻抗谱分析一、极化曲线1.绘制原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H),它们在数值上相等但符号相反,即:(1)I(Fe)的大小反映Fe在H+中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor。
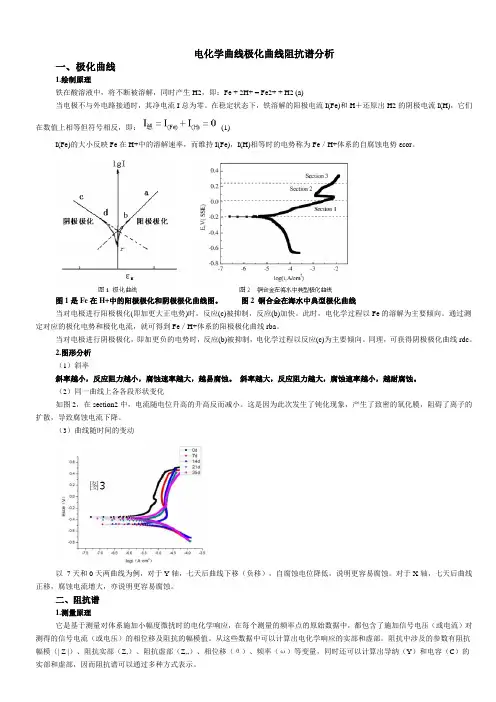
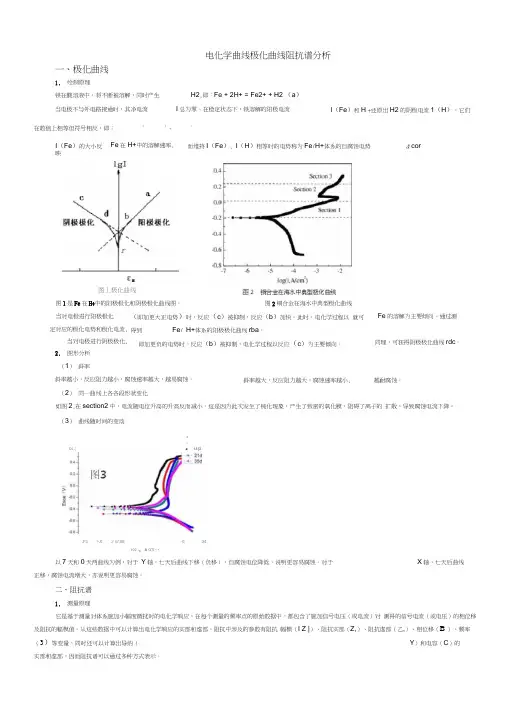
图1是Fe在H+中的阳极极化和阴极极化曲线图。
图2 铜合金在海水中典型极化曲线当对电极进行阳极极化(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以Fe的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H+体系的阳极极化曲线rba。
当对电极进行阴极极化,即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
同理,可获得阴极极化曲线rdc。
2.图形分析(1)斜率斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
斜率越大,反应阻力越大,腐蚀速率越小,越耐腐蚀。
(2)同一曲线上各各段形状变化如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱1.测量原理它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(| Z |)、阻抗实部(Z,)、阻抗虚部(Z,,)、相位移(θ)、频率(ω)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。


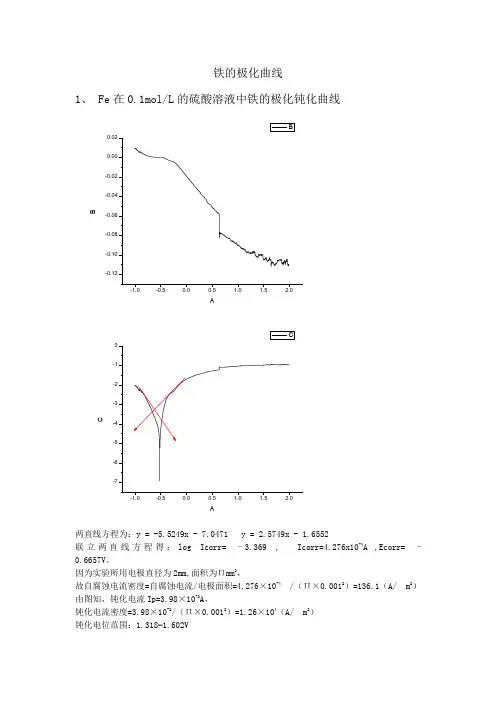
铁的极化曲线1、 Fe 在0.1mol/L 的硫酸溶液中铁的极化钝化曲线-1.0-0.50.00.51.01.52.0-0.12-0.10-0.08-0.06-0.04-0.020.000.02BA-7-6-5-4-3-2-10CA两直线方程为:y = -5.5249x - 7.0471y = 2.5749x - 1.6552联立两直线方程得:log Icorr= ‒3.369 , Icorr=4.276x10-4A ,Ecorr= ‒0.6657V 。
因为实验所用电极直径为2mm,面积为Πmm 2,故自腐蚀电流密度=自腐蚀电流/电极面积=4.276×10-4 /(Π×0.0012)=136.1(A/ m 2)由图知,钝化电流Ip=3.98×10-2A ,钝化电流密度=3.98×10-2/(Π×0.0012)=1.26×104(A/ m 2) 钝化电位范围:1.318−1.602V2、Fe 在1.0mol/L 的硫酸溶液中铁的极化钝化曲线-1.0-0.50.00.5 1.01.52.00.020.00-0.02-0.04-0.06-0.08BA-6-5-4-3-2-1CA两直线方程为: y = 1.8789x - 1.622y = -3.3109x - 4.973联立两直线方程得:log Icorr= ‒2.835 , Icorr=1.462x10-3A,Ecorr= ‒0.6657V 。
因为实验所用电极直径为2mm,面积为Πmm 2,故自腐蚀电流密度=自腐蚀电流/电极面积=1.462×10-3 /(Π×0.0012)=465.3(A/ m 2) 由图知,钝化电流Ip=4.46×10-2A ,钝化电流密度=4.46×10-2/(Π×0.0012)=1.42×104(A/ m 2) 钝化电位范围:0.583−1.324V3、Fe 在1.0mol/L 的HCl 溶液中铁的极化钝化曲线-1.0-0.50.00.51.01.52.0-0.035-0.030-0.025-0.020-0.015-0.010-0.0050.0000.0050.010BA-6-5-4-3-2-1CA两直线方程为:y = -1.9267x - 4.171y = 1.9989x - 2.1957联立两直线方程得:log Icorr= ‒3.202A , Icorr=6.280×10-4A ; Ecorr= ‒0.503V 。
电化学曲线极化曲线阻抗谱分析一、极化曲线1.绘制原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流在数值上相等但符号相反,即: 1 1 - 12.图形分析(1)斜率斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
(2)同一曲线上各各段形状变化如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱1.测量原理它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(I Z |)、阻抗实部(Z,)、阻抗虚部(乙,)、相位移(B )、频率(3)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。
I(Fe)的大小反映而维持I(Fe), I(H)相等时的电势称为Fe/H+体系的自腐蚀电势& corFe在H+中的溶解速率,图丄极化曲线图1是Fe在H+中的阳极极化和阴极极化曲线图。
当对电极进行阳极极化定对应的极化电势和极化电流,当对电极进行阴极极化,图2铜合金在海水中典型极化曲线(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以就可得到Fe/ H+体系的阳极极化曲线rba。
即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
Fe的溶解为主要倾向。
通过测同理,可获得阴极极化曲线rdc。
铁的极化曲线的测定、循环伏安法数据处理详细的数据处理步骤
一、数据导出
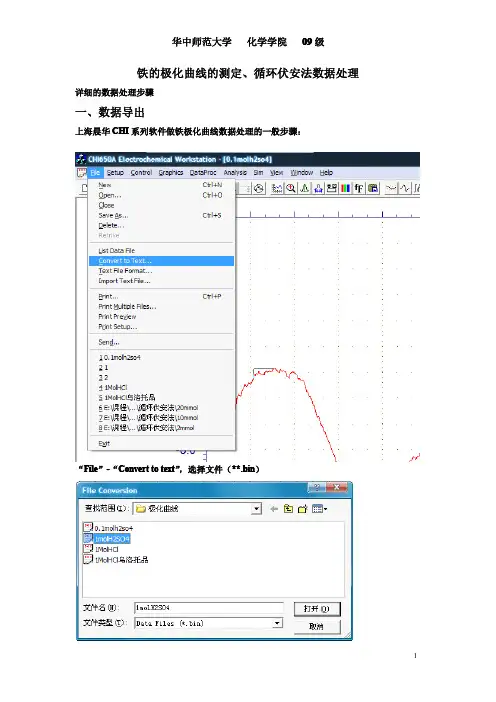
上海晨华CHI系列软件做铁极化曲线数据处理的一般步骤:
“File”-“Convert to text”,选择文件(**.bin)
选择相应文件点击“打开”,回到数据存放目录找到,文件名.txt。
二、数据导出或直接作图
先运行origin7.0,执行如下命令:“File”-“Import”-“Simple Single ACSII”,选择上一步导出的txt文件,将数据导入origin7.0,
数据导入后如下图:
第一、二列有用,如果会用origin7.0可以进行如下操作,将第二列数据取绝对值,并取lo log g 对数,用一、四列数据作图。
将一、四列选中点击“”,作图如下图:
Excel法:
因Excel无数据导入功能(或未发现),故先将文件导入origin7.0后,将其复制到Excel中进行处理。
将第二列绝对值,放入第三列,对第三列取以10为底的对数,放于第四列,一四列作图。
如下:
以上即是铁极化曲线的数据处理过程!能力有限敬请参考!。

极化曲线测定实验报告极化曲线测定实验报告引言:极化曲线测定实验是电化学领域中常用的实验方法之一。
通过测量电极在不同电位下的电流变化,可以得到极化曲线,从而分析电极的电化学性质和反应动力学过程。
本实验旨在通过测定铁电极的极化曲线,探究其电化学性质,并对实验结果进行分析和讨论。
实验装置和方法:本实验采用三电极系统,包括工作电极、参比电极和辅助电极。
首先,将铁片作为工作电极,银/银氯化银电极作为参比电极,铂丝作为辅助电极。
然后,将这三个电极分别插入电解液中,并使用电位扫描仪测量电位和电流的变化。
实验过程中,通过改变电位的斜率和扫描速率,可以得到不同条件下的极化曲线。
实验结果与讨论:在实验中,我们通过改变电位的斜率和扫描速率,得到了铁电极在不同条件下的极化曲线。
根据实验结果,我们可以观察到以下现象和规律:1. 极化曲线的形状:在正向扫描时,铁电极的极化曲线呈现出两个明显的区域:活化区和稳定区。
活化区是指电位较低的区域,此时电流较大,反应速率较快。
稳定区是指电位较高的区域,此时电流较小,反应速率较慢。
在反向扫描时,极化曲线的形状与正向扫描时相似,但是活化区和稳定区的位置会发生变化。
2. 极化曲线的斜率:极化曲线的斜率反映了电极的电化学活性和反应速率。
斜率越大,表示电极的活性越高,反应速率越快。
在实验中,我们可以通过改变电位的斜率来调节电极的活性,从而探究电极的电化学性质。
3. 极化曲线的扫描速率:扫描速率是指电位变化的速度。
在实验中,我们可以通过改变扫描速率来研究电极的反应动力学过程。
当扫描速率较慢时,电极的反应过程更加充分,可以观察到更多的电化学现象。
而当扫描速率较快时,电极的反应过程相对较快,可能会导致一些电化学现象无法观察到。
结论:通过极化曲线测定实验,我们可以得到电极的电化学性质和反应动力学过程。
实验结果显示,铁电极在不同电位下的电流变化呈现出明显的活化区和稳定区,斜率和扫描速率对电极的反应速率和动力学过程有重要影响。


腐蚀金属电极稳态极化曲线测量和数据处理一、实验目的:1、掌握恒电位测定极化曲线的原理和方法2、巩固金属极化理论,确定金属实施阳极保护的可能性。
初步了解阳极保护参数及其确定方法。
3、了解恒电位仪器及相关电化学仪器的使用。
4、测定铁在酸性介质中的极化曲线,求算自腐蚀电位、自腐蚀电流、掌握线性扫描伏安法和TAFEL方法测定极化曲线。
实验原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)Fe/HCl体系是-个二重电极,即在Fe/H+界面上同时进行两个电极反应:Fe Fe2+ + 2e (b)2H+ + 2e H2 (c)反应(b)、(c)称为共轭反应。
正是由于反应(c)存在,反应(b)才能不断进行,这就是铁在酸性介质中腐蚀的主要原因。
当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H),它们在数值上相等但符号相反,即:(1)IFe的大小反映Fe在H+中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor。
图12-1 Fe的极化曲线图12-1是Fe在H+中的阳极极化和阴极极化曲线图。
当对电极进行阳极极化(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以Fe的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H+体系的阳极极化曲线rba。
由于反应(c)是由迁越步骤所控制,所以符合塔菲尔(Tafel)半对数关系,即:(2)直线的斜率为bFe。
当对电极进行阴极极化,即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
同理,可获得阴极极化曲线rdc。
由于H+在Fe电极上还原出H2的过程也是由迁越步骤所控制,故阴极极化曲线也符合塔菲尔关系,即:(3)当把阳极极化曲线abr的直线部分ab和阴极极化曲线cdr的直线部分cd 外延,理论上应交于一点(z),z点的纵坐标就是,腐蚀电流Icor的对数,而z 点的横坐标则表示自腐蚀电势εcor的大小。
阳极极化曲线的测定实验报告阳极极化曲线的测定实验报告引言:阳极极化曲线是用于研究金属在电化学腐蚀过程中的行为的重要工具。
通过测定金属在不同电位下的电流密度,可以得到阳极极化曲线,从而了解金属的腐蚀行为及其抗腐蚀性能。
本实验旨在通过测定铁的阳极极化曲线,探究其腐蚀行为及其抗腐蚀性能。
实验方法:1. 准备工作:将实验所需的试样铁片进行清洗和抛光,确保表面光洁无杂质。
2. 搭建电化学腐蚀实验装置:将试样铁片作为阳极,配备铂丝作为对电极,以及参比电极。
将试样铁片浸入含有适量电解液的电解池中。
3. 测定阳极极化曲线:通过改变电位,测定不同电位下的电流密度,记录数据并绘制阳极极化曲线。
实验结果:通过实验测定,得到了铁的阳极极化曲线,如图1所示。
曲线呈现出三个明显的区域:主动腐蚀区、穿孔区和过氧化物区。
在主动腐蚀区,随着电位的增加,电流密度逐渐增大,但增速较慢。
这是由于铁表面的氧化膜逐渐变厚,形成一层保护膜,阻止了进一步的氧化反应。
在穿孔区,电流密度急剧增大,表明铁开始发生局部腐蚀。
这是由于氧化膜中存在缺陷,使得金属表面暴露在电解液中,导致局部腐蚀的发生。
在过氧化物区,电流密度逐渐减小,说明铁的腐蚀速率降低。
这是由于过氧化物的生成,形成了一层致密的氧化膜,有效地抑制了进一步的腐蚀反应。
讨论与分析:通过实验测定的阳极极化曲线,我们可以对铁的腐蚀行为及其抗腐蚀性能进行一定的分析与评价。
首先,从主动腐蚀区的曲线斜率可以得到铁的腐蚀速率。
曲线斜率越大,说明腐蚀速率越快。
通过对比不同金属的阳极极化曲线,可以评估铁的腐蚀性能与其他金属的相对抗腐蚀性能。
其次,在穿孔区的曲线上,可以观察到局部腐蚀的发生。
穿孔区的位置与腐蚀环境有关,不同腐蚀环境下金属的穿孔区位置不同。
通过观察穿孔区的位置,可以评估铁在不同腐蚀环境中的腐蚀抗性。
最后,在过氧化物区的曲线上,可以观察到铁的腐蚀速率减缓。
过氧化物的生成可以形成一层致密的氧化膜,有效地抑制了进一步的腐蚀反应。
极化曲线腐蚀电流与腐蚀电位1. 引言极化曲线是研究金属腐蚀过程中重要的工具之一。
通过测量极化曲线,可以了解金属在不同电位下的腐蚀行为,并确定其腐蚀电流和腐蚀电位。
本文将介绍极化曲线的概念、测量方法以及与腐蚀电流和腐蚀电位的关系。
2. 极化曲线的概念极化曲线是描述金属在外加电势下的电流密度变化情况的曲线。
它通常由三个区域组成:主动区、过渡区和从动区。
•主动区:当金属处于正常工作状态时,其表面通常保持较低的电流密度,这个区域被称为主动区。
•过渡区:当金属表面开始发生氧化或还原反应时,其电流密度逐渐增大,这个过程称为过渡区。
•从动区:当金属表面完全被氧化或还原时,其电流密度达到最大值,这个区域称为从动区。
3. 极化曲线的测量方法测量极化曲线通常使用电化学工作站或极谱仪。
以下是一般的测量步骤:1.准备工作:清洗待测试的金属样品,确保其表面干净无杂质。
2.设置电化学工作站或极谱仪:根据实验要求设置工作站的参数,如扫描速率、起始电位等。
3.测量极化曲线:将待测试的金属样品放置在电解槽中,通过改变外加电势的大小并记录对应的电流密度,得到极化曲线。
4.数据处理:根据测得的数据绘制极化曲线,并计算腐蚀电流和腐蚀电位。
4. 腐蚀电流与腐蚀电位的关系腐蚀电流和腐蚀电位是描述金属在腐蚀环境中耐久性能的重要参数。
4.1 腐蚀电流腐蚀电流是指金属在给定环境条件下发生氧化或还原反应时所产生的电流密度。
它可以通过测量极化曲线中从动区对应点处的电流密度来确定。
腐蚀电流的大小与金属的耐蚀性能密切相关,一般情况下,腐蚀电流越大,金属的耐蚀性能越差。
4.2 腐蚀电位腐蚀电位是指金属在给定环境条件下开始发生氧化或还原反应的电势。
它可以通过测量极化曲线中过渡区对应点处的电势来确定。
腐蚀电位的高低决定了金属在给定环境中是否会发生腐蚀反应。
一般情况下,腐蚀电位越低,金属的耐久性能越差。
4.3 腐蚀电流与腐蚀电位的关系在极化曲线上,从动区对应点处的电流密度与过渡区对应点处的电势之间存在一种关系。
实验4 铁的极化和钝化曲线的测定一、实验目的1.理解和掌握极化曲线测定的原理和实验方法。
2.学会用恒电位仪测定极化曲线的方法。
二、实验原理在研究可逆电池的电池反应和电动势的时候,电极处于平衡状态,与之相对应的电势是平衡电势φ平,随着电极上电流密度的增加,电极的不可逆程度愈来愈大,其电势值对平衡电势值的偏离也愈来愈大,在有电流通过电极时,电极电势偏离于平衡值的现象称为电极的极化。
根据实验测出的数据来描述电流密度与电极电势之间的关系曲线称为极化曲线。
通过极化曲线的测绘,可使我们对电极极化过程以及金属的腐蚀与保护等加深认识和理解。
在金属做阳极的电解池中通过电流时,通常发生阳极的电化学溶解过程,如下式所示:M=M n++ne阳极极化不大时,阳极溶解速度随电位变正而逐渐增大,这是金属正常的阳极溶解。
但在某些化学介质中,当阳极电位正移到某一数值时,阳极溶解速度随电位变正而大幅度降低,这种现象称为阳极的钝化。
处于钝化状态的金属的溶解速度是很小的,这是因为在金属表面生成了一层电阻高、耐腐蚀的钝化膜,这在金属防护以及作为电镀的不溶性阳极时,正是人们所需要的。
利用阳极的钝化,使金属表面生成了一种耐腐蚀的钝化膜来防止金属腐蚀的方法,叫做阳极的保护。
金属的钝化现象是常见的,人们已对它进行了大量的研究工作。
影响金属钝化过程及钝化性质的因素,可归纳为以下几点:1. 溶液的组成溶液中存在的氢离子、卤素离子以及某些具有氧化性的阴离子,对金属的钝化现象起着颇为显著的影响。
在中性溶液中,金属一般比较容易钝化,而在酸性或者某些碱性的溶液中,钝化则困难的多,这与阳极反应产物的溶解度有关。
卤素离子,特别是氯离子的存在,则明显的阻止了金属的钝化过程,已经钝化了的金属也容易被它破坏(活化),而使金属的阳极溶解速度重新增大。
溶液中存在某些具有氧化性的阴离子(如CrO42-)则可以促进金属的钝化。
2. 金属的化学组成和结构各种纯金属的钝化能力不尽相同,以铁、镍、铬三种金属为例,铬最容易钝化,镍次之,铁较差。
图1 Fe 的极化曲线物理化学实验备课材料实验10 铁的极化和钝化曲线的测定一、实验介绍任何实际的电极过程,总是要有电流通过,使其真实的电极电位偏离可逆电极电势(热力学电位),这种现象称为极化。
极化现象在电化学工业随处可见,且有利也有弊。
因此,加强对电极过程极化作用情况的测量和认识意义重大。
二、实验目的1. 测定铁在不同pH 溶液中的极化曲线。
2. 求算自腐蚀电位、自腐蚀电流、钝化电位范围、钝化 电流等电化学参数。
3. 学会使用CHI660A 电化学分析仪,掌握线性扫描伏安法和TAFEL 方法测定极化曲线。
三、实验原理铁在H 2SO 4溶液中,将不断被溶解,同时产生H 2,即:Fe + 2H + = Fe 2+ + H 2 (1)Fe /H 2SO 4体系是-个二重电极,即在Fe /H +界面上同时进行两个电极反应: Fe Fe 2+ + 2e (2)2H ++ 2e H 2 (3)反应(2)、(3)称为共轭反应。
正是由于反应(3)存在,反应(2)才能不断进行,这就是铁在酸性介质中腐蚀的主要原因。
当电极不与外电路接通时,其净电流I 总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H +还原出H 2的阴极电流I(H),它们在数值上相等但符号相反,即:(4)IFe 的大小反映Fe 在H +中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe /H +体系的自腐蚀电势εcor 。
图1是Fe 在H +中的阳极极化和阴极极化曲线图。
当对电极进行阳极极化(即加更大正电势)时,反应(3)被抑制,反应(2)加快。
此时,电化学过程以Fe 的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H +体系的阳极极化曲线rba 。
由于反应(3)是由迁越步骤所控制,所以符合塔菲尔(Tafel)半对数关系,即:(5) 直线的斜率为b Fe 。
当对电极进行阴极极化,即加更负的电势时,反应(2)被抑制,电化学过程以反应(3)为主要倾向。
极化曲线的测定及应用一、目的要求1.掌握恒电位法测定电极极化曲线的原理和实验技术。
通过测定金属铁在H2SO4 溶液中的阴极极化和阳极极化曲线求算铁的自腐蚀电位、自腐蚀电流和钝化电位范围、钝化电流等参数。
2.了解不同pH值、Cl-浓度、缓蚀剂等因素对铁电极极化的影响。
3.讨论极化曲线在金属腐蚀与防护中的应用。
二、原理Fe在H2SO 4 溶液中会不断溶解,同时产生H2。
Fe溶解:Fe -2e =Fe 2+。
H2析出:2H+ +2e =H2。
Fe电极和H2电极及溶液构成了腐蚀原电池。
其腐蚀反应为:Fe +2H+ = Fe 2+ + H2。
这是Fe在酸性溶液中腐蚀的原因。
当电极不与外电路接通时,阳极反应速率和阴极反应速率相等,Fe溶解的阳极电流I Fe与H2析出的阴极电流I H在数值上相等但方向相反,此时其净电流为零。
I=I Fe + I H=0。
I corr=I Fe=-I H≠0。
I corr值的大小反映净了Fe在H2SO 4 溶液中的腐蚀速率,所以称I corr为Fe在H2SO 4 溶液中的自腐蚀电流。
其对应的电位称为Fe在H2SO 4 溶液中的自腐蚀电位E corr,此电位不是平衡电位。
虽然,阳极反应放出的电子全部被阴极还原所消耗,在电极与溶液界面上无净电荷存在,电荷是平衡的。
但电极反应不断向一个方向进行,I corr≠0,电极处于极化状态,腐蚀产物不断生成,物质是不平衡的,这种状态称为稳态极化。
它是热力学的不稳定状态。
自腐蚀电流I corr和自腐蚀电位E corr可以通过测定极化曲线获得。
极化曲线是指电极上流过的电流与电位之间的关系曲线,即I=f(E)。
图27-1是用电化学工作站测定的Fe在1.0mol/L H2SO4 溶液中的阴极极化和阳极极化曲线图。
ar为阴极极化曲线,当对电极进行阴极极化时,阳极反应被抑制,阴极反应加速, 电化学过程以H2析出为主。
ab为阳极极化曲线,当对电极进行阳极极化时,阴极反应被抑制,阳极反应加速,电化学过程以Fe溶解为主。
电化学曲线极化曲线阻抗谱分析之樊仲川亿创作创作时间:二零二一年六月三十日一、极化曲线铁在酸溶液中, 将不竭被溶解, 同时发生H2, 即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时, 其净电流I总为零.在稳定状态下, 铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H), 它们在数值上相等但符号相反, 即: (1)I(Fe)的年夜小反映Fe在H+中的溶解速率, 而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor.图1是Fe在H+中的阳极极化和阴极极化曲线图. 图2铜合金在海水中典范极化曲线当对电极进行阳极极化(即加更年夜正电势)时, 反应(c)被抑制, 反应(b)加快.此时, 电化学过程以Fe的溶解为主要倾向.通过测定对应的极化电势和极化电流, 就可获得Fe/H+体系的阳极极化曲线rba.当对电极进行阴极极化, 即加更负的电势时, 反应(b)被抑制, 电化学过程以反应(c)为主要倾向.同理, 可获得阴极极化曲线rdc.(1)斜率斜率越小, 反应阻力越小, 腐蚀速率越年夜, 越易腐蚀. 斜率越年夜, 反应阻力越年夜, 腐蚀速率越小, 越耐腐蚀.(2)同一曲线上各各段形状变动如图2, 在section2中, 电流随电位升高的升高反而减小.这是因为此次发生了钝化现象, 发生了致密的氧化膜, 阻碍了离子的扩散, 招致腐蚀电流下降.(3)曲线随时间的变动以 7天和0天两曲线为例, 对Y轴, 七天后曲线下移(负移), 自腐蚀电位降低, 说明更容易腐蚀.对X轴, 七天后曲线正移, 腐蚀电流增年夜, 亦说明更容易腐蚀.二、阻抗谱它是基于丈量对体系施加小幅度微扰时的电化学响应, 在每个丈量的频率点的原始数据中, 都包括了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值.从这些数据中可以计算出电化学响应的实部和虚部.阻抗中涉及的参数有阻抗幅模(| Z |)、阻抗实部(Z,)、阻抗虚部(Z,,)、相位移(θ)、频率(ω)等变量, 同时还可以计算出导纳(Y)和电容(C)的实部和虚部, 因而阻抗谱可以通过多种方式暗示.2. Bode图Bode图是阻抗幅模的对数log| Z |和相角θ对相同时间的横坐标频率的对数logf的图.图4 Bode图阻抗:如果X是角频率为ω的正弦波电流信号, 则Y即为角频率也是ω的正弦电势信号.此时Y/X既称为系统的阻抗, 用Z暗示.1.溶液电阻(Rs)2.双电层电容(Cdl)3.极化阻抗(Rp)4.电荷转移电阻(Rct)5.扩散电阻(Zw)6.界面电容(C)7.电感(L)图6 两个时间常数3. Nyquist图电极的交流阻抗由实部z’和虚部z”组成, z=z’+j z”.Nyquist图是以阻抗虚部(-z”)对阻抗实部(z’)作的图.对纯电阻, 在Nyquist图上暗示为z’轴上的一点, 该点到原点的距离为电阻值的年夜小;对纯电容体系, 暗示为与z”轴重合的一条直线.图中的半圆弧就是容抗弧;后面的斜线是W扩散;感抗是低频的时候一个向下的收缩环.圆弧半径越年夜, 也就是极化电阻越年夜, 耐腐蚀越好.圆弧半径越小, 也就是极化电阻越小, 耐腐蚀越差.通过控制电极电位或者电流密度的值, 测定相应的电流密度或者电位的变动而获得的电极电位与电流密度的关系曲线, 被称为极化曲线.1.典范的、用来测试电极腐蚀速度的动电位极化曲线包括线性极化区、弱极化区和强极化区.在强极化区, 极化曲线(e-logi 图)基本是条直线, 这条直线可以用来获得电极的腐蚀速度, 而强极化区又叫Tafel区, 所以, 在不严格的说法中(通常是学生之间进行交流), 说“做个强极化曲线”、“做个Tafel曲线”(只在小木虫听到), 意思是做个动电位极化曲线, 而曲线要极化水平够年夜, 进入Tafel区.2.在分歧体系中, 动电位极化曲线的形状是分歧的.比如, 某些金属的动电位极化曲线在NaCl溶液中, 阳极极化80mV就可以进入Tafel区, 而在碱性溶液中, 却暗示出随着极化电位的增加(阳极极化同样超越80mV), 极化电流密度反而减少的现象, 即进入了钝化区.动电位极化曲线会有“钝化区”.这个钝化区和tafel 区一样, 是动电位极化曲线上的, 具有某种特性的一段区间.极化曲线获取信息1.腐蚀电位(E corr), 腐蚀电流(icorr)2.获得Tafel参数(阴极极化斜率ba, 阳极极化斜率bk)3.研究防腐蚀机理, 可以知道是阳极机制剂、阴极抑制剂或者是混合型抑制剂.4.通过腐蚀电流可以计算腐蚀抑制效率(IE%=1-i1.corr/i2.corr)由于自己电化学还不是特别了解, 可是最近投了一篇文章, 然后收到评委的回信, 其内容是:评委意见:Authors should remove the Ba value of CrN coating in Table 3, which is 1.218 V/dec because of the reliable Tafel region is not seen in relatedfigure due to passivation process.可是看图的话, 我感觉阳极有比力明显的塔菲尔区, 现在不知如何是好, 恳请年夜家给给意见和对图的看法!非常感谢塔菲尔的关系是 beta = dE/ d(log i).可是不能因为E-logi是直线关系就判断塔菲尔区. 正常的塔菲尔斜率应该在 0.12V / n 左右.n是(速率控制步的)电子传递数.也就是说, beta 最年夜不会远年夜于0.12V. 观察阳极曲线, 0 ~ 0.5V 这个区段.虽然看上去是直线, 可是这个斜率有 0.5V 那么高, 显然已经不是简单的塔菲尔关系了.而是因为概况钝化(发生氧化/氢氧化膜)而拔高了过电位.所以, 让你去失落阳极的塔菲尔斜率, 是因为它不是真正的塔菲尔区.阻抗谱半径越年夜说明阻抗越年夜, 相应的腐蚀电流就应该相对较小.做极化时可能会呈现阳极钝化, EIS对电极概况影响很小, 是不会发生钝化的.从我的极化曲线结果图中看不到阳极有钝化现象.扫描范围看需要, 只是为了确定腐蚀电位, 腐蚀电流这样的就可以在开路电压正负300mv就差未几了, 根据实际测试效果再调整一下.扫速一般要求比力慢, 可能毫伏/秒这样吧, 具体可以看看文献是多年夜.上至10mV/s, 下到0.1mV/s都有的.工作电极最好能够固定裸露面积, 圆形, 方形都有, 我觉得主要是保证每次测试的浸入面积一样自腐蚀电流越小, 耐蚀性越好, 其对应的阻抗谱的弧越年夜阻抗测试对样品影响不年夜而极化会对样品造成破坏, 1、一般先测试腐蚀电位, 2、做交流阻抗, 电位10mv 3、再做极化曲线。
铁的极化曲线
1、 Fe 在0.1mol/L 的硫酸溶液中铁的极化钝化曲线
-1.0
-0.5
0.0
0.5
1.0
1.5
2.0
-0.12
-0.10-0.08-0.06-0.04
-0.020.000.02B
A
-7
-6-5-4-3
-2-10C
A
两直线方程为:y = -5.5249x - 7.0471y = 2.5749x - 1.6552
联立两直线方程得:log Icorr= ‒3.369 , Icorr=4.276x10-4
A ,Ecorr= ‒0.6657V 。
因为实验所用电极直径为2mm,面积为Πmm 2
,
故自腐蚀电流密度=自腐蚀电流/电极面积=4.276×10-4 /(Π×0.0012)=136.1(A/ m 2
)
由图知,钝化电流Ip=3.98×10-2
A ,
钝化电流密度=3.98×10-2/(Π×0.0012)=1.26×104(A/ m 2
) 钝化电位范围:1.318−1.602V
2、Fe 在1.0mol/L 的硫酸溶液中铁的极化钝化曲线
-1.0-0.50.00.5 1.0
1.5
2.0
0.02
0.00-0.02-0.04
-0.06
-0.08
B
A
-6
-5-4-3
-2
-1
C
A
两直线方程为: y = 1.8789x - 1.622y = -3.3109x - 4.973
联立两直线方程得:log Icorr= ‒2.835 , Icorr=1.462x10-3A,Ecorr= ‒0.6657V 。
因为实验所用电极直径为2mm,面积为Πmm 2,
故自腐蚀电流密度=自腐蚀电流/电极面积=1.462×10-3 /(Π×0.0012)=465.3(A/ m 2) 由图知,钝化电流Ip=4.46×10-2A ,
钝化电流密度=4.46×10-2/(Π×0.0012)=1.42×104(A/ m 2) 钝化电位范围:0.583−1.324V
3、Fe 在1.0mol/L 的HCl 溶液中铁的极化钝化曲线
-1.0
-0.5
0.0
0.5
1.0
1.5
2.0
-0.035
-0.030-0.025-0.020-0.015-0.010
-0.0050.0000.0050.010B
A
-6
-5
-4
-3
-2
-1
C
A
两直线方程为:y = -1.9267x - 4.171y = 1.9989x - 2.1957
联立两直线方程得:log Icorr= ‒3.202A , Icorr=6.280×10-4A ; Ecorr= ‒0.503V 。
因为实验所用电极直径为2mm,面积为Πmm 2,
故自腐蚀电流密度=自腐蚀电流/电极面积=6.280×10-4 /(Π×0.0012)=199.8(A/ m 2)
自腐蚀速率与自腐蚀电流密度关系为:ν=3600MI/nF (其中M=56g/mol,n=2,F=96484C/mol) 故腐蚀速率:v=208.7g/(m 2·h) Fe 在盐酸中不钝化。
4、Fe 在含1%的乌洛托品的1.0mol/L 的HCl 溶液中铁的极化钝化曲线
-1.0
-0.5
0.0
0.5
1.0
1.5
2.0
-0.16
-0.14-0.12-0.10-0.08-0.06
-0.04-0.020.000.02B
A
-7
-6-5-4-3
-2
-1
C
A
两直线方程为:y = -3.8552x - 6.0255y = 4.3464x - 1.3712
联立两直线方程得:log Icorr=-3.838 A , Icorr=1.452×10-4A ; Ecorr= ‒0.567V 。
因为实验所用电极直径为2mm,面积为Πmm 2,
故自腐蚀电流密度=自腐蚀电流/电极面积=1.452×10-4 /(Π×0.0012)=46.2(A/ m 2)
自腐蚀速率与自腐蚀电流密度关系为:ν=3600MI/nF (其中M=56g/mol,n=2,F=96484C/mol) 故腐蚀速率:v=48.2g/(m 2·h)
加入1%乌洛托品后,Fe 在盐酸中的自腐蚀电流明显下降,抑制了Fe 的腐蚀。