有机化合物(三)——生活中常见的两种有机物
- 格式:doc
- 大小:147.50 KB
- 文档页数:3



人教版高中化学必修二:《生活中两种常有的有机物》●生活中两种常有的有机物乙醇教课方案●教材剖析及教材办理《生活中两种常有的有机物》是新课标人教版一般高中化学必修 2 第三章《有机化合物》第三节的内容,本节内容选用了乙醇和乙酸这两个生活中典型的有机物,并对乙醇和乙酸的构成、构造、主要性质以及在生活、生产中的应用进行了简单的介绍。
本节内容分 2 课时,第 1 课时介绍生活中常有的有机物——乙醇。
在初中化学中,只简单介绍了乙醇的用途,没有从构成和构造角度认识其性质、存在和用途。
乙醇是学生比较熟习的物质,又是典型的烃的含氧衍生物,所以,乙醇的构造和性质是本节的要点。
经过本节课的学习,让学生初步成立起官团对有机物性质的重要影响,建立“(构成)构造→性质→用途”的有机物学习模式,为此后学习其余的烃的衍生物打下优异的基础。
本课时实验内容许多,经过实验能培育学生的研究能力、操作能力、察看能力、剖析能力等。
为了使教课拥有更强的逻辑性,对教材处理以下:先联系生活及展现酒精灯,小结出乙醇的物理性质,依据乙醇的分子式猜想乙醇的构造,并经过实验考证乙醇的构造,构造决定性质,再学习乙醇的性质,并联系生活中的例子加深对性质的学习。
第 2 课时介绍乙酸,包括乙酸的分子构造特色、物理性质、化学性质、乙酸的用途等,乙酸的构造和性质是本课时的教课要点,特别是酯化反响的特色是要点难点。
经过联系生活引出乙酸,学习乙酸的构造,再学习其性质,要点剖析酯化反响。
●教课模式与学习方式设计在学生初中知识的基础上,突出从烃到烃的衍生物的构造变化,重申官能团与性质的关系,在学生的脑筋中逐渐成立烃基与官能团地点关系等立体构造模型,帮助学生打好进一步学习的方法论基础,同时鼓舞学生用学习到的知识解说常有有机物的性质和用途。
我设计的教课模式和学习方式以下:1、实验法:充足发挥学生主体作用,经过设计问题,实验研究,展现获得知识的过程,按“疑问→实验→思虑→指引→得出结论→应用”的模式进行教课,从而调换学生的内在动力,促进学生主动去研究知识; 2、情形激学法:创建问题的境界(酒精汽油的推行、饮酒脸红、酒后驾驶的查验等),激发学习兴趣,调换学生内在的学习动力,促进学生在境界中主动研究科学的奇妙。

第三节 生活中两种常见的有机物一、乙醇1、 分子结构乙醇的分子式C 2H 6O ,结构式为: 结构简式为CH 2CH 2OH 或C 2H 5OH 。
含有官能团—OH (羟基)【拓展知识点一】①醇:羟基不与苯环直接相连,称为醇。
②酚:羟基直接与苯环相连,称为酚。
注:⑴乙醇可以看作是乙烷分子中的氢原子被羟基取代后的产物。
⑵衍生物:烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物。
⑶官能团:决定有机化合物主要化学性质的原子或原子团。
⑷“-OH ”与“OH -”的区别例:下列有机物中,不属于烃的衍生物的是( )B. CH 3CH 2NO 2C. CH 3CH 2BrD.2、 物理性质3、 化学性质⑴乙醇与金属钠的反应(见书实验)乙醇在发生化学反应时,可以是C —O 键断裂,也可以是C —H 键或H —O 键断裂,从而发生不同的反应。
与活泼金属Na 、K 、Mg 等反应(①键断裂)2CH 3CH 2OH+2N a →2CH 3CH 2ONa+H 2↑此反应比钠与水反应缓和得多,说明乙醇羟基上氢原子不如水分子中的氢原子活泼。
⑵氧化反应a. 燃烧(断①②③④⑤)b. 催化氧化(①③键断裂)2 CH 3CH 2OH+O 2−−−−→−加热或g Cu A 2 CH 3CHO+2H 2O ①催化剂的反应原理:(分步)2Cu+O 2加热2CuO 2C 2H 5OH+2CuO −−→−加热2C 2H 4O+2H 2O+2Cu 总式:2 CH 3CH 2OH+O 2−−−−→−加热或g Cu A 2 CH 3CHO+2H 2O (现象:铜丝由红变黑,很快又变红) 羟基与连羟基的碳原子各脱去一个氢原子。
注:如果连羟基的碳原子上无氢原子,则该醇就不能在Cu 或Ag 的作用下被氧化,但可燃烧。
例1:乙醇在一定条件下发生化学反应,化学键断裂的位置如下所示,则乙醇在催化氧化时,化学键断裂的位置是( )例2:I.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯的外焰上加热,待铜丝表面变黑后立即把它插入盛有2mL 乙醇的试管里,反复操作几次。


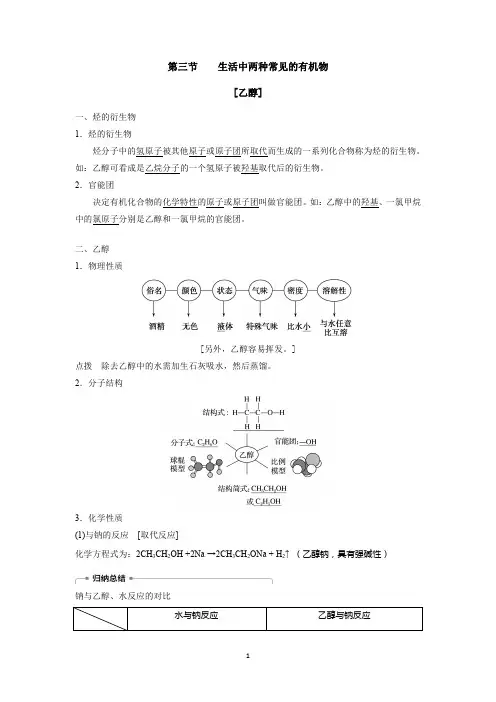
第三节生活中两种常见的有机物[乙醇]一、烃的衍生物1.烃的衍生物烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。
如:乙醇可看成是乙烷分子的一个氢原子被羟基取代后的衍生物。
2.官能团决定有机化合物的化学特性的原子或原子团叫做官能团。
如:乙醇中的羟基、一氯甲烷中的氯原子分别是乙醇和一氯甲烷的官能团。
二、乙醇1.物理性质[另外,乙醇容易挥发。
]点拨除去乙醇中的水需加生石灰吸水,然后蒸馏。
2.分子结构3.化学性质(1)与钠的反应[取代反应]化学方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑(乙醇钠,具有强碱性)钠与乙醇、水反应的对比水与钠反应乙醇与钠反应钠的变化钠粒浮于水面,熔成闪亮的小球,并快速地四处游动,很快消失钠粒开始沉于试管底部,未熔化,最终慢慢消失声的现象有“嘶嘶”声响无声响气体检验点燃,发出淡蓝色的火焰点燃,发出淡蓝色的火焰实验结论钠的密度小于水,熔点低。
钠与水剧烈反应,生成氢气。
水分子中羟基上的氢原子比较活泼钠的密度比乙醇的大。
钠与乙醇缓慢反应生成氢气。
乙醇中羟基上的氢原子相对不活泼反应的化学方程式2Na +2H 2O===2NaOH +H 2↑2Na +2CH 3CH 2OH ―→2CH 3CH 2ONa +H 2↑(2)氧化反应①燃烧化学方程式为:C 2H 5OH +3O 2――→点燃2CO 2+3H 2O 。
②催化氧化实验操作实验现象在空气中灼烧过的铜丝表面由黑变红,试管中的液体有刺激性气味化学方程式2CH 3CH 2OH +O 2――→Cu 或Ag△2CH 3CHO +2H 2O ③与强氧化剂反应乙醇可被酸性高锰酸钾溶液或酸性重铬酸钾溶液氧化,生成乙酸。
点拨在乙醇的催化氧化实验中,要把铜丝制成螺旋状,是为了增大接触受热面积,增强实验效果。
乙醇催化氧化的实质4.用途(1)用作酒精灯、火锅、内燃机等的燃料。
(2)用作化工原料。
(3)医疗上常用体积分数为75%的乙醇溶液作消毒剂。


生活中两种常见的有机物乙醇说课稿生活中两种常见的有机物乙醇说课稿1今天我说课的内容是普通高中课程标准实验教科书化学必修II第三章第三节《生活中两种常见有机物》的第一课时乙醇,下面我从七个方面谈谈我对这节课处理的一些看法:一、说教材分析(一)、本节课的地位和作用本节课的教学内容是选取生活中的典型代表有机物——乙醇。
乙醇是学生比较熟悉的生活用品,又是典型的烃的衍生物。
本节课主要从这种衍生物的组成、结构和性质出发,让学生知道官能团对有机物性质的重要影响,建立有机物“(组成)结构—性质—用途”的有机物学习模式,对学生了解学习和研究有机物的一般方法,形成一定的分析和解决问题的能力有着重要的意义。
本节内容安排在烃以后,是从烃过渡到烃的衍生物的重要环节,强调从烃到烃的衍生物的结构变化,官能团与性质的关系,对于学好本章书其它烃的衍生物的知识有着重要的承上启下及指导性的作用。
另外乙醇在实际生活、工农业生产、科学研究中应用十分广泛,因此学好本节知识,也具有比较重要的理论意义和现实意义。
(二)、教学三维目标1、知识与技能:通过对乙醇的分子结构、物理性质和化学性质的探究,使学生掌握乙醇的结构式、性质和用途。
了解羟基的特性,理解和掌握“官能团”的概念。
学会由事物的表象解析事物的本质、变化,进一步培养学生的综合探究能力、空间想象能力和创造性思维能力,通过从动手实验,规范学生操作,全面培养、提高学生的实验能力、观察能力和对实验现象的解析能力。
2、过程与方法:通过提示问题、讨论释疑、动手实验,学习对比、推断等多种科学探究方法。
3、情感态度与价值观:培养学生的审美意识和爱国主义情操;让学生体验科学探究的艰辛和乐趣,认识化学与人类生活密切关系,激发学生学习化学的积极性。
(三)、教学重点、难点1教学重点:乙醇分子结构推断过程,乙醇的性质和用途对教学重点确定的说明:将乙醇分子结构推断过程确定为重点的理论依据为布鲁纳的学习理论。
布鲁纳学习理论认为:“认识是一个过程,而不是一种产品。

(人教必修2)3.3.1《生活中两种常见的有机物》教学设计第一课时乙醇的结构与性质【情景导入】“无酒不成席”,当今社会酒已经成为人们餐桌上常见的饮品之一。
中国是最早酿酒的国家,中国的酒文化源远流长,有许多关于酒的脍炙人口的诗句,如:明月几时有,把酒问青天。
葡萄美酒夜光杯,欲饮琵琶马上催。
白日放歌须纵酒,青春做伴好还乡……这些咏叹酒的诗句证明酒是一种奇特而富有魅力的饮料,哪么其主要成分是什么呢?下面我们来细品一下它那“令人陶醉的醇香”吧!【板书】活动一:乙醇的分子结构及烃的衍生物【探究】:已知4.6克无水乙醇在氧气中完全燃烧,只生成8.8克CO2和5.4克H2O,则无水乙醇中含有哪几种元素?能确定其分子式吗?【交流】8.8克CO2 中含有C元素2.4克,5.4克H2O中含有H元素0.6克,则4.6克无水乙醇还含有O元素1.6克。
故乙醇中C、H、O原子个数比为:2∶ 6∶ 1,其最简式(实验式)为:C2H6O。
若要确定乙醇的分子式,还需要知道其相对分子质量,实验测得乙醇的相对分子质量为46,则可知其分子式为C2H6O。
【思考】阅读教材P74页内容,结合原子的成键规律,思考分子式为C2H6O的有机物有哪些可能的结构?【交流】乙醇分子分子式C2H6O,分子中有6个氢原子,根据我们学过的碳四价的原则,可能的结构式有两种:,其结构特征分别是甲式含有—OH原子团,乙式含有R —O—R(烃基)原子团。
【实验探究】完成教材P73实验3-2,并将实验现象记录在下面表格内。
【交流投影】实验操作实验现象①钠开始沉于试管底部,最终慢慢消失,产生无色可燃性气体;②烧杯内壁有水珠产生;③向烧杯中加入澄清石灰水不变浑浊实验结论乙醇与钠反应生成H2,说明乙醇分子里含有不同于烃分子里的氢原子存在,即乙醇的结构简式应该为CH3CH2OH,可以看成是乙烷中的1个氢原子被原子团-OH(羟基)所取代后的产物。
化学方程式:2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑注意:根据金属钠保存方法也可以说明金属钠不能与烷烃反应。

生活中两种常见的有机物——乙酸案例乙酸是一种简单的有机化合物,化学式为CH3COOH。
它是一种无色液体,具有刺激性气味,并且可以溶于水。
乙酸在生活中有着多种应用,下面将分别介绍乙酸在食品和化妆品中的应用。
首先,乙酸在食品中的应用非常广泛。
乙酸可用于酱料的制作,如醋和味淋。
醋中含有5-20%的乙酸,它具有酸味和醇香,可以提高菜肴的口感。
味淋中也含有乙酸,它是一种常用的调味品,在烹饪中常用于调配炖汤、调味调料等。
其次,乙酸在酒精饮料中也有应用。
酒精饮料中含有一定比例的乙酸,它可以提供酒精饮料的酸度和风味。
例如,啤酒中的乙酸可以增加啤酒的口感和醇香。
此外,一些果酒和葡萄酒中也含有乙酸,它能够增加酒的酸度,提升口感和香气。
乙酸还可以用于食品保鲜。
乙酸具有抑菌和防腐的作用,可以延长食品的保质期。
例如,腌制食品中常使用醋来调味和保鲜。
乙酸可以降低食品中的pH值,抑制微生物的生长。
此外,乙酸还具有抑制霉菌和细菌的作用,可以预防食品腐败。
另一方面,在化妆品中,乙酸也有着广泛的应用。
乙酸是一种弱酸,可以调节化妆品的酸碱度。
在化妆品中添加适量的乙酸可以使其具有更好的质感和稳定性。
例如,一些洗发水和护发素中含有乙酸,它可以调节洗发水和护发素的pH值,减少静电,使头发更加柔顺光滑。
此外,乙酸还可以用作化妆品中的溶剂。
乙酸是一种极性有机溶剂,可以溶解许多化妆品中的成分。
例如,一些化妆水和精华液中含有乙酸,它可以帮助其他成分更好地渗透皮肤,并提供额外的护肤效果。
总之,乙酸是一种在生活中广泛应用的有机物。
在食品中,乙酸可以用于调味和保鲜;在化妆品中,乙酸可以用于调节酸碱度和作为溶剂。
乙酸的应用使得我们的食品更加美味,化妆品更加有效。
然而,我们在使用乙酸时也需要注意适量使用,避免对身体和环境造成不必要的危害。
第三节生活中两种常见的有机物第一课时乙醇一、课标分析本节课遵循“从生活到化学,从化学到生活”的基本思路。
根据课程标准“通过以化学实验为主的多种探究活动,使学生体验科学探究的过程,激发学习化学的兴趣,强化科学探究意识,促进学习方式的转变,在实践中培养学生的创新精神和实践能力”的要求,本节课通过理论引导、科学假设、实践验证设计相关实验,以完成“乙醇的结构探究、乙醇的催化氧化和乙醇被强氧化剂氧化”的教学。
通过介绍“醉酒原理、生命不能承受之醉、酒驾的检测”及“在生产生活中的广泛应用”,培养学生辩证唯物主义世界观。
二、教材的内容、地位和作用《乙醇》是新课标人教版高中化学必修2第三章《有机化合物》第三节《生活中两种常见的有机物》第一课时的内容。
《普通高中化学课程标准》指出:知道乙醇的主要性质,认识其在日常生活中的应用。
乙醇作为联系烃和烃的衍生物性质的桥梁,在有机物的相互转化中处核心地位,与生产、生活联系紧密,是一种具有广泛用途的有机物,可进一步完善有机物的知识体系,为选修5《有机化学基础》学习打下基础。
三、教学目标分析1、知识与技能掌握乙醇的组成、分子结构与主要化学性质,了解它的主要用途。
通过乙醇的分子结构与化学性质的学习,充分理解官能团对性质的影响,学会由事物的表象分析事物的本质、变化,进一步培养学生综合运用知识、解决问题的能力。
2、过程与方法通过建立乙醇分子的立体结构模型,从结构角度初步认识乙醇的氧化的原理和实质。
从乙醇的组成、结构和性质出发,学习由“(组成)结构—性质—用途”研究烃的衍生物的方法。
从观察实验现象入手,分析产生实验现象的因果关系和本质的联系,培养多方面认识事物的能力。
3、情感态度与价值观知道乙醇在日常生活、工业生产中的广泛应用,形成运用知识解决实际问题的意识。
通过新旧知识的联系,激发学生学习的兴趣和求知欲望;通过分组实验,体验科学探究的过程,养成团结合作的品质,培养学生求实、严谨的优良品质。
有机化合物(三)——生活中常见的两种有机物
1.[2017·全国Ⅱ]下列由实验得出的结论正确的是()
3.[2016年Ⅲ卷,8]下列说法错误的是()
A.乙烷室温下能与浓盐酸发生取代反应B.乙烯可以用作生产食品包装材料的原料
C.乙醇室温下在水中的溶解度大于溴乙烷D.乙酸与甲酸甲酯互为同分异构体
4.判断下列说法的正误。
(1)[2016年Ⅰ卷,10]用长颈漏斗分离出乙酸与乙醇反应的产物( )
(2)[2018年Ⅰ卷,10] 92.0 g甘油(丙三醇)中含有羟基数为1.0N A ( )
(3)医用酒精的浓度通常为95% ( )
(4)碘易溶于有机溶剂,因此可用乙醇萃取碘水中的碘( )
(5)用食醋可除去热水壶内壁的水垢( )
(6)乙醇可被酸性KMnO4溶液氧化为乙醛,但不能氧化为乙酸( )
(7)乙醇、乙酸与Na2CO3溶液反应均产生CO2 ( )
(8)C2H185OH和CH3COOH发生酯化反应生成有机物CH3COOC2H5( )
(9)1 mol C2H5OH和1 mol CH3COOH在浓硫酸作用下加热,可以完全反应生成1 mol CH3COOC2H5( ) 5.下列关于有机物的说法正确的是()
A.乙醇、乙酸、乙酸乙酯都能发生取代反应,且都有同分异构体
B.汽油、煤油、植物油均为含碳、氢、氧三种元素的化合物
C.乙酸与丙二酸互为同系物
D.苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴
6.下列实验中,所采取的分离方法与对应原理都正确的是()
7.(2017·潍坊一模)下列说法中,不正确的是()
A.乙醇与金属钠反应时,是乙醇分子中羟基中的O—H键断裂
B.检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水
C.乙醇在一定条件下可氧化成CH3COOH
D.甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物
8.柠檬中含有大量的柠檬酸,因此被誉为“柠檬酸仓库”。
柠檬酸的结构简式如右图,则1 mol柠檬酸分别与足量的金属钠和NaOH溶液反应,最多可消耗Na和NaOH的物质的量分别为()
A.2 mol、2 mol B.3 mol、4 mol
C.4 mol、3 mol D.4 mol、4 mol
9.下列关于酯化反应说法正确的是()
A.用CH3CH182OH与CH3COOH发生酯化反应,生成H182O
B.反应液混合时,顺序为先加入乙醇,再加入浓硫酸,最后加入乙酸
C.乙酸乙酯不会和水反应生成乙酸和乙醇
D.用蒸馏的方法从饱和Na2CO3溶液中分离出乙酸乙酯
10.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如下图,下列
对该实验的描述错误的是()
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
11.关于有机物的说法正确的是()
A.b的同分异构体中含有羧基的结构有7种(不含立体异构)
B.a、b互为同系物
C.c中所有碳原子可能处于同一平面
D.a、b、c均能使酸性高锰酸钾溶液褪色
12.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:
(1)在a 中加入15 mL 无水苯和少量铁屑。
在b 中小心加入4.0 mL 液态溴。
向a 中滴入几滴溴,有白雾产生,是因为生成了______气体。
继续滴加至液溴滴完。
装置 d 的作用是_______________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a 中加入10 mL 水,然后过滤除去未反应的铁屑。
②滤液依次用10 mL 水、8 mL 10%的NaOH 溶液、10 mL 水洗涤。
NaOH 溶液洗涤的作用是__________________。
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
加入氯化钙的目的是____________________________。
(3) 经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必需的是________(填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a 的容积最适合的是________。
A.25 mL B.50 mL C.250 mL D.500 mL。