扩散与固相反应
- 格式:doc
- 大小:29.00 KB
- 文档页数:3





第七章 扩散与固相反应1、名词解释:非稳定扩散:扩散过程中任一点浓度随时间变化;稳定扩散:扩散质点浓度分布不随时间变化。
无序扩散:无化学位梯度、浓度梯度、无外场推动力,由热起伏引起的扩散。
质点的扩散是无序的、随机的。
本征扩散:主要出现了肖特基和弗兰克尔点缺陷,由此点缺陷引起的扩散为本征扩散(空位来源于晶体结构中本征热缺陷而引起的质点迁移);非本征扩散:空位来源于掺杂而引起的质点迁移。
正扩散和逆扩散:正扩散:当热力学因子时,物质由高浓度处流向低浓度处,扩散结果使溶质趋于均匀化,D i >0。
逆扩散:当热力学因子 时,物质由低浓度处流向高浓度处,扩散结果使溶质偏聚或分相,D i <0。
2、简述固体内粒子的迁移方式有几种?答 易位,环转位,空位扩散,间隙扩散,推填式。
3、说明影响扩散的因素?化学键:共价键方向性限制不利间隙扩散,空位扩散为主。
金属键离子键以空位扩散为主,间隙离子较小时以间隙扩散为主。
缺陷:缺陷部位会成为质点扩散的快速通道,有利扩散。
温度:D=D 0exp (-Q/RT )Q 不变,温度升高扩散系数增大有利扩散。
Q 越大温度变化对扩散系数越敏感。
杂质:杂质与介质形成化合物降低扩散速度;杂质与空位缔合有利扩散;杂质含量大本征扩散和非本征扩散的温度转折点升高。
扩散物质的性质:扩散质点和介质的性质差异大利于扩散;扩散介质的结构:结构紧密不利扩散。
4、在KCl 晶体中掺入10-5mo1%CaCl 2,低温时KCl 中的K +离子扩散以非本征扩散为主,试回答在多高温度以上,K +离子扩散以热缺陷控制的本征扩散为主?(KCl 的肖特基缺陷形成能ΔH s =251kJ/mol ,R=8.314J/mo1·K ) 解:在KCl 晶体中掺入10-5mo1%CaCl 2,缺陷方程为:2'22KCl K K cl CaCl Ca V Cl ∙⨯−−−→++则掺杂引起的空位浓度为'710K V -⎡⎤=⎣⎦欲使扩散以热缺陷为主,则''K K V V ⎡⎤⎡⎤>⎣⎦⎣⎦肖 即7exp()102s H RT-∆-> 即7251000exp()1028.314T -->⨯ 解得T>936.5K5、(1)试述晶体中质点的扩散机构及方式。


实验28 热重分析技术在固相反应研究中的应用一、实验目的固相反应是材料制备中一个重要的高温动力学过程,固体之间能否进行反应、反应完成的程度、反应过程的控制等直接影响材料的显微结构,并最终决定材料的性质,因此,研究固体之间反应的机理及动力学规律,对传统和新型无机非金属材料的生产有重要的意义。
本实验的目的:1.掌握TG法的原理,熟悉采用TG法研究固相反应的方法。
2.通过CaCO3-SiO2系统的反应验证固相反应的动力学规律─杨德方程。
3.通过作图计算出反应的速度常数和反应的表观活化能。
二、实验原理许多固体材料在在高温下加热时,因其中的某些组分分解逸出或固体与周围介质中的某些物质作用使固体物系的重量发生变化,如盐类的分解、含水矿物的脱水、有机质的燃烧等会使物系重量减轻,高温氧化、反应烧结等则会使物系重量增加。
热重分析法(Thermogravimetric Analysis.简称TG) 及微商热重法(derivative thermogravimetry,简称DTG 法)是在程序控制温度下,测量物质质量与温度关系的一种技术。
微商热重法所记录的是TG曲线对温度或时间的一阶导数,所得的曲线称为DTG曲线。
现在的热重分析仪常与微分装置联用,可同时得到TG- DTG曲线。
通过测量物系质量随温度或时间的变化可以间接地揭示固体物系反应的机理和/或反应动力学规律。
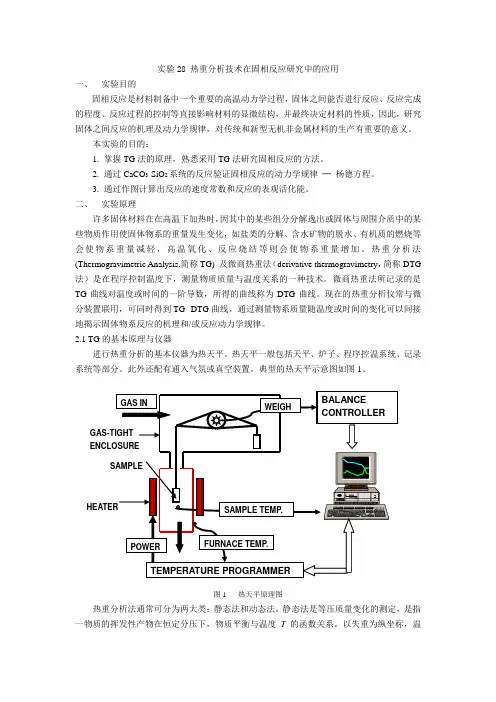
2.1 TG的基本原理与仪器进行热重分析的基本仪器为热天平。
热天平一般包括天平、炉子、程序控温系统、记录系统等部分。
此外还配有通入气氛或真空装置。
典型的热天平示意图如图1。
图1 热天平原理图热重分析法通常可分为两大类:静态法和动态法。
静态法是等压质量变化的测定,是指一物质的挥发性产物在恒定分压下,物质平衡与温度T的函数关系。
以失重为纵坐标,温度T为横坐标作等压质量变化曲线图。
等温质量变化的测定是指一物质在恒温下,物质质量变化与时间t的依赖关系,以质量变化为纵坐标,以时间为横坐标,获得等温质量变化曲线图。


扩散与固相反应扩散与固相反应7-1 试分析碳原⼦在⾯⼼⽴⽅和体⼼⽴⽅铁⼋⾯体空隙间跳跃情况,并以D =γr 2Γ形式写出其扩散系数(设点阵常数为a )。
(式中r 为跃迁⾃由程;γ为⼏何因⼦;Γ为跃迁频率。
)7-2 设有⼀种由等直径的A 、B 原⼦组成的置换型固溶体。
该固溶体具有简单⽴⽅的晶体结构,点阵常数A =0.3nm ,且A 原⼦在固溶体中分布成直线变化,在0.12mm 距离内原⼦百分数由0.15增⾄0.63。
⼜设A 原⼦跃迁频率Γ=10-6s -1,试求每秒内通过单位截⾯的A 原⼦数?7-3 制造晶体管的⽅法之⼀是将杂质原⼦扩散进⼊半导体材料如硅中。
假如硅⽚厚度是0.1cm ,在其中每107个硅原⼦中含有⼀个磷原⼦,⽽在表⾯上是涂有每107个硅原⼦中有400个磷原⼦,计算浓度梯度(a )每cm 上原⼦百分数,(b )每cm 上单位体积的原⼦百分数。
硅晶格常数为0.5431nm 。
7-4 已知MgO 多晶材料中Mg 2+离⼦本征扩散系数(D in )和⾮本征扩散系数(D ex )由下式给出2524860000249exp() cm 2545001210exp() cm ..in ex D RTD RT -=-=?- (a )分别求出25℃和1000℃时,Mg 2+的(D in )和(D ex )。
(b )试求在Mg 2+的ln D ~1/T 图中,由⾮本征扩散转变为本征扩散的转折点温度? 7-5 从7-4题所给出的D in 和D ex 式中求MgO 晶体的肖特基缺陷形成焓。
若欲使Mg 2+在MgO 中的扩散直⾄MgO 熔点2800℃时仍是⾮本征扩散,试求三价杂质离⼦应有什么样的浓度?7-6 若认为晶界的扩散通道宽度⼀般为0.5nm ,试证明原⼦通过晶界扩散和晶格扩散的质量之⽐为910()()gb v D d D -。
其中d 为晶粒平均直径;D gb 、D v 分别为晶界扩散系数和晶格扩散系数。

第七章 扩散与固相反应例 题7-1 试分析碳原子在面心立方和体心立方铁八面体空隙间跳跃情况,并以D =γr 2Γ形式写出其扩散系数(设点阵常数为a )。
(式中r 为跃迁自由程;γ为几何因子;Γ为跃迁频率。
)解:在面心立方晶体中,八面体空隙中心在晶胞体心及棱边中心。
相邻空隙连线均为[110]晶向,空隙间距为。
因而碳原子通过在平行的[110]晶面之间跳动完成扩散。
若取[110]为X 轴、]101[为Y 轴、[001]为Z 轴,则碳原子沿这三个轴正反方向跳动的机会相等。
因此碳原子在平行[110]晶面之间跳动的几率即几何因子γ=1/6。
在体心立方晶体中,八面体空隙中心在晶胞面心及核边中心,相邻空隙间距为a /2。
其连线为[110]晶向,可以认为碳原子通过在平行的[200]晶面之间来完成扩散,取[100]、[010]、[001]为X 、Y 、Z 轴。
碳原子沿这三个轴正反方向跳动机会均等,因而碳原子在平行的[200]晶面间跳动的几率γ=1/6。
在面心立方铁中2261==r γ代入2D r γ=Γ12)2(6122ΓΓa aD =⨯⨯=面心在体心立方铁中16γ=2r a =24)2(6122ΓΓa a D =⨯⨯=体心7-2 设有一种由等直径的A 、B 原子组成的置换型固溶体。
该固溶体具有简单立方的晶体结构,点阵常数a =,且A 原子在固溶体中分布成直线变化,在0.12mm 距离内原子百分数由增至。
又设A 原子跃迁频率Γ=10-6s -1,试求每秒内通过单位截面的A 原子数解:已知16s 101--⨯=Γ,16γ=;nm 30.==a r ;求扩散通量J 。
s cm 105110)1030(612226372---⨯=⨯⨯⨯==..r D Γγ每cm 3固溶体内所含原子数为322371073)1030(1个⨯=⨯-..2224222421201506337101481000121510148102210s cm ........dc dx J D dc dx ----=⨯⨯=-⨯=-=⨯⨯⨯=⨯7-3 制造晶体管的方法之一是将杂质原子扩散进入半导体材料如硅中。
固相反应法的扩散原理固相反应法是一种常用于合成无机材料的方法,它基于反应物在固体相中的扩散过程,常被用于合成无机材料、合成陶瓷、高温材料和催化剂等。
在固相反应法中,反应物通过扩散在固体相中发生反应,产生所需的产物。
固相反应法的扩散原理可以从多个角度来解释。
以下将从热力学、扩散动力学和固体反应机理三个方面进行讨论。
首先,从热力学角度来看,固相反应需要满足热力学的平衡条件。
这意味着反应混合物组分的化学势之差在反应过程中趋于零。
在固相反应中,反应物分子通过扩散逐渐相互接触,形成局部的处于平衡状态的小区域。
在这些小区域内,反应物由于浓度梯度和局部的温度梯度,会发生反应并释放出能量。
随着时间的推移,反应会逐渐在整个反应体系中进行,直到达到平衡状态。
因此,固相反应法的扩散原理与热力学平衡密切相关。
其次,从扩散动力学的角度来看,固相反应是通过固体颗粒之间的物质迁移实现的。
扩散作为固体相中的质量传递过程,是指物质在固体内部的非均匀分布的自发性移动。
固体颗粒之间存在浓度梯度,质量从梯度高的区域扩散到梯度低的区域。
在固相反应中,反应物的迁移路径通常是由固体颗粒的晶格结构以及物质扩散的速率决定的。
例如,在固相反应法中,反应物粉末的大小、形状和分布对反应速率和产物的物理性质具有显著影响。
因此,固相反应法的扩散原理与物质分子的迁移和扩散速率有关。
最后,从固体反应机理的角度来看,固相反应法是通过反应物的物质转移和相互作用实现的。
在固相反应中,反应物的化学成分从一个相转移到另一个相,进而形成产物。
通常,反应物的转移路径可以分为三个步骤:扩散、表面反应和体相反应。
首先,反应物通过扩散进入固体颗粒相互接触的位置。
然后,在固体颗粒的表面处发生反应,通常是一些中间生成物的生成和反应。
最后,中间生成物会继续在固体内部进行扩散和反应,直到形成所需的产物。
因此,固相反应法的扩散原理与反应物的物质转移和固体表面反应密切相关。
综上所述,固相反应法的扩散原理涉及热力学平衡、扩散动力学和固体反应机理等方面。
内外扩散对气固相催化反应的影响规律篇一:气固相催化反应是指将气体和固体材料之间的反应速率影响因素进行分析和优化,以实现高效的化学反应。
在气固相催化反应中,扩散是一个非常重要的因素,它影响着反应物的传输速率、反应速率和催化剂的寿命等。
本文将介绍气固相催化反应中扩散的影响规律,并探讨如何优化扩散条件以提高催化反应的效率和性能。
一、扩散对气固相催化反应的影响规律1. 扩散系数的影响扩散系数是指物质在两种不同介质之间传输的速率。
在气固相催化反应中,扩散系数取决于物质的相态、温度、压强等因素。
通常情况下,气体分子的扩散系数比固体分子的扩散系数更大,因此在气固相催化反应中,气体分子的扩散速率更快。
2. 温度的影响温度是影响物质扩散的重要因素。
通常情况下,随着温度的升高,扩散系数会减小,这意味着在气固相催化反应中,温度升高会使气体分子的扩散速率更快。
3. 压强的影响压强也是影响物质扩散的重要因素。
通常情况下,随着压强的增大,扩散系数会减小,这意味着在气固相催化反应中,压强增大会使气体分子的扩散速率更快。
4. 物质相态的影响物质相态也会影响扩散速率。
通常情况下,气体分子的扩散速率比固体分子的扩散速率更快。
这是因为气体分子的自由度更大,更容易在固体表面上自由移动。
二、如何优化扩散条件以提高催化反应的效率和性能在气固相催化反应中,优化扩散条件可以提高催化反应的效率和性能。
以下是几种优化扩散条件的方法:1. 选择合适的催化剂和反应条件选择合适的催化剂和反应条件可以优化催化反应的效率和性能。
例如,在选择催化剂时,可以考虑催化剂的活性、选择性、稳定性等因素。
在反应条件方面,可以考虑选择合适的温度、压强、气体浓度等因素。
2. 设计合理的扩散系统设计合理的扩散系统可以提高扩散速率,从而优化催化反应的效率和性能。
例如,可以采用多孔材料、纳米材料等来提高催化剂的表面活性,采用高温高压技术来提高气体分子的扩散速率。
3. 采用合适的添加剂采用合适的添加剂可以提高催化剂的表面积和活性,从而优化催化反应的效率和性能。
第七章扩散与固相反应§7-1 晶体中扩散的基本特点与宏观动力学方程一、基本特点1、固体中明显的质点扩散常开始于较高的温度,但实际上又往往低于固体的熔点;2、晶体中质点扩散往往具有各向异性,扩散速率远低于流体中的情况。
二、扩散动力学方程1、稳定扩散和不稳定扩散在晶体A中如果存在一组分B的浓度差,则该组分将沿着浓度减少的方向扩散,晶体A作为扩散介质存在,而组分B则为扩散物质。
如图,图中dx为扩散介质中垂直于扩散方向x的一薄层,在dx两侧,扩散物质的浓度分别为c1和c2,且c1>c2,扩散物质在扩散介质中浓度分布位置是x的函数,扩散物质将在浓度梯度的推动下沿x方向扩散。
的浓度分布不随时间变的扩散过程稳定扩散:若扩散物质在扩散层dx内各处的浓度不随时间而变化,即dc/dt=0。
这种扩散称稳定扩散。
不稳定扩散:扩散物质在扩散层dx内的浓度随时间而变化,即dc/dt≠0。
这种扩散称为不稳定扩散。
2、菲克定律(1)菲克第一定律在扩散体系中,参与扩散质点的浓度因位置而异,且随时间而变化,即浓度是坐标x、y、z和时间t函数,在扩散过程中,单位时间内通过单位横截面积的质点数目(或称扩散流量密度)j之比于扩散质点的浓度梯度△cD:扩散系数;其量纲为L2T-1,单位m2/s。
负号表示粒子从浓度高处向浓度低处扩散,即逆浓度梯度的方向扩散,对于一般非立方对称结构晶体,扩散系数D为二阶张量,上式可写为:对于大部分的玻璃或各向同性的多晶陶瓷材料,可认为扩散系数D将与扩散方向无关而为一标量。
J x=-D J x----沿x方向的扩散流量密度J y=-D J y---沿Y方向的扩散流量密度J z=-D J z---沿Z方向的扩散流量密度适用于:稳定扩散。
菲克第二定律:是在菲克第一定律基础上推导出来的。
如图所示扩散体系中任一体积元dxdydz在dt时间内由x方向流进的净物质增量应为:同理在y、z方向流进的净物质增量分别为:放在δt时间内整个体积元中物质净增量为:若在δt时间内,体积元中质点浓度平均增量δc,则:若假设扩散体系具有各向同性,且扩散系数D不随位置坐标变化则有:适用范围:不稳定扩散。
第七章 扩散与固相反应内容提要:晶体中原子(离子)的扩散是固态传质和反应等过程的基础。
本章讨论了扩散的两个问题。
一是扩散现象的宏观规律——菲克第一、第二定律,描述扩散物质的浓度分布与距离、时间的关系。
二是扩散微观机制,即扩散过程中原子迁移的方式。
在了解原子移动规律的基础上讨论了固相反应的扩散动力学方程。
杨德尔与金斯特林格方程的推导及其适用的范围。
简要介绍了影响固相反应的因素。
固体中质点(原子或离子)的扩散特点:固体质点之间作用力较强,开始扩散温度较高,但低于其熔点;晶体中质点以一定方式堆积,质点迁移必须越过势垒,扩散速率较低,迁移自由程约为晶格常数大小;晶体中质点扩散有各向异性。
菲克第一定律:在扩散过程中,单位时间内通过单位截面的质点数目(或称扩散流量密度)J 正比于扩散质点的浓度梯度c :)(zc k y c j x c i D D ∂∂+∂∂+∂∂-=∇-= 式中D 为扩散系数s m 2或s cm 2;负号表示粒子从浓度高处向浓度低处扩散,即逆浓度梯度的方向扩散。
菲克第一定律是质点扩散定量描述的基本方程,它可直接用于求解扩散质点浓度分布不随时间变化的稳定扩散问题。
菲克第二定律适用于求解扩散质点浓度分布随时间和距离而变化的不稳定扩散问题。
)(222222zc y c x c D t c ∂∂+∂∂+∂∂=∂∂ 扩散过程推动力是化学位梯度。
物质从高化学位流向低化学位是一普遍规律。
扩散系数的一般热力学关系式:)ln ln 1(i i i i N RTB D ∂∂+=γ式中i D 为i 质点本征扩散系数;i B 为i 质点平均速率或称淌度;i γ为i 质点活度系数;i N 为i 质点浓度。
)ln ln 1(i i N ∂∂+γ称为扩散系数的热力学因子。
当体系为理想混合时1=i γ,此时i i i RTB D D ==*。
*i D 为自扩散系数。
当体系为非理想混合时,有两种情况:(1)当0)ln ln 1(>∂∂+i i N γ,0>i D 为正扩散。
第十章扩散与固相反应
1.描述在金属固体中发生扩散时,原子是如何运动的。
指出扩散的条件。
2.有一球壳,内半径为r1,外半径为r2。
在T温度保温,有物质从球壳内
向球壳外扩散,当扩散达到平衡后,球壳内表面扩散物质的浓度为C1,外表面的浓度为C2,并测得在单位时间内从球壳内向球壳外扩散的物质总量为Q。
设扩散系数为常数。
求:
A,扩散系数。
B,r=(r1+r2)/2处的浓度。
3.指出第一定律、第二定律中的不同适用的场合。
4.钢可以在870℃渗碳也可以在930℃渗碳,问:A)计算钢在870℃和930℃
渗碳时,碳在钢(奥氏体)中的扩散系数。
已知D0=2.0×10-5m2s-1,Q=144×103J/mol。
B)在870℃渗碳要用多长时间才能获得930℃渗碳10小时的渗层深度?(渗层深度:在浓度-距离曲线中,某一浓度所对应的离表面的距离。
)
5.简述置换原子和间隙原子的扩散机制。
6.何谓柯肯达尔效应,简述柯肯达尔效应的意义。
7.简述晶体结构对扩散的影响。
8.若由MgO和Al2O3球形颗粒之间的反应生成MgAl2O4是通过产物层的
扩散进行的:
9.(1) 画出其反应的几何图形并推导出反应初期的速度方程。
10.(2) 若1300℃时DAl3+>DMg2+,O2-基本不动,那么哪一种离子的扩散
控制着MgAl2O4的生成?为什么?
11.镍(Ni)在0.1大气压的氧气中氧化,测得其重量增量(μg/cm2)如
下表:
(1)导出合适的反应速度方程;(2) 计算其活化能。
12.由Al2O3和SiO2粉末反应生成莫来石,过程由扩散控制,扩散活化能为
50千卡/摩尔,1400℃下,一小时完成10%,求1500℃下,一小时和四小时各完成多少?(应用扬德方程计算)
13.粒径为1μ球状Al2O3由过量的MgO微粒包围,观察尖晶石的形成,在
恒定温度下,第一个小时有20%的Al2O3起了反应,计算完全反应的时间。
(1) 用扬德方程计算
(2) 用金斯特林格方程计算
(3) 比较扬德方程、金斯特林格方程优缺点及适用条件。
14.当测量氧化铝-水化物的分解速率时,发现在等温反应期间,重量损失随
时间线性增加到50%左右,超过50%时重量损失的速率就小于线性规
律。
速率随温度指数增加,这是一个由扩散控制的反应还是由界面一级控制的反应?当温度从451℃增至493℃时,速率增大到10倍,计算此过程的活化能。
15.由Al2O3和SiO2粉末形成莫来石反应,由扩散控制并符合扬德方程,实
验在温度保持不变的条件下,当反应进行1小时的时候,测知已有15%的反应物起反应而作用掉了。
(1) 将在多少时间内全部反应物都生成产物?
(2) 为了加速莫来石的生产应采取什么有效措施?
16.试分析影响固相反应的主要因素。
17.如果要合成镁铝尖晶石,可供选择的原料为MgCO3、Mg(OH)2、MgO、
Al2O3·3H2O、γ-Al2O3、α-Al2O3。
从提高反应速率的角度出发,选择什么原料较好?请说明原因。