清华大学物理化学B-相平衡-2
- 格式:ppt
- 大小:722.00 KB
- 文档页数:47

清华大学考研物理化学化试题Document serial number【KKGB-LBS98YT-BS8CB-BSUT-BST108】1.有一绝热的刚性密闭容器内抽成真空,通过阀门和大气隔离,当阀门打开 时,空气(可视为理想气体)进入容器,此时容器内气体的温度将:(A)升高 (B)降低 (c)不变 (D)不能确定2.在标准压力P θ和383.15 K 时,水变为同温下的蒸气。
则该相变过程中,下 列哪个关系式不能成立(A) ΔG<0 (B) ΔH>0 (C)△S iso <O (D)△S sur <O3.某气体状态方程为m PV RT bP =+ (b 是大于零的常数),则下列结论正确的是(A)其焓H 只是温度T 的函数(B)其内能u 只是温度T 的函数(c)其内能和焓都只是温度T 的函数(D)其内能和焓不仅与温度T 有关,还与气体的体积Vm 或压力p 有关4.1mol 理想气体经历绝热膨胀过程温度从T1变化到T2,则下列关于功的计算式中哪一个是正确的 021()Q V U Q W W C T T =∆=+−−−→=- (A) 21()Cv T T - (B) 21()Cp T T -(c) 22111p V p V γ-- (D) 21()1R T T γ-- 5.已知C(石墨)和C(金刚石)在25℃和101325 Pa 下的标准摩尔燃烧焓分别为-393.4 kJ ·mol -1和 kJ ·mol -1,则该条件下金刚石的标准生成焓f m H Θ∆为:(A)-395.3 kJ?mol -1 (B)395.3 kJ?mol -1(C)-1.9 kJ?mol -1 (D)1.9 kJ?mol -16.C02在临界点处的自由度等于:(A)0 (B)1 (C)2 (D)37.对稀溶液的依数性产生的主要原因,下列表述中错误的是:(A)溶液的蒸气压较纯溶剂低(B)溶液中溶剂的化学势较纯溶剂低(c)溶液的焓较纯溶剂大(D)溶液的熵较纯溶剂大8.美国物理化学家J .Willard Gibbs 定义了状态函数G ,下列物理化学概念和 领域中不是这位科学家的贡献的是:(A)渗透压 (B)化学势 (c)相律 (D)系综理论9.对NaC1(s)与其饱和水溶液共存达平衡的两相系统,在同时考虑NaCl 与水 的电离情况下,多相系统的物种数和自由度分别为:(A)6,3 (B)6,2 (C)5,3 (D)5,2lO .下列对Bi .Cd 形成低共熔混合物的描述,正确的是:(A)低共熔点三相共存,自由度为O(B)低共熔混合物具有确定的化学组成(C)低共熔混合物是单一相合金(D)低共熔混合物是两相混合物11.反应22()2()C S O CO g +=,1/232600167.8/r m G J mol T K Θ-∆=--,若温度增加,则下列说法中正确的是:(A) r m G Θ∆变小,反应更完全; (B) r m G Θ∆变大,反应更不完全;(c) f K Θ变小,反应更不完全; (D) f K Θ变大,反应更完全。
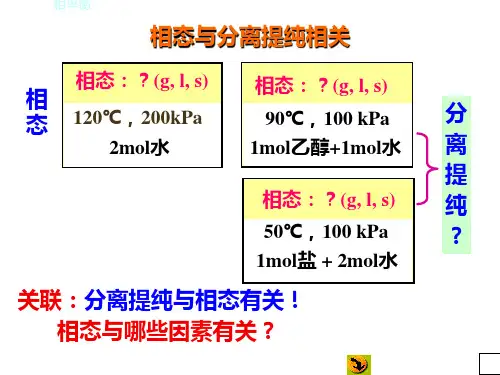

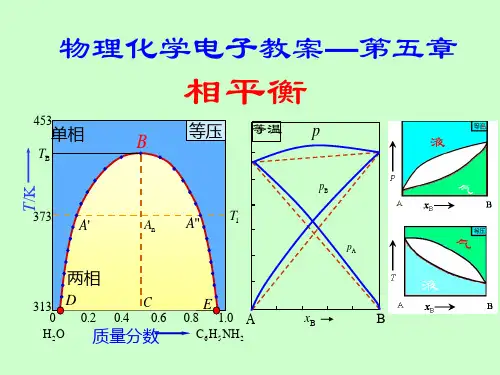



物理化学《相平衡》习题及答案2-3 选择题1、水煤气发生炉中共有)()()()(22g CO g CO g O H s C 、、、及)(2g H 5种物质,它们能发生下述反应:)(2)()(2g CO s C g CO ⇒+,)()()()(222g O H g CO g H g CO +⇒+,)()()()(22g CO g H s C g O H +⇒+,则此体系的组分数、自由度为( C )A.5、3B.4、3C.3、3D.2、22、物质A 与B 可形成低共沸混合物E ,已知纯A 的沸点小于纯B 的沸点,若将任意比例的A+B 混合在一个精馏塔中精馏,则塔顶的馏出物是( C )A.纯AB.纯BC.低共沸混合物D.都有可能3、克拉贝隆-克劳修斯方程适用于( C )A.)()(22g I s I ⇔B.)()(金刚石石墨C C ⇔C.),,(),,(222112p T g I p T g I ⇔D.)()(22l I s I ⇔4、将一透明容器抽成真空,放入固体碘,当温度为50℃时,可见到明显的碘升华现象,有紫色气体出现。
若温度维持不变,向容器中充入氧气使之压力达到100kPa 时,将看到容器中( C )A.紫色变深B.紫色变浅C.颜色不变D.有液态碘出现5、在一定温度下,水在其饱和蒸汽压下汽化,下列各函数增量中那一项为零( D )A.U ∆B.H ∆C.S ∆D.G ∆6、在一定外压下,多组分体系的沸点( D )A.有恒定值B.随组分而变化C.随浓度而变化D.随组分及浓度而变化7、压力升高时,单组份体系的沸点将( A )A.升高B.降低C.不变D.不一定8、进行水蒸气蒸馏的必要条件是( A )A.两种液体互不相容B.两种液体蒸汽压都较大C.外压小于101kPaD.两种液体的沸点相近9、液体A 与液体B 不相混溶。
在一定温度T ,当有B 存在时,液体A 的蒸汽压为( B )A.与体系中A 的摩尔分数成比例B.等于T 温度下纯A 的蒸汽压C.大于T 温度下纯A 的蒸汽压D.与T 温度下纯B 的蒸汽压之和等于体系的总压力10、氢气和石墨粉在没有催化剂时,在一定温度下不发生化学反应,体系的组分数是( A )A.2B.3C.4D.511、上述体系中,有催化剂存在时可生成n 种碳氢化合物,平衡是组分数为( A )A.2B.4C.n+2D.n12、相率适用于( D )A.封闭体系B.敞开体系C.非平衡敞开体系D.以达到平衡的多向敞开体系13、某物质在某溶剂中的溶解度( C )A.仅是温度的函数B.仅是压力的函数C.同是温度和压力的函数D.除了温度压力以外,还是其他因素的函数14、在实验室的敞口容器中装有单组份液体,对其不断加热,则看到( A )A.沸腾现象B.三项共存现象C.临界现象D.生化现象15、相图与相率之间的关系是( B )A.相图由相率推导得出B.相图由实验结果绘制得出,不能违背相率C.相图决定相率D.相图由实验结果绘制得出,与相率无关16、下述说法中错误的是( C )A.通过相图可确定一定条件下体系由几相构成B.相图可表示出平衡时每一相的组成如何C.相图可表示达到相平衡所需时间的长短D.通过杠杆规则可在相图上计算各相的相对含量17、三组分体系的最大自由度及平衡共存的最大相数为( D )A.3;3B.3;4C.4;4D.4;518、定容条件下)(4s HS NH 的分解压力为1θp 时,反应)()()(234g S H g NH s HS NH +⇔的标准平衡常数是( C )A.1B.1/2C.1/4D.1/819、水的三相点附近其蒸发热为44.821-⋅mol kJ ,熔化热为5.991-⋅mol kJ ,则在三相点附近冰的升华热约为( B )A.38.831-⋅mol kJB.50.811-⋅mol kJC.-38.831-⋅mol kJD.-50.811-⋅mol kJ20、在相图上,当物系点处于哪一点时,只存在一个相( C )A.恒沸点B.熔点C.临界点D.最低共沸点21、具有最低恒沸温度的某两组份体系,在其T-x 相图的最低点有( A )A.l g x x f ==;0B.l g x x f ==;1C.l g x x f >=;0D.l g x x f >=;122、80℃时纯苯的蒸汽压为0.991θp ,纯甲苯的蒸汽压为0.382θp ,若有苯-甲苯气、液平衡混合物在80℃时气相中苯的摩尔分数为30.0=苯y 则液相组成苯x 接近于( D )A.0.85B.0.65C.0.35 D0.1423、体系处于标准状态时,能与水蒸气共存的盐可能是: CA. Na 2CO 3B. Na 2CO 3 Na 2CO 3•H 2O Na 2CO 3•7H 2OC. Na 2CO 3 Na 2CO 3•H 2OD. 以上全否24.一个水溶液共有S 种溶质,相互之间无化学反应。



1化学反应速率与化学平衡34.3.1 可逆反应与化学平衡(一)化学反应的可逆性和可逆反应绝大多数化学反应都有一定可逆性:例如:N 2 (g) + 3 H 2 (g) 2 NH 3 (g)只有极少数反应是不可逆的:例如: 2 KClO 3(s) =2 KCl (s) + 3 O 2 (g)可逆反应:在同一条件下,能同时向两个相反方向进行的反应。
4(二)化学平衡化学平衡的特征:(1)系统的组成不随时间而改变;(2)化学平衡是动态平衡。
(3)平衡状态与达到平衡的途径无关;定义:可逆反应在一定条件下,正反应速率等于逆反应速率时,反应体系所处的状态。
4.3.1 可逆反应与化学平衡5在373 K 恒温槽中反应一段时间后,达到平衡,测得平衡时N 2O 4和NO 2 浓度。
0.1600.100NO 2开始0.370.0700.100N 2O 4从反应混合物0.0720.100NO 2开始0.370.0140N 2O 4从产物0.1200NO 2开始0.360.0400.100N 2O 4从反应物c 2(NO 2)/c (N 2O 4)平衡浓度起始浓度N 2O 4-NO 2体系的平衡浓度(mol/L )(373K )化学平衡的实例N 2O 4 (g) 2 NO 2(g)无色红棕色64.3.2 平衡常数1. 定义:在一定温度下,可逆反应达到平衡时,产物浓度的方程式计量系数次方的乘积与反应物浓度的方程式计量系数次方的乘积之比,为一常数,称为“平衡常数”。
用K 表示。
2. 意义:表示在一定条件下,可逆反应能进行的极限。
K 越大,正反应进行得越彻底。
7有关化学平衡常数的说明①化学平衡常数K 只是温度的函数。
②平衡常数不涉及时间概念,不涉及反应速率。
例如:N 2O 4(g) 2 NO 2(g)T /K 273 323 373K 5×10-4 2.2×10-2 3.7×10-12SO 2(g) + O 2(g) 2SO 3(g) K =3.6 ×1024(298K)K 很大,但常温下反应速率很小。