统计规律理想气体的压强和温度
- 格式:docx
- 大小:14.07 KB
- 文档页数:9



理想气体的压强及温度的微观解释在普通物理热学的教学中,对理想气体的压强、温度的学习和讨论时,学生对压强、温度的微观实质理解困难,特别是对宏观规律的微观解释与分析问题。
文章从理想气体分子模型的建立和统计假设的提出,对压强、温度的实质进行讨论,从而使学生得到正确理解,并学会用微观理论解释和研究宏观现象和规律的分析方法。
标签:理想气体;微观模型;压强;温度;微观本质在物理的学习和研究中,经常会讨论和分析一些物理现象和规律,很多物理现象和规律,是可以通过实验观察和验证的宏观规律,而表征分子、原子运动性质的微观量,很难用观察或实验直接测定。
宏观量与微观量之间必然存在着联系,要更深入地认识和研究宏观规律,必须对宏观规律的微观本质进行分析。
通过对理想气体的几个宏观规律与微观实质的关系对比和分析,帮助我们认识和理解气体动理论的有关规律,并掌握这一研究方法。
1 理想气体模型及状态方程1.1 理想气体模型。
所谓理想气体是指重力不计,密度很小,在任何温度、任何压强下都严格遵守气体实验定律的稀薄气体。
理想气体是一种理想化的物理模型,是对实际气体的科学抽象。
理想气体的微观特征是:分子间距大于分子直径10倍以上,分子间无相互作用的引力和斥力,分子势能为零,其内能仅由温度和气体的量决定,内能等于分子的总动能。
温度提高,理想气体的内能增大;温度降低,理想气体的内能减小。
实际气体抽象为理想气体的条件:不易被液化的气体,如氢气、氧气、氮气、氦气、空气等,在压强不太大、温度不太低的情况下,所发生的状态变化,可近似地按理想气体处理。
分子本身的线度与分子之间的距离相比可忽略不计,视分子为没有体积的质点;除碰撞瞬间外,分子之间及分子与容器壁之间没有相互作用力,不计分子所受的重力;分子之间及分子与器壁之间作完全弹性碰撞,没有能量损失,气体分子的动能不因碰撞而损失。
容器各部分分子数密度等于分子在容器中的平均密度n=NV,式中,n是气体分子数密度,N是气体的总分子数,V是气体容器的容积;沿空间各个方向运动的分子数目是相等的;气体分子的运动在各个方向机会均等,不应在某个方向更占优势,即全体分子速度分量vx、vy和vz的平均值vx=vy=vz=0。


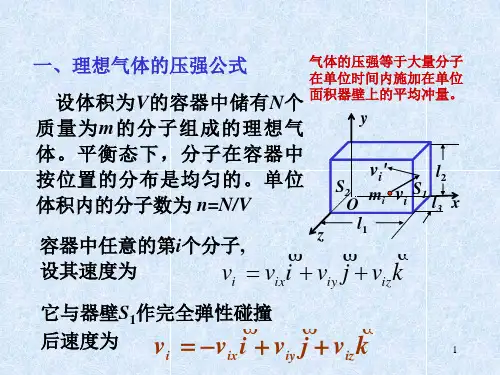





一、理想气体的压强公式1.压强的产生气体作用于器壁的压力是气体中大量分子对器壁不断碰撞的综合效果。
由于是大量分子对器壁的碰撞,就使得器壁受到一个持续的、均匀的压力的作用。
压强即为单位面积上作用器壁上的平均冲力。
2.气体压强公式的简单推导假设有一个边长为x ,y ,z 的长方形容器,其中含有N 个同类理想气体分子,每个分子质量均为m 。
在平衡状态下,长方形容器各个面的压强应当是相等的。
现在我们来推导作用在与x 轴垂直的面1A 的压强。
以第i 个分子为研究对象。
设在某一时刻其速度为k v j v i v v iz iy ix i ++=,它与器壁碰撞必受到器壁的作用力。
在此力的作用下,i 分子在x 轴上(以x 轴为研究对象,取标量式)的动量由ix mv 变为ix mv -。
根据动量定理,i 分子在x 轴上所受的冲量等于该分子在该坐标轴上的动量的增量,即:ixix ix i mv mv mv t f 2-==∆--i 分子对器壁的碰撞是间歇的,它从A 1面弹回,飞向A 2面与A 2面碰撞,又回到A 1面再作碰撞。
i 分子与A 1面碰撞两次,在x 轴上运动的距离为2x ,所需的时间为2x/v ix ,于是在单位时间内,i 分子作用在A 1面的次数是v ix /2x ,单位时间内i 分子作用在A 1面的冲力为x mv v x mv ix ix ix 2)/2(2-=-,这也就是容器壁对i 分子的平均冲力,由牛顿第三定律知道,i 分子施于器壁的冲力为xmv f ix i 2=N 个气体分子施于器壁的总冲力为上述单个分子给予器壁的冲力的总和(同类气体分子的质量相等),即)....(22221∑∑+++==xv v v m f F Nx x x i x 给上式右边上下同乘以N 得222221)....(x Nx x x i x v xNm N v v v x Nm f F ∑∑=+++==根据压强的定义,(1A 面的面积S=yZ ),则 22x x x x v nm v xyzNm yz F P === 其中n=N/V 为单位体积内的分子数,称为分子数密度。
209-统计规律、理想气体的压强和温度209统计规律、理想气体的压强和温度1、选择题1,理想气体中仅由温度决定其大小的物理量是(A )气体的压强 (B )气体的内能 (C )气体分子的平均平动动能 (D )气体分子的平均速率[ ]2,温度、压强相同的氦气和氧气,它们的分子平均动能ε和平均平动动能k ε的关系为(A )ε和k ε都相等(B )ε相等,而k ε不相等(C )k ε相等,而ε不相等(D )ε和k ε都不相等[ ]3,一瓶氢气和一瓶氧气温度相同,若氢气分子的平均平动动能为?J ,则氧气的温度为(A )100 K (B )200 K (C )273 K (D )300 K [ ]4,理想气体处于平衡状态,设温度为T ,气体分子的自由度为i ,则每个气体分子所具有的 (A )动能为kT i 2(B )动能为RT i 2(C )平均平动动能为kT i 2(D )平均平动动能为kT 23[ ]5,一氧气瓶的容积为V ,充了气未使用时的压强为1p ,温度为1T ,使用后瓶内氧气的质量减少为原来的一半,其压强降为2p ,则此时瓶内氧气的温度2T 为 (A ) 1212p p T (B )2112p p T (C )121p p T (D )2112p p T[ ]6,一个能量为1210?eV 宇宙射线粒子射入氖管中,氖管中有氖气 mol 。
如果宇宙射线粒子的能量全部被氖气分子所吸收而变为分子热运动能量,则氖气升高的温度为 (A )710?K (B )710?K (C )610? K (D )610?K[ ]7,设想在理想气体内部取一小截面dA ,则两边气体通过dA 互施压力。
从分子运动论的观点来看,这个压力施于dA 的压强为(A )k n p ε32=(B )k n p ε34=(C )kT p 23=(D )kT p 3=[ ]8,两瓶不同种类的气体,它们的温度和压强相同,但体积不同,则下列说法正确的是 (A )单位体积内的分子数相同,单位体积内的气体质量也相同 (B )单位体积内的分子数不相同,但单位体积内的气体质量相同 (C )单位体积内的分子数相同,但单位体积内的气体质量不相同(D )单位体积内的分子数不相同,单位体积内的气体质量也不相同[ ]9,在等体过程中,理想气体的压强增大到原来的100倍,其方均根速率(A) 减小到原来的1/100 (B) 减小到原来的1/10 (C) 增大到原来的100倍 (D) 增大到原来的10倍[ ]10,容积为V 的容器中,贮有1N 个氧分子、2N 氮分子和M kg 氩气的混合气体,则混合气体在温度为T 时的压强为(其中A N 为阿佛伽德罗常数,μ为氩分子的摩尔质量) (A )kT VN 1 (B )kT VN 2 (C )kT VMNAμ (D )kT N MN N VA )(121μ++[ ]11,阿佛伽德罗常数为A N ,某理想气体的摩尔质量为μ,则当该气体在压强为p ,气体质量为M 、体积为V 时的平均平动动能为 (A )MpV 23μ (B )MN pV A 23μ (C )MN pV A 25μ (D )MN pV A 27μ[ ]12,如图所示,AB 为一理想气体等温线,C 态与D 态在AB线的两侧,则D 态的温度与C 态的温度关系为(A )C D T T < (B )C D T T = (C )C D T T > (D )无法确定[ ]13,三个容器A 、B 、C 中装有同种理想气体,其分子数密度n 相同,方均根速率之比为4:2:1::222=C B A v v v ,则其压强之比C B A p p p ::为(A )1:2:4 (B )4:2:1 (C )8:4:1 (D )16:4:1 [ ]14,两瓶不同种类气体,体积不同,但温度和压强相同,k ε表示气体分子的平均平动动能,k n ε表示单位体积分子总的平均平动动能,则下列表述正确的是(A ) k ε相同,k n ε也相同(B ) k ε相同,k n ε不同(C ) k ε不同,k nε相同(D ) k ε不同,k n ε也不同[ ]15,处于平衡状态下的一瓶氦气和一瓶氮气的分子数密度相同,分子的平均平动动能也相同,则下列表述正确的是(A )温度、压强均不相同(B )温度相同,但氦气压强大于氮气的压强 (C )温度、压强均相同(D )温度相同,但氦气压强小于氮气的压强[ ]16,体积为?m 3的容器中含有?个氧气分子,如果其中压强为5?Pa ,则氧分子的平均平动动能为(A )? J (B )? J (C ) J (D )?J [ ]2、判断题1,从分子运动论的观点说明:当气体的温度升高时,只要适当增大容器的容积,就可使气体的压强保持不变。
2,理想气体是真实气体在压强趋于零时的极限情形,是一种理想化的模型,它严格尊从理想气体状态方程。
3,若盛有某种理想气体的容器漏气,使气体的压强、分子数密度各减为原来的一半,则气体分子的平均动能不变。
4,两瓶不同种类的气体,它们的体积不同,但它们的温度和压强相同,所以它们单位体积内的分子数一定相同。
5,在推导理想气体压强公式时,可以不考虑分子间的相互碰撞。
6,给自行车轮胎打气,使其达到所需要的压强,不管是夏天或冬天,打入胎内的空气质量一定相同。
7,理想气体的实验基础是(1)气体很容易被压缩;(2)气体分子可以到达它所能到达的任何空间;(3)平衡状态下,气体的温度和压强都不随时间改变。
8,在推导理想气体压强公式的过程中,利用了理想气体的假设、平衡态的条件和统计平均的概念。
9,气体处于平衡态时,其分子的平均速率不等于零,但分子的平均速度等于零,平均动量也等于零。
10,不管气体处于平衡态还是非平衡态,按统计规律性都有 222z y x v v v ==。
11,温度反映了组成系统的大量分子无规则运动的剧烈程度。
它是大量分子热运动的集体表现,所以对于单个分子不能说它的温度有多高。
12,在一封闭容器中装有某种理想气体,若气体的温度保持不变,当气体的压强增大时,气体的体积也同时增大。
13,由理想气体分子的平均平动动能与温度的关系kT vm 23212=可知,单个分子的温度就是理想气体的温度。
14,从气体动理论的观点来看,若理想气体分子的数密度越大,则压强越大;若分子平均平动动能越大,则压强也越大。
3、填空题1,温度为127 ℃的1 m 3 的理想气体中含有25 mol 的理想气体分子,那么该气体的压强应为_________ Pa 。
2,体积为?m 3的容器中含有?个理想气体分子,如果气体压强为5?Pa ,则该理想气体的温度为 K 。
3,有一瓶质量为M 的氧气,温度为T ,则氧分子的平均平动动能为。
4,一打足气的自行车内胎,在=t ℃ 时,轮胎中空气的压强为5?=p Pa ,则当温度变为=t ℃ 时,轮胎内空气的压强2p 为Pa 。
5,有一体积为510?m 3 的空气泡由水下 m 深的湖底处(温度为℃)升到湖面上。
若湖面的温度为℃,大气压强为5?=p Pa ,则气泡到达湖面时的体积为 m 3。
6,一定量的理想气体储于某一容器中,温度为T ,气体分子的质量为m ,根据理想气体分子模型和统计假设,分子速度在x 方向的速度分量平均值=xv 。
7,如果一个气体分子的平均平动动能等于一个电子由静止通过1V 电势差的加速作用所获得的动能,则此时气体分子的温度为 K 。
8,质量为1 kg 的氮气,压强为? Pa ,体积为 m 3,则在此条件下氮分子的平均平动动能为 J 。
9,在标准状态下,1cm 3中的氮分子数为。
10,一容积为10 cm 3的电子管,当温度为300 K 时,用真空泵把管内空气抽成压强为6105-?mmHg 的高真空,则此时管内的空气分子数为(760 mmHg =?Pa )。
11,温度为127℃时,一摩尔氧气具有的平均平动动能为 J 。
12,一容积为10 cm 3的电子管,当温度为300 K 时,用真空泵把管内空气抽成压强为6105-?mmHg 的高真空,则此时管内的空气分子的平均平动动能的总和为(760 mmHg =?Pa )。
13,在压强为?Pa 下,氮气分子的平均自由程为?m ,当温度不变,而平均自由程变为 mm 时,则其压强应为 Pa 。
14,一定量的理想气体储于某一容器中,温度为T ,气体分子的质量为m ,根据理想气体分子模型和统计假设,分子速度在x 方向的分量=2x v 。
15,温度为27℃ 时,1 mol 氧气具有的平均平动动能为 J 。
16,理想气体在温度为300 K ,压强为5? Pa 时,在1 m 3 内气体分子的平均平动动能的总和分别为 J/m 3。
4、计算题1,求在温度为30℃ 时氧气分子的平均平动动能,平均动能,平均能量以及3?kg 的氧气的内能(常温下,氧气分子可看成刚性分子)2,温度为0℃ 和100℃ 时理想气体分子的平均平动动能各为多少欲使分子的平均平动动能等于?J ,则气体的温度需多高3,在体积为?m 3的容器中,有内能为?J 的刚性双原子分子理想气体。
求:(1)气体的压强;(2)设分子总数为?个,则分子的平均平动动能及气体的温度。
4,试由理想气体压强公式和理想气体状态方程推导出理想气体分子的平均平动动能与温度的关系式,再由次推导出方均根速率与温度的关系式。
5,氢分子的质量为?kg ,如果每秒内有?个氢分子,以与墙面成045角的方向、?m/s 的速率撞击在面积为410?m 2的墙面上,试求氢气作用在墙面上的压强。
6,一容器内储有氧气,其压强为?=p Pa ,温度为27=t ℃。
求:(1)单位体积内的分子数;(2)氧气的质量密度;(3)氧分子的质量;(4)分子间的平均距离(分子所占的空间看作球状);(5)氧分子的平均平动动能。
7,某容器中装有质量为?=M kg 的氧气(视作刚性分子的理想气体),其温度300=T K 。
求:(1)氧气的内能;(2)当对氧气加热到某一温度时,测得此时的压强为5?=p Pa ,已知容器容积310?=V m 3,求此时氧气的内能。
8,体积为310?m 3的容器中装有非刚性双原子分子理想气体,其内能为3?J ,求:(1)气体的压强; (2)若分子总数为23?个氧气分子,求气体的温度和氧气分子的方均根速率。
9,质量为 ,温度为27℃ 的氮气,装在容积为 3的容器中,容器以100=vm/s 的速率作匀速直线运动,若容器突然停下来,定向运动的动能全部转化为分子热运动的动能,则平衡后氮气的温度和压强各增加多少相关文档:••••••••••更多相关文档请访问:。