化学周练十二
- 格式:doc
- 大小:381.50 KB
- 文档页数:2

周周练(第十二单元)一、我会选(每题5分,共50分)1.(淮安中考)下列食物中富含维生素的是()A.鸡蛋B.米饭C.黄瓜D.红烧肉2.(河北中考)缺铁容易对人体健康造成的阻碍是()A.患佝偻病 B.引发贫血C.产生龋齿 D.甲状腺肿大3.(上海中考)属于有机物的是()A.C60 B.COC.H2CO3 D.C2H6O4.(衡阳中考)化学源于生活,同时又服务于生活。
以下做法不合理的是()A.食物包装充氮气以防腐B.乘坐公交车出行实现“低碳”生活C.用甲醛溶液浸泡海产品以保鲜D.用灼烧并闻气味的方式区别天然纤维和合成纤维5.下列广告用语中,你以为正确的是()A.本饮料由天然物质配制而成,绝对不含有化学物质B.含氟牙膏能够预防龋齿C.经卫生部查验合格的矿泉水中含量最多的元素是钙,是一种健康饮料D.“超纯水”绝对卫生,对人体有利6.(广州中考)下列物品所利用的材料中,不属于有机合成材料的是()A.尼龙背包B.塑料瓶C.陶瓷花盆D.电话塑料外壳7.材料是社会文明进步的重要标志。
下列有关材料的说法正确的是()A.塑料属于有机高分子材料B.玻璃是一种复合材料C.玻璃钢属于金属材料D.棉花属于合成纤维8.(永州中考)“吃的营养”和“吃的健康”是人们普遍的饮食追求。
下列说法正确的是() A.多吃烧烤食物对成长大为有利B.过量摄入微量元素对躯体有利C.常吃蔬菜和水果能够补充维生素D.食用甲醛浸泡过的海产品有利于健康9.下列说法中,正确的是()A.废弃的生石灰会带来“白色污染”B.羊毛、棉花、蚕丝均属于天然纤维C.二氧化硫和二氧化碳是造成酸雨的要紧物质D.缺碘会致使甲状腺肿大,因此应大量摄入碘元素10.(怀化中考)下列说法正确的是()A.聚氯乙烯薄膜无毒,故可用于制食物包装袋B.食用加碘食盐可预防甲状腺肿大C.人体所需的能量全数由糖类和油脂提供,故不需摄入蛋白质D.微量元素对人体健康起着重要作用,故摄入量越多越好二、我会填(共34分)11.(12分)(张掖中考)化学与生活紧密相关,在厨房里蕴藏着许多化学知识。

2021年高二化学下学期第十二次周练试题1.肥皂溶于热的蒸馏水中,冷却后加入盐酸,得到的沉淀是()A.氯化钠B.高级脂肪酸钠C.高级脂肪酸D.苯甲酸2.下列反应中,液体植物油不能发生的反应是()A.加成反应B.氧化反应C.水解反应D.缩聚反应3.某种直链饱和脂肪酸甘油酯22.25 g,皂化时需3.00 g NaOH,则与这种脂肪酸中的碳原子数接近的数值是()A.15B.16C.17D.184.分析某油脂水解所得高级脂肪酸时,只测出两种不饱和脂肪酸。
已知原油脂的碘值为116 g(碘值是指与100 g油脂加成时消耗的碘的克数),下列各油脂的结构与题意相符的是()5.十二烷基苯磺酸钠是常用洗涤剂的主要成分。
其结构可用—°来表示,左端为链烃基,右端为极性基。
根据这一结构特点,试分析和回答下列问题:(1)该物质分子在其水溶液表面分布的结构示意图,应是下列各图中的_________(填写序号),理由是_______________________________________________________。
(2)进入水溶液中的该物质的分子,可能会以下列图中_________的结构形式存在(填写序号),理由是_____________________________________________________。
6.为进行Ⅰ项实验,从Ⅱ项中选出一种试剂,从Ⅲ项中选出一种合适的实验操作方法,并指出你所搭配的道理。
Ⅰ实验Ⅱ试剂Ⅲ操作方法答案(1)除去苯中的苯酚 A.CaO a.分液(1)(2)除去工业酒精中的水 B.饱和Na2CO3溶液 b.蒸馏(2)(3)除去乙酸乙酯中的乙酸 C.NaCl c.过滤(3)(4)除去肥皂中的甘油 D.NaOH d.盐析(4)7.芳香化合物A、B互为同分异构体,B的结构简式是。
A经①②两步反应得C、D和E。
B 经①②两步反应得E、F和H。
上述反应过程、产物性质及相互关系如下图所示。
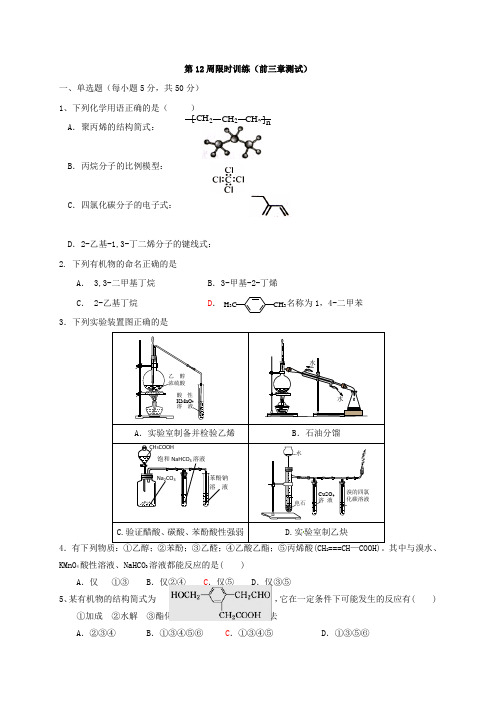
第12周限时训练(前三章测试)一、单选题(每小题5分,共50分)1、下列化学用语正确的是( )A .聚丙烯的结构简式:B .丙烷分子的比例模型:C .四氯化碳分子的电子式:D .2-乙基-1,3-丁二烯分子的键线式: 2. 下列有机物的命名正确的是A . 3,3-二甲基丁烷B .3-甲基-2-丁烯C . 2-乙基丁烷D .名称为1,4-二甲苯 3.下列实验装置图正确的是验室制乙炔42KMnO 4酸性溶液、NaHCO 3溶液都能反应的是( )A .仅 ①③B .仅②④C .仅⑤D .仅③⑤5、某有机物的结构简式为 ,它在一定条件下可能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去 A .②③④ B .①③④⑤⑥ C .①③④⑤D .①③⑤⑥[ CH 2CH 2CH 2]nH 3C CH 36.下列叙述正确的是( )A .甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色B .有机物 发生消去反应的有机产物有两种C .有机物A(C 4H 6O 2)能发生加聚反应,可推知A 的结构一定是CH 2===CH -COOCH 3D .可用溴水鉴别直馏汽油、四氯化碳和乙酸7.已知RCH===CHR′―――――→①O 3②Zn,H 2O RCHO +R′CHO。
在此条件下,下列烯烃被氧化后,产物中可能有乙醛的是( )A .CH 3CH===CH(CH 2)2CH 3B .CH 2===CH(CH 2)3CH 3C .CH 3CH 2-CH===CH -CH 2-CH 3D .CH 3CH 2CH===CHCH 2CH 3 8.由CH 3CH 2CH 2OH 制备 ,所发生的化学反应至少有:①取代反应;②消去反应;③加聚反应;④酯化反应;⑤还原反应;⑥水解反应中的( )A .①④B .②③C .②③⑤D .②④9.武兹反应是重要的有机增碳反应,可简单表示为2R -X +2Na―→R-R +2NaX ,现用CH 3CH 2Br 、C 3H 7Br 和Na 一起反应不可能得到的产物是( )A .CH 3CH 2CH 2CH 3B .(CH 3)2CHCH(CH 3)2C .CH 3CH 2CH 2CH 2CH 3D .(CH 3CH 2)2CHCH 3 10.拟除虫菊酯是一类高效、低毒的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如右图所示,下列 对该化合物叙述正确的是A .属于芳香烃B .不能与氢氧化钠溶液反应C .属于卤代烃D .在一定条件下可以发生加成反应二、填空11.(15分)写出下列反应的化学方程式:(1) 苯与液溴的取代反应: __ 。

化学第十二周作业一、选择题1.下列不属于化学变化的是()A.食物腐败 B.加热高锰酸钾制氧气 C.分离液态空气制氧气 D.炸药爆炸2.下列描述,属于物质的化学性质的是()A.通常状况下,氧气是一种无色无味的气体B.铁在潮湿的空气中易生锈C.水在4℃时密度最大D.铝丝能导电3.氧气是我们身边常见的物质,以下有关氧气的叙述不正确...的是()A 氧气具有可燃性 B 氧气能提供动植物呼吸C 氧气能支持燃烧D 某些物质不能在空气中燃烧,但在氧气中能燃烧4.下列说法中不正确的是()A原子、分子、离子都是构成物质的微粒 B.原子都是由原子核和核外电子构成的C.原子不能再分,但分子可再分D.在原子、分子、离子各微粒中,只有离子是带电荷的5.某同学用分子的观点解释下列现象。
其中错误..的是 ( )A 热胀冷缩──分子大小随温度的变化而改变B 花香四溢──分子不停地运动C 食物腐败──分子本身发生了变化D 酒精挥发──分子间空隙变大6.某婴儿配方奶粉部分营养成分的含量如下表所示,表中的“钙、磷、铁、锌”应理解为()A 金属 B 非金属 C 元素 D 分子7.根据你的生活经验,判断下列做法中不正确...的是()A 家用电器着火时用水扑灭B 炒菜时油锅着火,立即盖上锅盖C 用肥皂水检验液化气罐是否漏气D 煤气管道泄漏时立即关闭阀门并开窗通8.下列实验操作中,正确的是( )A B C D9.在实验室加热高锰酸钾制取氧气的实验中,有如下的几步操作,其中正确的是()①装入药品并固定试管②加热③将导管移出水面④收集氧气⑤停止加热⑥检查装置的气密性A ①⑥②④③⑤B ①⑥②④⑤③C ⑥①②④③⑤D ⑥①②④⑤③10.下图是表示气体分子的示意图,图中“●”和“Ο”分别表示质子数不同的两种原子,其中表示化合物的是 ( )A B C D11.某物质只含一种元素,则该物质不可能是 ( )A.混合物B.单质C.化合物D.纯净物12.鉴别空气、氧气、二氧化碳三瓶气体,最简单的方法是 ( )A.将气体分别通入蒸馏水中 B.将气体分别通入澄清的石灰水中C.将气体分别通入紫色石蕊溶液中 D.将燃着的木条分别伸入集气瓶中13. 下列是某同学对一些实验或生活现象的分析,其中分析或结论错误的是 ( )A 酥脆的饼干放置在空气中一段时间会变软,说明空气中含有水蒸气B 夏天吃剩下的食物要及时放入冰箱,因为食物缓慢氧化后会变质C 填充气球时,常用氦气代替氢气,因为氦气密度比氢气小D 膨化食品中通常充有氮气作保护气,因为氮气在通常情况下化学性质稳定14. 某些花岗岩石材中含有放射性元素氡,一种氡原子的质子薮为86,中子数为136,这种氡原子核外电子数为 ( )A、50B、86C、136D、22215. 下列化学反应中既不是化合反应也不是分解反应的是 ( )A. 铜+氧气−−→−点燃氧化铜 B. 二氧化碳+碳−−→−高温一氧化碳C. 氧化汞−−→−加热汞十氧气 D. 乙炔+氧气−−→−点燃二氧化碳+水16. 化学方程式2H2+O22H2O所表示的意义是()①氢气和氧气在点燃的条件下反应生成水②每两个氢分子和一个氧分子在点燃的条件下生成两个水分子③在氢气燃烧的反应中,氢气、氧气、水三种物质的质量比为4 ׃ 32 ׃ 36A、①③B、①②③C、②③D、①②17. 下列说法正确的是()①氧化反应一定是化合反应②化合物中至少含有两种元素③含氧的化合物就是氧化物④由同种元素组成的物质一定是单质⑤燃烧一定发光发热⑥缓慢氧化一定引起自燃A②③ B ①④ C ②⑤ D ①④⑥18.石英钟、电子表使用石英晶体代替传统钟表中的摆和游丝,提高了钟表计时的精确度。

2021年高三上学期化学周练12(实验班)含答案一、选择题(每小题只有一个正确选项)1、设N A为阿伏加德罗常数的数值,下列说法中正确的是()A.标准状况下,22.4L CHCl3含有的分子数为N AB.0.1mol/L的NH4NO3溶液中含有的氮原子数为0.2N AC.1molFe2+与足量的H2O2溶液反应,转移2N A个电子D.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6N A2.下列有关物质结构的表述正确的是()A.次氯酸的电子式: B.氯化钠的分子式:NaClC.二氧化碳的比例模型: D.Cl-的结构示意图:3.下列物质与其用途完全符合的是()①Na2CO3—制玻璃②SiO2—太阳能电池③AgI—人工降雨④NaCl—制纯碱⑤Al2O3—焊接钢轨⑥NaClO—消毒剂⑦Fe2O3—红色油漆或涂料⑧HF (aq)—雕刻玻璃A.①③④⑥⑦⑧B.①②③⑤⑥⑦⑧C.①③⑤⑦⑧D.①②③④⑤⑥⑦4.实验室需配制一种仅含五种离子(忽略水电离出的离子)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为5 mol/L,下面四个选项中能达到此目的的是()A.Na+、K+、SO42−、NO3−、Cl−B.Fe2+、H+、Br−、NO3−、Cl−C.Ca2+、K+、OH−、Cl−、NO3−D.Al3+、Na+、Cl−、SO42−、NO3−5.对于固定体积的密闭容器中进行的气体反应A(g)+B(g) C(s)+2D(g),可以说明在恒温下已达到平衡状态的是( )①反应容器中压强不随时间变化而变化②A气体和B气体的生成速率相等③混合气体的平均摩尔质量不随时间变化而变化④反应混合气体的密度不随时间变化而变化A.③④ B.②③ C.①③ D.①④6.X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X +2Y2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )A.33% B.40% C.50% D.65%7. 对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0.下列结论中不正确的是()A. 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则B. 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:nC. 若,则往含有气体的平衡体系中再加入的B,达到新平衡时,气体的总物质的量等于2aD. 若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小8. 某温度下,在密闭容器中发生如下反应,2M(g)+N(g) 2E(g)若开始时只充入2 mol E气体,达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入3 mol M和1 mol N的混合气体,达到平衡时M的转化率为()A. < 60%B. = 40%C. < 40%D. > 60%9. 甲、乙两容器都发生反应2A(g)+B(g) 3C(g),两容器温度和初始压强都相同。

①D③②AXBCXEFB2018学年上学期周末练习1. 有四种常见物质A 、B 、C 、D ,它们可以发生如下反应(反应条件省略): (I)H 2+A →B+C ;(Ⅱ)C →H 2+D ;(Ⅲ)B+D →A ;已知A 是黑色粉末,试推断D 是___,反应(I)属于_______(填反应类型)。
2. 有A 、B 、C 、D 、E 、F 六种化合物和甲、乙两种单质,其中C 是盐类化合物,它们在一定条件下有如下的转化关系:甲+A −−→−高温乙+B ; D +A →C +B ; C +E →F ↓(红褐色)+NaCl 。
确定A、D两种物质(写化学式):A ;D 。
3. 有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。
将其任意编号:A 、B 、C 、D 、E ,进行两两混合,其现象如下表:实 验 A+BA+EB+CB+E现 象产生沉淀 产生沉淀 产生沉淀 产生气泡(1)试推断并写出五种溶液中溶质的化学式。
A ,B ,C ,D ,E 。
(2)写出有关反应的化学方程式。
A+E B+E 4. 有A 、B 、C 、D 、E 五种化合物,它们在水溶液中反应关系如下:(1)试推断各物质的化学式: A BC D E(2)写出A 溶液与AgNO 3溶液反应的化学方程式 5. A 、B 、C 、D 、E 、F 、G 、H 是化学实验中常见的八种物质,它们之间有如图13所示的转化关系(其中E 是白色沉淀,A 和B 可发生中和反应): (1)写出B 、F 的化学式:B ___ F ____ (2)反应①的化学反应类型是_______ (3)反应②的化学方程式是________ (4)写出C →E 的化学反应方程式 6. 已知A 、B 、C 、D 、E 、F 为常见物质,其中A 、B 含有相同的元素,B 、E 为氧化物,C 、D 、F 都为单质。
它们相互转化的关系如右图所示(图中反应条件略(1)X 在反应①中起 作用。
2021-2021第二学期化学第十二周测试题温馨提示:1、全卷一共4页,满分是100分。
2、可能用到的相对原子质量:H—1 C—12 N--14 O—16 Mg—24 Ca—40Cu—64选择题答题卡:题号 1 2 3 4 5 6 7 8 9 10 答案题号11 12 13 14 15 16 17 18 19 20 答案一、选择题〔此题包括20小题,一共40分〕1.以下物质属于纯洁物的是 ( )A.黄铜 B.干冰 C.生铁 D.不锈钢2.以下变化中属于物理变化的是 ( )A.铁生锈了 B.苹果烂了 C.瓷碗碎了 D.蜡烛燃烧了3.专家提醒:虾类忌与维生素C同食。
以下食品中最好不要与海虾同食的是( )A.西红柿 B.瘦肉 C.米饭 D.鸡蛋4.以下物质的使用,不利于人体安康的是( )A.用食醋作调味剂 B.将“塑化剂〞添加到饮料中C.用碳酸钙作补钙剂 D.食品包装袋内充氮气防腐5.以下所示实验操作中,正确的选项是( )6.以下做法不符合“低碳〞理念的是〔〕A.用旧报纸制作铅笔杆 B.大力开展火力发电C.垃圾回收处理后用于发电 D.城公交车燃油改用天然气作燃料7.甲、乙两种固体物质的溶解度曲线如以下图所示,以下说法正确的选项是〔〕A.甲物质的溶解度大于乙物质的溶解度B.t1℃时,甲、乙两物质的溶解度相等,均为40gC.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数D.甲的溶解度受温度影响较小8.把金属X放入Cu(NO3)2溶液中,X外表有红色固体析出;假设放入Mg(NO3)2溶液中,无明显现象。
那么X、Cu、Mg三种金属活动性由强到弱的顺序正确的选项是〔〕A.Mg、X、Cu B.X、Mg、Cu C.Mg、Cu、X D.Cu、X、Mg9.合理使用化肥是农作物增产的有效措施之一。
以下物质中可用作复的是( )A.K2SO4 B.NH2NO3 C.NH4 H2PO4 D.Ca(H2P04)210.以下说法正确的选项是( )A.石灰水敝口放置于空气中,溶液质量增重B.进入久未开启的菜窖或者深洞前,要做灯火实验C.人体必需元素摄入量越多越有利于人体安康.D.穿用合成纤维制作的内衣有利予保护皮肤11.菜花节期间,我们站在地里就能闻到菜花的香味,这是因为( )A.分子能保持物质的化学性质 B.分子总在不断地运动C.分子有一定质量 D.分子间有间隔12.几种作物生长最适宜的pH范围如下:①甘草7.2~8.5 ②甘蔗6.0~8.0 ③大豆6.5~7.5 ④茶树5.0~5.5很多丘陵地区土壤为红色,呈弱酸性,你认为适宜种植( )A.① B.② C.③ D.④13.据报道:HY大地震引发福岛核电站爆炸后泄漏出放射性物质碘一131。
第十二周化学周清可能用到的相对原子质量:H-1、C-12、N-14、O-16、S-32、Ca-40 一、选择题(本大题包括15小题,每小题3分,共45分)1. 描述物质变化的成语有:①滴水成冰;②死灰复燃;③木已成舟;④火烧赤壁;⑤沙里淘金;⑥火上浇油;⑦百炼成钢;⑧花香四溢;⑨玉石俱焚,其中属于化学变化的是( ) A .②③④⑤⑥⑦ B .④⑤⑥⑦⑨ C .①③④⑤⑧⑨ D .②④⑥⑦⑨2、科学证明:空气中的微量臭氧(O 3),可抵抗阳光中紫外线对人体的损害。
制冷剂“氟里昂”是一种氯氟烃(以M 代替其化学式),它可破坏臭氧层,其反应过程可表示为: M + O 3 → MO + O 2 MO + O 3 → M + O 2 根据所学知识可知氯氟烃在反应中的作用是( )A 、氧化剂B 、还原剂C 、催化剂D 、稳定剂3.下列化学符号中数字表示的意义正确的是( ) A. CO 2:“2”表示一个二氧化碳分子含有两个氧原子 B. 2Na :“2”表示两个钠元素C. :“+2”表示镁离子带有两个单位正电荷D. S 2- :“2–”表示硫元素的化合价为负二价4.稀土元素又称“21世纪黄金”,广泛应用于电子、军事、石油化工等领域,硝酸铈铵(NH 4)2Ce(NO 3)6是稀土元素铈(Ce )的化合物,其中铈元素的化合价是( ) A 、+2 B 、+3 C 、+4 D 、+55.宏微结合是研究化学的重要思想。
如图所示,提起压在水面上方的活塞,容器中的水发生气化,则相同微小空间内微粒的变化最可能是( )6.下列物质的分类正确的是( )A .金属:铁、铝、水银B .单质:液氧、氮气、干冰C .氧化物:水、氧化铁、高锰酸钾+2 MgD.混合物:空气、冰水混合物、澄清石灰水7.下列有关分子、原子的说法中,错误的是( )A、香水要密封保存说明分子是不断运动和扩散的B、保持氧气化学性质的最小粒子是氧分子C、金属铁是由铁原子构成的D、分子可分,原子不可分8.下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是()A B C D9.长途运输鱼苗时,为了防止鱼苗缺氧,常在水中加入物质X,发生反应的化学方程式为:2X+2H2O=2Ca(OH)2+O2↑,其中X的化学式为()A.CaO B.CaO2 C.CaCO3D.CaCl210.如图所示是某反应前后的微观示意图,“” 和“” 表示两种不同的原子。
第十二周周末练习(无答案)九()班学号________ 姓名___________1.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是()选项物质操作方法A Fe(Fe2O3)加入过量稀盐酸,充分反应后过滤B Ca0粉末(CaCO3粉末)加足量的水,充分搅拌后过滤C NaOH溶液[Ca(OH)2溶液] 通入过量CO2气体,充分反应后过滤D CuSO4溶液(硫酸)加入过量Cu0粉末,加热,充分反应后过滤2.为除去物质中的杂质(括号内为杂质),所选试剂(过量)及操作方法均正确的是物质选用试剂操作方法A Cu(CuO) 氧气通入氧气并加热B CO2(HCl) 氢氧化钠溶液通过盛有氢氧化钠溶液的洗气瓶C CaCl2溶液(盐酸)碳酸钙粉末加入碳酸钙粉末充分反应后过滤D KCl溶液(K2CO3)氯化钙溶液加入氯化钙溶液充分反应后过滤3.为检测某化工厂排放的废液中是否含有S042﹣,同学们设计了如下方案,并进行了实验.方案步骤现象结论Ⅰ①取样品.滴加BaCl2溶液②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸①有白色沉淀产生②无明显现象废液中含有S042﹣Ⅱ①取样品,滴加过量②在步骤①的溶液中滴加BaCl2溶液①无明显现象②有白色沉淀产生废液中含有SO42﹣Ⅲ①取样品,滴加Ba(N03)2溶液②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸①有白色沉淀产生②无明显现象废液中含有S042﹣(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是.(2)方案Ⅰ和Ⅲ中,结论不成立的方案是,理由是.(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除的干扰.4.MnO2是一种重要的无机功能材料,粗Mn02(含有较多的Mn0和MnC03)的提纯是工业生产的重要环节。
下图是某研究性学习小组在实验室中模拟工业上粗Mn02转化为纯Mn02的工艺流程。
请回答下列问题:(1)操作A的名称是。
(2)NaCl03中氯元素的化合价为价。
高中化学学习材料唐玲出品高一化学周练12.26班级 座号 姓名1.下列变化属于固氮的是 ( )A .N 2与H 2在一定条件下反应生成NH 3B .NO 和O 2反应生成NO 2C .NH 3催化氧化为NOD .由NH 3制NH 4Cl 、(NH 4)2SO 4等2.关于氮气的性质的说法中,错误的是 ( )A .通常情况下,氮气性质很不活泼B .可在氧气中燃烧,生成NOC .在水中溶解度小(通常情况下)D .跟氢气在一定条件下发生反应,氮气是氧化剂3.氮气能大量存在于空气的根本原因是( ) A .氮气性质稳定,即使在高温下也很难跟其他物质发生反应B .氮气比空气轻,且不溶于水C .氮分子中两个氮原子结合很牢固,分子结构稳定D .氮气无氧化性,也无还原性,不跟其他物质反应4.在一定温度和压强下,将装有N 2和NO 2混合气体的试管倒立在水中,经足够长的时间后,试管内气体的体积缩小为原体积的53,则原混合气体中氮气与二氧化氮的体积比是 ( ) A .2:3 B .3:2 C .3:5 D .5:35.发射卫星的运载火箭,其推进剂引燃后发生剧烈反应,产生大量高温气体从火箭尾部喷出。
引燃后产生的高温气体主要是CO 2、H 2O 、N 2、NO ,这些气体均为无色,但在卫星发射现声看到火箭喷出大量红烟。
产生红烟的原因是( )A .高温下N 2遇空气生成NO 2B .NO 遇空气生成NO 2C .CO 2与NO 反应生成CO 与NO 2D .NO 和H 2O 反应生成H 2和NO 26.某同学弄清楚喷泉实验的原理后,有了一个创新的想法,如果改换一下烧瓶内的气体,改换一下胶头滴管和烧杯内的液体,也应该可以做喷泉实验。
他用课本上所用的装置实际做了一下,果真得到了美丽的喷泉。
那么,下列四种组合中不可能是该同学所设计的组合的是( ) A.氯化氢和水B.氧气和水C.二氧化碳和NaOH溶液D.氯气和NaOH溶液7.能鉴别Na2SO4、NH4NO3、KCl、(NH4)2SO4四种溶液(可以加热)的一种试剂是( ) A.BaCl2B.Ba(NO3)2C.B a(O H)2D.AgNO38.密度为0.91g.cm-3,质量分数为25%的氨水,用等体积的水稀释后,所得溶液中溶质的质量分数为()A.等于12.5% B .大于12.5% C.小于12.5% D.无法确定9.用加热法可以分离的一组物质是()A.氯化铵和消石灰 B.碳酸氢铵和过氧化钠C.氯化铵和氯化钠 D.碘和氯化铵10.将NH4HCO3在试管中加热,使放出的气体依次通过足量过氧化钠的干燥管、足量浓硫酸的洗气瓶,最后得到的气体是()A.NH3B.O2C.H2OD.CO211.检验某晶体是否为铵盐时,将待检物取出少量放在试管中,之后( ) A.加烧碱溶液,加热,用湿润的红色石蕊试纸放在试管口检验B.直接加热,用湿润的红色石蕊试纸放在试管口检验C.加烧碱溶液,加热向试管中滴加紫色石蕊试液D.加水溶解,滴加无色酚酞试液,观察是否变红12.如下图所示是实验室制取氨气的装置和选用的试剂,其中错误的是(双选) ( )13.制备干燥氨气所需的药品是( ) A.NH4Cl溶液、NaOH溶液、CaCl2固体 B.饱和氨水C.NaOH溶液、NH4Cl晶体、浓H2SO4 D.NH4Cl固体、碱石灰、消石灰14.已知NH3极易溶于水,而难溶于有机溶剂——CCl4,如下图所列装置中不适宜作NH3尾气吸收的是( )15.Cu粉放入稀H2SO4中,加热后无现象,当加入一种盐后,Cu粉质量减少,而溶液变蓝,同时有气体生成,此盐是()A.氯化物B.硫酸盐C.硝酸盐D.碳酸盐16.下列对于硝酸的认识,不正确的是()A、浓硝酸和稀硝酸都具有氧化性B、铜与硝酸的反应属于置换反应C、硝酸可氧化Fe2+D、可用铁或铝制品盛装浓硝酸17.3.2gCu与HNO3溶液(8mol/L,30ml)充分反应,HNO3溶液的还原产物有NO和NO2。
于都五中2010-2011学年高一化学周练(十二)
1.二氧化硅属于酸性氧化物,理由是
A.SiO2是非金属氧化物B.SiO2溶于水得到相应的酸
C.SiO2不能与任何酸反应D.SiO2与强碱反应生成盐和水2.关于硅的叙法不正确的是
A.高纯硅是良好的半导体
B.硅是制造太阳能电池的常用材料
C.单质硅既不能与酸反应又不能与碱反应
D.硅在地壳中含量居第二位,但在自然界中没有游离态的硅存在
3.下列说法不正确
...的是
A.钠在氧气中燃烧生成淡黄色的固体Na2O2,可做为呼吸面具的供养剂
B.液氯是氯气的水溶液,它能使干燥的有色布条褪色
C.氯气能与大多数金属化合,生成金属氯化物(盐)
D.氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸
4、能贮存在有玻璃塞的磨口试剂瓶里的试剂是()
A、HF溶液
B、KOH溶液
C、盐酸
D、水玻璃
5.下列关于对燃烧现象的认识中不正确的是
A.一定是氧化还原反应
B.一定发光放热
C.一定是化学反应
D.一定有氧气参与
6. 下列的各组离子在酸性溶液中能大量共存的是()
A、Na+、Fe2+、、NO3-、SCN—
B、Ca2+、K+、Cl—、NO3—
C、Al3+、K+、OH—、NO3—
D、Na+、Ca2+、SiO32—、Cl
7.自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,会产生明显的药品变质问题的是
A.NaNO3B.FeCl2C.Na2SO4D.AlCl3
8.有关下列反应产物的叙述,错误
..的是
A.在Cl2中点燃铁丝,有FeCl2生成
B.将Cl2通入水中,有HCl生成
C.将Cl2通入KBr溶液中,有Br2生成
D.将Cl2通入NaOH溶液中,有NaClO生成
9.已知反应①2BrO3- + Cl2 =Br2 +2ClO3-②5Cl2 + I2 +6H2O=2HIO3 +10HCl
③ClO3- +5Cl-+6H+=3Cl2 +3H2O,下列物质氧化能力强弱顺序正确的是
A.ClO3->BrO3->IO3->Cl2B.BrO3->Cl2>C1O3->IO3-
C.BrO3->ClO3->Cl2>IO3-D.Cl2>BrO3->C1O3->IO
10.人们已开始研究并试用新的自来水消毒剂,如用ClO2代替Cl2作自来水的消毒剂,其理由是:①ClO2是非金属氧化物;②ClO2有强氧化性;③由于Cl2会与水中的有机物反应生成对人体有害的物质
A.①②B.②③C.①③D.①②③11.下列关于氯水的叙述中,正确的是
A.新制的氯水盛放在棕色瓶中,放置于阴凉处
B.新制的氯水中含有氯气分子,氯分子可以杀菌、消毒
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水放置数天后酸性减弱
12、下列说法不正确的是()
A、氢气在氯气中安静的燃烧产生苍白色火焰
B、液氯不能使干燥的有色布条褪色
C、氯气在参加的所有反应中,只能得电子,化合价降低
D、氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸
班级______姓名_______得分_______
二、填空填(共40分)
13(5分)有X、Y、Z三种元素:
(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
(5)Z单质溶于X2Y中,所得溶液具有漂白性。
试写出其元素符号:X_______,Y_______,Z_______,以及化合物的分子式:XZ_______,X2Y_________。
14(12分)为了探究氯水的成份,某学生在氯水中分别加入下列物质,请分别写出实验的现象
..,结论
..(写分子或离子的化学式)和离子方程式
.....
(1)紫色石蕊试液
(2)FeCl2溶液
(3)Na2CO3溶液
(4)AgNO3—HNO3溶液
15(8分)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。
漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,写出该反应的化学方程式并标出电子转移的方向和数目:
(2)漂白粉的有效成分是(填化学式)。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化
学反应方程式。
16、(3分)石棉矿青石棉,其化学式为Na2Fe5Si8O22(OH)2写成氧化物的形式
为;
17.(12分)如图所示的组织之间的转化关系,回答下列有关问题。
(1)写出A、B、C、D各物质的名称:
A ,
B ,
C ,
D 。
(2)写出D→A的化学方程式
___________ 。
(3)写出下列变化的离子方程式:
B→C _____________________;
D→B ______________________。
附加题(15分)
18.由硅、铁、铝组成的试样19.4g均匀地分成等质量的两份:一份与足量的稀硫酸反应可产生气体aL;一份与足量的氢氧化钠溶液反应也能产生同种气体bL,合并两次所收集的气体共11.2L,试分析此试样的组成?(气体均在标准状况下测得其体积,且a=b)。