红外光谱讲义-研究生
- 格式:ppt
- 大小:3.81 MB
- 文档页数:87




三、红外辐射源能量光谱分布测试(一)实验目的1. 了解测量红外辐射源能量光谱分布的意义2. 掌握测量红外辐射源能量光谱分布的方法3. 理解物体的温度与红外辐射能量的关系(二)实验原理红外辐射(俗称红外线)是波长在0.78~1000μm 的一段电磁波谱,是人眼看不见的光线,只有借助于仪器才能探测到并转换成人们可感受的信息,如数字、图像、曲线等。
凡温度在绝对零度以上的物体均能够发出红外辐射,其辐射的峰值波长与物体的温度有确定的关系:T b m =λ 式中 λm ——物体辐射的峰值波长T —— 物体的温度B —— 常数 (2898μm ·K )此为辐射度学中的维恩位移定律,意为只要物体有温度,则一定有固定波长的辐射,自然界的物体温度如果在-40℃~3000℃(233K ~3273K )范围,则根据上述公式,峰值辐射波长在0.88~12μm 之间,即人们通常所说的红外波段。
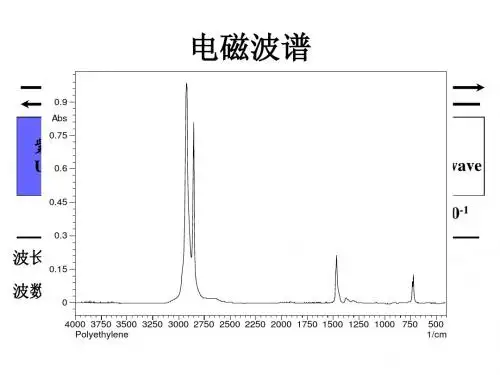
红外光谱仪器能将红外辐射源的辐射能量按波长的分布以曲线的形式给出。
我们可以清楚地看出一个红外辐射源在某个波长的相对辐射能量,进而可以验证维恩位移定律等红外辐射定律,并可以对红外辐射源进行深入的研究。
红外单色器的光学原理图如下图1 红外单色器光学原理图M1反射镜、M2准光镜、M3物镜,M4反射镜、M5 深椭球镜G 平面衍射光栅、S1入射狭缝、S2,S3出射狭缝、T 调制器入射狭缝、出射狭缝均为直狭缝,宽度范围0-2mm 连续可调,光源发出的光束进入入射狭缝1S ,1S 位于反射式准光镜2M 的焦面上,通过1S 射入的光束经2M 反射成平行光束投向平面光栅G 上,衍射后的平行光束经物镜3M 成像在2S 上。
(三)、实验仪器红外光栅光谱仪及配套附件;红外光源及驱动电源;电子稳压器;计算机及处理软件;打印机(四)、实验步骤首先按原理图检查各部分连接和摆放位置是否正确,经教师同意后,按下述步骤进行实验:1、打开红外辐射源的电源开关进行预热;2、打开计算机并进入相关程序,选定测量参数(相对强度、能量等),设置扫描波长范围、扫描间隔、幅度范围等参数;3、红外辐射源经预热达到稳定时,开始进行扫描,得到相应曲线;4、储测试结果,打印测试曲线;5、行相关计算,完成实验报告。


实验九红外光谱测定有机化合物的结构一、实验目的通过本实验,让学生复习红外光谱的基本原理,了解红外光谱仪的基本部件和光路走向。
通过实际操作,使学生了解红外光谱测定的样品处理及操作方法。
特别强调注意事项和简单谱图解析。
二、教学内容:1.红外光谱原理A. 光谱分析导论光谱分析法是基于物质对不同波长光的吸收、发射等现象而建立起来的一类光学分析法。
光谱是光的不同波长成分及其强度分布按波长或波数次序排列的记录,它描述了物质吸收或发射光的特征,可以给出物质的组成、含量以及有关分子、原子的结构信息。
由分子的吸收或发光所形成的光谱称为分子光谱(molecular spectrum),分子光谱是带状光谱。
B. 分子能级与分子光谱的形成分子具有不同的运动状态,对应每一种状态都有一定的能量值,这些能量值是量子化的称为能级。
每一种分子都有其特定的能级数目与能级值,并由此组成特定的能级结构。
处于基态的分子受到光的能量激发时,可以选择地吸收特征频率的能量而跃迁到较高的能级。
但是由于分子内部运动所牵涉到的能级变化比较复杂,分子吸收光谱也就比较复杂。
在分子内部除了电子运动状态外,还有核间的相对运动,即核的振动和分子绕着重心的转动。
每一种运动处在不同的能级上,因此分子具有电子能级、振动能级、转动能级。
红外光是波长范围为0.75~1000m的电磁波,可引起分子中基团的振动和转动能级跃迁,产生红外吸收光谱,也称分子振动-转动光谱。
C.红外光谱的产生当一束连续变化的各种波长的红外光照射样品时,其中一部分被吸收,吸收的这部分光能就转变为分子的振动能量和转动能量;另一部分光透过,若将其透过的光用单色器进行色散,就可以得到一带暗条的谱带。
若以波长或波数为横坐标,以百分吸收率为纵坐标,把这谱带记录下来,就得到了该样品的红外吸收光谱图,获得红外振动信息。
如下图,红外光谱图有以下三个基本参数:峰位:即吸收峰处于哪个波数区;峰强:即吸收峰面积或高度大小;峰形:即峰的宽窄度。



试验固体样品红外光谱的采集及分析当样品受到频率连续变化的红外光照耀时,分子汲取某些频率的辐射,并由其振动运动或转动运动引起偶极矩的净变化,产生的分子振动和转动能级从基态到激发态的跃迁,从而形成的分子汲取光谱称为红外光谱,又称为分子振动转动光谱。
,V ---------------- 频率V --------向V --------------- 能量 -------- 原子内电千跃卑号子内电孑跃用 振动跃迁红外光区可分成三个区:近红外区、中红外区、远红外区。
其中中红外区是讨论和应用最多的区域,一般说的红外光谱就是指中红外区的红外光谱。
区域名称 波长(Nm) 波数(Cm ・1) 能级跃迁类型近红外区 泛频区0.75-2.5 13158-4000 OH 、NH 、CH 键的倍频汲取 中红外区 基本振动区2.5-25 4000-400 分子振动/伴随转动 远红外区 分子转动区 25-300 400-10 分子转动波数(Cmj),它表示电磁波在单位距离(Cm)中振动的次数,波长和波数均反映了光的频率。
一、红外光谱的三要素1 .峰位分子内各种官能团的特征汲取峰只消失在红外光波谱的肯定范围,如:C=O 的伸缩振动一般在1700CmT 左右。
2 .峰强红外汲取峰的强度取决于分子振动时偶极矩的变化,振动时分子偶极矩的变化越小,谱带强度也就越弱。
一般说来,极性较强的基团(如C=O)振动,汲取强度较大;极性较弱的基团(如OC,NY 等)振动,汲取强度较弱;红外汲取强度分别用很强(Vs)、强(s)、中(m)、弱(W)表示.3 .峰形不同基团的某一种振动形式可能会在同一频率范围内都有红外汲取,如-OH 、-NH 的伸缩振动峰都在3400~3200cm 1,但二者峰外形有显著不同。
此时峰形的不同有助于官能团的鉴别。
远 外红中线波 无电 射频区200nm 40Onm 80Onm 2. 5 JA 15 ∖k Im 5m短 ------------------ 波长λ----------------------------- A 长光波造区及能量跃迁相关图常见官能团红外汲取特征频率表可见附录二、红外光谱仪的作用一是分析某化合物中是否含有某些官能团。
实验七:红外光谱法推测化合物结构一、目的要求1.通过推测化合物C7H6O2的结构,掌握用红外光谱推测化合物结构的原理和方法。
2.了解红外分光光度计的使用。
二、方法原理当已知化合物的分子式时,可以计算其不饱和度u,从而可推测化合物的类型。
然后根据红外图谱解析的程序,有的放矢地对测得的红外光谱图进行解析。
通过解析图谱中的主要吸收峰,可知道组成化合物的各基团及它们相互间的连接情况,就可推测可能的结构式。
最后与红外标准图谱对照以确定结构。
三、实验步骤本实验的制样方式是采用溴化钾压片法。
1.取0.5~2mg样品,于玛瑙研钵中研细。
2.于研钵中加入100~200mg事先研细至2μm左右,于110~150℃烘箱充分烘干(约需48小时)的KBr粉末,把样品与KBr粉末充分研磨均匀。
3.把上述均匀的混合物置于一定的模具中,在真空下加压成直径为5mm或13mm的半透明片子。
4.把此半透明片子放于红外分光光度计的样品窗口,在参比窗口放上空白的KBr片子,进行测谱。
5.取下测好的红外光谱图,进行图谱解析工作。
四、图谱解析化合物C7H6O2的不饱和度u=1+7+1/2(0-6)=5。
可能含有苯环。
测得的红外光谱图的各谱峰及其归属见下表功能团区的3077,3012 c m -1及1600,1582,1495,1451 c m -1以及指纹区的751,690cm -1等处的峰表示含有单取代苯环(对不饱和度贡献为4),而1684cm -1表示分子中含有羰基(对不饱和度贡献为1)。
此羰基出现在较低波数表示羰基与苯环共轭,同时根据3000~2500cm -1一系列的多重峰和特征的935cm -1(羰基上OH 的面外弯曲振动),可断定此羰基是属于羧基的。
因此可推测该化合物为苯甲酸。
C OOH根据分子式C 7H 6O 2,查SADTLER 标准图谱分子式索引,查得苯甲酸的红外标准图谱号码为779。
将实验测得的红外光谱图与标准图谱779号对照,完全一致。