《药品生产许可证》中生产范围分类及填写规则
- 格式:doc
- 大小:25.50 KB
- 文档页数:1

《药品生产许可证》的相关规定
《药品管理法》规定,开办药品生产企业,须经企业所在地省级药品监督管理部门批准并发给《药品生产许可证》。
无药品生产许可证的企业,不得生产药品。
《药品生产许可证》分正本和副本,具有同等法律效力,有效期为五年,持证企业应当在许可证有效期届满前6个月,按照规定申请换发《药品生产许可证》,《药品生产许可证》编号格式为“省份简称+四位年号+四位顺序号”分类码是对许可证内生产范围进行统计归类的英文字母串。
编码方法:大写字母用于归类产品类型(包括药品的类型和非药品的类型),其中药品的类型还需要进一步以小写字母区分其原料药、制技术型。
大写字母有H(表示化学药)Z(中成药)S(生物制品)T(按药品管理的体外诊断试剂)、Y(中药饮片)Q(医用气体)F(药用辅料)、J(空心胶囊)C(特殊药品)X(其他),并按此顺序排列,小写字母有a(原料药)、b(制剂)。
药品的类型字母HZSC 之后,应紧接其原料药、制剂属性的小写字母。
《药品生产许可》的变更分为许可事项变更和登记事项变更。
许可事项变更,是指企业负责人、生产范围、生产地址的变更。
登记事项的变更,是指企业名称、法定代表人、注册地址、企业类型等项目的变更。

国家食品药品监督管理局关于开展换发《药品生产许可证》工作的通知文章属性•【制定机关】国家食品药品监督管理局(已撤销)•【公布日期】2005.01.08•【文号】国食药监安[2005]17号•【施行日期】2005.01.08•【效力等级】部门规范性文件•【时效性】失效•【主题分类】药政管理正文*注:本篇法规已被:国家食品药品监督管理局关于废止和宣布失效的规范性文件目录(第二批)的公告(发布日期:2011年6月28日,实施日期:2011年6月28日)宣布失效国家食品药品监督管理局关于开展换发《药品生产许可证》工作的通知(国食药监安[2005]17号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为进一步加强药品生产的监督管理,巩固监督实施药品GMP成果,保证药品质量和人民用药安全有效,促进医药事业的健康发展,根据《药品管理法》、《药品管理法实施条例》、《药品生产监督管理办法》及有关规定,国家食品药品监督管理局决定2005年在全国范围内开展《药品生产许可证》的统一换发工作。
现将换证工作有关事项通知如下:一、各省、自治区、直辖市食品药品监督管理局(药品监督管理局)要高度重视,加强领导,精心组织本辖区换证工作,按照《药品管理法》及国家食品药品监督管理局的有关规定,制定具体换证工作方案,组织实施,并将换证工作方案抄送我局药品安全监管司。
二、换发《药品生产许可证》工作从2005年7月1日开始,至2005年12月31日结束。
凡依法持有《药品生产许可证》且有效期至2005年12月31日的药品生产企业,应按规定申请换发新版《药品生产许可证》;至2005年12月31日,依法持有《药品生产许可证》有效期尚未期满的药品生产企业,应申请更换新版《药品生产许可证》。
自2006年1月1日起,全部启用国家食品药品监督管理局统一印制的新版《药品生产许可证》,旧版《药品生产许可证》同时废止。
三、药品生产企业应在2005年6月30日前向所在地省(自治区、直辖市)食品药品监督管理局(药品监督管理局)提出换证申请,并报送以下资料:1.药品生产许可证登记表并附电子文档(见附件1,可从国家食品药品监督管理局网站直接下载后填写);2.原《药品生产许可证》正、副本复印件;3.《企业法人营业执照》或《营业执照》的正、副本复印件;4.《药品GMP证书》复印件;5.药品生产企业生产质量管理情况自查报告;6.药品生产企业接受监督检查(包括跟踪检查)及整改落实情况;7.不合格药品被质量公报通告情况及整改情况。

附件2 《药品生产许可证》生产范围填写规则一、《药品生产许可证》的生产范围应按《中华人民共和国药典》制剂通则及其他的药品国家标准填写,主要有以下剂型:大容量注射剂、小容量注射剂、粉针剂、冻干粉针剂、片剂、硬胶囊剂、软胶囊剂(胶丸)、颗粒剂、散剂、丸剂(蜜丸、水蜜丸、水丸、浓缩丸、糖丸、蜡丸、滴丸等)、口服混悬剂、合剂、口服溶液剂、口服乳剂、糖浆剂、酒剂、酊剂、茶剂、露剂、搽剂、洗剂、栓剂、涂剂、软膏剂、乳膏剂、眼用制剂(滴眼剂、洗眼剂、眼内注射溶液、眼膏剂、眼用乳膏剂、眼用凝胶剂、眼膜剂、眼丸剂、眼内插入剂)、耳用制剂、鼻用制剂、凝胶剂、贴剂、贴膏剂、膏药、锭剂、流浸膏剂、浸膏剂、煎膏剂(膏滋)、胶剂、膜剂、涂膜剂、糊剂、植入剂、冲洗剂、灌肠剂、吸入制剂、气雾剂、喷雾剂、进口药品分包装(注明剂型)。
其中,青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药等类别产品应同时在括弧内注明。
一种剂型既有注明类别品种也有其他普通品种,应在类别前加“含”字。
外用制剂应在制剂后加括弧注明外用,既有口服也有外用的制剂,应在制剂后括弧内注明含外用。
例如:片剂(头孢菌素类)片剂(头孢菌素类、抗肿瘤类)小容量注射剂(含激素类)颗粒剂胶囊剂(含头孢菌素类)冻干粉针剂片剂(含青霉素类、头孢菌素类)酊剂(外用)酊剂(含外用)。
二、原料药、无菌原料药的填写,正本上只注明类别,副本上在类别后括弧内注明其通用名称。
例如: 正本生产范围:原料药。
副本生产范围:原料药(***、***)。
三、生物制品应在正本上按预防用生物制品、治疗用生物制品、血液制品、体内诊断试剂、体外诊断试剂等分类填写,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:预防用生物制品。
副本生产范围:预防用生物制品(****疫苗、****)。
四、医疗用毒性药品、麻醉药品、精神药品、药品类易制毒化学品等特殊药品,应在正本上填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:医疗用毒性药品。

附件4:《药品生产许可证》生产范围填写规则一、《药品生产许可证》的生产范围应按《中华人民共和国药典》制剂通则及其他的药品国家标准填写,主要有以下剂型:大容量注射剂、小容量注射剂、粉针剂、冻干粉针剂、片剂、硬胶囊剂、软胶囊剂、颗粒剂、散剂、丸剂(蜜丸、水蜜丸、水丸、浓缩丸、微丸、糊丸、蜡丸)、滴丸剂、干混悬剂、混悬剂、合剂、口服液、口服溶液剂、乳剂、糖浆剂、酒剂、酊剂、茶剂、露剂、搽剂、洗剂、栓剂、涂剂、软膏剂、乳膏剂、眼膏剂、凝胶剂、透皮贴剂、巴布膏剂、橡胶膏剂、膏药、锭剂、流浸膏剂、浸膏剂、煎膏剂(膏滋)、胶剂、膜剂、滴眼剂、滴耳剂、滴鼻剂、气雾剂、喷雾剂、鼻喷剂、甘油剂、海绵剂、进口药品分包装(注明剂型)。
其中青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药应同时在括弧内注明。
一种剂型既有类别品种也有其它普通品种,应在类别前加“含”字;外用制剂应在制剂后加括弧注明外用,既有口服也有外用的制剂,应在制剂后括弧内注明含外用。
例如:片剂(头孢菌素类),片剂(头孢菌素类、抗肿瘤类),小容量注射剂(含激素类),颗粒剂,胶囊剂(含头孢菌素类),冻干粉针剂,片剂(含青霉素类、头孢菌素类),酊剂(外用),酊剂(含外用)。
二、原料药、无菌原料药、提取物的填写,正本上只注明类别,副本上在类别后括弧内注明其通用名称。
例如: 正本生产范围:原料药。
副本生产范围:原料药(***、***)。
三、生物制品应在正本上按疫苗、血液制品、血清抗毒素、生物工程产品、免疫制剂、体内诊断试剂、过敏原制剂、体细胞及基因治疗制剂等分类填写,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:疫苗。
副本生产范围:疫苗(****、****)。
四、体外诊断试剂的正本上只填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:体外诊断试剂。
副本生产范围:体外诊断试制(****、****)。
五、医疗用毒性药品、麻醉药品、精神药品、药品类易制毒化学品等特殊药品,应在正本上填写类别,副本上在类别后括弧内注明产品名称。

《药品生产许可证》申请表申请单位(盖章):
法定代表人(负责人)签字:
申请日期:
药品生产许可证登记表
填报企业:(公章)所在地:省、自治区、直辖市
填报日期:年月日
登记日期:年月日
国家药品监督管理局制
填报说明
一、企业名称、注册地址、法定代表人、企业类型按工商行政管理部门核准的内容填写。
二、生产地址应按企业药品生产的实际地址填写,有一处以上生产地址的,按顺序依次填写生产地址和生产范围。
例如:
企业名称:xxxx制药有限公司
注册地址:xx市xx区xx路xx号
1.生产地址:xx市xx区xx路xx号
生产范围:片剂、胶囊剂、颗粒剂、原料药(***)
2.生产地址:XX市XX经济技术开发区
生产范围:冻干粉针剂、大容量注射剂
三、固定资产计算单位:万元,平方米。
生产能力计算单位:万瓶、万支、万片、万粒、万袋、吨等。
四、电话号码前标明所在地区长途电话区号。
五、《药品生产许可证号》编号和生产范围统一按国家药品监督管理局统一规定的编号方法及分类填写规定填写。
《药品生产许可证号》编号由各省级药品监督管理部门填写。
六、药品生产许可登记编号及登记日期由各省级药品监督管理部门填写。
登记编号为:省、自治区、直辖市简称十年号十四位数字顺序号。
七、《药品生产许可证》登记表填写一式两份,应内容准确完整,字迹清晰。
企业基本情况登记表
注:填写空间不够,可另加附页。

附件4《药品生产许可证》生产范围填写规则一、《药品生产许可证》的生产范围应按《中华人民共和国药典》制剂通则及其他的药品国家标准填写,主要有以下剂型:大容量注射剂、小容量注射剂、粉针剂、冻干粉针剂、片剂、硬胶囊剂、软胶囊剂、颗粒剂、散剂、丸剂(蜜丸、水蜜丸、水丸、浓缩丸、糊丸、蜡丸)、滴丸剂、干混悬剂、混悬剂、合剂、口服液、口服溶液剂、乳剂、糖浆剂、酒剂、酊剂、茶剂、露剂、搽剂、洗剂、栓剂、涂剂、软膏剂、乳膏剂、眼膏剂、凝胶剂、透皮贴剂、橡胶膏剂、膏药、锭剂、流浸膏剂、浸膏剂、煎膏剂(膏滋)、胶剂、膜剂、滴眼剂、滴耳剂、滴鼻剂、气雾剂、喷雾剂、鼻喷剂、甘油剂、海绵剂、进口药品分包装(注明剂型)等。
其中青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药应同时在括弧内注明。
一种剂型既有类别品种也有其它普通品种,应在类别前加“含”字;外用制剂应在制剂后加括弧注明外用,既有口服也有外用的制剂,应在制剂后括弧内注明含外用。
例如:片剂(头孢菌素类),片剂(头孢菌素类、抗肿瘤类),小容量注射剂(含激素类),颗粒剂,硬胶囊剂(含头孢菌素类),冻干粉针剂,片剂(含青霉素类、头孢菌素类),酊剂(外用),酊剂(含外用)。
二、原料药、无菌原料药、提取物的填写,正本上只注明类别,副本上在类别后括弧内注明其通用名称。
例如: 正本生产范围:原料药。
副本生产范围:原料药(***、***)。
三、生物制品应在正本上按疫苗、血液制品、血清抗毒素、生物工程产品、免疫制剂、体内诊断试剂、过敏原制剂、体细胞及基因治疗制剂等分类填写,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:疫苗。
1副本生产范围:疫苗(****、****)。
四、体外诊断试剂的正本上只填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:体外诊断试剂。
副本生产范围:体外诊断试剂(****、****)。
五、医疗用毒性药品、麻醉药品、精神药品、药品类易制毒化学品等特殊药品,应在正本上填写类别,副本上在类别后括弧内注明产品名称。


四川省食品药品监督管理局《药品生产许可证》核发(变更)办事指南一、法定依据《中华人民共和国药品管理法实施条例》(2002年8月4日国务院令第360号公布,自2002年9月15日起施行)“第四条药品生产企业变更《药品生产许可证》许可事项的,应当在许可事项发生变更30日前,向原发证机关申请《药品生产许可证》变更登记;未经批准,不得变更许可事项。
原发证机关应当自收到申请之日起15个工作日内作出决定。
申请人凭变更后的《药品生产许可证》到工商行政管理部门依法办理变更登记手续。
”二、申请条件持有《药品生产许可证》的企业,许可事项依法发生变更。
《药品生产监督管理办法》(国家食品药品监督管理局第14号令)第14条规定:由(食品)药品监督管理部门核准的许可事项为:企业负责人、生产范围、生产地址。
三、申报资料申请变更《药品生产许可证》许可事项须提交以下资料各一份:1、企业申请变更《药品生产许可证》的书面报告、变更申请表;2、《药品生产许可证》正、副本原件、复印件各1套,营业执照复印件;3、《药品生产许可证登记表》并附电子版申请文件;(登陆国家食品药品监督管理局网站/下载“药品生产许可证管理系统”,按要求填报)(点击下载);4、不同变更项目需报送的材料5、企业法人出具的确保申报资料内容真实有效的保证函;6、凡申请企业申报材料时,申请人不是法定代表人或负责人本人,应当提交《授权委托书》1份;7、组织机构代码证复印件。
四、办理程序《药品生产许可证》应载明许可证编号、企业名称、法定代表人、企业负责人、企业类型、注册地址、生产地址、生产范围、发证机关、发证日期、有效期限等项目。
其中由食品药品监督管理部门核准的许可事项为:企业负责人、生产范围、生产地址、有效期限。
1、企业在许可事项发生变更30日前向省政府政务服务中心省食品药品监督管理局窗口提出申请;2、省食品药品监督管理局受理并审核(变更生产地址及生产范围须安排现场检查);3、审核合格的同意变更,不合格的由省食品药品监督管理局下达不予许可的书面决定,并说明理由,同时告知申请人享有依法申请行政复议或提起行政诉讼的权利;4、批准变更的,企业向工商行政管理部门办理企业注册登记的变更手续。

《药品生产许可证》相关基本知识
药品生产许可证是指由国家药品监督管理部门颁发的,允许企业从事药品生产活动的合法证明文件。
具体的相关基本知识包括:
1. 许可证的发放机构:药品生产许可证由国家药品监督管理部门或地方省级食药监管部门负责发放。
2. 申请条件:企业必须具备一定的生产规模、设备和技术条件,同时需要符合药品生产的相关法律法规。
3. 许可范围:许可证一般分为药品生产许可证和药品片剂生产许可证两类,分别允许企业从事不同种类的药品生产。
4. 许可证的有效期:药品生产许可证的有效期为5年,药品片剂生产许可证的有效期为3年。
5. 监督检查:持证企业需要接受药品监督管理部门的监督检查,确保药品生产过程符合相关法律法规和质量标准。
6. 处罚措施:如果企业在药品生产过程中存在违法违规行为,监管部门有权采取相应的处罚措施,包括暂停或撤销许可证等。
7. 许可证的重要性:持有药品生产许可证是企业合法经营的基本条件,没有许可证的企业不允许从事药品生产活动。
8. 市场准入要求:在贸易国际化时,企业需要获取药品生产许可证才可以进入其他国家市场进行销售和贸易活动。
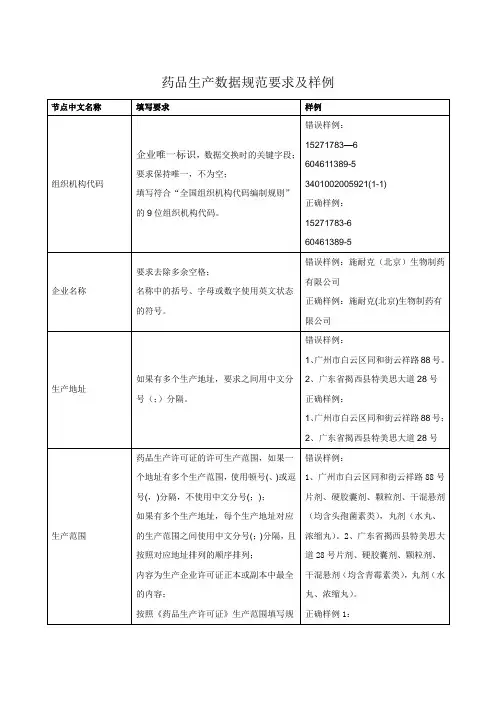
药品生产数据规范要求及样例
委托生产数据规范要求及样例
企业认证数据规范要求及样例(GMP)
药品批发企业数据规范要求及样例
药品零售企业数据规范要求及样例
企业认证数据规范要求及样例(GSP)
药品基本信息数据规范要求及样例
药包材料数据规范要求及样例
医院制剂基本信息数据规范要求及样例
医疗机构基本信息数据规范要求及样例
医疗器械生产数据规范要求及样例
医疗器械经营数据规范要求及样例
国产医疗器械基本信息数据规范要求及样例
医疗器械品种数据规范要求及样例
保健食品生产企业基本信息表
保健食品经营数据规范要求及样例
保健食品基本信息表
化妆品生产数据规范要求及样例
化妆品经营企业数据规范要求及样例
化妆品基本信息数据规范要求及样例
食品生产企业数据规范要求及样例
食品添加剂生产企业数据规范要求及样例
食品添加剂品种信息数据规范要求及样例
食品流通企业基本信息数据规范要求及样例
餐饮企业数据规范要求及样例
黑名单数据规范要求及样例。

附件3:
《药品生产许可证》有关项目填写说明
一、编号
许可证编号格式为“省份简称+四位年号+四位顺序号”。
示例:“编号:京20100001”或“编号:粤20100111”。
变更参考方法:企业变更名称等许可证项目,原许可证编号不变。
企业分立,在保留原许可证编号同时增加新的编号。
企业合并,原许可证编号保留一个。
二、分类码
是对许可证内生产范围进行统计归类的英文字母串。
(一)编码方法
大写字母用于归类产品类型(包括药品的类型和非药品的类型),其中药品的类型还需进一步以小写字母区分其原料药、制剂或提取物属性。
大写字母有H、Z、S、T、Y、Q、F、J、C、X,并按此顺序排列,小写字母有a、b、e。
药品的类型字母H、Z、S、C之后,应紧接其原料药、制剂或提取物属性的小写字母。
(二)字母代码释义
1.产品类型代码
H:化学药
Z:中成药
S:生物制品
T: 按药品管理的体外诊断试剂
Y:中药饮片
Q:医用气体
F: 药用辅料
J: 空心胶囊
C: 特殊药品
X: 其他(如中药配方颗粒等)
2.药品类型属性代码
a: 原料药
b:制剂
e:有国家标准的提取物
(三)代码应用示例
“分类码:HabeZab”或“分类码:HabZbeFJ”。
.。
《药品生产许可证》申请表申请单位(盖章):
法定代表人(负责人)签字:
申请日期:
药品生产许可证登记表
填报企业:
自治区、
(公章)I -
厶、/ 、
所在地:省、直辖市填报日期:年月日
登记日期:年月日
国家药品监督管理局制
填报说明
一、企业名称、注册地址、法定代表人、企业类型按工商行政管理部门核准的内容填写。
二、生产地址应按企业药品生产的实际地址填写,有一处以上生产地址的,按顺序依次填写生产地址和生产范围。
例如:
企业名称:xxxx 制药有限公司
注册地址:XX市XX区XX路XX号
1.生产地址:XX市XX区XX路XX号
生产范围:片剂、胶囊剂、颗粒剂、原料药(***)
2.生产地址:XX市XX经济技术开发区
生产范围:冻干粉针剂、大容量注射剂
三、固定资产计算单位:万元,平方米。
生产能力计算单位:万瓶、万支、万片、万粒、万袋、吨等。
四、电话号码前标明所在地区长途电话区号。
五、《药品生产许可证号》编号和生产范围统一按国家药品监督管理局统一规定的编号方法及分类填写规定填写。
《药品生产许可证号》编号由各省级药品监督管理部门填写。
六、药品生产许可登记编号及登记日期由各省级药品监督管理部门填写。
登记编号为:省、自治区、直辖市简称十年号十四位数字顺序号。
七、《药品生产许可证》登记表填写一式两份,应内容准确完整,字迹清晰。
企业基本情况登记表
注:填写空间不够,可另加附页。
精品文档
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求。
登记编号:
药品生产许可证登记表
申请单位:(公章)
所在地:省、自治区、直辖市
填报日期:2003年11月25日
受理日期:2003年11月25日
国家药品监督经管局制
填报说明
一、企业名称、注册地址、法定代表人、企业类型按工商行政经管部门核准的内容填写。
二、生产地址应按企业药品生产的实际地址填写,有一处以上生产地址的,按顺序依次填写生产地址和生产范围。
例如:企业名称:XXXX制药有限公司
注册地址:XX市XX区XX路XX号
1、生产地址:XX市XX区XX路XX号
生产范围:片剂、胶囊剂、颗粒剂、原料药(***)
2、生产地址:XX市XX经济技术开发区
生产范围:冻干粉针剂、大容量注射剂
三、固定资产计算单位:万元,平方M。
生产能力计算单位:万瓶、万支、万片、万粒、万袋、吨等。
四、电话号码前标明所在地区长途电话区号。
五、《药品生产许可证号》编号和生产范围统一按国家药品监督经管局统一规定的编号方法及分类填写规定填写。
《药品生产许可证号》编号由各省级药品监督经管部门填写。
六、药品生产许可登记编号及登记日期由各省级药品监督经管部门填写。
登记编号为:省、自治区、直辖市简称十年号十四位数字顺序号。
七、《药品生产许可证》登记表填写一式两份,应内容准确完整,字迹清晰。
企业基本情况登记表
生产剂型登记表
生产品种登记表
通过其他国家药品生产质量经管规范认证情况表
药品生产许可证审核表
变更记录
年检记录。
《药品生产许可证》相关基本知识药品生产许可证是指国家卫生健康委员会或者省级人民政府卫生健康主管部门颁发的,允许企业从事特定药品生产的许可证书。
以下是关于药品生产许可证的相关基本知识。
一、药品生产许可证的分类按照药品属性和使用范围的不同,药品生产许可证可分为非处方药生产许可证、中药饮片生产许可证、化妆品生产许可证和药用辅料生产许可证等。
1. 非处方药生产许可证:指用于预防、诊断和治疗一般病症的药品生产许可证,一般是指成人和儿童普通药品。
2. 中药饮片生产许可证:指中药饮片生产企业获得的许可证,用于中药饮片的生产。
3. 化妆品生产许可证:指用于化妆品生产企业获得的许可证,用于各种化妆品的生产。
4. 药用辅料生产许可证:指用于药用辅料生产企业获得的许可证,用于药品生产过程中所需的辅助材料的生产。
二、药品生产许可证的申请条件1. 企业法人资格:企业必须合法设立并具有法人资格。
2. 安全生产条件:企业必须具备符合国家安全生产要求的厂房、设备和环境。
3. 药品药品GMP认证:企业必须通过国家药品GMP认证,以确保生产的药品符合质量规范。
4. 资金实力:企业必须具备足够的资金实力,包括开展生产活动所需的资金和应急资金。
5. 专业技术人员:企业必须配备一定数量的药品生产相关专业技术人员,包括药品生产工艺、质量控制和安全管理等方面的专业人员。
三、药品生产许可证的申请流程1. 企业填写申请表:企业根据相关规定填写《药品生产许可证申请表》。
2. 提交申请材料:企业将填写完整的申请表以及相关的法人资格证明、安全生产许可证、GMP认证证书、企业资金证明和专业技术人员证明等材料提交至对应的卫生健康主管部门。
3. 审核和审评:卫生健康主管部门对申请材料进行审核和审评,包括对企业的设备、场地和技术人员等进行实地考察。
4. 发证:经过审核和审评合格后,卫生健康主管部门颁发药品生产许可证给企业。
四、药品生产许可证的有效期和管理1. 有效期:药品生产许可证的有效期为5年,到期后需要进行续签。
药品生产许可证登记表企业名称:广西XX制药有限公司(公章)填表日期:2007 年08月28日国家食品药品监督管理局制填表说明一、企业名称、注册地址、法定代表人、企业类型按工商行政管理部门核准的内容填写。
二、生产地址应按企业药品生产的实际地址填写,有一处以上生产地址的,按顺序依次填写生产地址和生产范围。
例如:1、生产地址:XX市XX区XX路XX号生产范围:片剂、胶囊剂、颗粒剂、原料药(***)2、生产地址:XX市XX经济技术开发区生产范围:冻干粉针剂、大容量注射剂三、生产能力计算单位:万瓶、万支、万片、万粒、万袋、公斤等。
四、电话号码前标明所在地区长途电话区号。
五、《药品生产许可证》编号和生产范围由各省、自治区、直辖市(食品)药品监督管理局按国家食品药品监督管理局统一规定的编号方法及分类填写规定填写。
六、《药品生产许可证登记表》申请编号由各省、自治区、直辖市(食品)药品监督管理局填写。
登记编号为:省、自治区、直辖市简称十年号十四位数字顺序号。
七、《药品生产许可证登记表》一式两份,内容应准确完整,字迹清晰。
注:①报送或发送的药品生产许可证登记表电子文档,应是填写电子填报软件导出生成的电子资料(文件后缀名为:xml),而不是打印后的Microsoft Word表格。
登记表电子填报软件下载地址:企业名称广西XX制药有限公司注册地址XX市XX区XX路XX号原药品生产许可证编号桂HbZb200600XX单位代码XXXXXX 注册地址邮编XXXXXX企业类型有限责任公司三资企业外方国别或地区及名称无企业始建时间XXXX年XX月XX日最近更名时间XXXX年XX月XX日法定代表人张XX职称高级工程师所学专业分析化学企业负责人李XX职称高级工程师所学专业分析化学质量负责人王XX职称高级工程师所学专业药师生产负责人张XX职称高级工程师所学专业药师职工人数(人)160 其中:技术人员(人)40高级职称(人)40 初中级职称(人)10研究生学历(人)10 大学本科专科学历(人)30固定资产原值(万元)1122 固定资产净值(万元)1100厂区占地面积(平米)15000 建筑面积(平米)10000上年度产值(万元)1000 上年度利润(万元)120原料药注册品种数0 制剂注册品种数26 其它类注册产品数0 常年生产品种数15 联系人张XX电话0771-58500XX 传真备注生产地址:XX市XX区XX路XX号生产范围:片剂、颗粒剂、口服溶液剂(含中药前处理和提取)企业全部制剂剂型,原料药、生物制品生产车间、其它产品名称,中药前处理及提取车间年生产能力计算单位制剂生产线数(条)已取得药品GMP证书号口服固体制剂车间10000 1 桂F00XX 备注注:填写空间不够,可另加附页。
《药品生产许可证》中生产范围分类及填写规则第一篇:《药品生产许可证》中生产范围分类及填写规则附件3:《药品生产许可证》中生产范围分类及填写规则一、《药品生产许可证》的生产范围应按《中华人民共和国药典》制剂通则及国家药品标准填写,主要有以下剂型:大容量注射剂、小容量注射剂、粉针剂、冻干粉针剂、片剂、硬胶囊剂、软胶囊剂、颗粒剂、散剂、丸剂(蜜丸、水蜜丸、水丸、浓缩丸、微丸、糊丸、蜡丸)、滴丸剂、干混悬剂、混悬剂、合剂、口服液、口服溶液剂、乳剂、糖浆剂、酒剂、酊剂、茶剂、露剂、搽剂、洗剂、栓剂、涂剂、软膏剂、乳膏剂、眼膏剂、凝胶剂、透皮贴剂、巴布膏剂、橡胶膏剂、膏药、锭剂、流浸膏剂、浸膏剂、煎膏剂(膏滋)、胶剂、膜剂、滴眼剂、滴耳剂、滴鼻剂、气雾剂、喷雾剂、鼻喷剂、甘油剂、海绵剂、进口药品分包装(注明剂型)。
其中青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药应同时在括弧内注明。
一种剂型既有类别品种也有其它普通品种,应在类别前加“含”字;外用制剂应在制剂后加括弧注明外用,既有口服也有外用的制剂,应在制剂后括弧内注明含外用。
例如:片剂(头孢菌素类),片剂(头孢菌素类、抗肿瘤类),小容量注射剂(含激素类),颗粒剂,胶囊剂(含头孢菌素类),冻干粉针剂,片剂(含青霉素类、头孢菌素类),酊剂(外用),酊剂(含外用)。
二、原料药、无菌原料药、中药提取物的填写,正本上只注明类别,副本上在类别后括弧内注明其国家药品标准规定的产品通用名称。
例如:正本生产范围:原料药。
副本生产范围:原料药(***、***)。
三、生物制品应在正本上按疫苗、血液制品、血清抗毒素、生物工程产品、免疫制剂、体内诊断试剂、过敏原制剂、体细胞及基因治疗制剂等分类填写,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:疫苗。
副本生产范围:疫苗(****、****)。
四、体外诊断试剂的正本上只填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:体外诊断试剂。
登记编号:药品生产许可证登记表
申请单位:(公章)所在地:省、自治区、直辖市填报日期:2003年11月25日受理日期:2003年11月25日
国家药品监督管理局制
填报说明
一、企业名称、注册地址、法定代表人、企业类型按工商行政管理部门核准的内容填写。
二、生产地址应按企业药品生产的实际地址填写,有一处以上生产地址的,按顺序依次填写生产地址和生产范围。
例如:企业名称:XXXX制药有限公司
注册地址:XX市XX区XX路XX号
1、生产地址:XX市XX区XX路XX号
生产范围:片剂、胶囊剂、颗粒剂、原料药(***)
2、生产地址:XX市XX经济技术开发区
生产范围:冻干粉针剂、大容量注射剂
三、固定资产计算单位:万元,平方米。
生产能力计算单位:万瓶、万支、万片、万粒、万袋、吨等。
四、电话号码前标明所在地区长途电话区号。
五、《药品生产许可证号》编号和生产范围统一按国家药品监督管理局统一规定的编号方法及分类填写规定填写。
《药品生产许可证号》编号由各省级药品监督管理部门填写。
六、药品生产许可登记编号及登记日期由各省级药品监督管理部门填写。
登记编号为:省、自治区、直辖市简称十年号十四位数字顺序号。
七、《药品生产许可证》登记表填写一式两份,应内容准确完整,字迹清晰。
企业基本情况登记表
企业基本情况登记表
生产剂型登记表
生产品种登记表
通过其他国家药品生产质量管理规范认证情况表
药品生产许可证审核表
变更记录
年检记录
11。
附件3:《药品生产许可证》中生产范围分类及填写规则
一、《药品生产许可证》的生产范围应按《中华人民共和国药典》制剂通则及国家药品标准填写,主要有以下剂型:
大容量注射剂、小容量注射剂、粉针剂、冻干粉针剂、片剂、硬胶囊剂、软胶囊剂、颗粒剂、散剂、丸剂(蜜丸、水蜜丸、水丸、浓缩丸、微丸、糊丸、蜡丸)、滴丸剂、干混悬剂、混悬剂、合剂、口服液、口服溶液剂、乳剂、糖浆剂、酒剂、酊剂、茶剂、露剂、搽剂、洗剂、栓剂、涂剂、软膏剂、乳膏剂、眼膏剂、凝胶剂、透皮贴剂、巴布膏剂、橡胶膏剂、膏药、锭剂、流浸膏剂、浸膏剂、煎膏剂(膏滋)、胶剂、膜剂、滴眼剂、滴耳剂、滴鼻剂、气雾剂、喷雾剂、鼻喷剂、甘油剂、海绵剂、进口药品分包装(注明剂型)。
其中青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药应同时在括弧内注明。
一种剂型既有类别品种也有其它普通品种,应在类别前加“含”字;外用制剂应在制剂后加括弧注明外用,既有口服也有外用的制剂,应在制剂后括弧内注明含外用。
例如:片剂(头孢菌素类),片剂(头孢菌素类、抗肿瘤类),小容量注射剂(含激素类),颗粒剂,胶囊剂(含头孢菌素类),冻干粉针剂,片剂(含青霉素类、头孢菌素类),酊剂(外用),酊剂(含外用)。
二、原料药、无菌原料药、中药提取物的填写,正本上只注明类别,副本上在类别后括弧内注明其国家药品标准规定的产品通用名称。
例如:正本生产范围:原料药。
副本生产范围:原料药(***、***)。
三、生物制品应在正本上按疫苗、血液制品、血清抗毒素、生物工程产品、免疫制剂、体内诊断试剂、过敏原制剂、体细胞及基因治疗制剂等分类填写,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:疫苗。
副本生产范围:疫苗(****、****)。
四、体外诊断试剂的正本上只填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:体外诊断试剂。
副本生产范围:体外诊断试制(****、****)。
五、医疗用毒性药品、麻醉药品、精神药品、药品类易制毒化学品等特殊药品,应在正本上填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:医疗用毒性药品。
副本生产范围:医疗用毒性药品(****、****)。
六、药用辅料在正本上只填写类别,副本上在括弧内注明产品名称。
中药饮片在正本上括弧内注明含毒性饮片,副本上应除括弧内注明含毒性饮片外,还应括弧内注明含直接服用饮片及相应的炮制范围,包括净制、切制、炒制、炙制、煅制、蒸制等。
医用氧等应在正本上填写类别,副本上在类别后括弧内注明产品名称。
空心胶囊直接填写。
以上类别之外的药品可直接填写通用名称。