Na2CO在乙醇中的溶解度 物质 溶解度(S)/g
NaOH
17.3
Na2CO3
<0.01
请你和化学兴趣小组的同学一起利用以上资料信息再设计实验
Ⅲ,证明CO2确实与NaOH发生了化学反应。 实验Ⅲ的操作为 。看到的
2
3
特别提醒利用思路(1)判断反应是否发生时常出现的问题:氢氧化 钠溶液中含有水,二氧化碳也能和水发生反应,必须设计对比实验 排除水对实验结果的影响。
(2)反应后的产物为碳酸钠,可以利用碳酸钠和氢氧化钠与酸(或 氯化钡、氯化钙等)反应的现象不同进行判断。
4
3.如何检验氢氧化钠溶液是否变质
4.氢氧化钠变质程度的方案设计 样品加入水溶解,逐滴滴入氯化钙溶液至不再产生沉淀为止,滴 入酚酞溶液后,若溶液变红,则部分变质,若不变红,则说明全部变质。
。
(2)实验Ⅱ中步骤二看到有白色沉淀析出,则发生反应的化学方程
式是
。
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应, 但却看不到明显的现象,原因是 。
7
【拓展延伸】现有下列信息:
资料卡片一
20 ℃ NaOH、Na2CO3在水中的溶解度 物质 溶解度(S)/g
NaOH 109
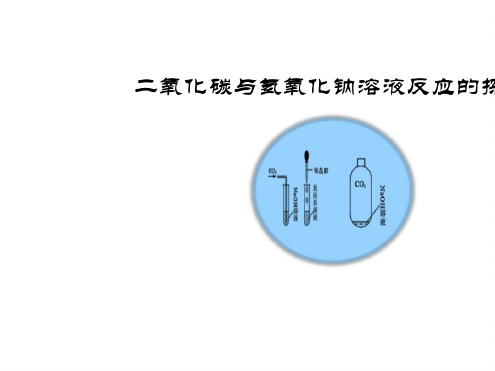
实验 氢氧化钠和二氧化碳反应的探究
1.原理 氢氧化钠能和二氧化碳反应,反应的化学方程式为CO2+2NaOH
=== Na2CO3+H2O。
2.验证氢氧化钠是否和二氧化碳反应的思路 (1)可以利用密闭的装置,根据氢氧化钠和二氧化碳反应后会导致 密闭容器中压强减小,从而引起现象的变化而判定。 主要装置及现象如下:
5
例题(2018·湖北黄冈中考)对比实验是化学研究中经常采用的方 法。化学兴趣小组的同学在研究CO2通入NaOH溶液后是否发生了 反应,设计了下列两组实验。请和化学兴趣小组的同学一起探究并 回答问题: