广东省2020中考化学复习提升试题:专题二_推断题_含答案
- 格式:doc
- 大小:120.50 KB
- 文档页数:8
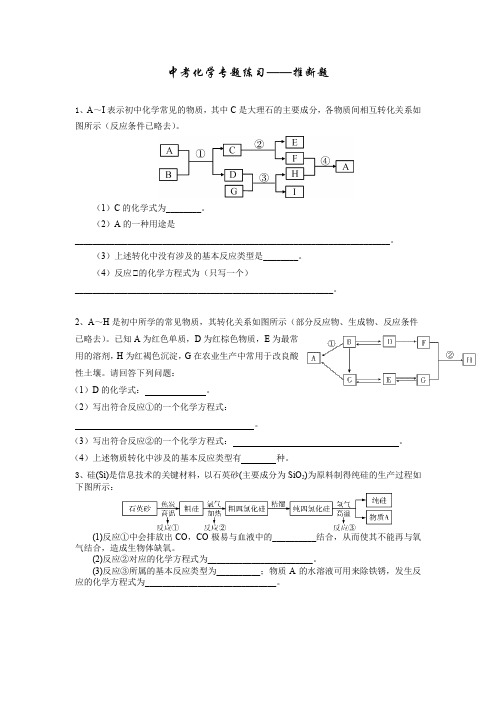
中考化学专题练习——推断题1、A~I表示初中化学常见的物质,其中C是大理石的主要成分,各物质间相互转化关系如图所示(反应条件已略去)。
(1)C的化学式为________。
(2)A的一种用途是________________________________________________________________________。
(3)上述转化中没有涉及的基本反应类型是________。
(4)反应③的化学方程式为(只写一个)___________________________________________________________。
2、A~H是初中所学的常见物质,其转化关系如图所示(部分反应物、生成物、反应条件已略去)。
已知A为红色单质,D为红棕色物质,E为最常用的溶剂,H为红褐色沉淀,G在农业生产中常用于改良酸性土壤。
请回答下列问题:(1)D的化学式:。
(2)写出符合反应①的一个化学方程式:。
(3)写出符合反应②的一个化学方程式:。
(4)上述物质转化中涉及的基本反应类型有种。
3、硅(Si)是信息技术的关键材料,以石英砂(主要成分为SiO2)为原料制得纯硅的生产过程如下图所示:(1)反应①中会排放出CO,CO极易与血液中的__________结合,从而使其不能再与氧气结合,造成生物体缺氧。
(2)反应②对应的化学方程式为________________________。
(3)反应③所属的基本反应类型为__________;物质A的水溶液可用来除铁锈,发生反应的化学方程式为______________________________。
4、整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法。
小丽在复习时,将Al、CO2、Ca(OH)2、HCl、CuSO4构建了如图知识网络图,图中短线“—”表示相连的两种物质能在一定条件下发生反应,C为蓝色溶液。
请回答:(1)物质A的固态称________;物质E的化学式________。

2023年广东省中考专题复习精选化学试题(二)(内容:物质的化学变化)可能用到的相对原子质量:C-12 O-16 S-32 H-1 N-14 C1-35.5 Ba-137 Hg-201 一、单项选择题(每题3分,共45分)1.《天工开物》中记载了古法造纸工艺。
下列步骤中一定发生了化学变化的是 ( ) A.煮楻足火 B.斩竹槌洗 C.日晒成干 D.覆帘压纸2.物质的性质决定其用途。
下列用途是利用物质物理性质的是 ( ) A.稀盐酸用于除铁锈 B.活性炭吸附异味 C.用熟石灰改良酸性土壤 D.酒精可以作燃料3.下列判断错误的是 ( )A.浓硫酸具有脱水性一化学性质B.浓硫酸是一种稠状的液体—物理性质C.NaOH 固体溶于水显碱性一物理性质D.NaOH 固体在空气中易变质一化学性质4.除了元素种类、原子种类不变外,化学反应前后肯定没有变化的还有 ( )A.分子数目B.原子数目C.物质种类D.分子种类5.关于2CO+O 2======CO 2的叙述正确的是 ( ) A.一氧化碳加氧气点燃等于二氧化碳B.2g 一氧化碳和1g 氧气反应生成2g 二氧化碳C.两个一氧化碳分子加一个氧分子等于两个二氧化碳分子D.56g 的一氧化碳和32g 的氧气完全反应能生88g 的二氧化碳 6.工业用盐亚硝酸钠(NaNO 3)与食盐很像,但有毒,亚硝酸钠分解生成一种有刺激性气味的气体,该气体可能是 ( ) A.NH 3 B.SO 2 C.N 2 D.NO 2 7.下列关于质量守恒定律的说法正确的是 ( )A.高锰酸钾分解后固体质量变小,符合质量守恒定律B.只要有气体参加或生成的反应均不遵守质量守恒定律C.10g 白糖完全溶于70g 水可得到80g 糖水,遵守质量守恒定律D.引燃密闭容器中的ag 氢气和bg 氧气,冷却后得到水的质量一定等于(a+b)g 8.已知某纯净物23g 在足量的氧气中充分燃烧后,生成4.4g 二氧化碳和2.7g 水。

中考二轮复习化学推断题专题练习(带答案)一、中考化学推断题1.已知A、B、C、D、E是初中化学中常见的五种物质,均含有同一种元素。
其中,A、B、D、E是不同类别的物质,B和C含有的元素完全相同,E是一种重要建筑材料的主要成分,它们在一定条件下的转化关系如图所示。
请你完成以下空白:(1)D的化学式为_____。
(2)请写出B→E反应的化学方程式:_____(3)A→C的反应基本类型是:_____(4)请说出C的一种用途:_____【答案】H2CO3 Ca(OH)2+CO2=CaCO3↓+H2O 化合反应作燃料或冶炼金属【解析】【分析】A、B、C、D、E是初中化学中常见的五种物质,均含同一种元素,B和C含有的元素完全相同,B、C可以相互转化,所以B、C是二氧化碳和一氧化碳,A会转化成二氧化碳和一氧化碳,所以A是碳,E是一种重要建筑材料的主要成分,E和B可以相互转化,所以B 是二氧化碳,C是一氧化碳,E就是碳酸钙,D与其它四种物质属于不同的类别,D和二氧化碳可以相互转化,所以D是碳酸,带入验证,推理正确。
【详解】由分析可知(1)D的化学式为H2CO3;(2)B→E的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;(3)A→C的反应是碳和氧气在点燃的条件下生成一氧化碳,此反应属于化合反应;(4)C是一氧化碳,可作燃料或冶炼金属。
【点睛】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
2.A、B、C、D是初中化学常见的物质,其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分,它们之间的转化关系如图所示(图中反应条件及部分反应物、生成物已省略)。
回答下列问题:(1)写出下列物质的化学式:A_____;B_____;C_____。
(2)实验室常用_____鉴别B和C。

一、中考初中化学推断题1.现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成。
为确定其组成,进行了如下图所示的实验(假设实验过程无损耗)。
请回答:(1)根据实验可以确定白色沉淀是________;原固体粉末中一定含有_____________,它的可能组成有____________种。
(2)若实验取固体粉末20g,生成白色沉淀10g,最后得到溶质质量分数为5.85%的X溶液200g(只含一种溶质),则X溶液中溶质的质量是____g,固体粉末由______________(填化学式,下同)组成,其中质量小于10g的是_____________________。
【答案】CaCO3(或“碳酸钙”) Na2CO3(或“碳酸钠”) 3 11.7 CaCO3、CaO、Na2CO3 CaCO3、CaO【解析】【分析】把固体粉末加入水中,得到白色沉淀,根据题给的物质可以判断该白色沉淀为碳酸钙,得到无色溶液与稀盐酸反应生成无色气体,可以判断在无色溶液中含有碳酸钠,而无色气体为二氧化碳,那么X就可能是氯化钠的溶液。
【详解】(1)在白色粉末中能产生白色沉淀,可知该白色沉淀应该为碳酸钙,又得到的无色溶液能够和稀盐酸反应生成气体,可以知道在固体粉末中一定含有碳酸钠,它可能的组合为:①碳酸钠,氧化钙;②碳酸钠,碳酸钙;③碳酸钠,氧化钙,碳酸钙等三种可能的组成;(2)根据(1)的解答可知X溶液为氯化钠溶液其质量为:200g×5.85%=11.7g,根据题意结合化学方程式,可以求出与盐酸反应的碳酸钠的质量为10.6g,进而可以判断出该固体粉末的组成为:CaCO3、CaO、Na2CO3 ,进而可以判断若白色沉淀质量小于10g,则原混合物的组成为氧化钙和碳酸钙,计算过程如下:设碳酸钠的质量为x2322Na CO+2HCl=2NaCl+H O+CO106117x11.7g106 x =117 11.7gx=10.6g这里我们求得的只是和盐酸反应的碳酸钠,总质量为20g,所以假如白色沉淀是固体粉末中的,则只有20g-10.6g=9.4g,而题目中得到的白色沉淀的质量是10g,也就是说白色沉淀并不是完全来自于原固体粉末中,而是有一部分是反应中生成的,即氧化钙和水反应生成了氢氧化钙,而氢氧化钙又和碳酸钠反应生成了碳酸钙沉淀,从而可以判断在混合物中含有氧化钙.故本题答案为:(1)CaCO3(或“碳酸钙”); Na2CO3(或“碳酸钠”); 3;(2)11.7; CaCO3、CaO、Na2CO3;CaCO3、CaO.2.实验室有一包白色粉末,可能含有 Na2SO4、Ba(NO3)2、K2CO3、KOH、CuSO4、Mg(NO3)2和KCl中的一种或几种,为了确定其成分,某化学兴趣小组进行了如下实验探究。

中考化学《推断题》专项试题1.A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如下图所示(部分生成物已省略):⑴写出反应⑴的化学方程式___________________________________________ 。
⑴写出反应⑴的化学方程式___________________________________________ ,该反应属于_______(填写基本反应类型)反应。
⑴含D的生产、生活用品腐蚀的过程,实际上是D与空气中的__________发生化学反应的过程。
2.由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲、乙是化合物。
图中“—”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质。
(部分反应物、生成物及反应条件略去)。
回答下列问题:(1)写出下列物质的化学式:A__________、C_________、甲__________;(2)写出乙→B反应的化学方程式______________________________。
3.A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):(1)写出⑴反应的化学方程式____________________;(2)D可能是____________(填化学式);(3)反应⑴的基本反应类型是__________.4.A~G都是初中化学常见物质,在高温或加热条件下可以发生如图所示的转化。
已知:A 是一种最常用的溶剂;常温下,C、D、F为气体,B、G为固体单质。
下列说法错误的是()A.A~G中共有4种氧化物B.反应⑴中,B一定发生了氧化反应C.反应⑴~⑴中只有2个反应属于置换反应D.E中含有氧元素,且氧元素的质量分数一定为20%5.A~F是初中化学常见物质。
专题二物质的转化与推断一、解题思路二、推断题常见的突破口1.常见物质的特征颜色和状态(1)常见的能发生分解反应的物质:H2O2、KClO3、KMnO4、H2O、H2CO3、CaCO3、Cu2(OH)2CO3等。
(2)常见的能发生置换反应的物质:①还原性单质(C、H2)+金属氧化物;②金属(H前)+酸;③金属+盐溶液。
4.特殊反应条件(1)通电:水通电分解。
(2)高温:碳酸钙分解、C+CuO、C+CO2、C+Fe2O3、CO+Fe2O3。
(3)加热:氯酸钾、高锰酸钾分解、H2+CuO、CO+CuO。
(4)催化剂:氯酸钾、过氧化氢分解。
5.物质的类别(2017、2014考)(1)常用作灭火剂的是CO2。
(2)农业上常用于改良酸性土壤的是Ca(OH)2(熟石灰)。
(3)工业上用于金属除锈的是盐酸和稀硫酸。
(4)人体胃液中用于帮助消化的酸是盐酸。
(5)可用作调味品的是NaCl。
(6)用于治疗胃酸的是Al(OH)3。
(7)用于人工降雨的物质是干冰(固态CO2)。
(8)可用作干燥剂的固体物质有CaO、NaOH,液体物质为浓硫酸。
(9)可用作补钙剂的是CaCO3。
(10)用于造纸、玻璃、纺织和洗涤剂生产的是Na2CO3。
(11)参与光合作用的气体为CO2。
(12)可供给呼吸、支持燃烧的是O2。
(13)可用于实验室检验水的存在的是无水硫酸铜。
7.物质的特殊性质(1)能使澄清石灰水变浑浊的气体是CO2。
(2)能使带火星的木条复燃的气体是O2。
(3)具有还原性的物质是C、CO、H2。
(4)在空气中燃烧生成CO2和H2O的物质是有机物。
(5)与酸反应产生能使澄清石灰水变浑浊的气体的物质是碳酸盐或碳酸氢盐。
(6)能使酚酞溶液变红(紫色石蕊溶液变蓝)的溶液显碱性。
(7)能使紫色石蕊溶液变红的溶液显酸性。
(8)能与碱反应生成能使酚酞溶液变红(紫色石蕊溶液变蓝)的气体的物质是铵盐。
(9)能与硝酸钡反应产生白色沉淀的是硫酸盐或碳酸盐。
一、中考初中化学推断题1.A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去),其中A为金属氧化物,E、F为金属单质,且F为紫红色,化学反应②和③的基本反应类型相同。
请按要求填空:(1)物质C的化学式为___________________。
(2)写出反应②的一个化学方程式_______________________________________。
(3)反应③的基本反应类型是__________________________。
(4)E、F和氢由强到弱的金属活动性顺序为________________________________。
【答案】H2O Fe + CuSO4= FeSO4+ Cu 置换反应 E 氢 F【解析】【分析】【详解】(1)A为金属氧化物,那么B为酸,可以是硫酸,因为D可以和金属单质E反应生成紫红色的金属单质F,所以可以判断C为水,根据金属单质F的颜色可以判断F为铜,所以D 就是硫酸铜,故本题答案为:H2O。
(2)根据(1)的分析可知E可以把铜从它的盐溶液中置换出来,所以E是比铜活泼的金属,我们可以定为铁,故本题答案为:Fe+CuSO4=FeSO4+Cu。
(3)反应③是酸与铁等活泼金属的反应,故属于置换反应,故本题答案为:置换反应。
(4)F为铜,E的活动性比铜强,并且能够和酸反应,所以应该在氢前,故本题答案为:E 氢 F。
2.垃圾回收,分类的关键确定垃圾的成分,是对垃圾进行分类的前提。
某校化学实验室收集到一包固体废弃物,可能是由碳、镁、氧化镁、氧化铜中的一种或者几种组成,为了确定其成分,在老师的指导下,同学们取样进行了如下实验:(1)气体A是_____。
(2)由固体B得到气体C属于_____(填基本反应类型)。
(3)原样品中一定含有的物质是_____。
【答案】H2化合反应碳、镁、氧化铜【解析】【分析】镁和稀盐酸反应生成氯化镁和氢气,氧化铜和盐酸反应会生成氯化铜和水,氧化镁和盐酸反应生成氯化镁和水,碳不会与稀盐酸反应,氯化铜和镁反应会生成氯化镁和铜,气体C 能使澄清石灰水变浑浊,所以气体C是二氧化碳,铜和氧气加热会生成氧化铜,碳和氧气反应会生成二氧化碳,样品中加入过量的稀盐酸,生成气体A,所以A是氢气,气体C能使澄清石灰水变浑浊,所以C是二氧化碳,所以样品中一定含有镁、碳,由于固体A能与AgNO3溶液反应,可确定固体A中一定含有Cu。
专题二推断题1.(2016年徐州)A、B、C、D四种物质之间的一步转化关系如图所示(部分反应物、生成物及反应条件未标出),它们均含有同种金属元素。
A是大理石的主要成分,B是氧化物,C为碱,D由两种元素组成。
下列判断错误..的是( )。
A.A的化学式为CaCO3B.D物质不属于盐C.表中未涉及的基本反应类型是置换反应D.B→C的化学方程式为CaO+H2O===Ca(OH)22.(2016年兰州)A~K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转换关系如下图所示。
回答下列问题:(1)D、F 的化学式为 D__________、F__________。
(2)①的基本反应类型为____________。
(3)反应②的化学反应方程式为____________________________________。
(4)气体 E 的用途是________________(写一条)。
3.(2015年汕尾)A~E是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种。
A可用于金属表面除锈,B可用来改良酸性土壤。
它们相互间发生反应或转化的关系如图所示(“—”表面两种物质间能发生反应,“→”表示两种物质间的转化关系)。
(1)A、C的化学式分别为________、________;D在生活和生产中的一种用途是______________。
(2)E→D反应的化学方程式为:______________________________________;B与D反应的化学方程式为:____________________________________。
4.(2015年莱芜)归类、分类、比较、推理是学习化学常用的方法。
现有A~F六种物质,均是由H、C、N、O、Cl、Na、Ca中的两种或三种元素组成。
请回答下列问题:(1)上述七种元素中属于金属元素的是__________(填元素名称)。
2020中考化学试题分类汇编专题二 物质的鉴别、鉴定、推断知识要点:1. 物质的鉴别:鉴别是通过化学实验将几种不同特性的物质区别开来。
如鉴别两瓶无色溶液哪瓶是NaCl 或KNO 3。
我们只要把NaCl 溶液中的Cl -检验出来,即可认定NaCl 溶液,另一瓶则是KNO 3溶液。
(1)常见离子鉴别的特效试剂H +和-OH :紫色石蕊试液或pH 试纸。
OH -:无色酚酞试液(可鉴别碱性溶液)——变红。
Cl -:AgNO 3溶液和稀HNO 3——有白色沉淀。
SO 42-:BaCl 2溶液和稀HNO 3——有白色沉淀。
-23CO :稀HCl 和石灰水——有CO 2↑。
-34PO :AgNO 3溶液——有黄色沉淀。
NH 4+Mg 2+Fe 3+Cu 2+OH -Cl -Ag +Ba 2+H +CO 32-SO 42-Ca 2+Cu 2+Mg 2+③ 一种试剂的鉴别:A. 几种溶液含不同阳离子时,常选用2)(OH Ba 溶液或NaOH 溶液做鉴别试剂。
B. 几种溶液含不同阴离子时,常选用强酸做鉴别试剂。
C. 几种溶液酸碱性不同时,常选用紫色石蕊做鉴别试剂。
D. 几种物质是金属或金属氧化物时,常选用稀强酸做鉴别试剂。
E. 一种试剂与四种溶液反应时,应是现象对比度大。
多数是有沉淀、有气体,既有沉淀又有气体、沉淀颜色不同,无明显现象。
F. 当给定的一种试剂不能鉴别出被检物时,可从已鉴别出的物质中找出一种试剂再鉴别。
④ 不同试剂的鉴别:A. 观察法:根据物理性质中颜色、气味、状态、溶解性等进行鉴别。
B. 热分解法:根据不同物质的热稳定性,利用产物的不同性质特征进行鉴别。
C. 相互作用法:根据两两混合后的不同现象进行鉴别。
2. 物质的鉴定:鉴定是根据待检物质的特性,通过不同的实验将物质的各组分逐一检验出来,从而确定某物质。
鉴定与“用实验方法确定或证明”等用语意义相同。
如:用化学方法证明某白色固体是硫酸铵。
在鉴定时不但要用化学实验检验白色固体是否是铵盐(含NH 4+),还要检验它是否是硫酸盐(含-24SO )。
专题二推断题1.(2016年徐州)A、B、C、D四种物质之间的一步转化关系如图所示(部分反应物、生成物及反应条件未标出),它们均含有同种金属元素。
A是大理石的主要成分,B是氧化物,C为碱,D由两种元素组成。
下列判断错误..的是( )。
A.A的化学式为CaCO3B.D物质不属于盐C.表中未涉及的基本反应类型是置换反应D.B→C的化学方程式为CaO+H2O===Ca(OH)22.(2016年兰州)A~K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转换关系如下图所示。
回答下列问题:(1)D、F 的化学式为 D__________、F__________。
(2)①的基本反应类型为____________。
(3)反应②的化学反应方程式为____________________________________。
(4)气体 E 的用途是________________(写一条)。
3.(2015年汕尾)A~E是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种。
A可用于金属表面除锈,B可用来改良酸性土壤。
它们相互间发生反应或转化的关系如图所示(“—”表面两种物质间能发生反应,“→”表示两种物质间的转化关系)。
(1)A、C的化学式分别为________、________;D在生活和生产中的一种用途是______________。
(2)E→D反应的化学方程式为:______________________________________;B与D反应的化学方程式为:____________________________________。
4.(2015年莱芜)归类、分类、比较、推理是学习化学常用的方法。
现有A~F六种物质,均是由H、C、N、O、Cl、Na、Ca中的两种或三种元素组成。
请回答下列问题:(1)上述七种元素中属于金属元素的是__________(填元素名称)。
(2)A属于氧化物是导致酸雨的气体污染物之一,组成A的两种元素的质量比为7∶8,则A的化学式为________。
(3)B、C常温下均为液体,且组成元素相同,B在一定条件下可生成C,写出该反应的化学反应方程式__________________________________________。
(4)D用于玻璃、造纸和洗涤剂的生成,E、F均由两种元素组成,取D溶液进行实验,操作和现象如图:写出D与E反应的化学方程式________________________________,F的化学式为________。
5.(2014年南昌)小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质玩化学拼图游戏(如右图),游戏规则要求图中相邻物质之间能发生反应。
其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一。
(1)C物质是________,A物质的用途是__________________________。
(2)D与E反应的化学方程式为:________________________________,反应的基本类型是______________。
(3)按游戏规则,下列能替代B物质的是________(填序号)。
①银;②氯化铁;③氯化钡;④氧化铜。
6.(2014年河北)A、B、C、D、E是初中化学常见的物质,它们之间的转化关系如图甲所示,部分反应条件、反应物及生成物已略去。
图乙所示的是A、B、D、E的相关信息(重叠部分表示两种物质的共同点)。
请回答下列问题:甲乙(1)A的化学式为________。
(2)反应②的基本反应类型为____________。
(3)物质E的用途之一为____________。
(4)反应④的化学方程式为:______________________________。
7.(2015年佛山)A~N是初中学过的物质。
D是相对分子质量为40的氧化物,A是不溶于水和稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。
右图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(注:难溶性碱加热分解生成对应的氧化物)。
(1)写出化学式:A________,N________。
(2)写出E→B的化学方程式:________________________________。
(3)由F生成E需加入的物质是____________。
(4)C在空气中燃烧生成D的实验现象是________________________________________。
C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3),该氮化物的化学式是________。
8.(2014年揭阳)已知A~F都是初中化学中的常见物质,其中A和C是无色无味气体,B是黑色粉末,D是红色固体,它们的转化关系如下图所示(部分生成物已省略)。
(1)反应①的现象为:澄清石灰水变浑浊,则E的化学式为____________;写出其反应的化学方程式:______________________________。
(2)B的化学式为________,写出反应②的实验现象:_______________________________,反应②属于________反应(填写基本反应类型)。
9.有属于酸、碱、盐的5种常见物质A、B、C、D、E,它们之间可以发生如下反应:(1)A+B→C+H2O;(2)C+H2SO4→D↓+A;(3)E+AgNO3→AgCl↓+C。
根据上述反应,推断下列各物质的化学式:A________;B________;C________;D________;E________。
10.(2016年江西)赣南的客家围屋如同城堡,可以抵御外敌入侵。
现有五种物质盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠作为围屋的守护“卫士”,只有相邻物质间能发生反应才能组成守护的防线(如图所示)。
其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分。
(提示:碳酸钡不溶于水)(1)A物质是____________。
(2)B与C反应的化学方程式为____________________________,A与E反应时的实验现象为____________________________。
(3)现有下列物质作为“外敌”分别对围屋发起进攻,若该物质与两位相邻的守护“卫士”都能发生反应才能攻破防线,那么能攻入围屋的物质是________(填序号)。
①铁②氧化铁③二氧化碳④氢氧化钡11.(2014年天津)在下图有关物质转化关系中,各物质均是初中化学常见的物质,其中A为红色金属单质,B能参与植物的光合作用。
C、D为黑色粉末,F为可用于改良酸性土壤的碱,G为难溶性物质,H为难溶性蓝色物质(图中部分生成物已省略)。
(1)用化学式表示:D________, G________。
(2)写出E与F反应的化学方程式:____________________________________。
(3)光合作用生成的淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化,同时放出热量,写出葡萄糖发生缓慢氧化反应的化学方程式:______________________________。
12.(2014年重庆)某同学为了绘制“叶脉书签”,用A、B两种固体(一种是盐,另一种是碱)配制了浸泡树叶的混合溶液,A、B的溶液以及它们的混合溶液存在如下关系:(1)反应③中的白色沉淀是CaCO3,则反应①中可以观察到的实验现象是________________________。
(2)A的名称是____________;B的化学式可以是____________。
(3)反应②的化学方程式是:________________________________。
13.(2014年南京)如下图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物。
胃液中含有适量的甲,可帮助消化。
图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物略去。
(1)写出甲的化学式________。
(2)①若乙在常温下为液体,丙可用来改良酸性土壤,则乙的化学式为________,丙的化学式为________。
②若乙在常温下为气体,且可由甲与大理石反应得到,则乙的化学式为________,丙能与①中丙发生复分解反应,其化学方程式为:__________________________________________(写出一个即可)。
③写出①中的乙和②中的乙发生化合反应的化学方程式:______________________。
14.(2014年河南)A、B、C、D均含有同一种元素,它们的转化关系如下图(部分物质和反应条件已略去)。
(1)若A是紫红色金属,D为难溶性碱,则D的化学式为__________,由C转化为A的化学方程式为:________________________________________。
(2)若A属于氧化物,其相对分子质量为56,A与水化合得B,C是白色难溶固体,则B的一种用途是________________________________________,由D转化为C的化学方程式为:____________________________________________。
专题二 推断题【演练·专项提升】1.B 解析:A 、B 、C 、D 四种物质均含有同种金属元素,根据“A 是大理石的主要成分”,可推测A 为碳酸钙,故A 正确;根据“B 是氧化物,C 为碱,D 由两种元素组成”,结合图框,则推测B 是氧化钙,C 为氢氧化钙,D 为氯化钙,故B 错误;A→B 为碳酸钙高温分解生成氧化钙和二氧化碳,为分解反应;A→D 为碳酸钙与稀盐酸反应,为复分解反应;B→D 为氧化钙与稀盐酸反应,为复分解反应;B→C 为氧化钙与水反应,为化合反应;C→D 为氢氧化钙与稀盐酸反应,为复分解反应;C→A 为二氧化碳与氢氧化钙反应,不是基本反应,则表中未涉及的基本反应类型是置换反应,故C 正确;B→C 的化学方程式为CaO +H 2O===Ca(OH)2,故D 正确。
2.(1)Cu(OH)2 CO 2 (2)复分解反应(3)Cu +2AgNO 3===2Ag +Cu(NO 3)2(4)燃料(或冶炼金属等)3.(1)HCl NaOH 作气体肥料(2)Na 2CO 3+2HCl===2NaCl +H 2O +CO 2↑Ca(OH)2+CO 2===CaCO 3↓+H 2O4.(1)钠、钙 (2)NO (3)2H 2O 2=====MnO 22H 2O +O 2↑(4)Na 2CO 3+CaCl 2===CaCO 3↓+2NaCl HCl解析:(2)形成酸雨的气体是氮的氧化物和二氧化硫,这里没有硫元素,所以A 只能是氮的氧化物,A分子中氮、氧原子的个数比=714∶816=1∶1,所以A 的化学式是NO ;(3)B 、C 常温下均为液体,且组成元素相同,B 在一定条件下可生成C ,所以B 是过氧化氢,C 是水;(4)D 用于玻璃、造纸和洗涤剂的生成,D 溶液滴入酚酞显色,所以D 是碳酸钠,E 、F 均由两种元素组成,滴入E 溶液,红色褪去生成白色沉淀,所以E 是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,所以F 是盐酸。