氯化氢合成装置工艺PPT课件
- 格式:ppt
- 大小:10.95 MB
- 文档页数:20









氯化氢合成生产工艺有效讲课教材一、概述工序生产任务(1).供给合格的氯化氢给单体工段;为本厂及用户提供优质的高纯盐酸。
(2).平稳氯气,保证全厂正常生产。
本工序原料及其特性一、氢的化学性质氢气易燃,在空气中燃烧,生成水。
2H2+O2=2H2O氢气在氯气中含4~96%,或在氧气中含5~95%,或在空气中含5~7%时,都可组成爆炸气体,遇明火或强光即发生爆炸。
原料氯气的性质二、氯气的物理性质a) 分子式:Cl2b) 分子量:c) 常温时是黄绿色、有刺激性气味。
d) 剧毒,国家规定空气中许诺的浓度为Le) 易液化,能溶于水,溶解度随温度的升高而降低。
f) Cl2在一个大气压下100克水中溶解氯气克数g) 氯气易溶于许多有机溶剂,如酒精、庚烷、四氯化碳等。
h) 氯气的一些物理数据氯的化学性质a) 氯气的化学性质很活泼,有很强的氧化性。
b) 氯气能够与所有金属和大多数非金属元素(N、O、C和稀有气体除外)直接化合。
2Ag+Cl2=2AgCl c) 氯气可与一些气体反映:点燃Cl2+H2= 2HCl+Qd) 氯气与些有机化合物反映:紫外线C6H6+3Cl2—→C6H6Cl6e )氯气与无机化合物反映:2NaOH+Cl2=NaClO+NaCl+H2Of) 氯气易溶于水中,并生成次氯酸和盐Cl2+H2O→HClO+HClHClO→HCl+[O]所释放的初生态氧是强氧化剂,对金属的侵蚀性极大。
g)氯气能与氢按必然比例混合成炸性气体,在明火、高温及日光的触发下,猛烈爆炸。
氯气与氢气混合爆炸极限:下限H2为5%,Cl2为95%,上限H2为%,Cl2为%。
高纯盐酸的质量指标标准(HG/2778-1996)氯化氢性质氯化氢(HCl)在常温下为无色、有刺激性嗅味的气体,熔点℃,沸点℃,比重。
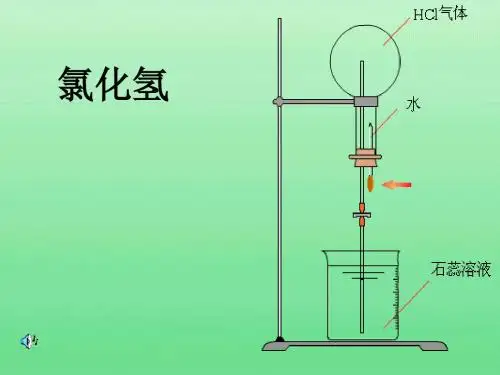
极易溶于水,并强烈地放热,其水溶液确实是盐酸,是经常使用的无机强酸之一。
纯的盐酸是无色液体,工业盐酸由于有铁、氯或有机杂质存在而呈黄色。
