第四章 红外光谱法
- 格式:ppt
- 大小:3.04 MB
- 文档页数:103




第四章炔烃二烯烃红外光谱(一)炔烃▪分子中具有一个碳碳叁键的开链不饱和烃——炔烃。
▪通式为CnH2n-2,碳碳叁键是炔烃的官能基。
4.1 炔烃的构造异构和命名1.炔烃的构造异构▪从丁炔开始,除碳链异构外,碳碳叁键位置的不同(位置异构)也可引起同分异构现象。
1-丁炔2-丁炔2. 炔烃的命名炔烃的系统命名法规则1)选含有碳碳叁键的最长碳链为主链。
2)从靠近叁键的一端开始编号,使叁键的位次尽可能小。
命名时要标出叁键的位置。
3) 其余取代基按烷烃的系统命名规则来命名。
4) 含有双键的炔烃命名时,一般先命名烯再命名炔,碳链编号以表示双键与叁键位置的两个数字之和取最小的原则。
1-戊炔2-戊炔3-甲基-1-丁炔4.2 炔烃的结构▪X光衍射和电子衍射等物理方法证明,乙炔分子是一个线性分子,所有碳原子和氢原子都分布在同一条直线上。
•sp杂化:由一个s轨道和一个p轨道参加的杂化,其结果形成了处于同一直线上的两个sp杂化轨道。
0.120 nm180 o C0.106 nmH乙炔分子中σ键的形成▪乙炔分子中,每个碳原子与另外两个原子形成了一个C sp-H s σ键和一个C sp-C sp σ键,在同一直线上,方向相反,故乙炔分子为线性分子。
乙炔分子中的π键▪每个碳原子上还各有两个未参加杂化的p轨道,互相平行,故这两个p轨道可侧面相互交盖而形成了两个π键,这两个π键并不是孤立分离的,其电子云对称分布在碳碳σ键键轴周围,类似圆筒性状。
参见图4-3。
▪碳碳叁键由一个σ键和两个π键组成。
乙炔键长缩短的原因1)s轨道的电子较p电子接近原子核,故杂化轨道的s成分越多,则在杂化轨道上的电子越接近原子核。
乙炔分子中的C sp-H s σ键,因sp杂化轨道的s成分大(50%),其电子云更靠近原子核。
2)乙炔分子中有两个形成π键,且sp杂化轨道参与了碳碳σ键的组成。
4.3 炔烃的物理性质∙炔烃的物理性质和烷烃、烯烃基本相似。
∙低级的炔烃常温常压下为气体,但沸点比相同碳原子数的烯烃略高。




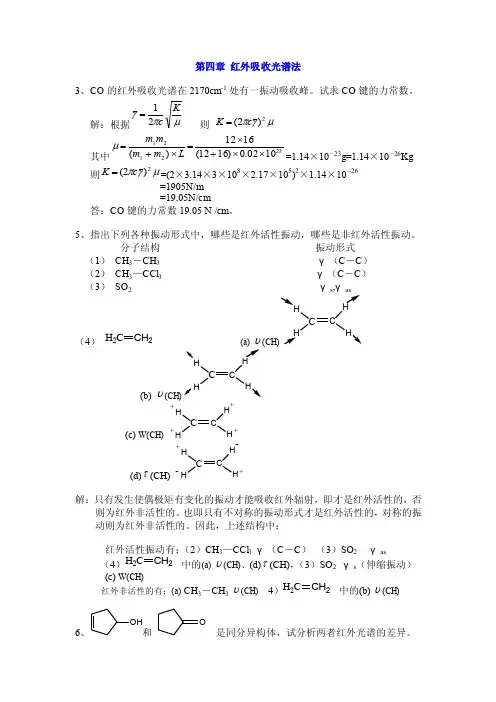
第四章 红外吸收光谱法3、CO 的红外吸收光谱在2170cm -1处有一振动吸收峰。
试求CO 键的力常数。
解:根据μπγKc 21= 则 μγπ2)2(c K = 其中2321211002.0)1612(1612)(⨯⨯+⨯=⨯+=L m m m m μ=1.14×10-23g=1.14×10-26Kg 则μγπ2)2(c K ==(2×3.14×3×108×2.17×105)2×1.14×10-26 =1905N/m=19.05N/cm答:CO 键的力常数19.05 N /cm 。
5、指出下列各种振动形式中,哪些是红外活性振动,哪些是非红外活性振动。
分子结构 振动形式(1) CH 3-CH 3 γ(C -C )(2) CH 3—CCl 3 γ(C -C )(3) SO 2 γs ,γ(4)H 2C CH 2 (a) υ(CH)CC(b) υ(CH)CH C (c) W(CH) C HHC H H ++++(d)τ(CH) C H H C H -++-解:只有发生使偶极矩有变化的振动才能吸收红外辐射,即才是红外活性的,否则为红外非活性的。
也即只有不对称的振动形式才是红外活性的,对称的振动则为红外非活性的。
因此,上述结构中:红外活性振动有:(2)CH 3—CCl 3 γ(C -C ) (3)SO 2 γas(4)H 2C CH 2 中的(a) υ(CH)、(d)τ(CH),(3)SO 2 γs (伸缩振动) (c) W(CH)红外非活性的有:(a) CH 3-CH 3 υ(CH) 4)H 2C CH 2 中的(b) υ(CH)6、OH 和 O是同分异构体,试分析两者红外光谱的差异。
答:由于OH中含有一个-OH 基团,因此在红外光谱中有一强吸收峰在3700~3100cm -1,且此分子中含有一个C=C 双键,因此在1680~1620cm -1也有一较弱的吸收峰。


第四章红外光谱分析法§4—1红外光谱简介红外辐射泛指位于可见光和微波段之间的那一部分电磁波谱.对有机化学家最有实际用处的是只限于4000—666厘米-1(2.5-15.0微米)之间的范围.最近,对近红外区14290—4000(0.7一2.5微米)和远红外区700—200厘米-1(14.3—50微米)的兴趣正在增加.在红外光谱分析中,一个十分简单的分子也可以给出一个非常复杂的红外光谱图.有机化学家就是利用这种光谱图的复杂性,将一个未知化合物的光谱图与一个可靠的标准品的光谱图相互比较,两张光谱图中峰对峰的完全一致对于鉴定就是最好的证据.除了光学对映体外的任何两个化合物均不可能给出相同的红外光谱图.虽然,红外光谱图是整个分子的特性,但是不管分子其余部分的结构如何,结果是某一特定的原子基团总是在相同的或者几乎是相同的频率处产生吸收谱带.正是这种特征谱带的不变性使化学家可以,通过简单的观察并参考有关特征基团频率的综合图嵌来获得有用的结构信息.我们将主要依靠这些特征基团频率.由于我们并不单纯依靠红外光谱图进行鉴定,因此,并不需要对红外光谱图进行详细的分析.根据我们的总的计划,在这里将提出为达到下列目的,所必需的理论:即把红外光谱图与其它的光谱数据一起用来确定分子结构.因为大多数大学的和工业的实验室都把红外分光光度计作为有机化学家的一种常备的基本工具,在这一章中将比其它各章较详细地叙述仪器和样品制备.红外光谱法作为实用有机化学家的一种工具,从已经出版书籍的数目可以明显地看到.在这些书中,有的是全部地、有的是部分地讨论了红外光谱法的应用。
.一、红外光的表征近红外(泛频区)0.75-2.5微米;13334-4000波数中红外(基频区) 2.5 -25 微米4000-400 波数远红外(转动区)25-1000微米400-10 波数由于中红外区能最深刻地反映分子内部所进行的各种物理过程以及分子结构方面的各种特性,对于解决分子结构和化学组成各种问题最为有效。
作业题第四章红外分光光度法第一节概述填空题1、红外光区位于 ______ 光区和________ 光区之间, 波长范围为_______________ ,习惯上又可将其细分为__________ 、 _________ 和 __________ 三个光区,应用较多的是________ 光区。
2、红外谱图纵坐标一般为,横坐标一般为。
简答题:红外分光光度法的特点。
H H H Clci" 'ci D. Cl" X H4、在有机化合物的红外吸收光谱中,出现在4000 1250cm—1频率范围的可用于鉴定官能团,这一段频率范围称为()A.指纹区B.倍频区C.特征区D.合频区5、第二节基本原理1、分子内部的运动方式有三种,即:_____ 、_____ 和 _____,相应于这三种不同的运动形式,分子具有______ 能级、______ 能级和____ 能级。
2、一般多原子分子的振动类型分为 _________ 振动和________ 振动。
3、乙烷的振动自由度是 ____________ 。
4、甲酸的振动自由度是 ____________ 。
判断题:1、对称结构分子,如H2O分子,没有红外活性。
()2、水分子的H— O— H对称伸缩振动不产生吸收峰。
()以上①、②、③、④四种烯的u c=c值为:A. ①为1650cm1;②为1678cm1;③为1657cm1:④ 为1781cm1B. ①为1781cm1;②为1657cm1;③为1650cm1:④ 为1678cm-1C. ①为1650cm1;②为1657cm1;③为1678cm1:④ 为1781cm1D. ①为1781cm1;②为1678cm1;③为1657cm1:④ 为1650cm-16、乙烯分子的振动自由度为:A.20B.13C.12D.6E.157、下列环烯化合物中,u C=c出现最低波数者为:A. B. C.D. E.选择题:1、试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰,频率最小的是()A C-HB N-HC O-HD F-H2、已知下列单键伸缩振动中C-C C-N C-O 键力常数k/(N ?cm1) 4.5 5.8 5.0 以用W-入/ 卩m 66.46 6.85 问C-C, C-N, C-O 键振动能级之差/ E顺序为()A C-C > C-N > C-OB C-N > C-O > C-CC C-C > C-O > C-ND C-O > C-N > C-C3、判断下列各分子的碳碳对称伸缩振动在红外光谱中哪个是非活性的()A. CH3—CH3B. CH3- CCI3C.8、下列合物中u c=c吸收强度最大的化合物为:A.R —CH= CHB.R —CH= CH- R(顺)C.R—CH= CH- R (反)D.R 1—CH= CH— R(顺)ER —CH= CH- COR (反)9、孤立甲基的弯曲振动一般为1380cm1,异丙基中的甲基裂分为1385cm1和1375cm1,叔丁基中的甲基裂分为1395cm1和1370cm1,造成裂分的原因是:A.分子的对称性B. 振动偶合C.费米共振 D. 诱导效应U C=O出现在1870cm1至1540cm之间,它们的u c=。