DNA扩增试剂盒 恒温扩增法
- 格式:docx
- 大小:92.81 KB
- 文档页数:4


恒温扩增技术综述(总6页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--摘要:恒温扩增技术是继PCR技术后发展起来的一门新型的体外核酸扩增技术。
目前主要的恒温扩增技术有:滚环核酸扩增、环介导等温扩增、链替代扩增、依赖核酸序列扩增和解链酶扩增。
它们都具有共同的特点:恒温、高效、特异、不需要特殊的仪器设备。
本文就现阶段恒温扩增技术的特点及其在动物疫病检测中的应用情况和前景做一综述。
关键词:恒温扩增;PCR引言:近年来,随着分子生物学技术的迅速发展,基于核酸检测的诊断方法已大量建立并广泛应用于动物疾病的实验室检测中,恒温扩增技术就是在此背景下出现的。
与其它的核酸扩增技术相比,恒温扩增有快速、高效、特异的优点且无需专用设备。
所以它一经出现就被许多学者认为是一种有可能与PCR 媲美的检测方法,目前主要的恒温扩增技术有:滚环核酸扩增(rolling circle amolification,RCA)、环介导等温扩增(loop-mediated isothermal amplification,LAMP)、链替代扩增(strand displacement amplification,SDA)、依赖核酸序列扩增(nucleicacid sequence based amplification,NASBA)和解链酶扩增(helix dependent amplification,HAD),这些技术各有特点,这也决定了它们在动物疾病检测中的应用情况,下面就它们的原理、特点及其在动物疫病检测中的应用情况进行综述。
1滚环核酸扩增1. 1 滚环核酸扩增的原理滚环核酸扩增(rolling circleamolification, RCA)是通过借鉴病原生物体滚环复制DNA 的方式而提出的[1],可分为线性扩增与指数扩增两种形式。
线性RCA 是引物结合到环状DNA 上后,在DNA 聚合酶作用下被延伸,产物是具有大量重复序列(与环状DNA 完全互补)的线状单链。
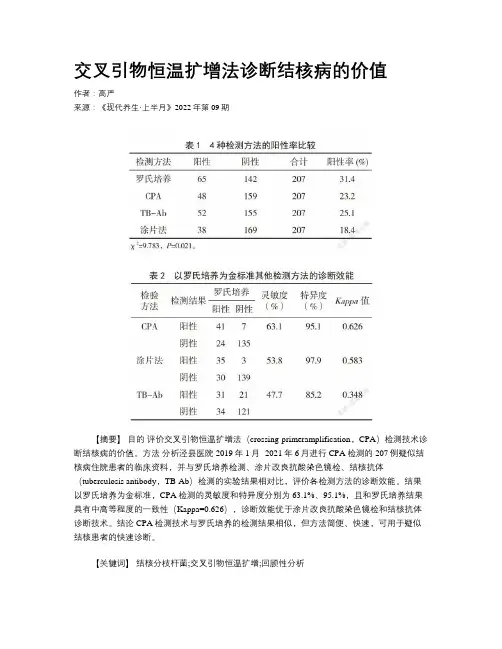
交叉引物恒温扩增法诊断结核病的价值作者:高严来源:《现代养生·上半月》2022年第09期【摘要】目的评价交叉引物恒温扩增法(crossing-primeramplification,CPA)检测技术诊断结核病的价值。
方法分析泾县医院2019年1月- 2021年6月进行CPA检测的207例疑似结核病住院患者的临床资料,并与罗氏培养检测、涂片改良抗酸染色镜检、结核抗体(tuberculosis antibody,TB-Ab)检测的实验结果相对比,评价各检测方法的诊断效能。
结果以罗氏培养为金标准,CPA检测的灵敏度和特异度分别为63.1%、95.1%,且和罗氏培养结果具有中高等程度的一致性(Kappa=0.626),诊断效能优于涂片改良抗酸染色镜检和结核抗体诊断技术。
结论 CPA检测技术与罗氏培养的检测结果相似,但方法简便、快速,可用于疑似结核患者的快速诊断。
【关键词】结核分枝杆菌;交叉引物恒温扩增;回顾性分析中图分类号 R521 文献标识码 A 文章编号 1671-0223(2022)17--02结核病是一种慢性传染病,由结核分枝杆菌(mycobacterium tuberculosis,MTB)引起。
2020年我國估计的结核病新患病人数为84.2万,估算的结核病发病率为59/10万,在结核病高负担国家中结核病新患病人数仅低于印度[1],结核病的防治依然严峻。
为了能有效防治结核病,需要在疾病早期能够有一种检测技术可以快速地检测并诊断出MTB。
传统的检测方法是从临床标本中(主要是痰液)经过抗酸染色或者培养来鉴定MTB,但它们各自都有优缺点。
随着检测技术不断发展,MTB的分子学检测技术得到广泛的应用。
交叉引物恒温扩增法(crossing-primeramplification,CPA)检测技术是其中一种快速分子诊断方法,它检测的是结核杆菌复合群特异性的IS16110序列。
在恒温条件下,可以一次性进行基因片段的特异性扩增和杂交,然后在密闭的一次性核酸检测装置中使用免疫层析技术,定性检测特异性扩增产物,是中国自主创新的技术[2]。

技术丨搞定恒温扩增分子诊断(RPARAA)展开全文2020-9-14|编辑: 归去来兮|查看: 114|评论: 0|来源: IVD学习笔记 | 作者:iAnny摘要: 分子诊断技术今日不同以往,着实借力突飞猛进,恒温扩增技术由于其扩增期间不需要特殊的仪器设备而更受瞩目。
恒温扩增方法有多种,今天就回顾RPA/RAA,让大家一文通俗搞定~~嗯啊, 如果有疑问,决定开小灶,包会!哈 ...分子诊断技术今日不同以往,着实借力突飞猛进,恒温扩增技术由于其扩增期间不需要特殊的仪器设备而更受瞩目。
恒温扩增方法有多种,今天就回顾RPA/RAA,让大家一文通俗搞定~~嗯啊, 如果有疑问,决定开小灶,包会!哈哈~~为了确保大家所认知的基本概念是一致的,请先了解以下名词解释•重组酶聚合酶扩增技术,RPA, recombinase polymerase amplification•重组酶介导的扩增技术,RAA, recombinase-aidamplification •重组酶,recombinase,同引物形成蛋白-核酸复合物,指导引物与模板结合,起到定位作用;帮助DNA 模板的解链和促使模板与引物之间发生链替换。
•单链DNA结合蛋白,SSB, single stranded DNA binding。
同置换出来的单链DNA结合,防止DAN配对两条链再次结合。
•DNA聚合酶,DNA polymerase,以DNA为模板,利用dNTP 合成子代DNA。
•核酸内切酶,endonuclease,可水解分子链内部磷酸二酯键生成寡核苷酸。
•Nfo,来源于细菌的核酸内切酶,且更倾向于作用于3′凹末端的双链DNA,参与DNA损伤修复。
RPA和RAA的工作原理相同点:•3种关键酶或蛋白:重组酶、单链结合蛋白和DNA聚合酶;•在37℃恒温下进行核酸快速扩增;唯一不同点:酶的来源不同,推测主要时因为专利限制问题。
•RPA的重组酶来源于T4噬菌体;•RAA的重组酶来源于细菌或者真菌。

PCR 基因扩增实验原理﹑仪器试剂和操作步骤实验原理:PCR(Polymerase Chain Reaction)-聚合酶链式反应,可以选择性扩增一段DNA序列。
其基本步骤是,首先将待扩增的模板DNA变性使之成为单链,DNA样品中,特异性的引物能够与其互补的序列杂交,在dNTPs和Taq酶存在时,就可以合成模板DNA的互补链,反应完成后,将反应混合物加热使DNA双链变性,温度下降后,过量的引物又可以开始第二轮的合成反应。
这种延伸—变性—退火—延伸的循环可以重复多次,使所需要的DNA片段得到特异性的扩增。
1.变性:加热使模板DNA在高温下(94℃)变性,双链间的氢键断裂而形成两条单链。
2.退火:使溶液温度降至50~60℃,模板DNA与引物按碱基配对原则互补结合.3.延伸:溶液反应温度升至72℃,耐热DNA 聚合酶以单链DNA为模板,在引物的引导下,利用反应混合物中的4种脱氧核苷三磷酸(dNTPs),按5ˊ→3ˊ方向复制出互补DNA上述3 步为一个循环,即高温变性、低温退火、中温延伸3个阶段。
从理论上讲,每经过一个循环,样本中的DNA量应该增加一倍,新形成的链又可成为新一轮循环的模板,经过25~30个循环后DNA可扩增106~109倍。
典型的PCR反应体系由如下组分组成:DNA模板、反应缓冲液、dNTP、MgCl2、两个合成的DNA引物、耐热Taq聚合酶。
影响PCR的主要因素PCR技术必须有人工合成的合理引物和提取的样品DNA,然后才进行自动热循环,最后进行产物鉴定与分析。
引物设计与合成目前只能在少数技术力量较强的研究院、所进行,临床应用只需购买PCR检测试剂盒就可开展工作,PCR自动热循环中影响因素很多,对不同的DNA样品,PCR反应中各种成份加入量和温度循环参数均不一致。
现将几种主要影响因素介绍如下。
一、温度循环参数在PCR自动热循环中,最关键的因素是变性与退火的温度。
如操作范例所示,其变性、退火、延伸的条件是:94℃60s, 37℃60s, 72℃120s,共25~30个循环,扩增片段500bp。

交叉引物恒温扩增技术在结核分枝杆菌检测中的应用毛秀军;李世明;葛晓励;张国强;孙绍秋;王惠良【摘要】目的:探讨交叉引物扩增技术(CPA)快速检测系统在结核病诊断中的价值。
方法收集唐山市第四医院2015年3~5月206例结核病就诊患者的痰液标本,其中肺结核患者95例(其中痰涂片阳性26例,阴性69例),非结核患者111例,分别采用RT‐PCR法实时荧光定量聚合酶链反应法(RT‐PCR)检测标本中的结核分枝杆菌,对结果进行统计分析。
结果涂片法、罗氏培养法、EasyNAT ® TB‐CPA 法检测初诊疑似肺结核患者痰液的灵敏度分别为:27.37%(26/95)、50.53%(48/95)、56.84%(54/95)、51.58%(49/95)。
以罗氏培养结果为诊断金标准,EasyNAT ® TB‐CPA 法灵敏度为89.58%(43/48),特异度94.94%(150/158);RT‐PCR法的灵敏度为83.33%(40/48),特异度94.30%(149/158);EasyNAT ® TB‐CPA与RT‐PCR法相比,总体一致性为98.54%(203/206), Kappa指数值为0.92。
结论TB‐CPA法在检测痰液标本中具有较高的临床应用价值,且方法简便、快速。
【期刊名称】《检验医学与临床》【年(卷),期】2016(013)008【总页数】3页(P1107-1109)【关键词】结核分枝杆菌;恒温扩增;培养法;交叉引物扩增技术【作者】毛秀军;李世明;葛晓励;张国强;孙绍秋;王惠良【作者单位】河北省唐山市第四医院 063001;河北省唐山市第四医院 063001;华北理工大学附属医院,河北唐山 063009;河北省唐山市中心血站 063000;河北省唐山市中心血站 063000;河北省唐山市滦南县医院 063500【正文语种】中文结核病是由结核分枝杆菌感染引起的慢性传染病,是全球最具威胁的传染病之一。

.158-微F物与感染Journal of Microbes and Infctons#June25,2020,15(3):158-165http:/i .cddoi:10.3969/j.issn.1673-6184.2020.03.004•论著・实时荧光核酸恒温扩增试验和定量反转录-聚合酶链反应对血清乙型肝炎病毒RNA定量检测的一致性评价黄晨璐1,许伟1,胡乾坤1,张小楠1,李强1,黄玉仙12,陈良11.复旦大学附属公共卫生临床中心,上海201508;2.复旦大学附属华山医院感染科,上海200040摘要:为评价实时荧光核酸恒温扩增试验(simultaneous amplification testing,SAT)与定量反转录-聚合酶链反应(quantitative reverse transcription-polymerase chain reaction,qRT-PCR)检测血清样本中乙型肝炎病毒(hepatitis B virus,HBV)RNA的相关性与一致性,本研究收集了在复旦大学附属公共卫生临床中心就诊的212例患者的血清样本,其中慢性乙型肝炎(chronic hepatitis B,CHB)患者HBV DNA(100IU/mL81例、HBV DNA V100IU/mL76例,以及作为对照的非HBV感染患者55例。
采用SAT和qRT-PCR方法分别检测所有血清样本中的HBV RNA,对检测结果进行统计学分析。
在HBV DNA(100IU/mL的CHB患者中,SAT和qRT-PCR的HBV RNA阳性检出率均为95.06%(77/81)*2种方法具有较好的相关性与一致性(R2=0.803和CCC=0.882)。
Bland Altman分析显示绝对偏倚为0.1log copies/mL,相对偏倚为0.97%。
配对t检验显示,结果无统计学差异(t=1.617,P=0.110)。
在HBV DNA V100IU/mL的CHB患者血清样本中,HBV RNA阳性检出率不同,SAT为98.68%(75/76),qRT-PCR为8&16%(67/76),2种方法相关性与一致性较差(R2=0.326和CCC=0.438)。

新冠病毒有几种检测方法新型冠状病毒肺炎(Corona Virus Disease 2019,COVID-19),世界卫生组织命名为“2019冠状病毒病”,简称新冠病毒,其有一定的潜伏期,通常在1-14天左右,大多3-7天出现发热、咳嗽、乏力等明显症状。
还有一些病人伴有腹泻、鼻塞与咽喉痛,如果病人症状严重,患病一周后产生低氧血症,呼吸困难等,极有可能引起急性呼吸窘迫症,那么新冠病毒有哪些检测方法?一、核酸检测核酸检测是新冠病毒检测的金标准,其显著特点是早期诊断准确率、灵敏度和特异性均较高,可证明患者体内是否存在新冠病毒感染。
疫情发生早期,主要采用核酸检测,为疑似患者进行检查诊断,若得到阳性结果,便确诊为新冠病毒感染。
核酸检测是利用一段包含新冠病毒信息的探针对患者样本中的核酸进行搜寻,一旦搜寻到,检测系统就会出现阳性结果以提示检验医生,说明可能存在新冠病毒感染;如果搜寻没有任何异常,说明可能无新冠病毒感染,检测系统也会呈现阴性结果。
核酸检测时结果不是百分百准确,要想提高结果的准确性,多数情况是采取两个探针进行搜寻。
核酸检测的过程包括采样、灭活、核酸提取、上机检测,自采样到出报告约6个多小时。
现今,新冠病毒的核酸检测方法包括PCR法、恒温扩增法、测序法和CRISPR检测法等,主要如下:1)PCR法。
具体指聚合酶链式反应,是扩增待测样本核酸的一种方法。
第二代PCR技术还称为荧光PCR法,主要是将荧光物质加入反应体系,利用专业设备进行荧光检测,通过定量方法计算模板。
这是普遍使用的核酸检测方法,一般在2-3小时后获得检测结果。
2)恒温扩增法。
该方法不需要改变样本温度,具体包括2类技术,一类省略了PCR高温解链环节,能合理应用特殊酶,如在LAMP技术中链置换DNA聚合酶与RPA重组酶、单链结合蛋白与链置换酶;另一类在DNA和RNA间进行转换以实现扩增,如NASBA和TMA均应用逆转录酶与RNA聚合酶。
恒温装置用在基层医疗机构进行扩增与层析检测,不会被场景环境限制。

性病衣原体恒温扩增核酸试纸条检测试剂盒说明书【产品名称】性病衣原体恒温扩增核酸试纸条检测试剂盒【英文名称】Chlamydia Trachomatis(CT)Isothermal Amplification Diagnostic Kit【包装规格】单管单人份,20人份/盒。
【预期用途】用于性病衣原体的快速筛查和检测。
仅供科研使用。
【检验原理】本试剂盒将病原体DNA 扩增、核酸杂交和核酸试纸条检测三种技术有机地融为一体,在恒温扩增反应液中加入两对性病衣原体(CT)特异性引物和一对特异性探针,一次性完成HP DNA 扩增及杂交过程,然后用一次性核酸检测装置(3号)对性病衣原体进行定性检测。
由于待测样本的扩增(PCR 管盖和石蜡油双重保护)和检测过程均在物理封闭条件下完成,所以本试剂盒具有防止实验室扩增物交叉污染,防止假阳性的效果。
【试剂盒组成】1 试剂盒A*装有恒温扩增反应液的反应管中包括除样本外的所有试剂。
上覆矿物油,以防止扩增中产生气溶胶,防止假阳性。
2 试剂盒B【储运条件及有效期】1.运输条件:试剂盒A 需要-20℃冷冻运输,运输过程中,试剂盒A 在-20℃-0℃内保存时间不超过五天;试剂盒B 可以常温运输。
2.储存条件:试剂盒A 在-20℃保存;试剂盒B 在2℃-30℃干燥保存。
3.有效期:有效期12个月【仪器及物品要求】1.恒温装置如:水浴锅、金属浴、各种型号PCR 仪等。
2.实验需要但未提供的材料:生理盐水【样本采集】CT 样本采集通常使用无菌棉拭子,且遵循一般病原体采集程序。
采集后的样本可立即用于测试,也可保存于-20℃或-80℃待测。
保存最好不超过6个月。
样本长途运送时应采用0℃冰壶。
【操作步骤】1. 样本处理及DNA 提取1.1取1ml 生理盐水加入样本试管中,充分振荡混匀,将液体转移至1.5ml 离心管中(若分泌物较多,则只取0.5ml),12,000rpm 离心5分钟,弃上清。
1.2向上述沉淀中加入40ul DNA 提取液,振荡混匀,(提取液内含不溶于水的物质,取样时需用加样器充分混匀后吸取。
![跨越式滚环核酸等温扩增目的DNA的引物对、试剂盒及其扩增方法[发明专利]](https://uimg.taocdn.com/012c5d3e6d85ec3a87c24028915f804d2b168700.webp)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201710250302.8(22)申请日 2017.04.17(71)申请人 河北农业大学地址 071000 河北省保定市灵雨寺街289号(72)发明人 张伟 马晓燕 檀建新 张先舟 杨倩 袁耀武 李英军 王志岩 张蕴哲 (74)专利代理机构 石家庄科诚专利事务所13113代理人 张红卫 贾彦虹(51)Int.Cl.C12Q 1/68(2006.01)C12N 15/11(2006.01)(54)发明名称跨越式滚环核酸等温扩增目的DNA的引物对、试剂盒及其扩增方法(57)摘要本发明公开了一种跨越式滚环核酸等温扩增目的DNA的引物对及含有该引物对的试剂盒,该引物对设计合理,特异性强,应用于跨越式滚环核酸等温扩增时,能实现引物自身不扩增而目的基因扩增的效果;本发明还提供了跨越式滚环核酸等温扩增目的DNA的扩增方法,它包括提取模板、扩增、检测步骤,在扩增过程中实现目的DNA扩增而引物自身不扩增的结果,该方法简单,过程易于控制,步骤简单,耗时短,成本低。
本发明适用于对目的DNA进行扩增。
权利要求书1页 说明书5页 附图1页CN 106868192 A 2017.06.20C N 106868192A1.一种跨越式滚环核酸等温扩增目的DNA的引物对,包括上游引物和下游引物,其特征在于:所述上游引物和下游引物之间的连续互补碱基小于或等于4对,所述上游引物和下游引物3’端和5’端的4个碱基中任意两个碱基不互补,所述上游引物和下游引物,至少有一条引物不具有二级结构,引物的GC含量为45-55%,Tm值为55-58℃。
2.一种跨越式滚环核酸等温扩增目的DNA的试剂盒,其特征在于:含有权利要求1所述引物对的试剂盒。
3.一种跨越式滚环核酸等温扩增目的DNA的扩增方法,其特征在于它按照如下的步骤顺序依次进行:(1)从样品中提取DNA为模板;(2)利用权利要求1的引物对或者权利要求2的试剂盒中引物对作为扩增的引物,进行SRCA扩增,得到扩增产物;(3)检测扩增产物,做出判断。

人线粒体DNA(mtDNA)核酸检测试剂盒说明书【名称】通用名:人线粒体DNA(mtDNA)核酸扩增检测试剂盒英文名:Human Mitochontriol DNA Fluorescence quantitative Polymerase Chain Reaction(PCR)Diagnostic kit汉语拼音:ren xian li ti DNA he suan kuo zeng jian ce shi ji he【目的】本试剂盒适用于检测人外周血、精液或组织等样本中线粒体DNA,用于生殖、胃肠功能紊乱以及遗传性相关疾病如男性不孕等疾病的辅助诊断以及药物疗效观察。
其检测结果仅供临床参考。
【原理】本试剂盒选取一对线粒体DNA(mtDNA)特异性引物和一条特异性荧光探针,应用碱裂解法提取DNA,后者在耐热DNA聚合酶(Taq酶)作用下,配以FQ-Buffer(内含Mg2+、Tris-HCl等)、四种核苷酸单体(dNTPs)等成分,通过PCR-荧光探针法提取扩增法对线进行扩增,从而达到快速实时定量检测线粒体DNA(mtDNA)之目的。
【组成】名称数量规格核酸提取液B4管500μl/管Taq酶系1管80μl/管mtDNA–PCR MIX1管960μl/管mtDNA阳性质控品1管50μl/管(1×107Copies/ml)阴性质控品1管500μl/管备注:红细胞裂解液(10×RCLB)等另行配备。
【标本采集、保存和运输】1.全血:用无菌注射器抽取受检者静脉血1毫升,注入无菌2ml EDTA2Na(或柠檬酸钠)抗凝管,立即混匀。
2.精液:无菌条件下取精液1-3ml,转至5ml洁净的离心管中,密闭送检。
3.组织:无菌条件下取待检组织0.1-0.5g,转至1.5ml洁净的离心管中,密闭送检。
3.保存和运输:标本可立即用于测试,2-8℃保存下不应超过24小时;-70℃以下长期保存。
避免反复冻融。
恒温扩增-层析法
恒温扩增-层析法(Loop-mediated isothermal amplification-lateral flow dipstick)是一种用于快速检测DNA的方法,该方法结合了恒温扩增(LAMP)和层析技术。
LAMP是一种在恒温条件下进行的DNA扩增技术,与PCR相比,LAMP不需要高昂的设备和复杂的步骤,并且具有高度特异性和敏感性。
层析技术则将扩增产物分离并清除杂质,在快速检测中具有重要作用。
恒温扩增-层析法将LAMP扩增产物与具有适当检测信号的金纳米颗粒结合,通过浸泡在试剂条内,可在几分钟内实现目标DNA的快速检测。
该方法已广泛应用于农业、环境卫生、临床医学等领域。
实时荧光恒温扩增技术实验流程实时荧光恒温扩增技术是一种常见的分子生物学实验技术,常用
于检测DNA序列的扩增、定量和分析。
其实验流程大致如下:
1. 样品制备:将待分析的DNA样品获取并纯化,通常采用常规的
提取方法,如血液、组织、细胞等。
2. 扩增反应体系:制备PCR反应混合液,包括DNA模板、引物
(一对)和扩增酶等,其中引物的设计及选择需根据具体实验需要。
3. 反应条件设定:设定反应的温度和时间等参数,如反应温度通
常设在60-65°C左右,时间取决于扩增片段的长度和PCR反应的效率。
4. 实时监测反应:在恒温扩增仪中,根据反应体系的不同,选择
合适的荧光染料,实时监测扩增过程,可得到扩增曲线,确定扩增产
物的数量和质量等信息。
5. 数据分析:根据实时监测得到的扩增曲线,可利用软件对扩增
产物的数量、含量进行定量和分析,比如利用常用的标准曲线法等方法。
总之,实时荧光恒温扩增技术是一种高效、快速、灵敏的分子生
物学实验技术,可广泛应用于医学、生物学等领域,为许多研究提供
了有力的工具。
D N A扩增试剂盒恒温扩增法The pony was revised in January 2021一、技术原理1. 产品描述本公司生产的DNA扩增试剂盒可用于人源性、动植物源性病原体及其他细菌、真菌、病毒、寄生虫等核酸的快速扩增。
本试剂盒通过Bst聚合酶、四种核苷酸单体(dNTPs)、引物等成分的作用,在恒温条件下(60~65℃)快速、特异地完成核酸扩增,并可借助显色液或相关仪器直接判断结果。
2. 产品规格二、详细信息型的核酸。
反应条件反应温度:63℃;反应时间:20 ~60min;反应仪器:恒温金属浴/ESE Tube Scanner/荧光PCR仪/GenieII/浊度仪。
检测方法染料法、浊度法、荧光法产品特点 1. 方便快捷:将反应液、酶、引物等混合均匀,20~60min便可观察结果;2. 特异性高:利用多条引物扩增目的基因的特异区域,确保扩增的准确性;3. 灵敏度高:最低可检测出1个拷贝的基因。
相关实验图片展示其它图片图1荧光指示剂(钙黄绿素)颜色变化图图2荧光指示剂(钙黄绿素)检测(ESE Tube Scanner)三、相关产品产品编号产品名称产品说明规格DRSR03荧光指示剂(钙黄绿素)本产品可作为恒温荧光扩增反应中的荧光指示剂,可根据颜色变化肉眼判断结果。
24测试/盒DASR06RNA扩增试剂盒(恒温扩增法)本试剂盒为细菌、真菌、病毒、寄生虫等病原体核酸(RNA)的恒温扩增通用试剂盒,集逆转录与核酸扩增于一体,20-60 min完成整个检测过程,同时有多种检测方式。
24测试/盒。