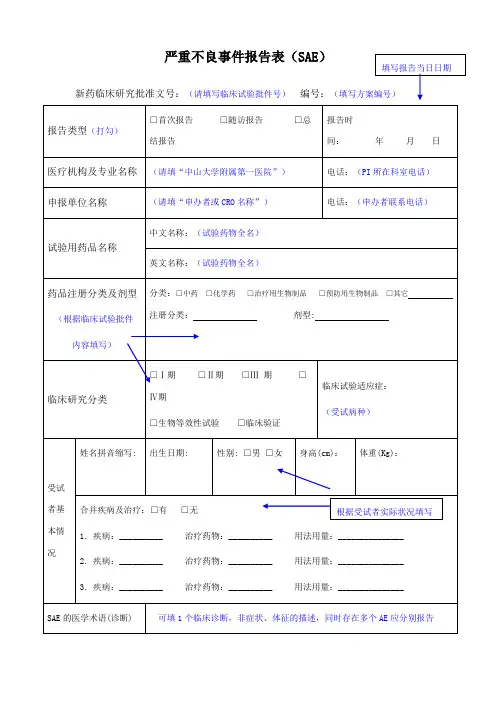
严重不良事件报告表(SAE)
- 格式:doc
- 大小:33.50 KB
- 文档页数:2
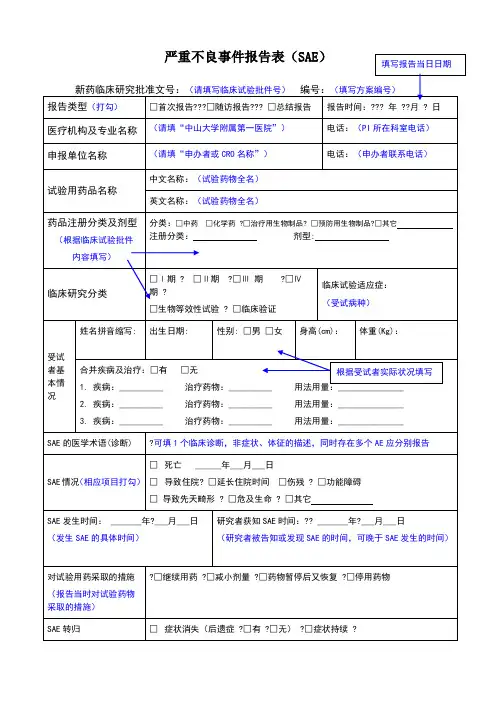
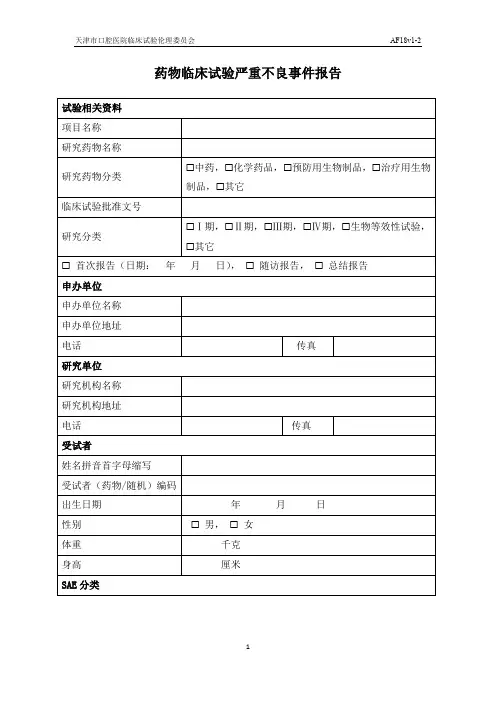
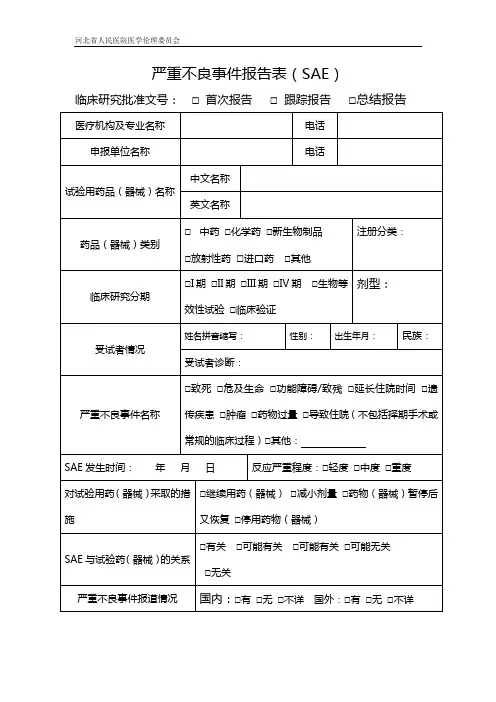

药物临床试验严重不良事件(SAE)报告表
内容填写要求:疾病诊断(只填写SAE发生时的合并疾病),严重程度(根据方案要求),开始时间,合并用药(只需填写SAE发生时的合并用药)
SAE发生及处理的详细情况:(包括受试者详细信息,相关病史,参加试验的情况和进展,SAE的发生、治疗及转归过程,SAE"∕能原因分析):
内容填写要求:
1.SAE的描述:AE开始日期,AE升级为SAE的日期。
相关症状体征,轻重程度(根据方案要求的分级),相关实验室检
查(是否超出正常值范围,判定及日期),事件的诊断,相关诊疗过程,事件符合SAE的标准.
2.请记录SAE的转归.(包括严重程度的变更以及转归的日期)
3.研究者对于SAE相关性的判断(不同SAE分开陈述),并提供判断的依据。
4 .如果患者住院,请记录出院小结(如有).
5 .如患者死亡,请记录死亡时间,死亡小结,抢救情况,尸检报告或其他死亡证明文件,死亡原因.
6 .如患者因SAE 退出研究,请注明.
7 .如以上信息缺失,请注明具体原因。
8 .请列出SAE 发生期间的合并用药,若未产生合并用药,可不填.
随访/总结报告格式:
随访/总结报告(.dd ):新的信息如下:(或:对之前上报的SAE 信息更正如下:)
1 .自首次报告后,该SAE 发生的转归、治疗及相关检查情况
2 .再次评价该SAE 。
试验用药的相关性
3 .明确是否恢复试验治疗或退出试验 申办者盖章
报告人科室/职称: 报告日期:
报告单位名称: 报告人签名:。



严重不良事件(SAE)报告什么是严重不良事件?严重不良事件(SAE)是指发生在临床试验中可能会危及受试者生命或健康的不良事件。
与其他不良事件(例如轻微不适)不同,SAE往往需要立即上报给监管机构和该试验的伦理委员会。
SAE也可以发生在药品和医疗器械的正式营销中,这时也需要进行临床研究以确认安全性和有效性。
SAE报告的流程1. 紧急处理SAE在发生SAE之后,研究人员应立即采取措施,尽可能减少潜在的风险和继续伤害。
这包括为患者提供紧急治疗、停止试验药物的使用、暂停试验流程、调整试验流程或终止试验等。
2. 上报SAE在紧急处理后,研究人员需要尽快将SAE报告给监管机构和伦理委员会。
这通常需要按照监管机构特定的SAE上报表格或表格模板提交报告,例如中国FDA的SAE报告表格。
3. 追踪SAE进展在提交SAE报告之后,研究人员需要监测SAE患者的进展情况,同时将其汇报给监管机构和伦理委员会。
这些报告可以包括SAE的病因学、症状、严重程度和治疗方法等信息,以及治疗效果和不良反应的监测结果。
除此之外,要及时调整伦理委员会的决策和试验计划。
4. SAE报告/追踪的时间点在报告SAE时,有一定时间限制,这通常是在SAE发生后24小时内或发现亚组后7个日历日内内报告。
对于中国而言,采用了《食品药品安全法》和中国FDA对“在中国进行药物和医疗器械的临床试验管理规定”,规定紧急报告的时间为24小时内。
对于非紧急的SAE报告,则需要在30天内提交报告。
5. SAE报告的必要性SAE报告对于临床研究的推动起着重要作用。
SAE报告不仅有助于确保研究人员能够充分了解试验中不良反应的情况,而且可以促进试验的透明性和公平性,提高患者与公众对试验的信任和接受度。
同时也为监管机构和伦理委员会提供了必要的依据,以评估受试者安全和试验质量。
结论总之,SAE的发生需要及时采取处理措施并报告给监管机构和伦理委员会,提高试验的透明性和公平性。

不良事件和严重不良事件报告SOP一、引言不良事件(Adverse Event, AE)和严重不良事件(Serious Adverse Event, SAE)是指在药物使用过程中产生的与药物有可能存在因果关系的有害反应。
为了确保药物的安全使用,必须对不良事件和严重不良事件进行及时、准确的报告和处理。
本文为不良事件和严重不良事件的报告及处理SOP(Standard Operating Procedure)。
二、定义1.不良事件:患者或试验对象在接受药物治疗或药物研究过程中,出现与药物暴露有可能相关的有害反应,包括预期的和非预期的。
2.严重不良事件:不良事件导致以下任何一种情况:危及生命,需要住院或延长住院,导致永久或严重残疾,威胁生命的,先天性异常或畸形。
三、报告责任1.监测人员:负责对临床试验过程中的不良事件进行监测和记录,并负责向研究者报告。
2.研究者:负责对不良事件进行评估,判断是否为严重不良事件,并及时报告给药物监管机构和伦理委员会。
3.药物监管机构:负责接受并处理药物不良事件的报告,保障药物的安全使用。
4.伦理委员会:负责审核研究者提交的严重不良事件报告,并提出建议和决策。
四、报告流程1.不良事件的监测和记录监测人员应定期对患者或试验对象进行随访,记录出现的不良事件,并将相关信息填写在不良事件报告表中,包括发生时间、症状描述、持续时间、严重程度等。
2.不良事件的评估和判断研究者应对收集到的不良事件进行评估,判断是否为严重不良事件。
评估应基于国家和国际上关于不良事件的定义和判断标准。
3.报告严重不良事件一旦判断为严重不良事件,研究者应立即向药物监管机构和伦理委员会进行报告。
报告内容应包括不良事件的描述、发生时间、因果关系评估、严重程度评估等信息。
报告方式可以采用书面报告、电子邮件或在线系统报告等。
4.处理不良事件研究者和药物监管机构应及时处理不良事件,包括调查、记录、分析和采取措施避免类似事件再次发生。