高二《化学反应原理》钢铁的析氢腐蚀与吸氧腐蚀 知识表格
- 格式:ppt
- 大小:155.00 KB
- 文档页数:1
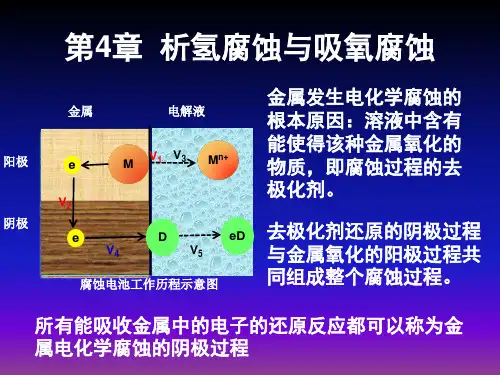








析氢腐蚀和吸氧腐蚀的条件当负极与电解质溶液不反应时,会发生吸氧腐蚀或析氢腐蚀①吸氧腐蚀:中性或弱酸性介质正极:2H2O +O2 +4e====4OH- 负极:Fe --- 2e ===Fe2+②析氢腐蚀: 酸性介质正极:2H+ + 2e ==== H2 负极:Fe --- 2e===Fe2+解释:①析氢腐蚀,在酸性较强的溶液中金属发生电化学腐蚀时放出氢气,这种腐蚀叫做析氢腐蚀。
在钢铁制品中一般都含有碳。
在潮湿空气中,钢铁表面会吸附水汽而形成一层薄薄的水膜。
②吸氧腐蚀是指金属在酸性很弱或中性溶液里,空气里的氧气溶解于金属表面水膜中而发生的电化学腐蚀。
吸氧腐蚀的阴极去极化剂是溶液中溶解的氧。
扩展资料:吸氧腐蚀是金属在空气中最普遍发生的一种腐蚀方式,在酸性、碱性和中性条件下都能发生作用。
发生机理是由于金属表面有水分,后通过原电池原理发生作用,使得金属(如:钢铁)被空气中的氧气腐蚀,产生生锈,由于此过程中需要消耗氧气,故名为:吸氧腐蚀或者耗氧腐蚀。
发生析氢腐蚀的体系标准电位很负的活泼金属大多数工程上使用的金属,如Fe正电性金属一般不会发生析氢腐蚀。
但是当溶液中含有络合剂时,正电性金属(如Cu,Ag)也可能发生析氢腐蚀。
⑴pH < 3时,阴极反应受活化极化控制。
⑵在弱氧化性和非氧化性酸溶液中,在反应速度不是很大时,阳极反应亦受活化极化控制。
⑶Fe在酸溶液中的腐蚀形态,一般是均匀腐蚀。
所以,Fe在酸溶液中的腐蚀可以当作均相腐蚀电极处理,作为活化极化控制腐蚀体系的典型例子。
1 阴极极化控制如Zn在稀酸溶液中的腐蚀。
因为Zn是高氢过电位金属,故为阴极极化控制。
其特点是腐蚀电位与阳极反应平衡电位靠近。
对这种类型的腐蚀体系,在阴极区析氢反应交换电流密度的大小将对腐蚀速度产生很大影响。
2 阳极极化控制只有当金属在酸溶液中能部分钝化,造成阳极反应阻力大大增加,才能形成这种控制类型。
有利于阳极钝化的因素使腐蚀速度减小。

析氢腐蚀和吸氧腐蚀
从动力学角度而言,析氢腐蚀比吸氧腐蚀进行得更快,一旦发生了析氢腐蚀,往往会造成很大的损失。
但是,在溶液中不论是碱性及酸性环境,氧电位都比氢电位高,而且中性、碱性环境占据了腐蚀环境的绝大部分(这种情况下析氢腐蚀不发生),所以以析氢腐蚀相比,吸氧腐蚀具更重要的意义。
析氢腐蚀,指的是钢铁制品在酸性较强的溶液中与质子反应发生时放出氢气的腐蚀。
如果钢铁制品使用不当或者保管不合理的话,它就会在潮湿空气中,吸附空气中的水蒸气而形成一层薄薄的水膜。
这层水膜中无疑可以吸收空气中的二氧化碳。
而二氧化碳与水反应生产的碳酸,又会使得使水里的氢离子增多。
这就构成无数个以铁为负极、碳为正极、酸性水膜为电解质溶液的微小原电池。
析氢腐蚀发生的速率很快。
(这个反应首先是个原电池反应,而且反应面积大,同时生成的氢气可以很快脱离体系,反应速率能不快么。
)吸氧腐蚀是指金属在酸性很弱或中性溶液里,空气里的氧气溶解于金属表面水膜中而发生的电化学腐蚀。
这个反应速率取决于
氧穿过空气/溶液界面进入溶液;
在溶液对流作用下,氧迁移到阴极表面附近;
在扩散层范围内,氧在浓度梯度作用下扩散到阴极表面;
在阴极表面氧分子发生还原反应,也叫氧的离子化反应。
这四个步骤显然比析氢腐蚀的步骤多且慢。
但在热力学的角度而言,它发生的趋势更大,而且应用的范围更广,所以就更有意义咯。