最新高中有机化学同分异构体
- 格式:doc
- 大小:28.50 KB
- 文档页数:6


高考化学同分异构体的知识点一、有机物的同分异构体1. 同分异构体的概念化合物具有相同的分子式,但具有不同结构的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
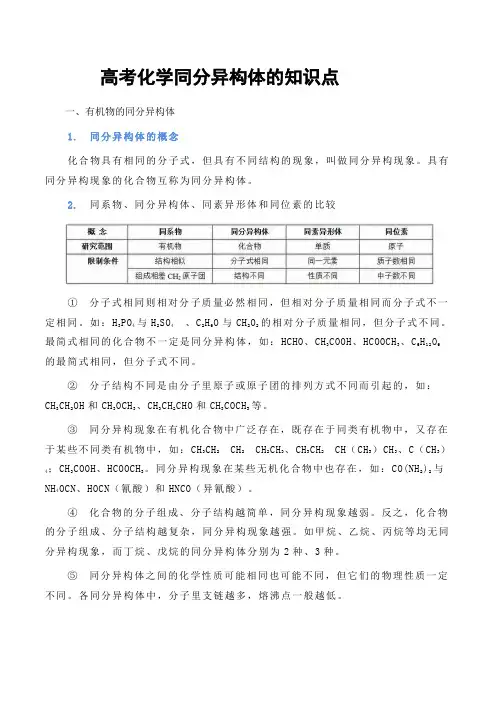
2. 同系物、同分异构体、同素异形体和同位素的比较①分子式相同则相对分子质量必然相同,但相对分子质量相同而分子式不一定相同。
如:H3PO4与H2SO4、C2H6O与CH2O2的相对分子质量相同,但分子式不同。
最简式相同的化合物不一定是同分异构体,如:HCHO、CH3COOH、HCOOCH3、C6H12O6的最简式相同,但分子式不同。
②分子结构不同是由分子里原子或原子团的排列方式不同而引起的,如:CH3CH2OH和CH3OCH3、CH3CH2CHO和CH3COCH3等。
③同分异构现象在有机化合物中广泛存在,既存在于同类有机物中,又存在于某些不同类有机物中,如:CH3CH2CH2CH2CH3、CH3CH2CH(CH3)CH3、C(CH3)4;CH3COOH、HCOOCH3。
同分异构现象在某些无机化合物中也存在,如:CO(NH2)2与NH4OCN、HOCN(氰酸)和HNCO(异氰酸)。
④化合物的分子组成、分子结构越简单,同分异构现象越弱。
反之,化合物的分子组成、分子结构越复杂,同分异构现象越强。
如甲烷、乙烷、丙烷等均无同分异构现象,而丁烷、戊烷的同分异构体分别为2种、3种。
⑤同分异构体之间的化学性质可能相同也可能不同,但它们的物理性质一定不同。
各同分异构体中,分子里支链越多,熔沸点一般越低。
二. 同分异构体的类型绝大多数有机物普遍存在同分异构现象,高中阶段的同分异构现象主要有4种情况。
即碳链异构、官能团位置异构、官能团类别异构和顺反异构。
1. 碳链异构碳链异构是指由于碳原子的连接次序不同引起的异构,如,正丁烷与异丁烷。
由于烷烃分子中没有官能团,所以烷烃不存在官能团位置异构和官能团类别异构,而只有碳链异构。
再如,CH3CH2CH2CH2CHO(戊醛)与(CH3)2CHCH2CHO(2-甲基丁醛)也属于碳链异构。

有机物存在同分异构体的条件
同分异构体是一种化学现象,也称为同分异构体或同分异构体,是指分子式相同但构型不同的有机化合物。
它们具有相同的分子式和分子量,但具有不同的结构和物理性质。
有机物存在同分异构体的条件如下:
分子组成相同:同分异构体的前提条件是它们的分子组成一样。
例如,苯和环己烯均具有分子式C6H6,因此可以存在同分异构体现象。
偶氮苯异构体:对于一些具有偶极矩的化合物,例如偶氮苯等,它们可以通过异构化来实现不同状态之间的转换。
圆环化物异构体:某些化合物,如环状化合物和杯状化合物,可能会出现不同的构象和异构体。
构型异构体:分子内官能团的构型会影响异构体的形成,例如化合物的立体异构体, 如2-溴-3-氯-2-氟丙烯存在E、Z异构体等。

有机化合物的同分异构体与命名同分异构体是指分子式相同但结构不同的化合物,在有机化学中占据着重要的地位。
同分异构体的存在导致了化学物质的复杂性,对于正确命名同分异构体可以帮助我们理解它们的结构和性质。
本文将探讨有机化合物的同分异构体与其命名方法。
一、同分异构体的概念和分类同分异构体是由于有机化合物的碳骨架可以以不同方式连接而产生的,即它们的分子式相同,但结构不同。
根据同分异构体的性质和结构特征,通常可分为以下几类:1. 结构异构体:分子内原子的连接顺序不同,使得同一分子的碳骨架结构不同。
例如,丙酮和乙醛就是结构异构体,它们的分子式均为C3H6O,但结构上的差异导致它们的性质和反应也不同。
2. 空间异构体:分子内原子的空间排列方式不同,使得同一分子的立体构型不同。
空间异构体又可分为顺式异构体和反式异构体。
例如,顺式-二氯乙烯和反式-二氯乙烯是二氯乙烯的两种空间异构体,它们的分子式均为C2H2Cl2,但空间构型上的差异导致它们的性质也不同。
3. 异构体间互变异构体:同一化合物可以通过键的移动或原子的重排而转变为不同结构的异构体。
例如,异丁烯和顺丁烯就是由转位反应相互转化的异构体,它们的分子式均为C4H8,但结构上的差异导致它们的性质和反应也不同。
二、同分异构体的命名规则为了区分同分异构体,需要对其进行合理的命名。
有机化合物的命名是遵循一定规则的,常用的命名方法有以下几种:1. 经典命名法:根据化合物的特性和结构确定其名称。
例如,乙醛和乙酸是同分异构体,乙醛的经典命名为乙基酚醛,乙酸的经典命名为乙酸。
经典命名法适用于较为简单的同分异构体。
2. 正规命名法:根据化合物的结构和功能团进行命名。
正规命名法是有机化学领域最常用的命名方法,主要依据IUPAC(国际纯粹和应用化学联合会)的命名规则。
例如,乙醛的正规命名为乙酸醛,乙酸的正规命名为乙酸。
正规命名法对于较为复杂的同分异构体具有普适性和准确性。
3. 功能团命名法:根据化合物中的功能团来进行命名。
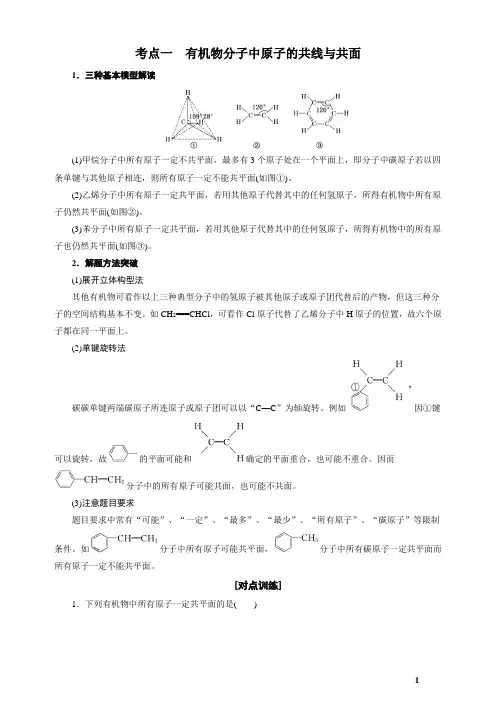
考点一有机物分子中原子的共线与共面1.三种基本模型解读(1)甲烷分子中所有原子一定不共平面,最多有3个原子处在一个平面上,即分子中碳原子若以四条单键与其他原子相连,则所有原子一定不能共平面(如图①)。
(2)乙烯分子中所有原子一定共平面,若用其他原子代替其中的任何氢原子,所得有机物中所有原子仍然共平面(如图②)。
(3)苯分子中所有原子一定共平面,若用其他原子代替其中的任何氢原子,所得有机物中的所有原子也仍然共平面(如图③)。
2.解题方法突破(1)展开立体构型法其他有机物可看作以上三种典型分子中的氢原子被其他原子或原子团代替后的产物,但这三种分子的空间结构基本不变。
如CH2===CHCl,可看作Cl原子代替了乙烯分子中H原子的位置,故六个原子都在同一平面上。
(2)单键旋转法碳碳单键两端碳原子所连原子或原子团可以以“C—C”为轴旋转。
例如因①键可以旋转,故的平面可能和确定的平面重合,也可能不重合。
因而分子中的所有原子可能共面,也可能不共面。
(3)注意题目要求题目要求中常有“可能”、“一定”、“最多”、“最少”、“所有原子”、“碳原子”等限制条件。
如分子中所有原子可能共平面,分子中所有碳原子一定共平面而所有原子一定不能共平面。
[对点训练]1.下列有机物中所有原子一定共平面的是()A.B.C.D.2.下列有机物分子中,所有原子一定处于同一平面的是()3.下列有关CH3—CH===CH—C≡C—CF3分子结构的叙述中,正确的是()A.6个碳原子有可能都在一条直线上B.6个碳原子不可能都在一条直线上C.6个碳原子不可能都在同一平面上D.所有原子有可能在同一平面上4.下列有关分子结构的叙述中正确的是()①除苯环外的其余碳原子有可能都在一条直线上②除苯环外的其余碳原子不可能都在一条直线上③12个碳原子不可能都在同一平面上④12个碳原子有可能都在同一平面上A.①②B.②③C.①③D.②④5.下列分子中的碳原子可能处在同一平面内的是()6.有机化合物X是一种医药中间体,其结构简式如图所示。

【高中化学】高中化学知识点:同分异构体同分异构现象和同分异构体:1.概念:化合物具有相同的分子式.但结构小同,因而产生了性质上的差异,这种现象叫同分异构现象。
具有同分异构现象的化合物互为同分异构体。
2.同分异构体的基本类型(1)碳链异构:指的是分子中碳骨架不同而产生的同分异构现象。
如所有的烷烃异构都属于碳链异构。
(2)边线异构:所指的就是分子中官能团边线相同而产生的同分异构现象。
如l一丁烯与2一丁烯、l一丙醇与2一丙醇、邻二甲苯与间二甲苯及对二甲苯。
(3)官能团异构:指的是有机物分子式相同,但具有不同官能团的同分异构体的现象。
常见的官能团异构关系如下表所示:(4)顺反异构:由于碳碳双键无法转动而引致分子中原子或原子团在空间的排序方式相同所产生的异构现象。
两个相同的原子或原子团排序在双键的同一侧的称作双键结构;两个相同的原子或原子团排序在双键的两侧的称作反式结构。
例如同分异构体的写法:1.烷烃的同分异构体的读法烷烃只存有碳链异构,其书写技巧通常使用“减碳法”,可以归纳为“两特别注意,四句话”。
(1)两注意:①选择最长的碳链为主链;②找出主链的中心对称线。
(2)四句话:主链由短至长、支链由Marciac贫,边线由心到边,轨域邻、间、对。
例如,c6h14的同分异构体可按此法完整写出(为了简便,在所写结构式中删去了氢原子):2.烯烃的同分异构体的读法分子共同组成合乎cnh2n的烃除烯烃外,除了环烷烃(n≥3),并且烯烃中双键的边线相同则结构相同,有的烯烃还存有顺反异构,所以烯烃的同分异构体比烷烃繁杂得多。
以c5h10为基准表明同分异构体的读法:共有5种烯烃,其中(2)还存在顺反异构体,5种环烷烃,共计11种。
3.苯的同系物的同分异构体的读法由于苯环上的侧链边线相同,可以构成多种同分异构体。
以c8h10为基准写下其属苯的同系物的同分异构体:判断同分异构体数目的方法:1.碳链异构和边线异构:先切除官能团,书写最久碳链,移动官能团的边线;再逐渐增加碳数,移动官能团的边线。


烃及烃的衍生物的同分异构体推导规律同分异构现象是有机物普遍存在的重要现象,也是有机物品种繁多的原因之一。
在学习有机化学时,同学们对推导有机物的同分异构体往往会感到困难。
在此,介绍下面的一些方法和推导规律进行有关的推导,即可避免重复,又不至于漏写。
一、推导烃的同分异构体:首先,对烷烃而言,可归纳为以下四点:1. 主链由长到短,短至主链碳原子数目不得少于或等于全部碳原子数的二分之一。
2. 支链的大小由整到散。
3. 支链的位置由“心”到“边”(末端碳原子除外)。
4. 支链的排布由相“对”,相“邻”到相“间”。
例一:分子式为C7H16的所有同分异构体的构造式(为清楚从简只用碳的骨架表示)分析:可按上述方法1. 先写出最长为七个碳原子的主链:C─C─C─C─C─C─C (1)2. 后写出少一个碳原子的直链作主链,把取下来的一个碳原子作为支链加到直链上,并由“心”到“边”地依次变动位置:C─C─c -C─C─C (2)│CC─C─C─C─C─C (3)│C3. 再写出少两个碳原子的直链,把取下来的两个碳原子作为支链加在这一直链上,先“整”加一个乙基,后“散”加两个甲基。
添加这些取代基时注意由“心”到“边”和由“对”、“邻“到“间”:C─C─C─C─C (4)│C│CC│C─C─C─C─C (对位) (5)│CC│C─C─C─C─C (对位) (6)│CC─C─C─C─C (邻位) (7)││C CC─C─C─C─C (间位) (8)││C C4. 取下三个碳原子,其余的四个碳原子(其数目大于全部碳原子数目的二分之一),还可组成“主链”。
但此时取下的三个碳原子再无“整”的可能,而只能“散”了。
C│C─C─C─C (9)││C C即C7H16只可能有上述九种同分异构体以上方法在推导烯烃,炔烃和芳香烃的同分异构体时也可应用,不过此时除了碳链异构外,还要考虑它们的官能团异构, 官能团位置异构和互变异构及立体异构。
二、推导烃的衍生物的同分异构体。

高中化学有机同分异构体技巧高中化学有机同分异构体技巧有机同分异构体是指分子式相同,但结构不同的有机化合物。
在高中化学中,了解有机同分异构体的概念及其技巧对于理解有机化学的基本原理和反应机理非常重要。
1. 了解同分异构体的概念:同分异构体是指分子式相同,但结构不同的化合物。
同分异构体的存在是由于碳原子的四个价电子可以与其他原子或基团形成多种不同的键合方式,从而导致分子结构的差异。
2. 分子式与结构的关系:同分异构体的分子式相同,但结构不同。
在分子式中,只包含了元素的种类和数量,而没有体现出它们的结构。
因此,同分异构体的结构可以通过分子式推断出来。
3. 碳骨架的不同连接方式:同分异构体的主要区别在于碳骨架的连接方式。
碳骨架可以是链状、环状或者有机官能团的连接。
同分异构体通过改变碳骨架的连接方式,可以形成不同的结构。
4. 功能团的位置和性质:同分异构体中的功能团的位置和性质也可以影响分子的结构。
在同一分子中,功能团的位置不同,可能导致分子性质的差异,如溶解性、反应性等。
5. 异构体的命名与区分:同分异构体需要进行命名和区分。
在高中化学中,主要采用IUPAC命名法来命名有机化合物。
根据IUPAC命名法,可以通过命名规则来区分同分异构体。
6. 反应机理的理解:同分异构体的存在对于理解有机化学的反应机理非常重要。
不同的结构可以导致不同的反应性质和反应路径。
通过研究同分异构体的反应,可以揭示有机化学反应的本质和机理。
总结起来,高中化学中掌握有机同分异构体的概念和技巧对于理解有机化学的基本原理和反应机理非常重要。
通过对同分异构体的研究,可以深入了解有机化合物的结构和性质,从而为进一步学习有机化学打下坚实的基础。