[23]黄钠铁矾渣制备透明铁黄的晶种研究
- 格式:pdf
- 大小:135.88 KB
- 文档页数:3
![一种透明氧化铁黄颜料的制备方法[发明专利]](https://uimg.taocdn.com/b07fd72fa200a6c30c22590102020740be1ecd1a.webp)
(10)申请公布号(43)申请公布日 (21)申请号 201410822939.6(22)申请日 2014.12.26C01G 49/02(2006.01)(71)申请人常熟洛克伍德颜料有限公司地址215500 江苏省苏州市常熟市辛庄镇北8号(72)发明人钱仁晋 戴金达 陈天宝 陆庆(54)发明名称一种透明氧化铁黄颜料的制备方法(57)摘要一种透明氧化铁黄颜料的制备方法,于常温搅拌通氮气保护下,将FeSO 4溶液加入到NaOH溶液中,加完后,于略高温度、600~800r/min、Qair=3~5L/min 下,通空气氧化1~3h,然后停止通入空气,降低搅拌速度到400~500r/min,加入表面活性剂,然后用稀硫酸缓慢调pH 到6,继续搅拌1~2h,所得料浆经过滤、洗涤后40~50℃烘干得铁黄成品。
本发明的透明氧化铁黄颜料的制备方法,不需要制备晶种,直接制得达到我国化工行业标准的透明氧化铁产品,同时具有工艺简单,生产成本低的优点。
(51)Int.Cl.(19)中华人民共和国国家知识产权局(12)发明专利申请权利要求书1页 说明书2页(10)申请公布号CN 104528832 A (43)申请公布日2015.04.22C N 104528832A1.一种透明氧化铁黄颜料的制备方法,其特征在于,包括下述步骤:溶液加入到NaOH溶液中,加完后,于略高温度、于常温搅拌通氮气保护下,将FeSO4600~800r/min、Qair=3~5L/min下,通空气氧化1~3h,然后停止通入空气,降低搅拌速度到400~500r/min,加入表面活性剂,然后用稀硫酸缓慢调pH到6,继续搅拌1~2h,所得料浆经过滤、洗涤后40~50℃烘干得铁黄成品。
溶液2.根据权利要求1所述的透明氧化铁黄颜料的制备方法,其特征在于:加完FeSO4后,于略高温度、700r/min、Qair=4L/min下,通空气氧化2h。
3.根据权利要求1所述的透明氧化铁黄颜料的制备方法,其特征在于:降低搅拌速度到450r/min,加入表面活性剂。

江淮十校2024届高三第一次联考化学试题(答案在最后)考生注意:1.本试卷满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。
必须在题号所指示的答题区域作答,超出答题区域书.......写的答案无效,在试题卷、草稿纸上答题无效....................。
可能用到的相对原子质量:H-1Li-7B-11C-12N-14O16Na-23S-32C1-35.5 Ca-40Fe-56Cu-6I-127Pb-207一、选择题(每小题3分,共42分)1.化学促进着科技的进步和社会的发展。
下列化学与生活的叙述正确的是A.食品袋里放入硅胶,可抗氧化B.漂白精中混入食醋,漂白效果更好C.宿州白土古镇的白瓷中含大量的SiO2、K2O和Fe2O3D.可穿戴式智能测温设备的测温芯片主要成分是硅酸盐【答案】B【解析】【详解】A.硅胶是干燥剂,硅胶无还原性,食品袋里放入硅胶,不能抗氧化,故A错误;B.漂白精中含有次氯酸钙,漂白精中混入食醋,生成次氯酸,漂白性增强,故B正确;C.白瓷的主体为白色,Fe2O3为红色,所以白瓷中不能含大量的Fe2O3,故C错误;D.芯片主要成分是单质硅,故D错误;选B。
2.安庆茯苓是安徽十大皖药之一,主治水肿、痰饮、脾虚泄泻、心悸、失眠。
茯苓酸(结构简式如图示)是茯苓的重要提取物之一,下列有关茯苓酸的说法正确的是A.常温下是气体B.分子中有6个手性碳C.分子中含4种官能团D.能发生缩合聚合反应【答案】D【解析】【详解】A .根据结构简式可知,该物质碳原子数大于5,相对分子质量较大,熔沸点较高,在常温下不是气体,选项A 错误;B .该物质中含7个手性碳原子,选项B 错误;C .该结构中含有碳碳双键、羟基、羧基3种官能团,选项C 错误;D .该物质中含有羟基和羧基,可以发生分子间缩合聚合反应,选项D 正确;答案选D 。
3.用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是ABCD除去CO 2气体中混有的HCl 杂质证明H 2CO 3比苯酚酸性强由CuSO 4溶液制取胆矾验证1-溴丙烷发生消去反应生成丙烯A.AB.BC.CD.D【答案】D 【解析】【详解】A .CO 2溶于水,降低CO 2溶解度应用饱和碳酸氢钠溶液,不是饱和食盐水,故A 错误;B .醋酸易挥发,生成的CO 2气体中含有醋酸蒸气,醋酸蒸气能与苯酚钠反应生成苯酚,对碳酸与苯酚钠的反应产生干扰,两装置之间再加一个盛碳酸氢钠溶液的洗气瓶,故B 错误;C .硫酸铜溶液得到胆矾,不能用蒸发结晶方法,通过冷却结晶方法制备胆矾,故C 错误;D .1-溴丙烷发生消去反应生成丙烯,通入溴的四氯化碳溶液中,溶液褪色,证明消去反应有不饱和烃的生成,故D 正确;答案为D 。


山东省淄博市2020—2021学年度高三模拟考试化学注意事项:1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Se 79一、选择题:本题共10小题,每小题2分,共20分。
每小题只有一个选项符合题意。
1.化学与生产、生活密切相关。
下列说法错误的是A.液氨可用作致冷剂B.新冠疫苗一般应冷藏存放,以避免蛋白质变性C.铝制餐具适宜用来蒸煮碱性食物D.防晒霜能减轻紫外线伤害的原因之一是其有效成分中含有 键2.下列有关实验安全和试剂回收处理的说法错误的是A.蒸馏实验中向沸腾的液体中补加沸石B.用3%过氧化氢消毒液擦洗伤口C.实验室中将未用完的白磷放回原试剂瓶D.用乙醇处理废弃药品中含有的少量金属钠3.下列操作能够达到实验目的的是4.W 、X 、Y 和Z 为原子序数依次增大的四种短周期主族元素。
W 与X 可形成一种红棕色有刺激性气味的气体;Y 的周期序数是族序数的3倍;Z 的最外层电子数与W 的电子总数相同。
下列叙述正确的是 A .第一电离能:X>W>YB .简单离子半径:Y>X>WC .简单氢化物的稳定性:X>WD .氧化物对应水化物的酸性:Z>W5.NF 3是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH 4HF 2)制得。
下列有关说法错误的是 A .NF 3的空间构型为平面三角形B .相关元素电负性由大到小的顺序为F>N>HC .NF 3和NH 4HF 2中N 原子的杂化方式均为sp 3D .NH 4HF 2晶体中微粒间的作用有离子键、共价键、配位键、氢键6.正丁醚常用作有机反应的溶剂,不溶于水,密度比水小,在实验室中可利用反应2CH 3CH 2CH 2CH 2OH 135−−−→浓硫酸℃CH 3(CH 2)3O(CH 2)3CH 3+H 2O 制备,反应装置如图所示。

绵阳实验高中2021级理科综合训练(2)命题:周建何琳琳陈磊组卷:赖维吉审题:陈飞龙周方文赵琴本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
满分300分。
相对原子质量:H 1 C12 O16 S32 Cu64 Zn65 B11第Ⅰ卷(选择题,共126分)一、选择题:本题共13小题,每小题6分,共78分。
每小题只有一个选项符合题意。
1.在致癌因子的作用下,正常动物细胞可转变为癌细胞。
有关癌细胞特点的叙述错误的是()A.细胞中可能发生单一基因突变,细胞间黏着性减少B.细胞中可能发生多个基因突变,细胞的形态发生变化C.细胞中的染色体可能受到损伤,细胞的增殖失去控制D.细胞中遗传物质可能受到损伤,细胞表面的糖蛋白减少2.基因型为Aa的某植株产生的“a”花粉中有一半是致死的,则该植株自花传粉产生的子代中AA:Aa:aa基因型个体的数量比为()A.3:2:1B.2:3:1C.4:4:1D.1:2:13.已知某种限制性内切酶在一线性DNA分子上有3个酶切位点,如图中箭头所指,如果该线性DNA分子在3个酶切位点上都被该酶切断,则会产生a、b、c、d四种不同长度的DNA片段。
现在多个上述线性DNA分子,若在每个DNA分子上至少有1个酶切位点被该酶切断,则从理论上讲,经该酶切后,这些线性DNA分子最多能产生长度不同的DNA片段种类数是()A.3B.4C.9D.124.用体外实验的方法可合成多肽链。
已知苯丙氨酸的密码子是UUU,若要在体外合成同位素标记的多肽链,所需的材料组合是:①同位素标记的tRNA①蛋白质合成所需的酶和ATP①同位素标记的苯丙氨酸①人工合成的多聚尿嘧啶核苷酸①除去了DNA和mRNA的细胞裂解液①翻译的场所核糖体A.①①①①B.①①①①C.①①①D.①①①5.水稻的某病害是由某种真菌(有多个不同菌株)感染引起的。
水稻中与该病害抗性有关的基因有3个(A1、A2、a);基因A1控制全抗性状(抗所有菌株),基因A2控制抗性性状(抗部分菌株),基因a控制易感性状(不抗任何菌株),且A1对A2为显性,A1对a为显性、A2对a为显性。

第5卷第2期 上海大学学报(自然科学版) Vol.5,No.2 1999年4月 JOURN AL OF S HAN GHAI UN IV ERS ITY(N ATURAL S CIEN CE) Apr.1999利用生产钛白的副产物硫酸亚铁制备透明铁黄华 彬 朱 萍 施利毅 唐述祥(化学与化工学院)提 要 本文介绍了利用生产钛白的副产物硫酸亚铁制备透明铁黄(T-FeO O H)的实验方法,考察了影响晶种质量及晶种氧化过程的主要因素.晶种制备过程控制温度为25℃,加入分散剂,静置熟化0.5h.氧化过程中控制p H值在8.5~9.0,温度35℃.反应24h后,将溶液过滤洗涤,真空烘干后即获得铁黄产品.样品粒子呈纺锤状,长轴平均120nm,短轴平均45nm,粒子间无明显的团聚,单分散性较好.关键词 硫酸亚铁;α-FeOO H;制备中图法分类号 X789Study on the Producing Process of Transparent Iron Oxidewith Ferrous Sulfate Originated from the By-productof Titanium Dioxide ProductionHua B in Zhu Ping Shi Liyi Tang Shuxiang(Schoo l o f Chemistr y and Chemical Enginee ring,Shanghai U niv er sity)Abstract:The producing pro cess of transpa rent iron oxide with ferrous sulfa te o riginated from the by-product of titanium dioxide is reported,and the facto rs that affect the quality a nd oxidiza-tion of crystal seeds w ere inv estig ated.The reactio n tempera ture of producing cry stal seeds w ere controlled at25℃.After sepa ra nt w as added,the depo sit w as kept for half an ho ur.The co ndi-tions of oxidizatio n process w ere co ntrolled a s p H8.5~9.0,reactio n tempera ture35℃a nd reac-tion period24hours.Through percola ting,wa shing and drying,transpa rent iro n o xide par ticles w ere o btained.The particles w ere spindly and mo nodispersed with the mea n majo r axis120nm and the m ea n mino r axis45nm.Key words:ferrous sulfate;T-FeOOH;productio n 我国的二氧化钛(俗称钛白)主要采用硫酸法生产.目前钛白的生产能力为130k T/a,每制取1t钛白将副产 3.5~4t的硫酸亚铁[1].该硫酸亚铁除部分用于净水剂与催化剂外,大部分被排放到江河湖泊,既污染了环境又浪费了宝贵的资源,其综合利用已引起了研究者的广泛关注.国内外从70年代中期即开始研究利用它制备氧化铁系颜料,并公开发表了一些研究成果[2-4].但由于所制备的主要是普通铁系颜料,在油漆中只能用于底漆等中低档领域,同时在生产过程中还要消耗大量的铁皮或铁粉,所以收稿日期:1998-07-08 上海市环保局、市科委资助项目(97JG05065) 华 彬,男,1967年生,博士,副教授;上海大学化学与化工学院环境科学与工程系,上海市延长路149号(200072)生产成本较高,利润较低,难以为大多数钛白生产厂家所接受.本课题提出利用生产钛白的副产物硫酸亚铁制备透明铁黄(α-FeOO H ),提高产品的价值,并从工艺着手,减少铁的用量,降低生产成本,这样就可以获得可观的经济价值,从而能够被广大的钛白生产厂、颜料化工厂所接受.透明铁黄平均粒径为100nm 左右,在透明介质中有着很好的透明性,它除具有普通氧化铁颜料的耐光、耐化学腐蚀、无毒等特点外,还具有良好的分散性、着色力以及强烈吸收紫外线能力.在美国、日本等国已有红、黄、橙等数种色泽的透明铁系颜料生产.国内只有少数厂家能够生产,成本较高,产量亦较小[5].这些颜料主要用于金属、木材、铝箔等底材上,也可作为部分替代品与价格昂贵的有机颜料配合使用,或用于塑料薄膜中,以屏蔽对紫外线敏感的物质.本文采用生产钛白的副产物硫酸亚铁制备透明铁黄,考察了操作条件对制备过程的影响,确定了产品的形貌及晶型.1 实验部分1.1 实验所用的试剂及设备见表1和表 2.表1 实验所用的试剂试剂名称规格生产厂商七水硫酸亚铁上海钛白粉厂碳酸氨分析纯上海试剂四厂氢氧化钠化学纯江苏南新助剂厂铁粉分析纯上海化学试剂厂六偏磷酸钠化学纯湖州食品化工有限公司去离子水自制表2 实验所用的主要设备仪器名称型号生产厂家温度控制仪 W M 2K-01上海长江医疗 器械厂电动搅拌机调速器 7321上海地理模型厂精密pH 计 pHS-3C 上海雷磁仪器厂搅拌器 JB-1上海第二分析 仪器厂电热真空恒温干燥箱上海医疗器械厂1.2 实验过程主要反应方程式为FeSO 4+(N H 4)2CO 3 =FeCO 3+(N H 4)2SO 4,(1)FeCO 3+H 2O =Fe(O H)2+CO 2,(2)4Fe(O H)2+O 2=4FeOO H+2H 2O,(3)实验工艺流程如图1所示.图1 实验工艺流程图称取111g FeSO 4·7H 2O (0.4mol),加入180ml 的去离子水溶解,加铁粉调p H 值,加热,保温0.5h 后过滤除钛[6].称取16g NaO H 和21.8g (N H 4)2CO 3各加入180ml H 2O 和100ml H 2O 中,将它们加入精制后的硫酸亚铁溶液中,控制反应温度为25℃,溶液中出现白色沉淀,加入0.5g 的分散剂六偏磷酸钠,静置熟化0.5h.控制pH 值在8.5~9.0,温度35℃,通空气氧化,通气速率0.06m 3/h .反应过程中溶液颜色由白色到墨绿到橙黄.大约24h 后,将溶液过滤洗涤,80℃下真空烘干后即获得铁黄产品.产品的晶型由X 射线衍射仪(XRD,DM AX /γB 型,日本Rig aku 公司)测定,粒径由透射电子显微镜(T EM ,JEM -1200E X Ⅱ型,日本Jel 公司)测定.2 实验结果与讨论2.1 粒子的晶型利用XRD 测定样品的晶型如图2所示.与JCPDS 卡对照,可以确定样品为α-FeOO H .2.2 样品的形貌利用T EM 测定样品的形貌如图3所示.从图中可见,铁黄粒子呈纺锤状,长轴平均120nm,短轴平均45nm ,粒子间无明显的团聚,单分散性较好.·136· 上海大学学报(自然科学版) 第5卷图2 样品的X RD图谱图3 样品的T EM 照片2.3 影响晶核质量的主要因素影响晶核质量的主要因素有三价铁离子、反应温度、分散剂的加入量及硫酸亚铁浓度.2.3.1 三价铁离子的影响在FeSO 4溶液中,(N H 4)2CO 3与NaO H 作沉淀剂,主要得到FeCO 3沉淀,为了制得色相纯正的透明铁黄粒子,沉淀时应避免三价铁化合物产生,因为在将FeCO 3(或Fe(O H)2)氧化成α-FeOOH 过程中反应温度为35℃左右,在这样低的温度下,三价铁化合物(如Fe (O H )3)不能完全脱水生成α-FeOO H ,制得的透明铁黄中将夹杂有Fe (O H )3,这会使产品色相暗红.为此在制备晶种的溶液中加入微量的铁粉,以抑制三价铁化合物的产生.2.3.2 温度的影响制备铁黄晶种时,温度将影响晶核的稳定性.在生成沉淀时溶液中尚余有硫酸亚铁,这部分亚铁一般以络合物形式存在.低温下络合物较稳定,温度升高,络合物将分解,使得这部分亚铁氧化生成非晶体沉淀.如果亚铁氧化后沉淀于已生成的α-FeOO H 晶核上则造成部分铁黄晶种长大,引起晶核大小不一.用这样的晶种制造铁黄,产品的色光将发萎,而且产率较低.同时温度过高还会导致四氧化三铁的生成,使晶种发黑.由于以上原因,制备铁黄晶种时,温度控制在10~30℃,本实验取25℃左右,以确保晶种的质量.2.3.3 分散剂的影响分散剂的加入,可使FeCO 3沉淀形成的晶种单分散性较好,且可抑制晶种的长大及杂晶γ-FeOO H 的生成.实验中在晶种溶液中加入溶解于50ml 去离子水的0.5g 六偏磷酸钠分散剂,以保证晶种的单分散性,控制晶种的长大.2.3.4 硫酸亚铁浓度的影响硫酸亚铁浓度越高,制取晶种的数量越多,且颗粒小,在以后的氧化过程中,虽然粒子小、数量多的晶种使氧化时间增长,但可使单位产量增大,色光进展平稳.所以实验中采取饱和硫酸亚铁溶液.2.4 影响晶种氧化的主要因素影响晶种氧化的主要因素有晶种的浓度、反应温度、溶液pH 值及空气流量.2.4.1 晶种的浓度、溶液pH 值的影响晶种浓度太低,单位反应器体积产量低,且氧化反应较速度快,粒子的色光不宜控制.晶种浓度太高,虽然单位反应器体积产量高,但由于溶液过于稠密,粒子或分子扩散速度小,氧化反应速度慢,生产周期长.因此在晶种氧化前,将溶液稀释一倍.氧化时pH 值太高(超过10)易形成杂晶,pH 太低(低于7)粒子粒径不易控制.本研究取pH 值在8.5~9.0.2.4.2 氧化反应温度及空气流量的影响氧化反应温度越高,氧化反应速度越快,但产品粒子的色光易偏红.氧化反应温度越低,氧化反应周期越长,且容易造成二价亚铁粒子未氧化就进入铁黄晶格,形成杂晶,色光发萎.本研究氧化时,控制温度为35℃,氧化周期约24h ,产物粒子颜色为橙黄.氧化过程中,通入的空气流量越大,氧化反应速率越快,粒子的单分散性较好,但产品的色光难以控制.本研究取空气流量为0.06m 3/h.为保证气泡分布均匀、直径小,采用多孔砂芯空气分布器.3 结 论(1)利用生产钛白的副产物硫酸亚铁制备了透明铁黄,实验条件下得到的产物粒子呈纺锤状,长轴平均120nm,短轴平均45nm,粒子间无明显的团聚,单分散性较好.(2)影响晶核质量的主要因素有三价铁离子、反应温度、分散剂的加入量及硫酸亚铁浓度.(3)影响晶种氧化的主要因素有晶种的浓度、反应温度、溶液p H 值及空气流量.通过控制这些条件,可以控制产物粒子的形态.(下转168页)·137·第2期 华 彬等:利用生产钛白的副产物硫酸亚铁制备透明铁黄不对称性.因此旋光性聚酰胺的合成还必须使用旋光性的单体以引入不对称结构因素.图1 碳链长度对旋光性的影响3 结 论以上的实验结果表明,旋光性聚酰胺可以由二元胺和二元酰氯采用不可逆的界面缩聚方法获得.所得聚酰胺的旋光方向与单体旋光方向没有必然的联系,它一方面取决于结构单元的构型,同时它更多地取决于聚合物在溶液中的空间构象.在不对称因素存在的条件下,聚合物结构的刚性愈强,构象稳定性愈好,则所得聚合物的旋光能力愈高.参 考 文 献1 Brig g s J C,Hodge P,Zha ng Z P.Asymm etric sy nthesis by reduc tio n o r by oxidatio n o f pro chiral substra tes ab-sor bed into chiral polymer suppo rts.React Poly m,1993,19(1,2):73~802 Ander sso n L I ,O 'Sha nnessy D J ,M o sbach K .M o lecu-la r r eco gnitio n in sy nthetic po ly mer s :pr epa ration of chi-ra l stationar y phases by molecular imprint of a mino acidamides.J Chro matog r ,1990,513:167~1793 Nishiyama I ,Go odby J W .Effect of po ly meriza tio n onthe stability of antifer ro elect ric liquid -cry sta lline phase:liquid-cr ystalline proper ties o f so me chir al acry la tes and their co r respo nding po lya cry lates.J M ater Chem,1993,3(2):169~1824 刘引烽,张荣群,章科健等.旋光性高分子的旋光能力(上).高分子通报,1995(3):159~1625 刘引烽,张荣群,章科健等.旋光性高分子的旋光能力(下).高分子通报,1995(4):220~226(上接137页)参 考 文 献1 吉 祥.谈谈我国钛白粉生产的现状及有关问题.中国涂料,1995(2):12~152 Kang Y S ,Risbud S ,Ra bo lt J F ,et al .Synthesis andcharac terization o f nanome ter-size Fe 3O 4a nd γ-Fe 2O 3par ticles.Chem Ma ter ,1996(8):2209~22113 M ac Do nald J .T ra nspa rent iro n oxides in coating s.Pig -ments ,1996(7):20~234 杨宗志.世界合成氧化铁颜料工业概况(Ⅱ).涂料工业,1995(2):27~315 黄平峰.我国合成氧化铁颜料生产现状及发展方向.无机盐工业,1996(6):13~166 华 彬,施利毅,施 卫等.生产钛白的副产物硫酸亚铁的精制研究.上海大学学报,1999,5(1):59~61·168· 上海大学学报(自然科学版) 第5卷。

黄铁矾废渣的综合利用①蓝元桢 钟福新 张 志(梧州师专生化系,广西 贺州 542800)[摘 要]本文阐述了用工业除铁排出的黄钠铁矾废渣与硫酸亚铁和氢氧化钠反应制取氧化铁黑和回收硫酸钠的工艺和操作方法。
为黄铁矾废渣的综合利用拓出新路。
[关键词]黄铁矾废渣;综合利用;氧化铁黑 在湿法冶金和化工生产中,当有较大量的铁需要除去时,目前多采用生成具有良好过滤性能的黄铁矾[M2Fe(SO4)4(O H)12,M =N a+、K+、N H+4]沉淀来代替传统的氢氧化铁除铁工艺。
然而用这种方法每除去1kg 的铁就有2.5~3.0kg的黄铁矾废渣的生成。
黄铁矾是N a+、K+、N H+4的硫酸盐与碱式硫酸铁的复盐,只是在pH值1.5~2.5的较强酸性条件下稳定,pH升高或受热就会水解或分解产生对环境有污染的物质。
因此大量的黄铁矾废渣如果不加以处理和利用而长期堆放,不仅占用地盘和浪费资源,还会在日晒雨淋等自然条件下发生化学变化而对环境造成污染。
所以在黄铁矾除铁工艺广泛利用的同时,对黄铁矾废渣的处理利用问题也应当引起重视。
本文就利用黄钠铁矾[N a2Fe (SO4)4(O H)12]废渣制取铁黑(Fe3O4)颜料及回收硫酸钠的工艺和操作方法进行探讨研究。
1 实验部分1.1 原料黄钠铁矾 某硫酸铜车间除铁废渣,净化后干品含铁32.3%。
硫酸亚铁 某钛白粉厂副产,含FeSO4 7H2O97.2%。
固体氢氧化钠 工业品级,从化工商店购买。
1.2 实验步骤硫酸亚铁溶于沸水,静置,过滤。
滤液倾入反应器,加入黄钠铁矾,搅拌,加热,逐滴加2m o l L-1N aO H溶液,控制pH值在4.5~5. 5范围,在80~90℃温度下反应约12h。
取样脱水与标准色相对比,相同(或相近)后停止反应。
倾出过0.043mm孔径湿筛,抽滤;水洗;烘干,粉碎得氧化铁黑产品。
滤液净化,浓缩,结晶,脱水得无水硫酸钠产品。
2 结果与讨论2.1 影响铁黑质量的因素2.1.1 黄钠铁矾的提纯黄钠铁矾的纯度是影响铁黑质量的重要因素。
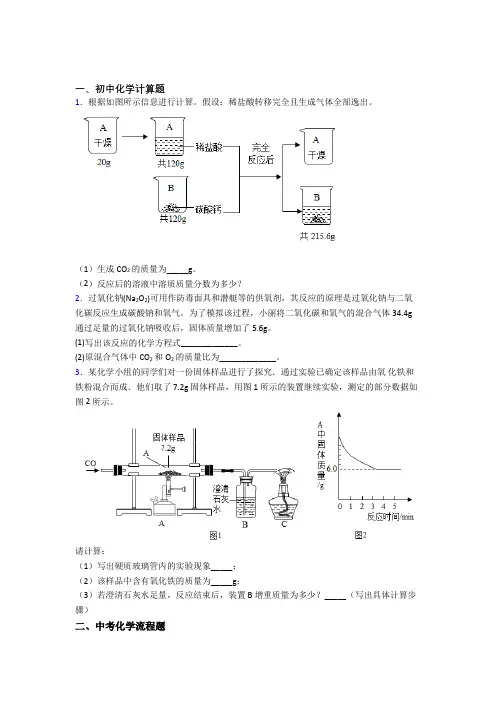
一、初中化学计算题1.根据如图所示信息进行计算。
假设:稀盐酸转移完全且生成气体全部逸出。
(1)生成CO2的质量为_____g。
(2)反应后的溶液中溶质质量分数为多少?2.过氧化钠(Na2O2)可用作防毒面具和潜艇等的供氧剂,其反应的原理是过氧化钠与二氧化碳反应生成碳酸钠和氧气。
为了模拟该过程,小丽将二氧化碳和氧气的混合气体34.4g 通过足量的过氧化钠吸收后,固体质量增加了5.6g。
(1)写出该反应的化学方程式_____________。
(2)原混合气体中CO2和O2的质量比为_____________。
3.某化学小组的同学们对一份固体样品进行了探究.通过实验已确定该样品由氧化铁和铁粉混合而成.他们取了 7.2g 固体样品,用图 1 所示的装置继续实验,测定的部分数据如图 2 所示。
请计算:(1)写出硬质玻璃管内的实验现象_____;(2)该样品中含有氧化铁的质量为_____g;(3)若澄清石灰水足量,反应结束后,装置 B 增重质量为多少?_____(写出具体计算步骤)二、中考化学流程题4.垃圾合理化回收利用可以减少污染,节约资源。
黄铁矿制硫酸会产生大量废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)可制备黄钠铁矾净水剂和高档颜料铁红(Fe2O3),其流程如图:已知:①“固体3”为黄钠铁矾,化学式为:NaFe3(SO4)2(OH)6。
②“溶液4”是含有Na+的可溶盐。
③通过调节pH范围可使某种金属沉淀。
下表是物质开始沉淀与沉淀完全的pH。
NaFe3(SO4)2(OH)6Fe(OH)3Mg(OH)2开始沉淀的pH 1.6 2.08.1沉淀完全的pH 1.8 3.29.4(1)NaFe3(SO4)2(OH)6中铁元素的化合价为______,为使铁元素以黄钠铁矾形式沉淀完全,步骤3调节pH的数值范围为______,溶液3中溶质的成分是______(任写一种)。
(2)“氧化”过程中,需要加入一种将Fe2+氧化为Fe3+的物质,工业上最好选用______。

黄钠铁矾除铁原理
嘿,朋友们!今天咱就来唠唠黄钠铁矾除铁原理。
你们知道吗,这黄钠铁矾就像是一个超厉害的“铁捕手”!
比如说,咱把含有铁的溶液当成是一个满是“小淘气铁离子”的大操场。
这些小淘气们到处乱跑,让我们很头疼。
但是黄钠铁矾一出现,哇塞,情况可就不一样啦!它就好像一个有魔力的大网,一下子就把那些小淘气铁离子给抓住啦,嘿,你说神奇不神奇!
它到底是怎么做到的呢?其实呀,黄钠铁矾有它独特的本事呢。
它能和铁离子结合在一起,形成一种稳定的化合物,就像是两个好朋友手牵手一样牢固。
这不就是像警察抓住小偷,给牢牢地铐起来一样嘛!然后呢,这些“铁小偷”就没办法再捣乱啦。
咱再仔细想想,在工业生产中,如果没有黄钠铁矾这个厉害的角色,那得有多少铁离子到处惹事呀!那生产出来的产品质量能好吗?哎呀呀,不敢想哦!
所以说呀,黄钠铁矾除铁原理可太重要啦!它就像是我们的大救星,帮我们解决了铁离子这个大麻烦。
让我们的工业生产能够顺顺利利地进行。
我
们可得好好感谢这个神奇的黄钠铁矾呀!说真的,要是没有它,咱还真不知道该怎么办呢!
观点结论:黄钠铁矾除铁原理非常重要且神奇,在工业生产等领域发挥着关键作用,值得我们深入了解和重视。

黄钠铁矾法从古至今,许多文献都提及了“黄钠铁矾法”。
据说,它来源于古代印度,发源于古代印度科学家索喇罗(Thalero)的研究。
索喇罗(Thalero)意识到,古代印度精英社会在日常生活中使用金属矿物来制作工艺品,如餐具、银饰及宝石。
这些矿物中最为有名的就是黄钠铁矾,它具有着独特的特性,能够赋予工艺品非凡的光彩,令之美丽可爱。
关于“黄钠铁矾法”的具体内容,可说是有三大步骤:第一步,以黄钠铁矾为原料,先用水磨碎成细小颗粒,再小心地筛选掉砂砾,并把它们放入烘炉,以网状状烧制成熔砂(熔铁);第二步,将熔砂(熔铁)放入坩埚中,大火烧制,以使之能够融入木炭;第三步,以金属块或其他器物,将木炭中的熔砂(熔铁)压缩成黄钠铁矾炉铁,然后再将其制成锻件。
在这个过程中,索喇罗(Thalero)透过操作促使黄钠铁矾中包含的元素完整性维持,以达至良好的金属制品品质。
而黄钠铁矾也因此被普遍应用于工艺品的制作之中,同时也用它来改善金属器物的易用性、耐久性等要素。
今日,黄钠铁矾仍被广泛应用于工艺品的制作之中。
比如,黄钠铁矾制品有可以经久耐用,表面富有光泽的金属碗,像是餐具、首饰等等。
此外,现代黄钠铁矾也被应用于船舶、工程机械的生产制造,而且经过科学技术的发展,现代黄钠铁矾制品的表面往往会被塑料覆盖以增强耐腐蚀性以及易维修性。
黄钠铁矾法的优点可说是极多,不仅可以获得高质量的金属制品,而且制作过程也比较安全,使用方便,而且可以节约材料。
尤其是在现代社会,黄钠铁矾法也在得到越来越多人的关注,已成为国际金属制品行业的重要成员。
因此,黄钠铁矾法早已成为现代金属行业的典范,它的重要性不言而喻。
总之,“黄钠铁矾法”历史悠久,具有多方面的优点。
它不仅体现了古代印度科学家索喇罗(Thalero)所开创的划时代的科学技术,也使得如今金属制品制作更加安全、效率更高,而且更加节能环保,可谓是印度古代科技的佳作。

摘要本文主要研究黄钠铁矾法回收电镀污泥中的有价金属的优化工艺流程以及采用固化方法处理在回收工艺过程中产生的废渣(浸出渣和净化渣)的最佳配方,并且提出废渣制砖的方案,不但要达到废渣无害化的目的,还要实现废渣资源化。
本试验研究的结果略述如下:①在回收有价金属试验中,铜的回收率达95%,镍的回收率达72%,铬的去除率达100%;②固化处理废渣的最佳配方是:废渣:水泥:砂:煤灰=1:2:1.67:0.3(本试验用的废渣由浸出渣与净化渣按质量比为2:1 混合而成),经浸出试验证明,固化体的浸出液中铜、镍、铬的含量符合GBA5085.3-1996 的浸出液毒性标准,浓度全部低于1.0mgL;③制砖最佳配方为:废渣:水泥:沙:煤灰=2.5:40:50:7.5(百分比),经测试,抗压强度达33.70MPa,可用于制造非承重墙体砖等。
关键词:电镀污泥黄钢铁矾法废渣固化制砖A Study on the Comprehensive Utilization andDisposal of Electroplating SludgeAbstractThe extraction of valued metals from the electroplating sludge is investigated using the Jarosite process in this paper.The best ratio of mixture used to solidify thewaste slag(includeing extraction slag and purification slag)which is produced after the extraction of valued metals is determined.A good program for brick formationusing the waste slagis obtained.Our investigation aims to recoverresources from the sludge and make the waste slag innocuous.The test results are concluded as 3 points as follows.First,in the extraction test,the recovery of Cu and Ni from the sludge is 95% and 72% respectively,and Cr in the sludge is removed completely.Second,the best ratio of solidification mixture is “slag:cement:sand:fly ash=1:2:1.67:0.3”,and the leach tests of solidified mixture prove that the leach efficiency of Cr can reach the GB5085.3-1996 toxicity standard set by the Government.Third,the best prescription for brick formation is “slag:cement:sand:fly ash=2.5:40:50:7.5(percentage ratio)”,whose compression strength reaches 33.70Mpa,in accordance to the strength standard of non-bearing partition.Key Words:electroplating sludge,Jarositeprocess,waste slag,solidification, brick formation第一章工艺流程概述一. 前言电镀污泥是使用化学方法处理电镀废水的必然产物,也是检验电镀厂是否有处理电镀废水的标志。