生物膜离子通道
- 格式:doc
- 大小:170.00 KB
- 文档页数:7

生物膜离子通道的研究进展生物膜是所有生物体中的重要组成部分,它包围着细胞和细胞器,起到保护和维持内外环境稳定的作用。
离子通道是生物膜中一类特殊的蛋白质,它们具有高度选择性和通透性,能够帮助离子在细胞膜上通过膜层。
由于它们对神经传递、肌肉收缩和能量代谢等生理过程发挥着至关重要的作用,离子通道成为生命科学中一个备受研究的重点。
近年来,生物膜离子通道的研究得到了飞速的发展。
科学家们通过统计方法和生物物理学手段,在离子通道蛋白质的三维结构、物理化学特性、功能及调控等方面取得了许多进展。
下面将分别从这几个方面展开介绍。
1. 三维结构研究随着X射线晶体学和电镜技术等的进步,生物膜离子通道的三维结构逐渐被揭示。
2003年,科学家们首次将人类离子通道超家族(superfamily of ion channels)的核糖体膜蛋白1(Rhomboid protease)的结构解析出来,从而揭露了一类新型膜蛋白质在细胞内切割调节中的结构和功能。
此外,更为复杂的离子通道如钠通道、钾通道、钙通道、氯离子通道等的结构也得到了不断深入的研究。
科学家们可以通过这些结构信息,更深入地理解离子通道的通透性、选择性和调控机制,为药物的设计和诊断工具的开发提供了更为丰富的信息。
2. 物理化学特性研究离子通道的物理化学特性研究是生物物理学的重要研究方向,通过这种方式可以探究离子通道的电学、热学、机械学、光学等特性。
科学家们运用单通道电生理学技术、黑膜技术和热力学等手段,研究了离子通道的开放/封闭动力学和稳态行为,发现了许多新奇的特性,如离子通道的分子动态行为、选择性和通透性调节、离子通道蛋白质与其他蛋白质的相互作用等。
通过这些研究,人们可以进一步理解离子通道蛋白质的构象和活性。
3. 功能研究离子通道在维持细胞功能和健康方面发挥着重要作用,因此离子通道的功能研究一直是生物科学的热门领域之一。
离子通道的功能与其调控及与其他蛋白质的相互作用密切相关,可以通过特定的信号通路激活或者关闭离子通道,进而影响其离子流通和细胞的活动。
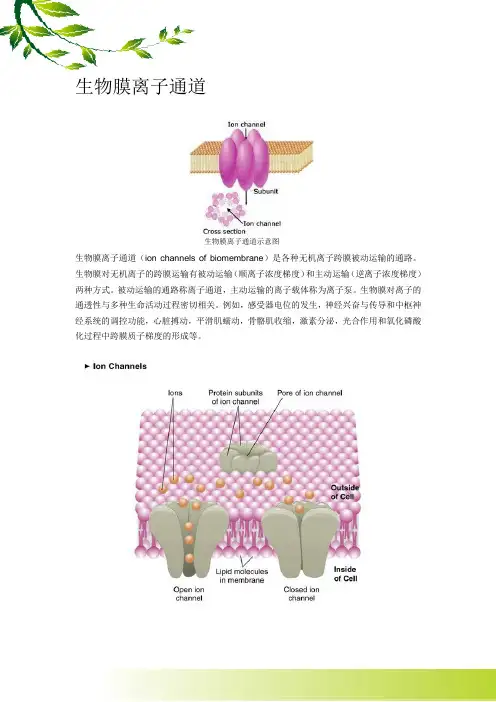
生物膜离子通道生物膜离子通道示意图生物膜离子通道(ion channels of biomembrane)是各种无机离子跨膜被动运输的通路。
生物膜对无机离子的跨膜运输有被动运输(顺离子浓度梯度)和主动运输(逆离子浓度梯度)两种方式。
被动运输的通路称离子通道,主动运输的离子载体称为离子泵。
生物膜对离子的通透性与多种生命活动过程密切相关。
例如,感受器电位的发生,神经兴奋与传导和中枢神经系统的调控功能,心脏搏动,平滑肌蠕动,骨骼肌收缩,激素分泌,光合作用和氧化磷酸化过程中跨膜质子梯度的形成等。
细胞膜离子通道细胞膜上离子通道的功能,除了可以调节细胞内外的渗透压,也是维持细胞膜电位的重要分子,而神经细胞要进行讯号传导,便是靠离子的进出以造成膜电位的变化。
虽然科学家对于细胞膜上离子通道已有相当程度的了解,对于离子通道所具有的特殊选择性,也从能蛋白质的结构大略获得解释,但是一直缺乏一套完整详细的分子作用机制。
原因是,要做出膜蛋白三维结构的高解析度影像,非常不容易。
1998年,麦金农做出了链霉菌的离子通道蛋白质KcsA的高解析三维结构影像,并首度从原子层次去了解离子通道的作用方式。
KcsA离子通道中有一种“滤嘴”,能让钾离子(K+)通过,却不允许同族元素中体积更小的钠离子(Na+)通过,这令科学家百思不得其解。
但是麦金农根据KcsA的立体结构,发现离子通道中“滤嘴”边上的四个氧原子的位置,恰好跟钾离子在水溶液中的情况一样,亦即滤嘴边上的氧与水分子的氧距离相同,所以钾离子能够安然通过通道,一如在水中一样;但钠离子尺寸较小,无法顺利接上滤嘴边上的四个氧原子,因此只能留在水溶液,而无法轻易穿过通道。
而离子通道的开关会受到细胞的控制,麦金农发现,离子通道的底部有个闸门,当离子通道接收到特定的讯号,离子通道蛋白质结构便会发生改变,因此造成闸门的开关。
麦金农对于钾离子通道的结构与作用机制的研究,是生物化学、生物物理等领域的一大突破,也为神经疾病、肌肉与心脏疾病的新药物开发,指引了新的方向。

细胞生理学中的离子通道和受体分析细胞生理学是研究细胞在生物体内活动的科学,它关注细胞内分子机制的生理学过程,包括细胞内信号传导、代谢、分化和细胞周期等方面。
其中,离子通道和受体分析是细胞生理学研究的重要方向。
离子通道是细胞生物膜上的特殊蛋白分子,它可以通过调节离子进出细胞,起到调控细胞电位、钙离子浓度等生理过程的作用。
离子通道可以分为离子选择性通道和非选择性通道两种类型。
离子选择性通道是指只允许某种类型的离子通过的通道,例如钙离子通道、钾离子通道等;而非选择性通道则是所有离子都可以通过的通道,例如Na+/K+通道。
离子通道的活性可以受到多种信号的调控,包括电压、配体结合、细胞内信号分子等。
电压依赖型离子通道是最常见的一种离子通道,它的活性是以细胞膜的电势变化为基础。
例如,钾离子通道的活性是受到细胞内的钾离子浓度和膜电位的调控。
当细胞内的钾离子浓度增加或细胞膜电位降低时,钾离子通道会打开,允许更多的钾离子进入细胞。
这一过程是神经元兴奋性传导的基础,也被应用于药物研发和治疗中。
另一方面,配体依赖型离子通道则是受到配体分子结合的调控。
例如,神经递质乙酰胆碱能够结合到肌肉细胞上的乙酰胆碱受体,从而激活钠离子通道,使神经信号传导到肌肉细胞中。
因此,阻断乙酰胆碱受体的结合或阻止钠离子通道的活性,可以用于肌肉松弛等疾病的治疗。
与离子通道不同,受体则是细胞表面蛋白分子,它可以接受外界信号分子的结合,从而引起细胞内的信号转导。
受体主要分为离子通道受体和酪氨酸激酶受体两种类型。
离子通道受体是指通过配体分子结合来调节离子通道活性的受体,例如NMDA受体,是钙离子通道受体中最复杂的一种。
它不仅可以与谷氨酸结合来调节钙离子通道活性,还可以与多种信号分子相互作用,调节神经元发育、突触可塑性等方面。
酪氨酸激酶受体则是受到酪氨酸激酶酶活性调控的受体,例如胰岛素受体、生长因子受体等。
这些受体可以促进细胞增殖、分化等生理活动,也可以通过突变或异常表达导致癌症等疾病的发生。

初二生物离子通道类型与功能离子通道是细胞膜上负责调节离子传输的重要结构。
它们根据离子选择性、结构特征和调节方式的不同,被分为多种类型,并具有不同的功能。
本文将探讨常见的离子通道类型及其功能。
1. 钠离子通道(Sodium ion channels)钠离子通道是一种在细胞膜上调节钠离子进出的通道。
它们分为电压门控钠离子通道、配体门控钠离子通道和补偿钠离子通道。
电压门控钠离子通道是一类电位依赖性通道,可以感知细胞膜电位的变化并调节钠离子的通透性。
这种通道在动作电位的生成和传导过程中起着重要作用。
配体门控钠离子通道受到细胞外信号分子的结合而开启或关闭。
例如,神经递质乙酰胆碱能够与乙酰胆碱受体结合,导致钠离子通道开启,进而触发神经冲动的传导。
补偿钠离子通道是一类在细胞溶酶体膜上起到离子平衡的作用。
它们保持细胞内外的钠离子浓度差异,维持正常的细胞功能。
2. 钾离子通道(Potassium ion channels)钾离子通道是一类控制细胞内外钾离子平衡的通道。
同样,它们可以分为电压门控钾离子通道和配体门控钾离子通道。
电压门控钾离子通道具有钠离子通道相似的电位依赖性特点,但通透性不同。
在神经细胞中,钾离子通道在动作电位的复极过程中扮演关键角色。
配体门控钾离子通道受到分子信号的调控,例如细胞外钾离子浓度的变化或细胞外神经递质的结合。
这类通道在细胞兴奋性调节中起到调节作用,维持细胞内外离子浓度的平衡。
3. 钙离子通道(Calcium ion channels)钙离子通道是一类控制细胞内外钙离子浓度的通道。
它们有许多亚型,包括电压门控钙离子通道、配体门控钙离子通道和补偿钙离子通道。
电压门控钙离子通道在神经和心肌细胞中起到调节电位和信号转导的作用。
当细胞膜产生电位变化时,这种通道会调节钙离子的通透性,从而触发细胞内的信号级联反应。
配体门控钙离子通道受到细胞外配体结合而开启或关闭。
这类通道在神经递质释放和神经元之间的突触传递中起到调节作用。

生物膜中的离子通道与传输机制生物膜是细胞外与细胞内环境之间的物理隔离屏障,对细胞内外物质交换起着重要的作用。
生物膜由磷脂双层以及膜蛋白等多种分子构成,其中离子通道是生物膜中的重要成分之一。
离子通道可以让离子定向地穿越膜,保证了细胞内外的离子浓度差,维持了正常的细胞生理活动。
本文将从离子通道的发现历程、分类及传输机制三个方面,介绍生物膜中的离子通道。
一、离子通道的发现历程早在20世纪50年代,科学家就已经意识到细胞膜是具有选择通透性的物质屏障,但对离子的穿透机制却不甚了解。
1960年代初期,Hodgkin和Huxley对神经元膜电位的研究首次提出了离子通道的概念。
他们通过电生理技术,观察到了离子通道的存在,并系统地研究了通过离子通道的钠离子、钾离子等离子体系的穿透机制。
这项工作为细胞膜电位的传递机制提供了新的认识。
随后,生物学家们不断地发掘各种类型的离子通道。
通过逐一研究它们的通透性、特异性和调节机制等特征,科学家们已经发现了许多种不同类型的离子通道。
二、离子通道的分类根据离子通道的特异性和调控机制,可以将其分为多种类型。
其中,最常见的包括压力调节离子通道、电压门控离子通道、化学门控离子通道、内源锁定离子通道和非门控离子通道等。
这些离子通道有分布在细胞膜内部的学名叫做内向型离子通道;有限制细胞外离子到达细胞内的外向型离子通道;还有分布在细胞内膜的可协同作用的离子通道。
这些不同类型的离子通道的作用可相互协调,维持正常生理活动。
三、离子通道的传输机制离子通道的传输机制是指不同类型、不同调节机制的离子通道穿越细胞膜的方式。
离子通道的传输机制和其类型密切相关。
压力调节离子通道是一种通过压力甚至物理变化进行开关操作的离子通道。
细菌及植物细胞膜上的压力调节离子通道就是通过物理变化感受细胞膜的机械变化,并通过特定的门控机制来让离子定向地穿透膜。
相比之下,电压门控离子通道和化学门控离子通道是通过细胞内外环境的电势或化学信号作为触发信号,在离子通道上开启或关闭,从而把离子从一侧传递到另一侧。

生物物理学中的离子通道生物物理学是一个研究生命体系科学的分支,其中离子通道是一个极为重要的研究领域。
离子通道指的是一种具有通透性的膜蛋白,能够调节细胞膜电位和离子浓度,以维持生物体的正常生理状态。
本文将从离子通道的结构、功能和应用等方面进行讨论。
一、离子通道的结构离子通道主要分为两类:电压门控离子通道和配体门控离子通道。
其中,电压门控离子通道是以细胞内部和外部的电压作为信号控制其开启和关闭,而配体门控离子通道则是通过与某种特定分子的结合来调节其开放状态。
离子通道的结构包括两个主要的部分:孔道和门。
孔道指离子通道内部留下的空隙,门则是其控制开启和关闭的部分。
一般来说,孔道是由多个膜蛋白单体组成的,这些单体之间通过膜蛋白间连,形成一个大的空间。
门则是由离子通道蛋白质的不同结构特征组成的,包括螺旋、β折叠、外环及其它结构。
二、离子通道的功能离子通道的功能十分重要,其具有以下几个方面:1.调节细胞膜电位离子通道能够增加或减少细胞膜的电位,辅助神经细胞或肌肉细胞产生动作电位或肌动蛋白等运动蛋白的收缩。
2.调节离子浓度通过离子通道,细胞可以调节不同离子(如钠、钾、钙等)的浓度,以保持正常生理环境。
3.调控细胞分化和增殖近期研究表明,离子通道不仅可以改变细胞膜电势,也可能参与细胞分化和增殖的过程。
4.参与信号传导过程离子通道能够传导化学或电信号,从而形成神经或组织间的信号传递。
三、离子通道的应用由于离子通道在细胞内的重要作用,其研究应用十分广泛。
以下是其中几个例子:1.立体定向放射治疗颅内肿瘤离子通道的电生理性质让它在放射治疗方面具有潜在的优势。
通过改变跨膜电势,能够有效地调控肿瘤细胞的生长和凋亡,达到治疗目的。
2.开发治疗神经退行性疾病的新型药物神经退行性疾病(如阿尔茨海默病等)的治疗还处在研究阶段,而离子通道则被证实在神经传导方面具有重要的作用,因此,通过合成新型药物来调控离子通道的活性,被认为是缓解神经退行性疾病的可行方案。

生物体内离子通道的结构与机制离子通道是一种重要的生物分子,它们能够在生物体内调节离子的流动,从而影响神经传导、肌肉收缩、内分泌和代谢等生命活动。
离子通道广泛存在于细胞膜上,以不同的方式调节离子的通透性,包括电压门控通道、配体门控通道、机械门控通道等。
本文将重点探讨离子通道的结构与机制。
1. 离子通道的结构离子通道是由蛋白质组成的,其主要结构包括跨膜螺旋、内环、外环、膜域等四部分。
其中跨膜螺旋是离子通道最为基本的结构,它主要由多个膜螺旋结构组成,并通过水分子形成离子通道的中心孔道。
内环和外环则分别位于离子通道的内外侧,它们起到调节离子通道开关的作用,可以是电压门控或配体门控。
膜域则是离子通道膜螺旋的一部分,使离子通道嵌入细胞膜并稳定其位置。
另外,离子通道的膜螺旋通常具有数个不同的氨基酸残基。
这些残基对于离子的选择性、传导能力和门控特性都至关重要。
在电压门控通道中,某些氨基酸残基通过改变电场分布来影响通道的开放和关闭;在配体门控通道中,则是特定的信号分子与通道结合,从而导致通道的开放和闭合。
2. 离子通道的机制离子通道的机制广泛应用于生理学和药理学研究中。
离子通道的开放和关闭是通过不同的机制实现的。
其中,电压门控通道的开放和关闭受到细胞膜电位的控制,当细胞膜内外电位差达到一定程度时,离子通道发生构象变化从而开放或关闭。
配体门控通道则是通过特定的信号分子在离子通道上的作用来控制它们的开放和关闭。
离子通道的选择性是指不同通道具有不同的离子选择性。
这是由于离子通道中的氨基酸残基对离子的尺寸和电荷具有不同的偏好性造成的。
大多数离子通道通过尺寸选择性来排除过大或过小的离子,而电荷选择性则由离子通道的环境和残基之间的相互作用决定。
另外,离子通道的通道倍数也是其重要特征之一。
许多离子通道形成多个具有相同结构和功能的倍体,从而增加了离子通道的通透性和灵敏性。
例如,钠离子通道常常是四个亚基构成的四面体结构,而钙离子通道则是膜上两个钙离子通道蛋白结构相互缠结的形式。

离子通道的工作原理
离子通道是细胞膜上的一类疏水膜蛋白,具有亲水孔道,能够选择性通透不同离子,如K+、Na+、Ca2+、Cl-等。
它们的工作原理主要依赖于跨膜电位的变化。
当离子通道打开时,不同离子会根据其浓度差和电位差通过通道进行移动。
这一过程是由细胞膜内外带电离子的浓度差驱动的。
一旦在细胞膜内外创造出带电离子的浓度差,电位差产生的电场力就可以瞬间驱动离子运动。
不同类型的离子通道对膜电位的变化有不同的反应。
例如,电压门控离子通道的孔道开放与关闭受细胞膜两边的膜电位调节,去极化(膜内电压高于膜外电压)或超极化(膜外电压高于膜内电压)可以调节不同离子通道的开放和关闭。
在神经细胞中,离子通道的开闭影响跨膜电位的变化,从而影响神经信号的传递速度。
例如,钾离子通道的开放有助于钾离子的外流,降低膜电位,而钠离子通道的开放则有助于钠离子的内流,增加膜电位。
这些离子的移动会在很短的时间内引起电信号的变化,进而实现快速神经传导。
综上所述,离子通道通过选择性通透不同离子来实现对细胞膜内外离子平衡的调节,对神经传导、肌肉收缩等生理过程起着关键作用。
如需更具体的信息,建议阅读生物科学类文献或请教专业人士。



生物离子通道的结构与功能解析生物离子通道是一种特殊的蛋白质结构,它们能够存在于生物膜的各种类型的细胞中,并且起着在细胞内外离子流动方面的极其重要的作用。
离子通道是通过微小的氨基酸夹紧和、电静力作用而产生空间内部的结构,从而使得跨过细胞膜的离子具有极大的选择性,能够对钠和钾等重要离子进行高效甄别,并促进它们在细胞膜上进行流动。
在本文中,我们将探讨生物离子通道的结构和功能,并分析它们如何为我们提供重要的细胞活动支持。
生物离子通道的结构生物离子通道的结构紧密包含蛋白质中的单个或多个氨基酸残基。
在这些残基中,某些会在离子通道膜中构成一定结构,从而形成了极为有序的通道。
这些有序的通道产生了一系列微小的楔形缺口,这些缺口可以被钠、钾和其他离子选择性地辨识和选择。
在离子通道的选择性方面,这些性质与蛋白质的生物化学性质和晶体学性质有关。
在许多例子中,生物离子通道通过调节将细胞中的C离子(正离子)和An离子(负离子)分开来实现选择。
这些通道通常由离子选择性滤器(pore)引导,滤器中的亲水氨基酸残基天然地与离子相互作用。
此外,离子通道的形态特点还决定了区分多种不同离子的空间构象详见的特殊能力,并根据缺口大小确定了离子向细胞外或细胞内的转移速率。
离子通道的功能离子通道在多种生物过程中扮演着至关重要的角色。
通过调节细胞内和外部的K或Na等离子浓度,离子通道为神经和肌肉细胞提供了极为关键的细胞活动支持。
例如,钠通道与神经细胞的作用不仅仅是在干扰信号传导方面,它还能够调节细胞内外的离子平衡,从而控制细胞膜激活和抑制状态的产生。
另一方面,钾通道可通过调节细胞内的离子流动以控制人体水分平衡,维持心肌功能,对一系列神经调节发挥重要作用。
这些通道可以透过许多影响细胞动力学、代谢调节和信号传导的因素,例如调节细胞内外环境、激活信号以及药物和生理作用等。
离子通道研究进展目前,离子通道的研究仍处于快速发展阶段。
离子通道细胞学的研究是非常有价值的,它能够显示带有不同离子的分离效应以及介导细胞的异常外流等生理过程。
动植物细胞膜离子通道的结构和功能动植物细胞膜离子通道是维持细胞内外正常物质交换的重要机制。
细胞膜是由磷脂双分子层和包围其外侧的蛋白质组成的,离子通道则是由蛋白质形成的。
这些蛋白质能够穿过细胞膜,形成离子通道,让特定类型的离子在细胞膜上形成一定的流动。
因此,离子通道对于细胞内外环境的调节至关重要。
在细胞膜上,离子通道的结构分为两种类型:膜蛋白和离子通道蛋白。
其中,膜蛋白以α螺旋结构为主,通道中心内侧是亲水的氨基酸侧链,而通道周围则与脂质双层相容,保证通道的特异性和选择性。
离子通道蛋白则通常为跨膜蛋白,通过一个或数个膜螺旋形成通道。
这些离子通道的结构使得其具有很高的选择性。
离子通过通道时,首先需要符合通道宽度和几何形状的要求。
此外,通道内还存在能够相互作用的小分子,如阻止钾离子通过的鸟嘌呤核苷酸。
这些作用力的综合作用使离子通道仅能传递特定种类的离子。
例如,钠通道可以传递钠离子,但不能传递氯离子。
钾通道则仅能传递钾离子,但不能传递钠离子。
这种选择性非常重要,因为它能够使细胞针对不同的离子浓度梯度进行调节。
同时,离子通道还能够受到许多生化物质的调节,从而进一步增强其功能。
例如,神经元的钠通道和钾通道会随着细胞膜电位的变化而打开或关闭。
而某些离子通道,如钙通道,则可以通过配体或细胞中的第二信使(如cAMP或cGMP)来调节。
这些作用机制的存在使得细胞膜离子通道能够在复杂的细胞生理学过程中发挥重要作用,如神经传递和肌肉收缩。
在动植物细胞中,离子通道的分布、类型和数量都存在着显著差异。
例如,在动物细胞中,钠、钾和钙都有对应的通道,但在植物细胞中只有氟离子通道。
植物细胞的离子交换机制主要是通过离子转运蛋白完成的。
总体而言,动植物细胞膜离子通道的多样性和复杂性使其在细胞内外物质交换和细胞生理学中发挥着重要的作用。
离子通道的选择性、调节和分布不仅能够维持细胞内外环境的稳定,而且能够支持许多细胞生理学过程,并为药物研发提供重要的靶标。
一.名词解释1.胞间连丝:是指贯穿细胞壁、胞间层,连接相邻细胞原生质体的管状通道。
2.温周期现象与光周期现象:在自然条件下气温是呈周期性变化的,许多生物适应温度的某种节律性变化,并通过遗传成为其生物学特性,这一现象称为温周期现象。
生物在暴露于阳光期间对变化产生的反应,尤指通过生物过程显示出来的反应称光周期现象。
3.质壁分离与质壁分离复原:如果把具有液泡的细胞置于水势较低的溶液中,液泡失水,细胞收缩,体积变小。
由于细胞壁的伸缩性有限,而原生质体的伸缩性较大,随着细胞继续失水,原生质层便和细胞壁分离开来,这种现象被称为质壁分离。
如果把发生了质壁分离的细胞浸在水势较高的稀溶液或清水中,外液中的水分又会进入细胞,液泡变大,整个原生质层很快会恢复原来的状态,重新与细胞壁想贴,这种现象称为质壁分离复原。
4.根系的主动吸水与被动吸水:由根系代谢活动而引起的根系吸水过程称为主动吸水。
由蒸腾拉力引起的根系吸水称为被动吸水。
5.植物的水分临界期与最大需水期:指植物在生命周期中对水分最敏感、最易受伤害的时期。
一般而言,植物水分临界期多处于花粉母细胞四分体形成期,此时若缺水,使性器官发育不正常。
植物的最大需水期指植物生活周期中需水最多的时期。
6.大量元素与微量元素:植物生命活动必需的、且需要量较多的一些元素,它们约占植物体干重的0.01-10%,有C、H、O、N、P、S、K、Ga、Mg等9种元素。
植物生命活动必需的、而需要量很少的一类元素。
它们约占植物体干重的10(-5)-10(-3)%,有Fe、Mn、Zn、Cu、B、Mo、Cl等。
7.RuBP羧化酶与PEP羧化酶:核酮糖二磷酸羧化酶,催化1,5-二磷酸核酮糖和CO2生成二分子甘-3-磷酸甘油酸反应的酶。
亦称羧基歧化酶。
催化以磷酸烯醇型丙酮酸为底物,固定CO2形成草酰乙酸的酶,简称PEP羧化酶8.CO2饱和点与CO2补偿点:光合速率随CO2浓度增高而增加,当光合速率达到最大值时CO2浓度即为CO2饱和点。
1.1 生物膜早期研究离子通道的早期研究主要来源于电生理学研究。
早在1890 年, 德国的物理化学家Wilhelm Ostwald(1909 年诺贝尔化学奖获得者),基于人工合成的胶质膜实验,提出活细胞产生的电信号可使离子在细胞中穿梭理论。
到了1900年,他的这种电化学思想才被认可,后来研究表明,膜电位本质上是电化学。
到了上世纪初期(1902-1912年)伯恩斯坦(J.Betnstein,1902)最先提出“膜学说”并用此解释生物电的产生。
他认为静息时细胞膜只对钾离子有通透性,由于细胞内外钾离子浓度不同,因此两侧出现内负外正的电位差。
当细胞受到刺激而兴奋时,细胞膜暂时失去对离子的选择性,所有离子都能通过,因此,膜两侧的电位差暂时消失。
到了1925年,Michaelis 提出可能存在窄离子通道。
在早期膜生物物理研究阶段,兴奋膜离子理论从未经试验验证的假说发展成为公认的理论,这一时期的主要贡献在于确定生物点活动与离子通透性的关系,但尚未明确建立离子通道的概念。
1.2 离子通道经典研究时期在1950-1960期间,两位英国科学家Hodgkin 和Huxley,基于乌贼大轴突为材料作的生理实验,使用电压钳位技术,证实跨膜电位决定于细胞膜的离子通透性,从而对钾、钠离子通透性变化作了详细的分析并提出著名的“Na+,K+双通道模型”和离子学说。
Hodgkin 和Huxley 的离子学说解释了生物电的起源。
他们也因此共同获得1963 年的诺贝尔生物医学奖。
到了1965-1975年:Hille 基于药理学的方法,研究钠钾通道结构以及选择性通透机制,同时Armstrong基于有关肌肉兴奋收缩偶联的实验,研究门控与膜电压之间的关系。
俩人皆因对离子通道选择通透性及门控机制的突出研究贡献共同获1999年拉斯克医学奖。
这一时期是离子通道的经典研究时期,离子通道模型的建立以及通道选择性和通透性机制的研究都有了很大突破,为离子通道的进一步飞跃发展研究做了很好的铺垫。
生物膜上离子通道的电生理学特性生物膜是细胞内外的一个重要屏障,对维持细胞内外环境的稳定性和调节细胞外和内物质的交换具有重要意义。
膜上离子通道作为维持细胞内外环境平衡的主要机制之一,具有重要的生理和病理功能。
离子通道可以通过信号转导、维持细胞电位稳定性、维持细胞内外离子浓度平衡以及调节神经肌肉兴奋等多种生理功能,在多种疾病中的功能异常会导致疾病的发生和发展。
因此,分子生物学、细胞生物学和生物物理学等多个学科对离子通道的研究逐渐深入。
离子通道的特性包括电学本性、氧化还原敏感性、细胞信号转导的作用以及参与疾病等多方面的特性。
其中,电生理学特性是离子通道研究中最基本和重要的特性之一。
下面,我们就来探讨生物膜上离子通道的电生理学特性。
1. 感受器电压门控机制生物膜上离子通道的电生理学最突出的特点之一是感受器门控机制。
这种机制是指离子通道的开放状态受到细胞膜内外电场分布的影响。
因此,这种开关机制是离子通道的一个特殊功能,可被用于细胞膜的神经和肌肉细胞的调节。
感受器电压门控通道是目前发现的最多的离子通道类型。
这种类型的通道有两个感受器作为门控,分别处于通道的内部和外部,内外两者间相距不超过0.33纳米。
当神经脉冲到达细胞膜时,产生的电场可以使得感受器发生构象变化,从而改变离子通道的开放状态。
这样的机制使得离子通道能快速响应外界的刺激,起到紧急反应的作用。
2. 离子选择性离子选性是离子通道的另一个重要电生理学特性,是指离子通道在不同类型的离子之间有不同的选择性。
离子通道是区分离子种类的主要机制,其精准度对于细胞内外环境成分的调节具有重要意义。
离子通道的选择性取决于其结构和特定氨基酸残基的构成。
那些在通道内侧和外侧共同积累的氨基酸残基为其具有特定的选择性。
所以大多数离子通道均能分辨不同类型的离子,如钠、钾、氯等。
这样的选择性机制能够维持细胞膜上离子的平衡,帮助细胞保持正常的生理功能。
3. 原位记录技术生物膜上离子通道的研究需要离子通道的原位记录技术。
离子通道在细胞功能调节中的作用细胞是生物体最基本的结构单元。
通过细胞内各种化学反应的发生,维持着生物体内稳定有序的运转。
而这些化学反应能够顺利进行的前提,就是需要保持细胞内外环境的电位平衡和离子浓度平衡。
而这些平衡状态,依赖于细胞膜上的离子通道。
本文将从离子通道的定义、类型、电势依赖性以及功能等方面,来介绍离子通道在细胞功能调节中的作用。
一、离子通道的定义和类型细胞膜上存在大量的蛋白质通道,可以让离子在细胞膜两侧之间进行转运。
而离子通道则是一种具有高度特异性的通道蛋白。
通道蛋白是由完全足够的氨基酸序列形成的一个或多个亚单位的超大分子。
离子通道分为离子选择性通道和非选择性通道两类。
离子选择性通道根据通过通道的离子类型,又可分为钾通道、钠通道、钙通道等。
非选择性通道则包括压敏离子通道和氨基酸敏感离子通道等。
压敏离子通道因其响应机制与压力有关,被广泛应用于传感和机械感受领域。
而氨基酸敏感离子通道因其响应机制与氨基酸结合有关,主要参与感觉系统的功能调节。
二、离子通道的电势依赖性离子通道能够实现离子的选择性导通,是因为其对于特定离子具有较高的亲和力。
而在细胞内外环境之间存在一定的电势差,采用正电荷离子如钠离子从高电势端向低电势端运动,采用负电荷离子如钾离子则相反。
因此,离子通道的开放和关闭与细胞膜电势状态密切相关,称为电势依赖性。
离子通道的电势依赖性和离子选择性,是细胞内外环境之间进行离子转运的决定性因素。
细胞膜电位的变化可以导致离子通道的状态发生改变,这种状态改变对离子浓度的控制起到了重要的作用。
三、离子通道在细胞功能调节中的作用十分重要。
细胞膜上的离子通道不仅负责实现细胞内外环境的电位平衡和离子浓度平衡,而且也直接参与了细胞内信号的传递和细胞膜上的各种膜电位变化。
细胞在代谢过程中,会产生一些物质,这些物质可以扮演的信号分子,使细胞膜上的离子通道开放和关闭,传递相关的信号信息。
此外,离子通道也参与到神经传递中。
生物膜离子通道生物膜离子通道示意图生物膜离子通道(ion channels of biomembrane)是各种无机离子跨膜被动运输的通路。
生物膜对无机离子的跨膜运输有被动运输(顺离子浓度梯度)和主动运输(逆离子浓度梯度)两种方式。
被动运输的通路称离子通道,主动运输的离子载体称为离子泵。
生物膜对离子的通透性与多种生命活动过程密切相关。
例如,感受器电位的发生,神经兴奋与传导和中枢神经系统的调控功能,心脏搏动,平滑肌蠕动,骨骼肌收缩,激素分泌,光合作用和氧化磷酸化过程中跨膜质子梯度的形成等。
细胞膜离子通道细胞膜上离子通道的功能,除了可以调节细胞内外的渗透压,也是维持细胞膜电位的重要分子,而神经细胞要进行讯号传导,便是靠离子的进出以造成膜电位的变化。
虽然科学家对于细胞膜上离子通道已有相当程度的了解,对于离子通道所具有的特殊选择性,也从能蛋白质的结构大略获得解释,但是一直缺乏一套完整详细的分子作用机制。
原因是,要做出膜蛋白三维结构的高解析度影像,非常不容易。
1998年,麦金农做出了链霉菌的离子通道蛋白质KcsA的高解析三维结构影像,并首度从原子层次去了解离子通道的作用方式。
KcsA离子通道中有一种“滤嘴”,能让钾离子(K+)通过,却不允许同族元素中体积更小的钠离子(Na+)通过,这令科学家百思不得其解。
但是麦金农根据KcsA的立体结构,发现离子通道中“滤嘴”边上的四个氧原子的位置,恰好跟钾离子在水溶液中的情况一样,亦即滤嘴边上的氧与水分子的氧距离相同,所以钾离子能够安然通过通道,一如在水中一样;但钠离子尺寸较小,无法顺利接上滤嘴边上的四个氧原子,因此只能留在水溶液,而无法轻易穿过通道。
而离子通道的开关会受到细胞的控制,麦金农发现,离子通道的底部有个闸门,当离子通道接收到特定的讯号,离子通道蛋白质结构便会发生改变,因此造成闸门的开关。
麦金农对于钾离子通道的结构与作用机制的研究,是生物化学、生物物理等领域的一大突破,也为神经疾病、肌肉与心脏疾病的新药物开发,指引了新的方向。
离子通道蛋白和载体蛋白的异同相同点:化学本质均为蛋白质、分布均在细胞的膜结构中、都有控制特定物质跨膜运输的功能不同点:1.通道蛋白参与的只是被动运输,在运输过程中并不与被运输的分子结合,也不会移动,并且是从高浓度向低浓度运输,所以运输时不消耗能量。
2.载体蛋白参与的有主动运输和协助扩散,在运输过程中与相应的分子结合,并且会移动。
在主动运输过程中由低浓度侧向高浓度运动,且消耗代谢能量;在协助扩散过程中,由高浓度侧向低浓度侧运动,不消耗代谢能。
(注;协助扩散也属于被动运输)被动运输科技名词定义中文名称:被动运输英文名称:passive transport其他名称:被动转运定义:离子或小分子在浓度差或电位差的驱动下顺电化学梯度穿膜的运输方式。
所属学科:细胞生物学(一级学科);细胞生理(二级学科)本内容由全国科学技术名词审定委员会审定公布目录1被动运输一、简单扩散1二、协助扩散1体蛋白主要有离子载体和通道蛋白两种类型(一)离子载体1(二)通道蛋白门通道可以分为四类(图5-4):1图5-4 各类离子通道1、配体门通道12、电位门通道13、环核苷酸门通道14、机械门通道15、水通道分类展开编辑本段被动运输一、简单扩散自由扩散也叫自由扩散(free diffusing),特点是:①沿浓度梯度(或电化学梯度)扩散;②不需要提供能量;③没有膜蛋白的协助。
某种物质对膜的通透性(P)可以根据它在油和水中的分配系数(K)及其扩散系数(D)来计算:P=KD/t,t为膜的厚度。
脂溶性越高通透性越大,水溶性越高通透性越小;非极性分子比极性容易透过,小分子比大分子容易透过。
具有极性的水分子容易透过是因水分子小,可通过由膜脂运动而产生的间隙。
非极性的小分子如O2、CO2、N2可以很快透过脂双层,不带电荷的极性小分子,如水、尿素、甘油等也可以透过人工脂双层,尽管速度较慢,分子量略大一点的葡萄糖、蔗糖则很难透过,而膜对带电荷的物质如:H+、Na+、K+、Cl—、HCO3—是高度不通透的事实上细胞的物质转运过程中,透过脂双层的简单扩散现象很少,绝大多数情况下,物质是通过载体或者通道来转运的。
离子、葡萄糖、核苷酸等物质有的是通过质膜上的运输蛋白的协助,按浓度梯度扩散进入质膜的,有的则是通过主动运输的方式进行转运。
主动运输二、协助扩散也称促进扩散(faciliatied diffusion),其运输特点是:①比自由扩散转运速率高;②存在最大转运速率;在一定限度内运输速率同物质浓度成正比。
如超过一定限度,浓度再增加,运输也不再增加。
因膜上载体蛋白的结合位点已达饱和;③有特异性,即与特定溶质结合。
条件:对应所运输物质的蛋白质,顺浓度差。
编辑本段体蛋白主要有离子载体和通道蛋白两种类型(一)离子载体离子载体(ionophore),是疏水性的小分子,可溶于双脂层,提高所转运离子的通透率,多为微生物合成,是微生物防御被捕食或与其它物种竞争的武器,离子载体也是以被动的运输方式运输离子,可分成可动离子载体(mobile ion carrier)和通道离子载体(channel former)两类:可动离子载体:如缬氨霉素(valinomycin)能在膜的一侧结合K+,顺着电化学梯度通过脂双层,在膜的另一侧释放K+,且能往返进行(图5-2)。
其作用机理就像虹吸管可以使玻璃杯中的水跨越杯壁屏障,向低处流动一样。
此外,2,4-二硝基酚(DNP)、羰基-氰-对-三氟甲氧基苯肼(FCCP)可转运H+,离子霉素(ionomycin)、A23187可转运Ca2+。
图5-2 缬氨霉素的分子结构通道离子载体:如短杆菌肽A(granmicidin)是由15个疏水氨基酸构成的短肽,2分子的短杆菌肽形成一个跨膜通道,有选择的使单价阳离子如H+、Na+、K+按化学梯度通过膜,这种通道并不稳定,不断形成和解体,其运输效率远高于可动离子载体(图5-3)。
图5-3 短杆菌肽构成的通道(二)通道蛋白通道蛋白(channel protein)是衡跨质膜的亲水性通道,允许适当大小的离子顺浓度梯度通过,故又称离子通道。
有些通道蛋白形成的通道通常处于开放状态,如钾泄漏通道,允许钾离子不断外流。
有些通道蛋白平时处于关闭状态,即“门”不是连续开放的,仅在特定刺激下才打开,而且是瞬时开放瞬时关闭,在几毫秒的时间里,一些离子、代谢物或其他溶质顺着浓度梯度自由扩散通过细胞膜,这类通道蛋白又称为门通道(gated channel)。
编辑本段门通道可以分为四类(图5-4):配体门通道(ligand gated channel)、电位门通道(voltage gated channel)、环核苷酸门通道(Cyclic Nucleotide-Gated Ion Channels)和机械门通道(mechanosensitive channel)。
不同通道对不同离子的通透性不同,即离子选择性(ionic selectivity)。
这是由通道的结构所决定的,只允许具有特定离子半径和电荷的离子通过。
根据离子选择性的不同,通道可分为钠通道、钙通道、钾通道、氯通道等。
但通道的离子选择性只是相对的而不是绝对的,比如,钠通道除主要对Na+通透外,对NH4+也通透,甚至于对K+也稍有通透。
编辑本段图5-4 各类离子通道1、配体门通道表面受体与细胞外的特定物质(配体ligand)结合,引起门通道蛋白发生构象变化,结果使“门”打开,又称离子通道型受体。
分为阳离子通道,如乙酰胆碱、谷氨酸和五羟色胺的受体,和阴离子通道,如甘氨酸和γ-氨基丁酸的受体。
N型乙酰胆碱受体[1]是目前了解较多的一类配体门通道。
它是由4种不同的亚单位组成的5聚体,总分子量约为290kd。
亚单位通过氢键等非共价键,形成一个结构为α2βγδ的梅花状通道样结构,其中的两个α亚单位是同两分子Ach相结合的部位(图5-5)。
Ach门通道具有具有三种状态:开启、关闭和失活。
当受体的两个α亚单位结合Ach 时,引起通道构象改变,通道瞬间开启,膜外Na+内流,膜内K+外流。
使该处膜内外电位差接近于0值,形成终板电位,然后引起肌细胞动作电位,肌肉收缩。
即是在结合Ach时,Ach门通道也处于开启和关闭交替进行的状态,只不过开启的概率大一些(90%)。
Ach释放后,瞬间即被乙酰胆碱酯酶水解,通道在约1毫秒内关闭。
如果Ach存在的时间过长(约20毫秒后),则通道会处于失活状态。
筒箭毒和α银环蛇毒素可与乙酰胆碱受体结合,但不能开启通道,导致肌肉麻痹。
图5-5 乙酰胆碱受体2、电位门通道电位门通道(voltage gated channel)是对细胞内或细胞外特异离子浓度发生变化时,或对其他刺激引起膜电位变化时,致使其构象变化,“门”打开。
如:神经肌肉接点由Ach门控通道开放而出现终板电位时,这个电位改变可使相邻的肌细胞膜中存在的电位门Na+通道和K+通道相继激活(即通道开放),引起肌细胞动作电位;动作电位传至肌质网,Ca2+通道打开引起Ca2+外流,引发肌肉收缩。
根据对Na+、K+、Ca2+通道蛋白质的结构分析,发现它们一级结构中的氨基酸排列有相当大的同源性,属于同一蛋白质家族,是由同一个远祖基因演化而来。
K+电位门通道由四个α亚单位(I-IV)构成(图5-6),每个亚单位均有6个(S1-S6)跨膜α螺旋节段,N和C 端均位于胞质面。
连接S5-S6段的发夹样β折叠(P区或H5区),构成通道的内衬,大小可允许K+通过。
K+通道具有三种状态:开启、关闭和失活。
目前认为S4段是电压感受器,S4高度保守,属于疏水片段,但每隔两个疏水残基即有一个带正电荷的精氨酸或赖氨酸残基。
S4段上的正电荷可能是门控电荷,当膜去极化时(膜外为负,膜内为正),引起带正电荷的氨基酸残基转向细胞外侧面,通道蛋白构象改变,“门”打开,大量K+外流,此时相当于K+的自由扩散。
K+电位门它和Ach配体门一样只是瞬间(约几毫秒)开放,然后失活。
此时N端的球形结构,堵塞在通道中央,通道失活,稍后球体释放,“门”处于关闭状态。
链霉菌(Streptomyces lividans)的钾离子通道KcsA也是由四个亚单位构成的,但每个亚基只有两个跨膜片段,结构较为简单。
1998年,Roderick MacKinnon 等用X射线衍射技术获得了高分辨的KcsA 通道图像,发现离子通透过程中离子的选择性主要发生在狭窄的选择性过滤器中。
选择性过滤器长1.2nm,孔径约为0.3nm(K+脱水后直径约0.26nm),内部形成一串钾离子特异结合位点,从而只有钾离子能够“排队”通过通道。
河豚毒素(Tetrodotoxin,TTX)能阻滞钠通道,毒素带正电荷的胍基伸人钠通道的离子选择性过滤器,和通道内壁上的游离羧基结合,毒素其余部分堵塞通道外侧端,妨碍钠离子进入,导致肌肉麻痹。