6章-亲核取代反应
- 格式:ppt
- 大小:3.92 MB
- 文档页数:166

亲核取代反应机理
亲核取代反应是一种有机合成化学反应。
其机理基于亲核试剂(通常为碱性)攻击有机化合物中的卤化碳原子,从而将卤素原子替换为亲核试剂中的基团。
这个反应过程通常在惰性溶剂(如二甲基亚砜)中进行,并且加热会显著提高反应速率。
一般来说,亲核取代反应可以通过初始的亲核试剂的进攻路径,伴随着有机化合物分子的结构改变,逐步构建反应前体、反应中间体和反应产物的化学键。
在这个反应中,亲核试剂的缺点是被取代的卤化碳原子所产生的正电荷带动原子间的化学反应,产生新化学键。
总的来说,亲核取代反应是一种常见的有机合成技术,可以用于制备各种重要的有机化合物。
这个反应的机理和条件可以根据具体的化学实验进行调整和优化,以达到目标产物的高产率和高纯度。

化学反应中的亲核取代反应化学反应是物质之间发生变化的过程,其中亲核取代反应是一种重要的反应类型。
亲核取代反应是指一个亲核试剂与一个电子不足的反应物发生反应,亲核试剂中的亲核基团取代掉反应物中的一个离去基团。
这种反应在有机合成中具有广泛的应用,可以用于合成各种有机化合物。
亲核取代反应可以分为两类:亲核试剂为中性物质的亲核取代反应和亲核试剂为离子的亲核取代反应。
中性物质的亲核取代反应通常发生在有机化合物中,而离子的亲核取代反应则发生在无机化合物或离子中。
中性物质的亲核取代反应中,亲核试剂通常是一种带有孤对电子的原子或分子,如氨、水、醇等。
这些亲核试剂通过与反应物中的电子不足的原子或分子发生反应,形成新的化学键。
例如,氨与醛反应可以生成胺,水与酰氯反应可以生成醛或酮。
离子的亲核取代反应中,亲核试剂通常是带有正电荷的离子,如氢离子、钠离子等。
这些亲核试剂通过与反应物中的带有负电荷的离子或原子发生反应,形成新的化学键。
例如,氢离子与氢氧根离子反应可以生成水,钠离子与氯离子反应可以生成氯化钠。
亲核取代反应的速率通常受到多种因素的影响,如反应物浓度、温度、溶剂等。
在一些情况下,亲核取代反应可能会出现竞争性反应,即不同的亲核试剂与反应物中的不同位置发生取代反应。
这时,反应的选择性就成为一个重要的问题。
在有机合成中,亲核取代反应可以用于合成各种有机化合物,包括药物、农药、染料等。
通过选择不同的反应条件和亲核试剂,可以实现对目标化合物的选择性合成。
亲核取代反应还可以用于构建碳-碳键和碳-杂原子键,从而构建复杂的有机分子。
总之,亲核取代反应是化学反应中的一种重要反应类型,广泛应用于有机合成中。
通过选择不同的亲核试剂和反应条件,可以实现对目标化合物的选择性合成。
亲核取代反应的研究对于发展新的有机合成方法和合成新的有机化合物具有重要意义。

第六章芳香环上的取代反应芳香环上的取代反应与饱和碳原子上的取代反应相似,有亲电取代、亲核取代和自由基取代反应。
在亲电反应中进攻试剂是正离子或偶极分子中正的一端,离去基团在离去时必须失去它的电子对,它们是弱的Liews酸,最常见的离去基团是氢(以H+形式离去)。
在亲核反应中进攻试剂是负离子或具有未共用电子对的原子或基团。
离去基团在离去时以最大的可能携带其键合电子。
离去后以负离O等即为弱的碱、自由基取代反应是另子或分子的形式存在,如Br-、-OTS和H2一种情况将在以后讨论。
6-1 亲电取代反应最简单的芳环是苯环,从苯的结构可知,苯的离域π轨道使苯环六个碳原子组成的平面上下集中着带负电的电子云,对苯环碳原子起着屏蔽作用,从而不利于亲核试剂的进攻,相反却有利于亲电试剂的进攻,发生亲电取代反应。
6-1-1 反应历程1.π和σ-络合物在亲电取代反应中,无论是正离子还是极性试剂中正电荷的部分进攻芳环,首先遇到的是芳环上的π电子云,因此反应的第一步可能是进攻的亲电试剂与芳环上离域的π电子相互作用。
例如硝酰正离子进攻苯环,可能是其中氮原子的空轨道与苯环的π轨道交盖,通过π电子的离域发生微弱的结合生成π-络合物。
由于是通过电荷转移形成的,也称电荷转移络合物。
在π-络合物的形成中,芳烃作为电子的给予体,试剂作为电子的接受体,它们通过电荷转移而结合,是非常松弛的,这意味着给予体和接受体两者的分轨道都未发生明显的变化,在多数情况下,它们之间的结合是很弱的(4-20KT/mol),以至络合物的组分能够迅速地发生逆反应而复原。
例如:+II2甲苯与氯化氢生成的π络合物,即使在-78℃的低温情况下两组分之间也能很快建立平衡。
CH3+Cl H CH 3ClH若作同位素试验,用氯化氘(DCl )代替氯化氢(HCl )在很长的时间内也未发现D 与H 的交换。
说明亲电试剂并没有与环上任何一个碳原子发生键合作用而生成离子。
即没有C-D 键生成,故可证明没有发生D 与H 的交换。

有机化学基础知识亲核取代反应和亲电取代反应有机化学是研究含有碳元素的化合物的科学,其中涉及了许多的反应类型和机理。
亲核取代反应和亲电取代反应是其中两种重要的反应类型,它们在有机合成中具有广泛的应用。
本文将详细介绍亲核取代反应和亲电取代反应的基本概念、机理和应用。
一、亲核取代反应亲核取代反应是指一个亲核试剂与一个电子亏损的化合物之间的反应,亲核试剂中的亲核物质与电子亏损的原子或官能团发生亲电子进攻,形成新的化学键。
亲核取代反应的机理一般分为两步骤:亲核物质的亲电子进攻和原有官能团的离去。
在亲核取代反应中,亲核试剂可以是阴离子(如氢氧根离子、溴根离子等)或中性分子(如水、醇等)。
而被取代的官能团通常是卤代烃、羰基化合物等。
亲电子进攻的位置取决于取代基的取向效应、立体效应等因素。
亲核取代反应有许多经典的例子,如Sn2反应、醇的酸性取代反应、酯的加水分解等。
Sn2反应是最典型的亲核取代反应之一,其中亲核试剂(通常为阴离子)直接在反应过渡态中与受保护的碳原子发生亲电子进攻。
亲核取代反应在有机合成中具有重要的应用价值。
它们可以用于制备具有特定官能团的化合物、构建碳碳或碳氧化合物的键等。
二、亲电取代反应亲电取代反应是指一个亲电试剂与一个电子富余的化合物之间的反应,亲电试剂中的亲电子物种与电子富余的原子或官能团发生亲电子进攻。
亲电取代反应通常可分为两个阶段:亲电子进攻和亲电子离去。
在亲电取代反应中,亲电试剂可以是正离子(如卤素离子、硫酸酯离子等)或中性分子(如酮、卤代烃等)。
而被取代的官能团通常是亲合电子能力较强的原子或官能团,如羟基、氨基等。
亲电取代反应有很多经典的例子,如卤代烃的取代反应、羟基的酸性取代反应等。
卤代烃的取代反应中,亲电试剂中的亲电子物种会与卤代烃中的卤素原子发生亲电子进攻,从而取代卤素。
亲电取代反应在有机合成中也有广泛的应用。
它们可以用于制备具有特定官能团的化合物、构建碳碳或碳氧化合物的键等。

有机化学基础知识点取代反应的机理和规律有机化学是研究有机物(含碳元素)的合成、性质和结构等方面的科学。
在有机化学中,取代反应是一种常见的反应类型,它涉及到一个原子或基团取代另一个原子或基团的过程。
了解取代反应的机理和规律是掌握有机化学基础知识的重要一环。
一、取代反应的机理1. 亲核取代反应机理亲核取代反应是指一个亲核试剂(如NH3、Br-等)攻击一个有机化合物中的亲电中心,使其离开并被亲核试剂取代的反应。
亲核试剂中的亲核部分在反应中发挥了重要作用。
亲核取代反应机理主要包括以下几个步骤:(1)亲核试剂攻击:亲核试剂中的亲核部分与有机化合物中的亲电中心发生攻击反应,形成一个中间体。
(2)中间体重排:中间体发生重排反应,使得取代基得以稳定排列。
(3)离去基离去:离去基离开中间体,并与溶剂或离去基之间形成新的化学键。
(4)生成产物:最后生成的产物是一个被亲核试剂取代了一个原有基团的化合物。
2. 亲电取代反应机制亲电取代反应是指一个亲电试剂(如H+, Br+, AlCl3等)攻击一个有机化合物中的亲核中心,使其离开并被亲电试剂取代的反应。
亲电试剂中的亲电部分在反应中发挥了重要作用。
亲电取代反应机制主要包括以下几个步骤:(1)亲电试剂攻击:亲电试剂中的亲电部分与有机化合物中的亲核中心发生攻击反应,形成一个中间体。
(2)中间体重排:中间体发生重排反应,使得取代基得以稳定排列。
(3)离去基离去:离去基离开中间体,并与溶剂或离去基之间形成新的化学键。
(4)生成产物:最后生成的产物是一个被亲电试剂取代了一个原有基团的化合物。
二、取代反应的规律1. Sn1和Sn2反应Sn1反应和Sn2反应是亲核取代反应中的两种常见机制。
Sn1反应是典型的两步反应,第一步是亲电离子形成,第二步是亲核试剂攻击。
Sn2反应是典型的一步反应,在反应中,亲核试剂直接攻击有机化合物中的亲电中心,并与离去基同时发生。
Sn1反应适用于三级卤化合物等离子体生成较容易的化合物;Sn2反应适用于一级卤化合物等亲电离子形成较困难的化合物。

有机化学基础知识点碳原子的亲核取代反应亲核取代反应是有机化学中重要的反应类型之一。
在这篇文章里,我将介绍碳原子的亲核取代反应的基础知识点。
亲核取代反应是一种化学反应,涉及到一个亲核试剂攻击一个电子云密度较低的碳原子,并将其取代。
这种反应可以发生在饱和碳原子上,也可以在环上的碳原子上发生。
1. 亲核试剂的选择亲核试剂是亲核取代反应中至关重要的一部分。
常见的亲核试剂包括卤代烷、醇、胺等。
选择适当的亲核试剂可以有效地促进反应的进行。
2. 亲核试剂的攻击在亲核取代反应中,亲核试剂攻击碳原子的位置非常重要。
碳原子可以通过两种方式进行亲核攻击:SN1和SN2机理。
- SN1机制:这是一种两步反应,首先,亲核试剂离去一个离子,形成一个带电的中间体。
然后,亲核试剂攻击中间体上的位点,取代离去的离子。
- SN2机制:这是一种一步反应,亲核试剂直接攻击碳原子,并同时取代离去的基团。
3. 碳原子的离去基团在亲核取代反应中,碳原子上的离去基团是影响反应速率和反应机理的重要因素。
常见的离去基团包括卤素原子、氨基和醇基等。
不同的离去基团会导致不同的反应速率和产物选择。
4. 反应条件的影响亲核取代反应的条件也会对反应的进行产生影响。
常见的反应条件包括溶剂的选择、温度和反应时间等。
选择合适的反应条件可以提高反应的收率和选择性。
5. 反应机理的解释了解亲核取代反应的机理对于理解反应过程和预测产物是非常重要的。
通过观察亲核试剂攻击碳原子的位置、反应速率以及产物选择等因素,可以确定反应机理。
在总结中,亲核取代反应是有机化学中基本的反应类型之一。
了解碳原子的亲核取代反应的基础知识点可以帮助我们理解反应机理、预测产物以及进行有机合成的设计。
当然,亲核取代反应还有很多细节和应用等待我们深入探索和学习。

有机化学基础知识点整理亲核取代反应的机理与应用有机化学基础知识点整理亲核取代反应的机理与应用亲核取代反应(nucleophilic substitution reaction)是有机化学中一类重要的反应类型,它涉及到亲核试剂(nucleophile)与底物(substrate)之间的反应。
这类反应在有机合成和药物化学等领域具有广泛的应用。
本文将对亲核取代反应的机理和应用进行整理。
一、亲核取代反应的机理亲核取代反应的机理可以分为两步:亲核试剂的进攻和负离子离去。
以下将以醇与卤代烷的反应为例来说明。
1. 亲核试剂进攻:醇作为亲核试剂,其亲电性中心是氧原子上的孤电子对。
亲核试剂进攻底物,将亲电性中心与底物的反应中心连接起来,形成中间体。
中间体的稳定性对反应速率起到重要作用。
2. 负离子离去:经过亲核试剂的进攻,底物的反应中心得到了一个新的基团,此时底物上的卤素离去。
在反应中,卤素上的原子带负电荷,形成负离子离去。
负离子的离去速率也会影响整个反应的速率。
亲核取代反应的机理可以继续细分,根据亲核试剂的种类和底物的不同,反应机制也会有所差异。
研究亲核取代反应的机理有助于我们理解反应的速率和选择性,为有机合成的设计和优化提供依据。
二、亲核取代反应的应用亲核取代反应在有机合成中具有广泛的应用。
以下列举几个常见的案例:1. 醇的取代反应:醇可以通过与卤代烷反应发生取代反应,生成醚。
这种反应常用于合成醚类化合物。
例如,乙醇与溴乙烷反应生成乙基乙醚。
2. 酯的水解反应:酯可以通过与水或醇反应发生水解反应,生成相应的酸或醇。
这种反应常用于酯类的加水解反应或酯的酸化反应。
例如,乙酸乙酯与水反应生成乙醇和乙酸。
3. 醛酮的取代反应:醛和酮可以通过与亲核试剂反应发生取代反应,引入新的官能团。
这种反应常用于醛酮类化合物的合成。
例如,丙酮与苯胺反应生成N-苯基丙酮。
4. 羧酸的酯化反应:羧酸可以与醇反应发生酯化反应,生成酯。
这种反应常用于酯类化合物的合成。

亲核取代反应讲解
亲核取代反应是有机化学常见的一种反应。
在这种反应中,一个亲核试剂汇合一个有机反应物,并且代替了原有的基团。
在这个反应中,亲核试剂成为了新的基团。
这种反应是在有机化学中广泛运用的,非常有用。
它可以用于构建长链分子,连接分子,以及进行化学变换,制造新化合物。
现在,让我们跟着下面的步骤学习一下如何进行亲核取代反应。
1. 首先,你需要准备好亲核试剂。
亲核试剂可以是任何一种有活性的物质,其分子中含有一个亲核中心,例如氨基、羟基、硫代锰酸根、氰根、卤素根等。
在这个过程中,亲核试剂将代替原有的基团。
2. 准备好需要反应的有机化合物。
选定有机化合物,将其与亲核试剂混合,具体反应条件需要根据不同化合物的特性进行调整。
3. 进行反应。
在进行反应时,通常需要一定的触发条件。
例如,需要加热、催化、加压等。
这些条件可以影响反应速率和产率。
4. 产物的分离与纯化。
完成反应后,需要对产物进行分离和纯化。
这可以通过各种方法进行,例如渗透色谱、薄层色谱、皮尔斯等方法。
通过以上步骤,亲核取代反应就完成了。
这个反应可以进行多次,生成不同的产物,依据不同的具体反应条件,可以得到不同的产物类型。
总之,亲核取代反应是有机化学中非常常见的一种反应。
通过学会这个反应,可以制造许多新型材料和化合物。
即使在化学实验室或制造工厂等工作中,软硬件机器人也可以准确地掌握这个技术,帮助实验者进行研究和开发不同的产物。

有机化学反应方程式总结亲核取代反应亲核取代反应是有机化学中常见的一类反应。
在亲核取代反应中,亲核试剂(通常是带负电荷的离子或具有亲核性质的分子)与电子不足的溶液中的有机化合物发生反应,取代原有的官能团或取代子基。
这些反应在有机合成中具有重要的应用价值,因此对亲核取代反应的了解至关重要。
以下是几种常见的亲核取代反应及其对应的反应方程式:1. 醇的亲核取代反应醇的亲核取代反应常见的有醇的取代和醚的形成反应。
例如,溴代烷与醇发生取代反应,生成溴代醚和水。
反应方程式如下:R-OH + HBr → R-Br + H2O2. 烯烃的亲核取代反应烯烃是一类具有高度不饱和度的有机分子,容易与亲核试剂发生亲核取代反应。
例如,乙烯与溴化氢反应,发生加成反应生成溴代乙烷:CH2=CH2 + HBr → CH3CH2Br3. 酸的亲核取代反应酸的亲核取代反应是指酸与亲核试剂反应,生成酸的盐类或酯。
例如,乙酸与氨反应生成乙酰胺:CH3COOH + NH3 → CH3CONH24. 酯的亲核取代反应酯的亲核取代反应通常涉及酯键的断裂和取代。
例如,酯与碱反应生成相应的酸盐:R-COOR' + NaOH → R-COONa + R'OH5. 酰卤的亲核取代反应酰卤是一类常见的有机化合物,容易与亲核试剂发生取代反应。
例如,酰氯与水反应生成相应的酸:R-COCl + H2O → R-COOH + HCl6. 醛和酮的亲核取代反应醛和酮是有机化合物中常见的官能团,容易与亲核试剂发生取代反应。
例如,醛和酮与氨反应生成相应的胺:R1-CO-R2 + NH3 → R1-CO-NH2 + R2H上述只是亲核取代反应的一些常见例子,实际上亲核取代反应有很多不同的类型,具体的反应机理和生成物取决于反应条件和反应物的性质。
总结:亲核取代反应是有机化学中常见的反应类型,通过与亲核试剂的反应,有机化合物发生取代反应。
醇的取代反应、烯烃的加成反应、酸的盐类或酯的生成、酯键的断裂和取代、酰卤的取代反应、以及醛和酮的胺的生成等都是亲核取代反应的例子。

有机化学基础知识点整理亲核取代反应的机理有机化学基础知识点整理:亲核取代反应的机理亲核取代反应是有机化学中一类重要的反应类型,它是指亲核试剂(通常是带有孤对电子的分子或离子)与有机化合物发生反应,将其替代掉。
本文将对亲核取代反应的机理进行整理。
一、亲核试剂的特性和作用亲核试剂一般是带有孤对电子的分子或离子,具有以下特性和作用:1. 孤对电子的存在:亲核试剂通过孤对电子攻击有机分子中的反应中心进行取代反应。
2. 拉断键:亲核试剂与反应物形成化学键时,需要拉断原有的化学键。
3. 中性或带正电:亲核试剂可以是中性分子,也可以是带正电的离子。
二、亲核取代反应的机理亲核取代反应的机理可分为三个关键步骤:亲核试剂的加入、化学键的形成和产物生成。
1. 亲核试剂的加入:亲核试剂向反应物靠近,并通过孤对电子攻击反应物中的反应中心,形成化学键。
这一步是反应的速率决定步骤。
2. 化学键的形成:在形成新的化学键的同时,原有的化学键被拉断,形成过渡态。
亲核试剂和反应物之间会发生电子重新分配的过程。
3. 产物生成:经过化学键形成和原有键的断裂后,形成了新的化学物质,即产物。
三、亲核取代反应的机制亲核取代反应的机制可以分为两种类型:S_N1和S_N2反应机制。
1. S_N1反应机制:S_N1反应机制是指亲核试剂首先取代离子化的反应物上的离去基团,然后再形成新的化学键。
其关键特点如下:- 易产生重排:由于反应物中离去基团的离去速度决定反应的速率,因此在离去基团稳定性较差的情况下,易产生重排反应。
- 两步反应:S_N1反应机制经历两个步骤,第一步是离去基团的离去形成离子化的反应物,第二步是亲核试剂与离子化的反应物发生反应。
2. S_N2反应机制:S_N2反应机制是指亲核试剂直接与反应物发生反应,形成新的化学键。
其关键特点如下:- 一步反应:S_N2反应机制只经历一个步骤,即亲核试剂与反应物同时发生反应,形成新的化学键。
- 全程立体控制:S_N2反应机制中反应的速率不仅取决于亲核试剂的浓度,还受到空间位阻的影响。
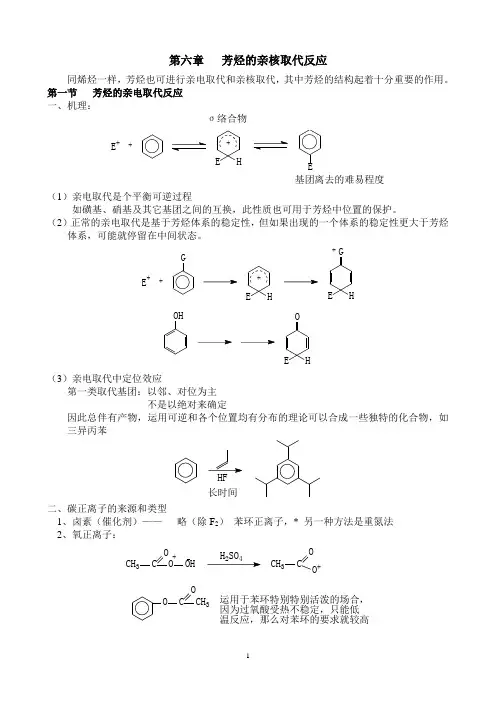
第六章 芳烃的亲核取代反应同烯烃一样,芳烃也可进行亲电取代和亲核取代,其中芳烃的结构起着十分重要的作用。
第一节 芳烃的亲电取代反应 一、机理:σ络合物E +++HE E基团离去的难易程度(1)亲电取代是个平衡可逆过程如磺基、硝基及其它基团之间的互换,此性质也可用于芳烃中位置的保护。
(2)正常的亲电取代是基于芳烃体系的稳定性,但如果出现的一个体系的稳定性更大于芳烃体系,可能就停留在中间状态。
E +++GHEGE H+OHOE H(3)亲电取代中定位效应第一类取代基团:以邻、对位为主不是以绝对来确定因此总伴有产物,运用可逆和各个位置均有分布的理论可以合成一些独特的化合物,如三异丙苯长时间二、碳正离子的来源和类型1、卤素(催化剂)—— 略(除F 2) 苯环正离子,* 另一种方法是重氮法2、氧正离子:CH 3C O O +24CH 3COO +OC OCH 3运用于苯环特别特别活泼的场合,因为过氧酸受热不稳定,只能低温反应,那么对苯环的要求就较高3、氮型正离子(i )+NO 2 硝基正离子 +NO 亚硝基正离子亚硝酸酯RO NONH 2OONH 2NO 2(ii )重氮离子 N ≡N +C l适用于苯环特别活泼的场合,理由同上+OHN N OH 偶合N N +Cl4、碳型正离子 两种形式: CH 2+(烷基化) +C=O (酰化) (i )不饱和体系在酸的催化下:(质子催化)H +CH 3C NCH 3C NH CH 3CH O H+CH 3C HOHOH +OHCH 2例:酚醛树脂的合成OHCH 2OHCH 2CH 2OH又例:氯甲基化:HCHO ,ZnCl 2,HCl其实经历了一取代过程(ii )羟基化合物的脱水,在酸性条件下OH H +(iii )卤代烷烃在路易斯酸催化 (iv )CO 2OHCH2OHOH CO2KOHOHOHCOOH起保护作用的OHOHBrOHOH5、其它正离子SOOOH磺酸型P ClCl磷型6、相互取代反应CH3OCH3CH3OCH3NO2+CH3OCH3NO2NO2第二节 芳香族的亲核取代 一、SN 2历程一般条件下,芳香族上的任何基团都稳定不易取代 此情况同烯烃但当邻、对位有强吸电子基团时,该官能团可被取代。
亲核取代反应类型
亲核取代反应是有机化学中的一类重要反应类型,它通常涉及亲核试剂(通常是亲核试剂的电子富集部分)与有机分子中的亲电部分(通常是电子亏损部分)之间的化学反应。
这种类型的反应在有机合成中非常常见,因为它们允许在有机分子中引入新的官能团或发生结构改变。
以下是一些常见的亲核取代反应类型:
1.亲核取代反应:亲核试剂中的亲核离子或亲核基团与有机分子
中的亲电部分发生取代反应。
例如,卤代烷可以与氢氧根离子(OH-)发生亲核取代反应,生成醇。
2.亲核芳烃取代:在芳香烃化合物中,亲核试剂可以取代芳香环
上的卤素或其他官能团。
例如,苯环上的氟原子可以被亲核试剂取代,生成新的芳香化合物。
3.亲核加成反应:亲核试剂加成到有机分子中的多键上,通常是
双键。
例如,亲核试剂可以加成到烯烃上,生成醇或其他官能团。
4.亲核亲核反应:在这种反应中,两个亲核试剂相互作用,通常
会形成新的化学键。
这种类型的反应在有机合成中也很重要。
5.亲核取代酰基基团:亲核试剂可以与酰基化合物中的羰基碳发
生取代反应,通常会生成新的酯或酰胺。
这些反应类型是有机化学中的基本反应类型,它们为有机化学家提供了丰富的工具来构建有机分子和合成复杂的有机化合物。
不同的亲核试剂和底物可以产生多种不同类型的亲核取代反应。
亲核取代反应一.亲核取代反应机理。
亲核取代反应是指有机分子中的与碳相连的原子或原子团被作为亲核试剂的某原子或原子团取代的反应。
反应分为SN1型(单分子取代反应),与SN2型双分子取代反应。
1.SN1型(单分子取代反应)第一步是碳原子上正电荷增加,离去基团负点性增加,经过过渡态(1)并最终解离,生成活性中间体碳正离子与离去基团负离子。
由于这一步反应的活化能较高,速率较慢,所以这一步是反应的决速步。
第二步是活性中间体的碳正离子与亲和试剂作用,生成反应产物。
这一步仅需少量能量,速率很快。
反应特点:(1)SN1反应的决速步是中心碳原子与离去基团之间化学键的异裂。
反应速率只取决于一种分子的浓度,因此,它在动力学上是一级反应。
(2)一般是一个两步反应。
第一步生成的碳正离子采取SP2杂化,是平面构型。
故若反应物的中心碳原子是手性碳,反应产物一般是一对等量的对映异构体的混合物——外消旋体。
(3)反应中间体生成的碳正离子导致反应有重排的趋势。
2.SN2型(双分子取代反应)反应中,离去基团离开中心碳原子的同时,亲核试剂与中心碳原子发生部分键合,无中间体生成。
有机反应中,将两种分子参与决速步的亲核取代反应陈伟双分子亲核取代反应。
反应特点:(1)SN2反应是一步反应,只有一个过渡态。
(2)在SN2反应中,亲核试剂进攻中心碳原子是总是从离去基团溴原子的背面沿着碳原子和离去基团连接的中心线方向进攻。
这个过程会使得碳原子与三个未参与反映的键发生翻转,这种翻转称为瓦尔登翻转,又称构型翻转。
二.影响亲核取代反应的因素1.烃基结构的影响。
对SN1反应,主要考虑碳正离子的稳定性。
对SN2反应,主要取决于过渡态形成的难易,也就是空间效应的影响。
2.离去基团的影响。
离去基团的性质对SN1和SN2将产生相似的影响:离去基团的离去能力越强,亲核取代反应越易进行。
对于离去基团:键能越弱,离去基团的稳定性越好,该离去基团的离去能力就越强。
3.亲核试剂的影响仅对SN2有影响。
亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去.2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应.3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应。
其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应.从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4)正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH—、CN-、X—、H2O、NH3等有机类亲核试剂:ROH、RO—、PhO-、RS—、RMgX、RCOO-等4、反应机理类型分类:(1)双分子亲核取代反应(S N2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N2反应机理一般式表示为:Nu-+R X[Nuδ-···R···Xδ- ] NuR+X—例如,溴甲烷与OH—的水解反应:(2)单分子亲核取代反应(S N1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部.当分子解离后,碳正离子马上与亲核试剂结合,速率极快,是快的一步。