第三章_亲核取代反应
- 格式:ppt
- 大小:1.48 MB
- 文档页数:58


亲核取代反应讲解
亲核取代反应是有机化学常见的一种反应。
在这种反应中,一个亲核试剂汇合一个有机反应物,并且代替了原有的基团。
在这个反应中,亲核试剂成为了新的基团。
这种反应是在有机化学中广泛运用的,非常有用。
它可以用于构建长链分子,连接分子,以及进行化学变换,制造新化合物。
现在,让我们跟着下面的步骤学习一下如何进行亲核取代反应。
1. 首先,你需要准备好亲核试剂。
亲核试剂可以是任何一种有活性的物质,其分子中含有一个亲核中心,例如氨基、羟基、硫代锰酸根、氰根、卤素根等。
在这个过程中,亲核试剂将代替原有的基团。
2. 准备好需要反应的有机化合物。
选定有机化合物,将其与亲核试剂混合,具体反应条件需要根据不同化合物的特性进行调整。
3. 进行反应。
在进行反应时,通常需要一定的触发条件。
例如,需要加热、催化、加压等。
这些条件可以影响反应速率和产率。
4. 产物的分离与纯化。
完成反应后,需要对产物进行分离和纯化。
这可以通过各种方法进行,例如渗透色谱、薄层色谱、皮尔斯等方法。
通过以上步骤,亲核取代反应就完成了。
这个反应可以进行多次,生成不同的产物,依据不同的具体反应条件,可以得到不同的产物类型。
总之,亲核取代反应是有机化学中非常常见的一种反应。
通过学会这个反应,可以制造许多新型材料和化合物。
即使在化学实验室或制造工厂等工作中,软硬件机器人也可以准确地掌握这个技术,帮助实验者进行研究和开发不同的产物。





有机化学反应方程式总结亲核取代反应亲核取代反应是有机化学中常见的一类反应。
在亲核取代反应中,亲核试剂(通常是带负电荷的离子或具有亲核性质的分子)与电子不足的溶液中的有机化合物发生反应,取代原有的官能团或取代子基。
这些反应在有机合成中具有重要的应用价值,因此对亲核取代反应的了解至关重要。
以下是几种常见的亲核取代反应及其对应的反应方程式:1. 醇的亲核取代反应醇的亲核取代反应常见的有醇的取代和醚的形成反应。
例如,溴代烷与醇发生取代反应,生成溴代醚和水。
反应方程式如下:R-OH + HBr → R-Br + H2O2. 烯烃的亲核取代反应烯烃是一类具有高度不饱和度的有机分子,容易与亲核试剂发生亲核取代反应。
例如,乙烯与溴化氢反应,发生加成反应生成溴代乙烷:CH2=CH2 + HBr → CH3CH2Br3. 酸的亲核取代反应酸的亲核取代反应是指酸与亲核试剂反应,生成酸的盐类或酯。
例如,乙酸与氨反应生成乙酰胺:CH3COOH + NH3 → CH3CONH24. 酯的亲核取代反应酯的亲核取代反应通常涉及酯键的断裂和取代。
例如,酯与碱反应生成相应的酸盐:R-COOR' + NaOH → R-COONa + R'OH5. 酰卤的亲核取代反应酰卤是一类常见的有机化合物,容易与亲核试剂发生取代反应。
例如,酰氯与水反应生成相应的酸:R-COCl + H2O → R-COOH + HCl6. 醛和酮的亲核取代反应醛和酮是有机化合物中常见的官能团,容易与亲核试剂发生取代反应。
例如,醛和酮与氨反应生成相应的胺:R1-CO-R2 + NH3 → R1-CO-NH2 + R2H上述只是亲核取代反应的一些常见例子,实际上亲核取代反应有很多不同的类型,具体的反应机理和生成物取决于反应条件和反应物的性质。
总结:亲核取代反应是有机化学中常见的反应类型,通过与亲核试剂的反应,有机化合物发生取代反应。
醇的取代反应、烯烃的加成反应、酸的盐类或酯的生成、酯键的断裂和取代、酰卤的取代反应、以及醛和酮的胺的生成等都是亲核取代反应的例子。

第3章 亲核取代反应练习题
1、(6101)写出下列反应产物,有立体化学也应注明。
2、(6103)写出下列反应产物,有立体化学也应注明。
3、将化合物I 、II 、III 在乙酸中的溶剂解速率由小到大排序,并解释原因?
4、比较下面两个化合物在乙酸中的溶剂解速率的大小,并解释原因?
5、下面两个化合物在乙酸中的发生溶剂解反应,化合物I 得到完全消旋化的产物,而化合物II 的反应产物仍然有部分旋光,为什么?
6、比较下面三个化合物在乙酸中的溶剂解速率的大小,并解释原因?
7、下面四个化合物发生亲核取代反应的速率不同,请给出合理解释?
ClCH 2CH 2CH 2CH 2NH 2KOH 2HO CH 2CH 2Cl Ca(OH)2CH 2
CH 2Cl O -k 乙酸解113.2
H 3
H 3
148k 相对Me 3CBr
110-310-710-13
8、下列反应在不同溶剂中的反应速率不同,请给出合理解释?
9、下列反应在不同溶剂中的反应速率不同,请给出合理解释?
10、简述休斯-英戈尔德(Hughes-Ingole)规则的基本内容。
11、如何高效地获得纯净伯胺(RNH2)?请举例说明。

亲核取代反应一.亲核取代反应机理。
亲核取代反应是指有机分子中的与碳相连的原子或原子团被作为亲核试剂的某原子或原子团取代的反应。
反应分为SN1型(单分子取代反应),与SN2型双分子取代反应。
1.SN1型(单分子取代反应)第一步是碳原子上正电荷增加,离去基团负点性增加,经过过渡态(1)并最终解离,生成活性中间体碳正离子与离去基团负离子。
由于这一步反应的活化能较高,速率较慢,所以这一步是反应的决速步。
第二步是活性中间体的碳正离子与亲和试剂作用,生成反应产物。
这一步仅需少量能量,速率很快。
反应特点:(1)SN1反应的决速步是中心碳原子与离去基团之间化学键的异裂。
反应速率只取决于一种分子的浓度,因此,它在动力学上是一级反应。
(2)一般是一个两步反应。
第一步生成的碳正离子采取SP2杂化,是平面构型。
故若反应物的中心碳原子是手性碳,反应产物一般是一对等量的对映异构体的混合物——外消旋体。
(3)反应中间体生成的碳正离子导致反应有重排的趋势。
2.SN2型(双分子取代反应)反应中,离去基团离开中心碳原子的同时,亲核试剂与中心碳原子发生部分键合,无中间体生成。
有机反应中,将两种分子参与决速步的亲核取代反应陈伟双分子亲核取代反应。
反应特点:(1)SN2反应是一步反应,只有一个过渡态。
(2)在SN2反应中,亲核试剂进攻中心碳原子是总是从离去基团溴原子的背面沿着碳原子和离去基团连接的中心线方向进攻。
这个过程会使得碳原子与三个未参与反映的键发生翻转,这种翻转称为瓦尔登翻转,又称构型翻转。
二.影响亲核取代反应的因素1.烃基结构的影响。
对SN1反应,主要考虑碳正离子的稳定性。
对SN2反应,主要取决于过渡态形成的难易,也就是空间效应的影响。
2.离去基团的影响。
离去基团的性质对SN1和SN2将产生相似的影响:离去基团的离去能力越强,亲核取代反应越易进行。
对于离去基团:键能越弱,离去基团的稳定性越好,该离去基团的离去能力就越强。
3.亲核试剂的影响仅对SN2有影响。
第八章卤代烃8.4 亲核取代反应机理卤代烃中的C-X 键为极性键,电子云明显偏向卤素一边当遇上亲核试剂时,发生取代反应,卤素X 带着一对电子离去,如下式所示:(Nucleophilic Substitution Reaction ,S N )•为什么溴代叔丁烷水解是一级反应,而溴甲烷水解是二级反应?•其根本原因是反应机理不一样单分子亲核取代机理Monomlecular NucleophilicSubstitution1SNS N1 = 单分子亲核取代,1代表单分子重排是SN 1反应的特征现象也是支持SN1机理的重要实验证据重排是SN 1反应的特征,也是支持SN1机理的重要实验证据。
如果一个亲核取代反应中有重排现象,那么这种取代一般都是SN1机理。
但要注意,如果某亲核取代反应中没有重排,则不能否定SN1机理存在的可能性。
因为并不是所有的SN1反应都会发生重排。
双分子亲核取代机理Bimolecular NucleophilicSubstitution2SNS2 反应势能图N•一步反应•过渡态能量最高•不发生重排Br C ....–....HOBr C ....–....HO CBr δ –....HO ....Br C ....–....HO CBr δ –....HO ....C HO ........Br8.4.2影响反应机理及其活性的因素烃基结构的影响离去基团的影响亲核试剂的影响溶剂效应相对速度C HH H 1.0C Br H CH 3H 1.7C CH 3CH 3H 45C CH 3CH CH 3100,000,000在S N 1反应中烃基结构的影响溴代烃在甲酸水溶液中水解反应的相对S N 1速度为:(CH3)2CHBr(CH3)2CHBrCH3BrCH CH Br(CH3)2CHBr叔卤(CH3)3CBr相对速度C C HH H H H 1.0C C H HH H CH 30.28C C HH CH 3H CH 0.036C C H H CH 3CH 3CH 0.0000042当伯卤代烃β-位上有侧链时,S N 2反应速度也有明显下降。
亲核取代反应及其影响因素航03班 林三春 2010011556摘要:本文分为四部分。
第一部分论述了亲核取代反应的组成部分:亲核试剂、离去基团、反应底物,特地列出了常见的亲核试剂、常见的离去基团。
第二部分论述了亲核取代反应机理,主要论述了四种:SN1、SN2、离子对机理和邻近基团参与机理,其中还包括各种机理的实验现象验证,以及对反应产物的影响,如对构型的影响。
第三部分论述了亲核反应的影响因素,主要有烃基、离去基团、溶剂和亲核试剂四种,详细地说明了这四种因素如何影响反应。
给出了判断离去基团的好坏,以及比较亲核试剂的亲核性的方法。
最后一部分论述了亲和取代反应与消除反应的竞争关系,其中包括SN1与E1竞争,SN2与E2竞争。
主要以卤代烃为例阐述的。
在论述的同时,还附有适当的图示,以及实验数据,通过比较等手段,使得论述更加有说服力。
全文通过这四个部分,详细、全面地介绍了亲核取代反应。
正文:亲核取代反应,简称SN 亲核取代反应,通常发生在带有正电或部分正电荷的碳上,碳原子被带有负电或部分负电的亲核试剂(Nu:-)进攻而取代。
一、亲核取代反应的重要组成成分:亲核取代反应中涉及到的三个重要组成成分为:亲核试剂、离去基团、反应底物。
称为反应底物。
进攻反应底物的试剂CH30Na (或CH3O —)是带着电子对与碳原子结合成键的,它本身具有亲核性,称为亲核试剂,一般用Nu 表示。
这类反应之所以称为亲核取代也正是因为它是由亲核试剂进攻反应底物而引起的取代反应。
反应底物上的溴原子带着电子对从碳原子上离去,所以Br-;称为离去基团,一般用L 表示。
该取代反应是在与溴相连的那个碳原子上进行的,常称该碳原子为中心原子,或反应中心。
.一般的亲核取代反应可以用如下的通式表示: 。
其中R —L 为反应底物,L —为离去基团,Nu —为亲核试剂,弯箭头表示电子转移的方向。
1、亲核试剂:亲核性是指:带负电荷或孤对电子的试剂即亲核试剂对亲电子原子的进攻的能力。
亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去。
2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应。
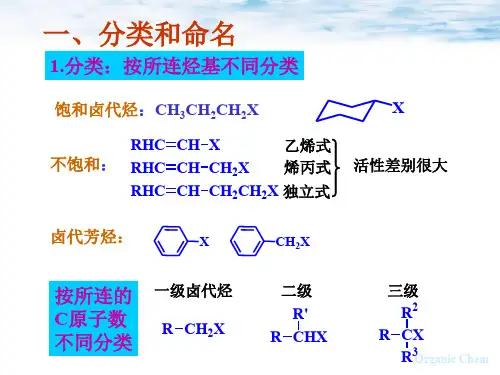
3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应。
其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应。
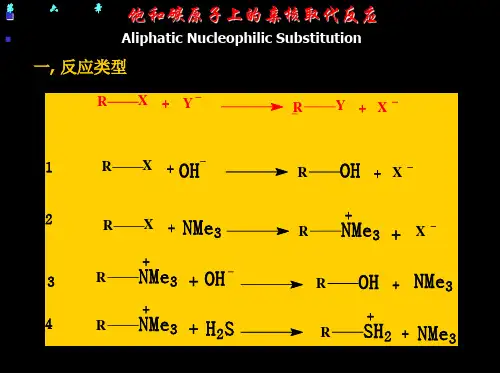
从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4) 正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH -、CN -、X -、H 2O 、NH 3等有机类亲核试剂:ROH 、RO -、PhO -、RS -、RMgX 、RCOO -等4、反应机理类型分类:(1)双分子亲核取代反应(S N 2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N 2反应机理一般式表示为:Nu -+ R X [Nuδ-···R···X δ- ] NuR + X -例如,溴甲烷与OH -的水解反应:(2)单分子亲核取代反应(S N 1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部。
亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应.在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去。
2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应.3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应.其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应。
从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4) 正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH-、CN—、X-、H2O、NH3等有机类亲核试剂:ROH、RO-、PhO-、RS-、RMgX、RCOO-等4、反应机理类型分类:(1)双分子亲核取代反应(S N2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N2反应机理一般式表示为: Nu-+R X[Nuδ—···R···Xδ- ] NuR+X—例如,溴甲烷与OH-的水解反应:(2)单分子亲核取代反应(S N1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部.当分子解离后,碳正离子马上与亲核试剂结合,速率极快,是快的一步。
教学目标:掌握各种因素对亲核取代反应机理的影响。
教学重点:烷基结构、亲核试剂、溶剂等因素对S N1和S N2反应的影响教学安排:H i, H3— >H4; 40min基本概念:溶剂解:溶剂作为亲核试剂的亲核取代反应,称为溶剂解或溶剂解反应。
溶剂解反应可根据所用的溶剂是水、乙醇还是乙酸,分别称为水解、乙醇解,乙酸解等。
卤代烷的亲核取代反应,既可按S N2亦可按S N1机理进行,但究竟按何种机理进行呢?这与卤代烷结构,离去基团亲核试剂和溶剂的性质等诸因素有关,下面分别讨论。
一、烷基结构的影响1.烷基的结构对S N2反应的影响在卤代烷的 S N2反应中,如果中心碳原子上连接的取代烷基(支链)越多,它们对亲核试剂从碳卤键背后进攻中心碳原子的空间位阻就越大,使得发生有效碰撞的概率大为下降;而在过渡态时众多的支链与中心碳原子要保持在同一个平面内,其张力是很大的,这就使形成过渡态需要有非常高的活化能,这些都将导致卤代烷进行S N2反应的活性下降,反应速率减小。
例如,I-与下面各溴代烷的丙酮溶液中于25 C发生S N2反应时的相对反应速率为:相对转化速CSI2)CfeBr > CaHsBr〉(CHa) sCHBr > (CHoJjCBr$0 1 a 4210^ 】尸如果在卤代烷的俟碳原子上连有支链烷基时,对S N2反应的速率也有明显的影响,即卤代烷中心碳(a碳)原子上连接的烷基体积越大,其空间位阻越大,不利于亲核试剂的攻击。
例如,在C2H5OH溶剂中C2H5ONa与下面各溴代烷于 55C发生 S N2反应的相对反应速率为:反应物CH3CH 2B CH3CH2CH2B (CH 3)2CHCH 2B (CH 3)3CCH 2B r r r r相对速率100 28 3.0 4.2 X O-4综上所述,卤代烷进行S2反应时,在其它条件相同时,不同结构卤代烷的反应活性次序为:RX的亲核取代轲性:;(%X > i°RX > 2°RX >S H2反应时立体隹阻2.烷基的结构对S N1反应的影响在S N1反应中,由于决定反应速率的步骤是碳正离子的生成。