碱性磷酸酶米氏常数测定
- 格式:docx
- 大小:58.46 KB
- 文档页数:3




碱性磷酸酶km值测定实验报告碱性磷酸酶 Km 值测定实验报告一、实验目的1、掌握测定碱性磷酸酶(ALP)Km 值的原理和方法。
2、了解底物浓度对酶促反应速度的影响。
3、熟悉分光光度计的使用。
二、实验原理碱性磷酸酶是一种广泛分布于人体各脏器器官中的酶,在骨、肝、肠、胎盘等组织中含量较高。
它能催化磷酸酯的水解反应,产生无机磷酸和醇、酚等物质。
在酶促反应中,反应速度(v)与底物浓度S之间的关系可用米氏方程表示:v = VmaxS /(Km + S) ,其中 Vmax 为最大反应速度,Km 为米氏常数。
Km 值是酶的一个重要特征常数,它表示酶与底物的亲和力。
Km 值越小,酶与底物的亲和力越大;反之,Km 值越大,酶与底物的亲和力越小。
本实验通过测定不同底物浓度下的酶促反应速度,以反应速度 v 对底物浓度S作图,通过双倒数作图法(LineweaverBurk 作图法),即1/v 对 1/S作图,可求得碱性磷酸酶的 Km 值。
三、实验材料与仪器1、材料碱性磷酸酶提取液磷酸苯二钠溶液(不同浓度)01mol/L 氢氧化钠溶液004mol/L 碳酸钠溶液05mol/L 三氯乙酸溶液2、仪器分光光度计恒温水浴锅移液器试管、刻度吸管等四、实验步骤1、准备试剂配制不同浓度的磷酸苯二钠溶液:0005mol/L、001mol/L、002mol/L、003mol/L、004mol/L。
配制显色剂:将 01mol/L 氢氧化钠溶液和 004mol/L 碳酸钠溶液按4:1 的体积比混合。
2、反应体系设置取 7 支干净的试管,按下表加入试剂:|试管编号|1|2|3|4|5|6|7|||||||||||磷酸苯二钠溶液(mL)|000|020|040|060|080|100|_____||蒸馏水(mL)|100|080|060|040|020|000|_____||37℃预温5min 后,各加入05mL 碱性磷酸酶提取液,立即混匀,37℃水浴准确反应 15min||反应结束后,各加入 05mL 05mol/L 三氯乙酸溶液终止反应|3、显色与比色各管加入 45mL 显色剂,充分摇匀。



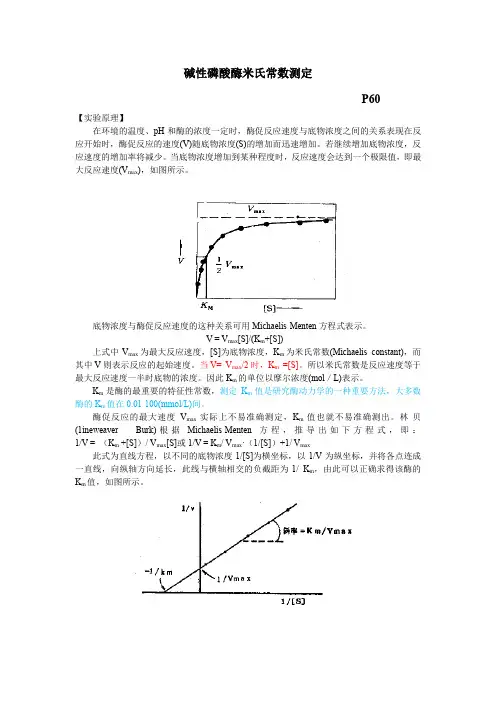
碱性磷酸酶米氏常数测定P60【实验原理】在环境的温度、pH和酶的浓度一定时,酶促反应速度与底物浓度之间的关系表现在反应开始时,酶促反应的速度(V)随底物浓度(S)的增加而迅速增加。
若继续增加底物浓度,反应速度的增加率将减少。
当底物浓度增加到某种程度时,反应速度会达到一个极限值,即最大反应速度(V max),如图所示。
底物浓度与酶促反应速度的这种关系可用Michaelis-Menten方程式表示。
V = V max[S]/(K m+[S])上式中V max为最大反应速度,[S]为底物浓度,K m为米氏常数(Michaelis constant),而其中V则表示反应的起始速度。
当V= V max/2时,K m=[S]。
所以米氏常数是反应速度等于最大反应速度一半时底物的浓度。
因此K m的单位以摩尔浓度(mol/L)表示。
K m是酶的最重要的特征性常数,测定K m值是研究酶动力学的一种重要方法,大多数酶的K m值在0.01-100(mmol/L)间。
酶促反应的最大速度V max实际上不易准确测定,K m值也就不易准确测出。
林-贝(1ineweaver - Burk)根据Michaelis-Menten方程,推导出如下方程式,即:1/V = (K m +[S])/ V max[S]或1/V = K m/ V max·(1/[S])+1/ V max此式为直线方程,以不同的底物浓度1/[S]为横坐标,以1/V为纵坐标,并将各点连成一直线,向纵轴方向延长,此线与横轴相交的负截距为-1/ K m,由此可以正确求得该酶的K m值,如图所示。
本实验以碱性磷酸酶为例,测定不同底物浓度的酶活性,再根据Lineweaver-Burk法作图,计算其K m值。
可以作为碱性磷酸酶底物的物质很多,底物反应的酶对于不同的底物有不同的K m值。
本实验以磷酸苯二钠为底物,由碱性磷酸酶催化水解,生成游离酚和磷酸盐。
酚在碱性条件下与4-氨基安替比林作用,经铁氰化钾氧化,生成红色的醌衍生物,颜色深浅和酚的含量成正比。



碱性磷酸酶的分离纯化及比活性与米氏常数测定一、实验原理(1).碱性磷酸酶的分离纯化1. 机械破碎法制备肝匀浆低浓度乙酸钠:低渗破膜低浓度乙酸镁:保护和稳定AKP2.有机溶剂沉淀法分离纯化AKP加入不同有机溶剂重复离心正丁醇:沉淀部分除AKP的蛋白质33%丙酮、30%乙醇:溶解AKP50%丙酮、60%乙醇:沉淀AKP(2).比活性测定1.比活性的定义*单位重量的蛋白质样品中所含的酶活性单位。
*通常用每毫克蛋白质具有的酶活性单位来表示。
*用以鉴定酶的纯化程度,是酶分离提纯完成的评价指标之一。
2.测定样品的比活性必须测定:*每毫升样品中的酶活性单位数。
*每毫升样品中的蛋白质毫克数。
3.磷酸苯二钠法测定碱性磷酸酶活性反应原理(3).米氏常数测定K m 即为米氏常数,V max为最大反应速度*如上式表示,米氏常数是反应速度为最大值的一半时的底物浓度,因此,米氏常数的单位为mol/L。
当反应速度等于最大速度一半时,即V= 1/2 V max, K m = [S]*吸光度表示不同底物浓度时的酶反应速度。
以吸光度的倒数作纵坐标,以底物浓度的倒数作横坐标,按Lineweaver-Burk作图法可求出Km值。
二. 器材721分光光度计台式离心机恒温水浴锅微量移液器托盘天平匀浆器试管三. 试剂1. 0.5mol/L醋酸镁溶液称取醋酸镁5.3625g溶于蒸馏水中,稀释至50ml.2. 0.1mol/L醋酸钠溶液称取醋酸钠0.0820g溶于蒸馏水中,稀释至10ml.3. 0.01mol/L醋酸镁---醋酸钠溶液取0.5mol/L醋酸镁溶液2ml及0.1mol/L醋酸钠溶溶液10ml,混合均匀后加蒸馏水稀释至100ml.4. 丙酮(分析纯).5. 95%乙醇(分析纯).6. Tris缓冲液(Ph8.8) 称取Tris 6.05g,用蒸馏水溶解成50ml,为0.1mol/L Tris液,取0.1mol/L Tris液10ml,加0.5mol/L醋酸镁2ml,加蒸馏水80ml,再用1%醋酸调pH至8.8,然后用蒸馏水稀释至100ml.7. 0.01mol/L基质液称取磷酸苯二钠(C6H5PO4Na2.2H2o) 0.3g,4-氨基安替比林0.15g,分别溶于煮沸冷却后的蒸馏水中;两液混合并蒸馏水稀释至50ml,加0.2ml氯仿防腐,盛于棕色瓶中,冰箱内保存,可用一星期; 临用时与等量0.1mol/L pH10的碳酸盐缓冲液混合即可.8. 0.1mol/L pH10的碳酸盐缓冲液称取无水碳酸钠0.318g及碳酸氢钠0.168g溶于蒸馏水,稀释至50ml.9. 碱性溶液量取0.5mol/L氢氧化钠溶液与0.5mol/L碳酸氢钠溶液各20ml,混合后加蒸馏水至100ml.10. 0.5%铁氰化钾溶液称取铁氰化钾0.25g和硼酸0.75g,各溶于20ml蒸馏水中,溶解后两液混合均匀,再加蒸馏水至50ml,置棕色瓶中暗处保存.11. 0.1mol/L醋酸镁溶液称取醋酸镁0.2145g溶于蒸馏水中,稀释至10ml.12. 酚标准液(0.1mg/ml).四.实验步骤(1). “碱性磷酸酶分离纯化”实验操作。
碱性磷酸酶米氏常数测定
P60
【实验原理】
在环境的温度、pH和酶的浓度一定时,酶促反应速度与底物浓度之间的关系表现在反应开始时,酶促反应的速度(V)随底物浓度(S)的增加而迅速增加。
若继续增加底物浓度,反应速度的增加率将减少。
当底物浓度增加到某种程度时,反应速度会达到一个极限值,即最大反应速度(V max),如图所示。
底物浓度与酶促反应速度的这种关系可用Michaelis-Menten方程式表示。
V = V max[S]/(K m+[S])
上式中V max为最大反应速度,[S]为底物浓度,K m为米氏常数(Michaelis constant),而其中V则表示反应的起始速度。
当V= V max/2时,K m=[S]。
所以米氏常数是反应速度等于最大反应速度一半时底物的浓度。
因此K m的单位以摩尔浓度(mol/L)表示。
K m是酶的最重要的特征性常数,测定K m值是研究酶动力学的一种重要方法,大多数酶的K m值在0.01-100(mmol/L)间。
酶促反应的最大速度V max实际上不易准确测定,K m值也就不易准确测出。
林-贝(1ineweaver - Burk)根据Michaelis-Menten方程,推导出如下方程式,即:1/V = (K m +[S])/ V max[S]或1/V = K m/ V max·(1/[S])+1/ V max
此式为直线方程,以不同的底物浓度1/[S]为横坐标,以1/V为纵坐标,并将各点连成一直线,向纵轴方向延长,此线与横轴相交的负截距为-1/ K m,由此可以正确求得该酶的K m值,如图所示。
本实验以碱性磷酸酶为例,测定不同底物浓度的酶活性,再根据Lineweaver-Burk法作图,计算其K m值。
可以作为碱性磷酸酶底物的物质很多,底物反应的酶对于不同的底物有不同的K m值。
本实验以磷酸苯二钠为底物,由碱性磷酸酶催化水解,生成游离酚和磷酸盐。
酚在碱性条件下与4-氨基安替比林作用,经铁氰化钾氧化,生成红色的醌衍生物,颜色深浅和酚的含量成正比。
故可以从标准曲线上查知酚的含量,从而计算化学反应速度。
反应式如下:
【实验方法】
一.底物浓度对酶促反应速度的影响
(1) 取6支试管,作好标记,按下表操作。
管号123456
0.04mol/L 基质液/mL0.10 0.20 0.30 0.40 0.80 0.0 0.1mol/L碳酸盐缓冲液/mL0.70 0.70 0.70 0.70 0.70 0.70
蒸馏水/mL 1.10 1.00 0.90 0.80 0.40 1.20
37℃水浴5min
血清/mL0.10 0.10 0.10 0.10 0.10 0.10 最终基质浓度/mmol∙L-1 2.00 4.00 6.00 8.00 16.00 0.00
(2) 加入血清后,各管混匀并且立即记录时间,将上述各管置37℃水浴中准确保温15 分钟。
(3) 保温结束,立即加碱性溶液1.1mL终止反应。
(4) 各管分别加入0.3%4-氨基安替比林1.0mL,0.5%铁氰化钾2.0mL,充分混匀,放置10分钟,以6号空白管作对照,于510nm波长处比色测定,根据酚标准曲线计算酚含量。
(5) 以各管基质浓度的倒数1/[S]为横坐标,以各管反应速度的倒数1/V(µmol.L-1.min-1为单位)作纵坐标,作图求出K m值。
二.酚标准曲线的绘制
(1) 取洁净干燥试管6支,按下表依次加入试剂。
管号123456 0.1mg/mL 酚标准溶液/mL0.0 0.05 0.10 0.20 0.30 0.40
蒸馏水/mL 2.0 1.95 1.90 1.80 1.70 1.60
37℃水浴5min
碱性溶液/mL 1.10 1.10 1.10 1.10 1.10 1.10 0.3% 4-氨基安替比林/mL 1.0 1.0 1.0 1.0 1.0 1.0
0.5% 铁氰化钾/mL 2.0 2.0 2.0 2.0 2.0 2.0
(2) 混匀后室温放置15分钟,于510nm波长处比色。
(3) 以酚含量(μg)为横坐标,吸光度为纵坐标,绘制酚标准曲线。
【实验结果】
酚含量。