高考化学氯气及其化合物重要方程式
- 格式:doc
- 大小:126.00 KB
- 文档页数:2

高中化学方程式大全和重要离子方程式高中化学方程式总结高考总复习之高中化学方程式总结化学第一册第一章卤素第一节氯气1、2 Na Cl 2 点燃 2 NaCl2、Cu Cl 2 点燃CuCl 23、 2 Fe 3Cl 2 点燃 2 FeCl 34、H2 Cl 2 点燃(光照) 2 HCl5、 2P 3Cl 点燃 2 PCl 326、PCl 3 Cl 2 PCl 57、 Cl 2 H 2 O HCl HClO8、 2 Ca ( OH )2 2 Cl 2 Ca ( ClO )2 CaCl 2 2H 2O9、Ca(ClO)2 CO 2 H 2 O CaCO 3 2 HClO10、2 NaOH Cl 2 NaClO NaCl H 2 O11、4HCl MnO 2 MnCl 2 2H 2O Cl 212、2 KMnO 4 16 HCl (浓)2MnCl 2 2 KCl 5Cl 28 H 2 O13、2 HClO 见光O 22 HCl第二节氯化氢14、NaCl H 2 SO (浓)4 NaHSO 4 HCl15、NaHSO 4 NaCl Na 2 SO 4 HCl17、 HCl AgNO3AgCl HNO318、 NaClAgNO3AgClNaNO 319、 KClAgNO3AgCl KNO320、 2 HCl CaCO 3CaCl2H 2 O CO 2 第三节氧化还原反应21、 CuOH 2 Cu H 2 O22、 C4HNO 3CO 24NO 2 2H 2O23、 4 Zn10 HNO (极稀) 4 Zn () NH 4NO 3 3H 2O 3NO 3 224、 11 P 15 CuSO 424H 2O5 Cu 3 P 6H 3PO 415H 2SO 425、 KClO36HCl (浓)3 Cl 2KCl3H 2O26、 4 Mg10 HNO(极稀)4Mg ( NO )NH 4NO 33H 2O33 227、 K 2Cr 2O76 Fe 3 O4 31 H 2SO4 Cr ( SO ) 9 Fe (SO ) K 2SO4 31 H 2O24 324 328、 2 KNO 33C SK 2 S N 2 3CO 2第四节卤族元素29、 H30、 H2F 2 2HF2 Br 2 2 HBr31、H 2I 22 HI32、 2 NaBr Cl 22 NaCl Br 233、 2KI Cl 2 2 KCl I 234、 2 KI Br 22 KBrI 235、 NaBrAgNO3AgBrNaNO 336、 KI AgNO 3AgIKNO337、 2 AgBr 光照2 Ag Br 2第二章摩尔反应热第一节摩尔38、 C O 2 CO 239、Mg 2 HCl MgCl 2 H 2第二节气体摩尔体积40、 Zn 2HCl ZnCl 2 H 2第三节物质的量浓度41、 2 NaOH H2SO4 Na 2 SO 4 2 H 2 O第四节反应热42、C(固)O (气)2 点燃CO (气)2 393 .5kJ43、 2 H (气)2 O (气)2 2H 2 O(气)483 .6 kJ44、 2 H (气)2 O (气)2 2H 2 O(液)571 .6 kJ45、C(固)H 2O(气)CO (气)H (2气)131 .3kJ第三章硫硫酸第一节硫46、2Cu S Cu 2 S47、Fe S FeS48、S H 2 H 2S49、S高温CS 2 C50、S点燃O 2 SO 251、3S 6 KOH 2K 2S K2SO4 3H2O 第二节硫的氢化物和氧化物52、H2S H 2 S53、2H2S 3O2(足)点燃2SO 22H 2O54、2H2S O 2 (不足)点燃2 S2H 2O点燃2H 2O 3S 55、2H2S SO256、H 2S Br2 S2 HBr57、FeS 2 HCl FeCl 2 H 2 S58、CuSO 4 H 2 S CuS H2SO459、PbAc 2 H 2 S PbS 2 HAc60、 H 2S NaOH NaHS H 2 O61、 NaHS NaOH Na 2 S H 2 O62、 H 2S 2 NaOH Na 2 S 2H 2O (60、61 结合)63、H2S 2 FeCl 3 S 2 FeCl 2 2 HCl64、H2SO(4 稀)FeS FeSO 4 H 2 S65、SO2 H 2 O H2SO366、 2SO 2 O 2 V2O5 2SO 367、SO3 H 2 O H2SO468、Na2SO3H2SO4 Na 2 SO 4 H2O SO269、SO2 2 NaOH Na 2 SO 3 H 2 O70、SO2 CaO CaSO 371、SO2 2Ca ( OH )2 CaSO 3 H 2 O72、SO73、SO74、 SO75、 SO 2CaSO 3 H 2 O Ca ( HSO 3)2 22H 2S 3S 2H 2O2Cl 2 2H 2O 2 HCl H2SO4 2Br 2 2H 2O 2 HBr H2SO476、 5SO 2 2 H 2 O 2 KMnO 4MnSO 4 K 2 SO 4 2 H 2 SO 4 第三节硫酸的工业制法高温78、2SO2 O2 V2O5 2SO 379、H2O SO3 H2SO4第四节硫酸硫酸盐80、C 2H 2SO (4浓)CO81、S 2H 2SO (4浓)3SO 2 2SO 2 2H 2O 22 H 2 O82、P H(浓)H3PO4 SO 2 2H 2O 2SO483、H2S H 2SO (4 浓)S SO2 2H 2O84、Cu 2H 2SO (4 浓)CuSO 4 SO 2 2H 2O85、BaCl86、BaCl87、BaCl 2H2SO4 BaSO 4 2 HCl2Na 2SO 4 BaSO 4 2 NaCl 2 Na 2CO3 BaCO 3 2 NaCl88、BaCO 3 2 HCl BaCl 2 H 2 O CO 289、BaCO 3 2 HNO 3 Ba ( NO 3)2 H 2 O CO 290、Na2CO3 H2SO3 Na 2 S H 2 O CO 291、2H2SO3 O 2 2H 2SO 492、2 Na2SO3O2 2Na 2 SO 493、2CaSO 3 O 2 2 CaSO 494、2 Fe 6 H(浓)()3SO 2 6H 2O 2SO4 Fe 2 SO 4 395、2 NaBr 2H 2SO (4浓)Br 2 SO 2 Na 2 SO 4 H 2 O96、2 NaCl H 2SO (4浓)Na 2 SO 4 2 HCl浓H2SO 412 C 11H 2O97、C11H22O11第四章碱金属第一节钠98、 4 Na O 2 Na O99、 2 NaO 2Na 2 O 2100、 2 Na点燃2 NaClCl 2101、 2 Na S 研磨Na 2 S102、 2 Na 2H 2O 2 NaOH H 2103、 2 Na 2H 2OCuSO 4Cu ( OH )2 Na 2 SO 4 H 2第二节钠的氧化物104、 Na 2OH 2 O2 NaOH105、 2 Na 2 O 22H 2O 4 NaOH O 2106、 Na2OCO 2 Na 2 CO 3107、 2 Na 2 O 22CO 2 2 Na 2 CO 3 O 2108、 Na 2 O2HCl2 NaClH 2 O109、 Na2O24 HCl 4 NaCl 2H 2O O 2 110、 Na 2 CO 3 2 HCl2 NaClCO 2 H 2 O 111、 NaHCO 3 HCl NaCl CO 2 H 2 O 112、 2 NaHCO3Na 2 CO 3CO 2H 2 O113、 NaHCO114、 2 NaHCO3NaOH Na 2 CO 3 H 2 O3 Ca ( OH )(少量)CaCO3Na 2CO3 2 H 2O2115、 NaHCO3Ca ( OH )(足量)CaCO3NaOHH 2O2116、 Na 2 CO 3 117、 Na 2 CO 3 BaClCaCl22BaCOCaCO332 NaCl2 NaCl118、 Ca ( HCO 3)22 HCl CaCl 2 2 CO 22H 2O119、 Ca ( HCO3)22NaOHCaCO 3 Na 2 CO 3 2H 2 O 120、 NaHSO HClNaClSO H O第三节碱金属元素121、4 Li点燃O 2 2Li 2 O122、K点燃KO 2 O 2123、2 M X 2 2 MX ( M 表示氧族元素, X 代表卤族元素)124、2 M H 2 2 MH125、2 M 2H2O 2MOHH 2第五章物质结构元素周期律本章内容、性质特殊,所有化学反应方程式均融在其他章节中。

备战高考化学氯及其化合物的综合热点考点难点及详细答案一、 高中化学氯及其化合物1.已知Cl 2在70℃的NaOH 水溶液中,能发生氧化还原反应后可生成NaClO 与NaClO 3现有63.9g Cl 2,将其通入到足量70℃的NaOH 水溶液中,反应完全后测得溶液中NaClO 与NaClO 3的物质的量比为4:1,并得到500mL 溶液。
(1)写出Cl 2在70℃的NaOH 水溶液中发生上述反应的化学方程式______。
(2)计算完全反应后溶液中NaClO 、NaClO 3物质的量浓度____、______。
【答案】9Cl 2+14NaOH=4NaClO+NaClO 3+9NaCl+7H 2O 0.8mol/L 0.2mol/L【解析】【分析】先通过氯元素化合价的对比判断NaClO 与NaClO 3是氧化产物,氯气得电子化合价降低的产物是还原产物,所以还原产物是氯化钠,根据氧化还原反应中得失电子数相等配平方程式,从而得出反应中被氧化的Cl 2与被还原的Cl 2的物质的量之比。
【详解】(1)该反应中NaClO 与NaClO 3是氧化产物,氯化钠是还原产物,反应完全后测得溶液中NaClO 与NaClO 3的物质的量比为4:1,根据氧化还原反应中得失电子数相等配平方程式,所以该方程式为:9Cl 2+14NaOH=4NaClO+NaClO 3+9NaCl+7H 2O ;(2)49.7g Cl 2的物质的量为63.9g 71g /mol =0.9mol ,根据反应9Cl 2+14NaOH=4NaClO+NaClO 3+9NaCl+7H 2O 可知,生成NaClO 与NaClO 3的物质的量分别为0.9mol 40.4mol 9⨯=、0.9mol 10.1mol 9⨯=,完全反应后溶液中NaClO 、NaClO 3物质的量浓度分别为0.4mol 0.8/0.5mol L L =、0.1mol 0.2/0.5mol L L=。
高考化学必备专题——氯气和卤族元素(附参考答案)【高考预测】氯为非金属的代表元素,在生产生活中用途广泛。
不仅在选择题中对其及其化合物经常考察外,还利用元素推断题、工业流程题、实验题等考察氯的结构、在周期表中位置、氯水的成分、以及氯化钠溶液的电解等相关知识和实验。
一、知识网络1.氯及其化合物2.卤素及其化合物二、重点知识(一)氯气的性质及用途1.物理性质:常温下,氯气是黄绿色、有刺激性、能溶于水、比空气重、易液化的有毒气体。
2.化学性质:氯气的化学性质很活泼的非金属单质。
(1)与金属反应(与变价金属反应,均是金属氧化成高价态)如:①2Na +Cl2 2NaCl (产生白烟) ②Cu +Cl2 CuCl2(产生棕黄色的烟) ③2Fe +3Cl22FeCl3(产生棕色的烟)注:常温下干燥的氯气或液氯不与铁反应,所以液氯通常储存在钢瓶中 (2)与非金属反应 如:①H2+Cl22HCl (发出苍白色火焰,有白雾生成)——可用于工业制盐酸H2+Cl22HCl (会发生爆炸)——不可用于工业制盐酸 ②2P +3Cl22PCl3(氯气不足;产生白雾) 2P +5Cl22PCl5(氯气充足;产生白烟)(3)与水反应:Cl2+H2O = HCl +HClO (4)与碱反应Cl2+2NaOH = NaCl +NaClO +H2O (用于除去多余的氯气) 2Cl2+2Ca(OH)2 = Ca(ClO)2+CaCl2+2H2O (用于制漂粉精) Ca(ClO)2+CO2+H2O = CaCO3↓+2HClO (漂粉精的漂白原理) (5)与某些还原性物质反应 如:①2FeCl2+Cl2 = 2FeCl3②2KI +Cl2 = 2KCl + I2(使湿润的淀粉-KI 试纸变蓝色,用于氯气的检验) ③SO2+Cl2+2H2O = 2HCl + H2SO4 (6)与某些有机物反应如:①CH4+Cl2 CH3Cl + HCl (取代反应) ②CH2=CH2+Cl2 → CH2ClCH2Cl (加成反应) 例1:(2013·上海化学·7)将X 气体通入BaCl2溶液,未见沉淀生成,然后通入Y 气体,有沉淀生成,X 、Y 不可能是【答案】B3.氯水的成分及性质氯气溶于水得黄绿色的溶液----氯水。


高三化学高考必记的化学方程式一、非金属元素的反应1. 卤族元素(1)氯气H 2+Cl 2=====点燃2HCl2Fe +3Cl 2=====点燃2FeCl 3Cl 2+H 2O===HCl +HClO2NaOH +Cl 2===NaClO +NaCl +H 2O2Ca(OH)2+2Cl 2===Ca(ClO)2+CaCl 2+2H 2O6FeBr 2+3Cl 2===4FeBr 3+2FeCl 3(氯气少量)2FeBr 2+3Cl 2===2FeCl 3+2Br 2(氯气过量)[活学巧用] 氯水成分复杂,性质多样:强酸性——H +的性质;杀菌、漂白性——HClO 的性质;强氧化性——Cl 2的性质。
氯气溶于水,但不溶于饱和食盐水,因此可用饱和食盐水除去Cl 2中的HCl 。
Cl 2与NaOH 溶液的反应被用于实验室除去多余的Cl 2,常出现在框图推断中。
[易错警示] 氯气与FeBr 2溶液反应时,一定要注意二者量的关系,Cl 2首先氧化的是Fe 2+,然后氧化Br -;但Cl 2与FeI 2溶液反应时,首先氧化的是I -,然后氧化Fe 2+。
根据得失电子守恒可得出相应反应的离子方程式,如等物质的量的Cl 2与FeBr 2在溶液中反应时,其离子方程式为2Fe 2++2Cl 2+2Br -===2Fe 3++4Cl -+Br 2。
(2)含氯化合物2HClO=====光照2HCl +O 2↑Ca(ClO)2+CO 2+H 2O===CaCO 3↓+2HClONaClO +2HCl===NaCl +Cl 2↑+H 2OMnO 2+4HCl(浓)=====△MnCl 2+Cl 2↑+2H 2O[活学巧用] HClO 可作漂白剂和杀菌剂是由于HClO 具有强氧化性,长时间放置的氯水易变质是由于HClO 在光照条件下极易分解,所以新制的氯水需避光保存。
(3)卤素单质间的置换反应Cl 2+2NaBr===Br 2+2NaClCl 2+2NaI===I 2+2NaClBr 2+2KI===2KBr +I 2[活学巧用] 以上反应可用于比较Cl 2、Br 2、I 2氧化性(非金属性)的强弱或与CCl 4、淀粉溶液相结合用于溶液中Br -、I -的检验。

关于氯气的方程式全文共四篇示例,供读者参考第一篇示例:氯气,化学式Cl₂,是一种常见的化学物质,具有刺激性气味和有毒性。
它是一种无色、非金属的气体,在常温下具有较高的密度,容易被制备和储存。
氯气主要用于水处理、消毒和工业生产中的一些化学反应。
氯气的合成反应可以用下面的方程式表示:Cl₂(g) = 2NaCl(s) + H₂(g)这是一种简单的反应方程,描述了氯气的制备方法。
在这个方程中,氯气是由氯化钠固体和盐酸溶液反应生成的。
氯气可以通过电解水产生氢气和氯气的分解。
这个过程在工业上被广泛应用,用来生产氯气和氢气。
氯气在水中的溶解过程也可以用化学方程式表示:Cl₂(g) + H₂O(l) = HCl(aq) + HOCl(aq)这个方程式描述了氯气在水中的溶解产生氯化氢和次氯酸。
这些产物都是有毒的化学物质,因此在处理氯气时需要特别注意安全。
氯气还可以和有机物发生反应,产生氯代烃等有机氯化合物。
氯气还可以参与四氯化碳的合成过程:C(s) + 2Cl₂(g) = CCl₄(l)这个方程式描述了氯气和碳的反应,生成四氯化碳。
四氯化碳是一种有机化合物,具有多种用途,例如作为溶剂、冷却剂和消防剂。
由于其对环境的破坏作用,四氯化碳的使用受到了限制。
除了以上几种反应,氯气还可以和其他化学物质发生多种反应,产生各种不同的产物。
在实际的化学生产和实验中,氯气的反应性和毒性需要被严格控制,以确保操作人员的安全。
氯气的用途也在不断扩展,比如在医药领域中作为消毒剂、在冶金工业中作为还原剂等。
氯气是一种重要的化学物质,在工业生产和实验研究中都有着广泛的应用。
通过了解氯气的方程式和反应特性,我们可以更好地利用这种化学物质,同时也应该注意保护环境和人体健康。
希望本文能够帮助读者更好地理解氯气的性质和用途。
第二篇示例:氯气,化学式为Cl2,是一种极具毒性的化学气体,具有刺激性的气味。
在工业中,氯气被广泛用于制造化学品、消毒和净化水等领域。
课时17 氯及其重要化合物知识点一 氯及其化合物的性质【考必备·清单】 1.氯气的性质 (1)物理性质[名师点拨] 实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,使极少量的Cl 2飘进鼻孔即可。
(2)化学性质①与金属反应:与变价金属反应生成高价金属氯化物。
与铁反应:2Fe +3Cl 2=====点燃2FeCl 3。
与铜反应:Cu +Cl 2=====点燃CuCl 2。
②与非金属反应与H 2反应:H 2+Cl 2=====点燃2HCl 。
③与水或碱反应(填写化学方程式)④与某些还原性物质反应(书写离子方程式)与FeCl 2溶液2Fe 2++Cl 2===2Fe 3++2Cl -2.次氯酸和次氯酸盐的性质(1)次氯酸(HClO)①不稳定性次氯酸分解反应的化学方程式为2HClO=====光照2HCl +O 2↑。
②强氧化性能将有色物质氧化为无色物质,作漂白剂;杀菌、消毒。
③弱酸性向NaClO 溶液中通入少量CO 2,离子方程式为ClO -+CO 2+H 2O===HCO -3+HClO 。
[名师点拨] 向NaClO 溶液中通入CO 2(不论是少量还是过量),均生成HCO -3和HClO 。
原因是酸性:H 2CO 3>HClO>HCO -3。
(2)次氯酸盐 ①漂白液②漂白粉[名师点拨] ①向Ca(ClO)2溶液中通入SO 2生成的是CaSO 4而不是CaSO 3。
②次氯酸盐(ClO-)不论是在酸性、碱性还是中性条件下,均具有强氧化性,均能氧化I -、Fe2+、SO2-3、S2-等还原性离子。
【夯基础·小题】1.判断正误(正确的打“√”,错误的打“×”)。
(1)Cl2具有很强的氧化性,在化学反应中只能作氧化剂()(2)过量的铁粉在少量氯气中加热,充分反应后产物为FeCl2()(3)氯水显酸性,可用pH试纸测定氯水的pH()(4)新制氯水必须用棕色瓶密封保存,光照氯水有气泡逸出,该气体是氯气()(5)氯气可以使湿润的有色布条褪色,所以氯气具有漂白性()(6)漂白粉溶液在空气中失效的离子方程式:ClO-+CO2+H2O===HClO+HCO-3()答案:(1)×(2)×(3)×(4)×(5)×(6)×2.氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是()A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟B.通常状况下,干燥的氯气能和Fe反应C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸解析:选B Cl2与铁的反应需要加热,所以在通常状况下,干燥的Cl2不能与Fe反应。

第1讲氯及其重要化合物[课程标准]1.结合真实情境中的应用实例或通过实验探究,了解氯及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。
2.结合实例认识卤素及其化合物的多样性,了解通过化学反应可以探索物质性质、实现物质转化,认识物质及其转化在促进社会文明进步、自然资源综合利用和环境保护中的重要价值。
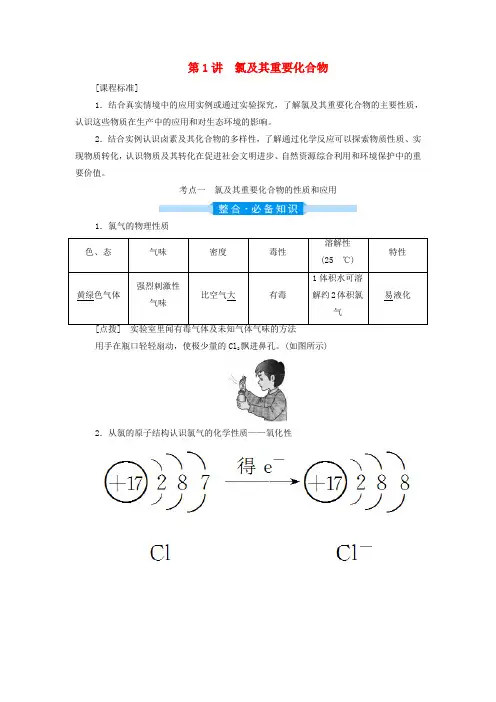
考点一氯及其重要化合物的性质和应用1.氯气的物理性质色、态气味密度毒性溶解性(25 ℃)特性黄绿色气体强烈刺激性气味比空气大有毒1体积水可溶解约2体积氯气易液化[点拨] 实验室里闻有毒气体及未知气体气味的方法用手在瓶口轻轻扇动,使极少量的Cl2飘进鼻孔。
(如图所示) 2.从氯的原子结构认识氯气的化学性质——氧化性3.从化合价的角度认识氯气的化学性质——歧化反应氯气与水或碱反应,氯元素的化合价既有升高又有降低,因而氯气既表现还原性又表现氧化性。
4.从平衡的角度理解氯水的成分和性质(1)氯水中存在三个平衡关系 ①Cl 2+H 2O HCl +HClO ②HClO H ++ClO -③H 2OH ++OH -(2)根据可逆反应的特点,可得出氯水中存在的各种微粒。
①三种分子:H 2O 、Cl 2、HClO 。
②四种离子:H +、Cl -、ClO -和OH -。
(3)氯水性质的多重性新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒不同。
[点拨] ①干燥的Cl 2没有漂白性,但Cl 2能使湿润的有色布条褪色,起漂白作用的是HClO 。
②1 mol Cl 2与强碱完全反应转移的电子数为N A ,而1 mol Cl 2与水充分反应转移的电子数小于N A (可逆反应)。
5.次氯酸和次氯酸盐的性质 (1)次氯酸次氯酸见光分解的化学方程式:2HClO=====光照2HCl +O 2↑。
(2)次氯酸盐①漂白液——“84”消毒液有效成分为NaClO ,它与洁厕灵(主要成分盐酸)混合会立即产生氯气,其离子方程式为ClO -+Cl -+2H +===Cl 2↑+H 2O 。
卤素及其化合物方程式总结一、与氯气有关的方程式:1)氯气与金属单质反应① Cl2+ Na─ (现象 )② Cl2+ Fe─ (现象 )③ Cl2+ Cu─ (现象 )2)氯气与非金属单质反应① Cl2+ H2─ (现象 )②Cl2+ P─ (现象 )3) 氯气与水反应① Cl2+ H2O─4)氯气与碱溶液反应① Cl2+ NaOH─ (用途 )② Cl2+ Ca(OH)2─ (用途 )③ Cl2+ KOH─④ Cl2+ Ca(OH)2─5) 氯气与某些盐溶液反应① Cl2+ Na2S─② Cl2+ FeCl2─③ Cl2(少量)+ FeBr2─④ Cl2(足量)+ FeBr2─⑤ Cl2+ Na2SO3+ H2O─⑥ Cl2+ NaBr─⑦ Cl2+ NaI─⑧ Cl2+ NaHSO3+ H2O─⑨ Cl2+ Na2CO3+ H2O─⑩ Cl2+ NaHCO3+ H2O─6)氯气与其它化合物反应:① Cl2+ H2S─② Cl2+ SO2+ H2O─③Cl2+ HBr─7) 氯气与有机物的反应Cl2+ CH4─ Cl2+ C6H6─8)实验室制氯气方程式:① MnO2+ HCl(浓)─② KMnO4+ HCl(浓)─③ K2Cr2O7+ HCl(浓)─④ MnO2+ NaCl(S)+ H2SO4(浓)─⑤ KClO3+ HCl(浓)─9)工业制氯气方程式二、与HCl有关的方程式1)与活泼金属反应① Fe+ HCl─②Zn+ HCl─2) 与碱性氧化物反应:① Fe2O3+ HCl─② CaO+ HCl─3) 与盐溶液反应① AgNO3+ HCl─②CaCO3+ HCl─③ Na2CO3+ HCl(少量)─④ Na2CO3+ HCl(过量)─⑤ 3Na2CO3+ 4HCl─⑥ Na2SO3+ HCl(过量)─4)与含C=C或C≡C的不饱和有机物或氨基酸或羧酸盐或酚钠反应① CH2=CH2+ HCl→② CH≡CH+ HCl→③ NH2-CH2-COOH+ HCl→④ C6H5ONa+ HCl→⑤ CH3-COONa+ HCl→⑥NH2-CH2-COONa+ HCl→三、其它① HClO─② NaClO+ CO2+ H2O─③ Ca(ClO)2+ CO2+ H2O─④ NaCl─。
高考化学专题题库∶氯及其化合物的综合题含答案解析一、 高中化学氯及其化合物1.实验室迅速制备少量氯气可利用如下反应:KMnO 4+HCl(浓)→KCl +MnCl 2+Cl 2↑+H 2O(未配平),此反应常温下就可以迅速进行。
请回答下列问题:(1)上述反应中被氧化的元素是_________。
当生成3.36L (标准状况下)Cl 2时,转移电子的物质的量为_________。
(2)如果上述化学方程式中KMnO 4化学计量数是1,则HCl 的化学计量数是_________。
(3)实验室通常利用MnO 2与浓盐酸共热反应制得氯气,据此可知KMnO 4、Cl 2、MnO 2三种物质的氧化性由强到弱的顺序为________。
(4)酸性KMnO 4溶液与Fe 2+反应生成Mn 2+,该反应的离子方程式是________。
(5)下列物质既有氧化性,又有还原性的是________(填字母代号)。
A .I -B .HClC .MnCl 2D .Cl 2【答案】Cl 0.3mol 8 422KMnO MnO Cl >>232425Fe MnO 8H 5FeMn 4H O +-+++++=++ BCD 【解析】【分析】比较氧化还原反应中物质的氧化性和还原性时,若两物质在同一反应中,则满足氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物;若两物质在两个不同反应中时,可借助一个“桥”,即第三者产生联系,若找不到第三者,需比较反应条件,反应条件越高,氧化剂的氧化能力或还原剂的还原能力越弱。
【详解】对于反应KMnO 4+HCl(浓)→KCl +MnCl 2+Cl 2↑+H 2O ,KMnO 4+5e -→MnCl 2,2HCl-2e -→Cl 2↑,依据电子守恒,则为2KMnO 4+10e -→2MnCl 2,10HCl -10e -→5Cl 2↑,再考虑质量守恒,即可配平2KCl +2MnCl 2,最后配HCl 。
氯及其重要化合物一、氯气及其化合物的性质及应用 1.氯气的物理性质2.氯气的化学性质(1)与金属反应与变价金属反应生成□06最高价态金属氯化物。
①与铁反应:□072Fe +3Cl 2=====点燃2FeCl 3。
②与铜反应:□08Cu +Cl 2=====点燃CuCl 2。
(2)与非金属反应与H 2反应:□09H 2+Cl 2=====点燃或光照2HCl ,(3)与水反应溶于水的氯气部分与水反应,离子方程式为 □14Cl 2+H 2O H ++Cl -+HClO 。
(4)与碱反应与NaOH 溶液反应,离子方程式为 □15Cl 2+2OH -===Cl -+ClO -+H 2O 。
(5)与还原性无机化合物反应①与碘化钾溶液反应:□16Cl 2+2I -===I 2+2Cl -。
②与SO 2水溶液反应:□17Cl 2+SO 2+2H 2O===2Cl -+SO 2-4+4H +。
③与FeCl 2溶液反应:□182Fe 2++Cl 2===2Fe 3++2Cl -。
3.次氯酸的性质(1)不稳定性:□192HClO=====光照2HCl +O 2↑(填化学方程式);氯水须现用现配,保存在□20棕色瓶中,置于□21冷暗处。
(2)强氧化性①能将有机物中有颜色物质氧化为无色物质,作漂白剂。
②杀菌、消毒。
(3)弱酸性NaClO溶液中通入少量CO2,化学方程式为□22ClO-+CO2+H2O===HClO+HCO-3。
4.漂白粉的性质二、氯气的制备1.实验室制取、收集氯气的装置2.氯气的工业制备(1)电解饱和食盐水(氯碱工业) 化学方程式:□092NaCl +2H 2O=====通电2NaOH +Cl 2↑+H 2↑;离子方程式:□102Cl -+2H 2O=====通电2OH -+Cl 2↑+H 2↑。
(2)电解熔融的氯化钠化学方程式:□112NaCl(熔融)=====通电2Na +Cl 2↑。
三、卤素的性质、卤素离子的检验 1.卤素单质性质的相似性(1)都能与大多数金属反应,如2Fe +3Br 2===□012FeBr 3,但I 2与Fe 反应生成□02FeI 2。
高考化学氯及其化合物综合经典题含详细答案一、高中化学氯及其化合物1.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成都有着重要的应用。
(1)NaClO中Cl的化合价为____,有较强的___(填氧化、还原)性。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO42-,此反应的离子方程式为____。
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为____。
【答案】+1 氧化 2ClO3-+SO2=2ClO2+SO42- 2:5【解析】【分析】(1)根据化合物中正负化合价的代数和为0;根据次氯酸盐中Cl的化合价分析判断;(2)①KClO3与SO2在强酸性溶液中反应生成ClO2、硫酸根离子;②根据得失电子守恒计算。
【详解】(1)NaClO中Na为+1价,O为-2价,化合物中总化合价为0,则Cl为+1价;次氯酸盐中+1价的氯元素易得到电子,具有较强氧化性,故答案为:+1;氧化;(2)①KClO3与SO2在强酸性溶液中反应可制得ClO2,根据氧化还原反应的规律,同时应生成硫酸钾,反应的离子方程式为:2ClO3-+SO2=2ClO2+SO42-,故答案为:2ClO3-+SO2=2ClO2+SO42-;②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,反应中ClO2为氧化剂,Cl 元素化合价由+4价降低为-1价,Mn2+为还原剂,元素化合价由+2价升高到+4价,氧化剂和还原剂得失电子数目相等,则氧化剂和还原剂的物质的量之比为2∶5,故答案为:2∶5。
【点睛】本题的易错点为(2)②,要注意氧化还原反应的计算的一般方法的应用,解答本小题,也可以书写出反应的方程式再分析计算。
2.氯及其化合物在工农业生产和人类生活中有着重要的作用。
回答下列问题:(1)25℃时将氯气溶于水形成“氯气-氯水”体系,该体系存在多个含氯元素的平衡关系,其中之一为:Cl2(溶液)+H2O HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。
高考化学元素化合物主要的方程式总结一、卤族元素1、铁与氯气点燃:2Fe +3Cl 2 −−→−点燃2FeCl 32、铜与氯气点燃:Cu +Cl 2−−→−点燃 CuCl 23、钠与氯气点燃:2Na +Cl 2−−→−点燃 2NaCl4、氢气与氯气点燃或光照:H 2+Cl 2−−→−点燃 2HCl5、氯气与水:Cl 2+H 2O HCl +HClO6、氯气与硫化氢:H 2S +Cl 2→S ↓+2HCl7、氯化亚铁溶液与氯气:2FeCl 2 + Cl 2→2FeCl 38、氯气与二氧化硫1:1溶于水:SO 2+Cl 2+2H 2O →2HCl +H 2SO 49、SO 2使溴水褪色:SO 2+Br 2+2H 2O →2HBr +H 2SO 410、SO 2使碘水褪色:SO 2+I 2+2H 2O →2HI +H 2SO 411、氯气和NaOH 溶液:Cl 2+2NaOH →NaCl +NaClO +H 2O12、工业制漂粉精:2Cl 2+2Ca(OH)2→CaCl 2+Ca(ClO)2+2H 2O13、漂粉精漂白原理(用盐酸):Ca(ClO)2+2HCl →CaCl 2 +2HClO14、漂粉精溶液中通CO 2: Ca(ClO)2 +2CO 2+2H 2O →Ca(HCO 3)2 +2HClO15、工业制氯气: 2NaCl +2H 2O −−→−通电H 2↑+Cl 2↑+2NaOH 16、次氯酸的不稳定性: 2HClO −−→−光照2HCl+O ₂↑ 17、次氯酸的电离方程式: HClO ⇌H ++ClO - 18、实验室制氯气: 4HCl(浓)+MnO 2−→−∆MnCl 2+Cl 2↑+2H 2O 19、高锰酸钾和浓盐酸不加热制氯气: 2KMnO 4+16HCl(浓)→2KCl+2MnCl 2+5Cl 2↑+8H 2O 20、工业制盐酸: 2NaCl +2H 2O −−→−通电H 2↑+Cl 2↑+2NaOH ,H 2+Cl 2−−→−点燃2HCl 21、实验室制盐酸: H 2SO 4(浓)+2NaCl (s )−→−∆Na 2SO 4+2HCl↑ 22、铁和盐酸: Fe+2HCl →FeCl 2+ H 2↑23、氢氟酸电离方程式: HF ⇌H + + F -24、氟气和水: 2F 2+2H 2O →4HF+O 2 ↑25、锌和碘蒸气 : Zn + I 2 → ZnI 226、氟气和氢气: H +F →2HF27、溴和氢气: Br 2 + H 2 −→−∆ 2 HBr28、碘蒸气和氢气:I 2 + H 2 ⇌ 2 HI29、氯气和溴化钠:Cl 2+2NaBr →Br 2+2NaCl30、氯气和碘化钾:Cl 2+2KI →2KCl+I 231、溴和碘化钾:2KI + Br 2 →2KBr + I 232、铁和溴:2Fe +3Br 2 →2FeBr 333、碘和铁: Fe +I 2→FeI 234、氯化亚铁和溴单质:6FeCl 2+3Br 2→2FeBr 3 + 4FeCl 335、少量氯气和溴化亚铁:6FeBr 2+3Cl 2→2FeCl 3 + 4FeBr 336、足量氯气和溴化亚铁: 2FeBr 2+3Cl 2→2FeCl 3 + 2Br 237、少量氯气与碘化亚铁:FeI 2+Cl 2→FeCl 2+I 238、用硝酸银和稀硝酸检验X-(离子方程式):Cl- + Ag + → AgCl↓ 39、AgX 见光分解:AgX −−→−光照Ag+X 2 二、氧族元素 1、硫和铁加热: Fe + S −→−∆FeS 2、硫和铜加热:2Cu+S −→−∆Cu 2S 3、氯气和过量的铁加热:2Fe+3Cl 2−→−∆2FeCl 3 4、氯气和铜点燃:Cu+Cl 2−−→−点燃CuCl 2 5、铁和氧气点燃:3Fe + 2O 2 −−→−点燃 Fe 3O 4 6、铜和氧气点燃:2Cu + O 2−→−∆2CuO 7、汞和硫:HgS+O 2−→−∆Hg+SO 2 8、硫和氧气:S+O 2−−→−点燃SO 2 9、硫和氢气点燃: S+H 2−→−∆H 2S 10、硫和浓硫酸反应:S+2H 2SO 4(浓)−→−∆2H 2O+3SO 2↑ 11、用氯酸钾制氧气:2KClO 3 −−→−∆2MnO 2KCl+3O 2↑ 12、用双氧水制氧气:2H 2O 2 −−→−2MnO 2H 2O + O 2↑13、氯气和氢硫酸:H 2S+Cl 2→S+2HCl14、氢硫酸在空气中变浑浊:2H 2S+O 2 →2S↓+2H 2O15、硫化氢气体在足量的氧气中燃烧:2H 2S+3O 2→2H 2O+2SO 216、硫化氢气体在少量的氧气中燃烧: 2H 2S+O 2→2H 2O+2S ↓17、SO 2和H 2S 混合:2H 2S+SO 2→2H 20+3S ↓18、SO 2 被氧气氧化: 2SO 2 + O 2 ⇌ 3SO 319、SO 2 被水吸收:H 2O+SO 2→H 2SO 3→20、SO2 和氯气1:1通入水中:Cl 2+SO 2+2H 2O →2HCl+H 2SO 421、SO 2 使溴水褪色:SO 2 + Br 2 +2H 2O →H 2SO 4 +2HBr22、SO 2 使碘水褪色:SO 2+2H 2O+I 2→H 2SO 4+2HI.23、SO 2 通入足量澄清石灰水:SO 2+Ca(OH)2→CaSO 3↓+H 2O24、实验室制取H 2S :FeS+2HCl → FeCl 2+H 2S ↑25、实验室检验H 2S :CuSO 4+H 2S →CuS↓+H 2SO 426、实验室吸收H 2S :CuSO 4+H 2S →CuS↓+H 2SO 427、实验室制取SO 2:Na 2SO 3+H 2SO 4(浓)→Na 2SO 4+SO 2↑+H 2O28、实验室吸收SO 2;:SO 2+2NaOH →Na 2SO 3+H 2O29、 NaOH 和过量SO 2:SO 2+NaOH →NaHSO 330、铜和浓硫酸: Cu+2H 2SO 4(浓)−→−∆CuSO 4+2H 2O+SO 2↑ 31、碳和浓硫酸: C+2H 2SO 4(浓)−→−∆CO 2↑+2SO 2↑+2H 2O 32、硫化氢和浓硫酸:H 2S+3H 2SO4 →4SO 2↑+4H 2O三、氮族1、氮气和氧气:N 2+O 2→2NO2、氮气和氢气::N 2+3H 2−−−−−−→−高温、高加压、催化剂2NH 3 3、氮气和金属镁高温: N 2+3Mg −−→−高温Mg 3N 2 4、NO 和氧气:2NO+O 2→2NO 25、NO 2 和水: 3NO 2+H 2O →2HNO 3+NO6、工业制氨气:N 2+3H 2−−−−−−→−高温、高加压、催化剂2NH 3 7、实验室制氨气:2NH 4Cl+Ca(OH)2−→−∆ CaCl 2+2NH 3↑+2H 2O8、氨气和水: NH 3+H 2O ⇌NH 3.H 2O9、一水合氨的电离:NH 3.H 2O ⇌NH4+ + OH -10、一水合氨受热分解: NH 3·H 2O −→−∆NH 3↑+ H 2O 11、氨气和氯化氢气体:HCl+NH 3→NH 4Cl12、氨气和硫酸: H 2SO 4 +2 NH 3 → (NH4)2SO 413、氨气和硝酸:HNO 3 + NH 3 → NH 4NO 3 14、氨气和氧气: 4NH 3+3O2−−→−点燃2N 2+6H 2O 15、氯化铵受热分解:NH 4Cl −→−∆NH 3+HCl 16、碳酸氢铵受热分解:NH 4HCO 3−→−∆NH 3↑+CO 2↑+H 2O 17、硝酸见光分解: 4HNO 3−−→−光照 4NO 2 ↑+ O 2↑ + 2H 2O 18、铜和浓硫酸: Cu+2H 2SO 4(浓)−→−∆CuSO 4+2H 2O+SO 2↑ 19、铜和稀硝酸(离子方程式):3Cu+8H ++ 2NO 3-→3Cu 2+ +2NO↑+4H 2O 20、碳和浓硝酸加热:Cu+4HNO 3(浓)−→−∆Cu(NO 3)2+2NO 2↑+2H 2O 四、碳族 1、碳和氧气(不足)加热:2C+O 2−−→−点燃2CO 2、氧气(充足)加热:C+O 2−−→−点燃 CO 2 3、碳和浓硝酸加热:C+4HNO 3(浓)−→−∆CO 2↑+4NO 2↑+2H 2O 4、工业上用CO 还原氧化铁冶炼铁:Fe 2O 3+3CO −−→−高温. 2Fe+3CO 2 5、CO 和氧化铜: CuO + CO −→−∆ Cu + CO 2 6、工业上制取CO 2:CaCO 3−−→−高温CaO+CO 2↑ 7、实验室制取CO 2 : CaCO 3+2HCl →CaCl 2+H 2O+CO 2↑8、NaOH 溶液中通入少量CO 2(离子): CO 2+2OH -→CO 32-+H 2O 9、NaOH 溶液中通入过量CO 2(离子):CO 2+ OH -→HCO 3- 10、澄清石灰水中通入少量CO 2(离子):Ca 2++ 2OH - +CO 2→CaCO 3↓+ H 2O11、澄清石灰水中通入过量CO 2(离子): OH - + CO 2→HCO 3-12、Na 2SiO 3溶液中通入少量CO 2:Na 2SiO 3+CO 2+H 2O →Na 2CO 3+H 2SiO 3↓13、Na 2SiO 3溶液中通入过量CO 2:Na 2SiO 3+2CO 2+2H 2O →2NaHCO 3+H 2SiO 3↓14、NaAlO 2溶液中通入少量CO 2(离子):2AlO 2- + CO 2 (少)+ 3H 2O →2Al(OH)3↓ + CO 32-15、NaAlO 2溶液中通入过量CO 2(离子):AlO 2- + CO 2 (过)+ 2H 2O →Al(OH)3↓ + HCO 3-16、Mg 和CO 2高温:2Mg+CO 2−−→−高温2MgO+C 17、CO2和水反应:CO 2 + H 2O → H 2CO 318、碳酸电离方程式:H 2CO 3 ⇌H ++HCO 3-; HCO 3- -⇌(H +)+(CO 3)2-19、CaC 2制乙炔气体: CaC 2+2H 2O →Ca(OH)2+C 2H 2↑五、镁和铝 1、Mg + O 2:2Mg + O 2 −−→−点燃2MgO 2、Mg+H2O :Mg+H 2O →Mg(OH)2+H 2↑ 3、Mg+N 2:3Mg+N 2−−→−点燃Mg 3N 2 4、Mg+CO 2 : 2Mg+CO 2−−→−点燃2MgO+C 5、MgCl 2 和氨水:MgCl 2+2NH 3•H 2O →Mg (OH )2↓+2NH 4Cl 6、氢氧化镁受热分解:Mg(OH)2−−→−加热MgO + H 2O 7、铝和氧气: 4 Al + 3 O 2−−→−点燃 2 Al 2O 3 8、铝和水: 2Al+6H 2O →2Al(OH)3↓+3H 2↑ 9、铝和硫加热:2Al+3S −−→−加热Al 2S 3 10、铝和稀硫酸:2Al+3H 2SO 4→Al 2(SO 4)3+3H 2↑11、铝和氢氧化钠溶液:2 Al+2NaOH+2H 2O →2NaAlO 2+3H 2↑ 12、铝和四氧化三铁::8Al+3Fe 3O 4−−→−高温4Al 2O 3+9Fe 13、铝和二氧化锰:4Al+3MnO 2−→−∆2Al 2O 3+3Mn 14、铝和浓硫酸加热:发生钝化15、铝和硝酸汞: 2Al + 3Hg(NO 3)2 → 2Al(NO 3)3 +3Hg 16、铝和稀硝酸加热:Al +4HNO 3 −→−∆Al(NO 3)3 +NO ↑ +2H 2O 17、Al 2O 3+H 2SO 4:Al 2O 3+3H 2SO 4→Al 2(SO 4)3+3H 2O18、Al 2O 3+NaOH(离子):Al 2O 3+2OH -→2AlO 2-+H2O . 19、氢氧化铝和硫酸(离子):Al(OH)+3H + →Al 3+ + 3H O20、氢氧化铝和氢氧化钠:Al(OH)3 + NaOH →NaAlO 2 + 2H 2O21、氢氧化铝电离:Al(OH)3 ⇌Al 3+ + 3OH -22、氯化镁溶液呈酸性(离子):Mg 2++H 2O ⇌Mg(OH)2+2H +23、氯化铝呈酸性(离子):Al 3++3H 3O ⇌Al (OH )3+3H +24、氯化铝和少量氢氧化钠(离子):Al 3+ +3OH -→Al(OH)3↓25、氯化铝和足量氢氧化钠(离子):Al 3+ + 4OH - → AlO 2- + 2H 2O26、氯化铝和足量氨水(离子):Al 3++3NH 3H 2O →Al(OH)3↓+3NH 4+27、偏铝酸钠和少量盐酸(离子):AlO 2- +H 2O+H +→Al(OH)3↓28、偏铝酸钠和足量盐酸(离子):AlO 2- +4H +→Al 3+ +2H 2O29、偏铝酸钠和少量二氧化碳(离子): 2AlO 2- +CO 2+3H 2O →2Al(OH)3↓+CO 32-30、偏铝酸钠和足量二氧化碳(离子): AlO 2- +CO 2+2H 2O →Al(OH)3↓+ HCO 3-31、偏铝酸钠和氯化铝: AlCl 3 + 3NaAlO 2 + 6H 2O → 3NaCl + 4Al(OH)3 ↓32、工业炼钠: 2NaCl (熔融)−−→−通电2Na+Cl 2↑ 33、工业冶炼镁: MgCl 2(熔融)−−→−通电Mg+Cl 2↑ 34、工业冶炼铝: 2Al ₂O ₃−−→−通电4Al + 3O ₂↑ 六、铁和铜 1、铁和氧气: 3Fe+2O 2−−→−点燃Fe 3O 4 2、铜和氧气: 2Cu+O 2−→−∆2CuO 3、铁和氯气: 2Fe+3Cl 2−−→−点燃2FeCl 3 4、铜和氯气: Cu+Cl 2−−→−点燃CuCl 2 5、铁和硫加热: Fe + S −→−∆FeS 6、铜和硫: 2Cu+S −→−∆Cu 2S 7、铁和液溴: 2Fe +3Br 2 →2FeBr 38、铁和碘蒸气: I 2+Fe →FeI 29、铁和稀盐酸: Fe+2HCl →FeCl 2+H 2↑ 10、Fe+H2O(气): 3Fe+4H 2O −→−∆Fe 3O 4+4H 2 11、铁和氯化铜: Fe+CuCl 2→FeCl 2+Cu12、铁和硫酸铁(离子): Fe + 2Fe 3+ → 3Fe 2+13、铜和硫酸铁(离子): 2Fe 3+ + Cu → 2Fe 2+ + Cu 2+14、铁锈和盐酸: Fe 2O 3+6HCl →2FeCl 3+3H 2O15、铜和浓硫酸(加热): Cu+2H 2SO 4(浓)−→−∆CuSO 4+SO 2↑+2H 2O 16、铜和浓硝酸: Cu+4HNO 3(浓)→Cu(NO 3)2+2NO 2↑+2H 2O17、铜和稀硝酸(离子方程式): 3Cu + 2 NO 3 - + 8 H + →3 Cu 2+ + 2 NO(气体) + 4 H 2O18、氯化亚铁和氢氧化钠(离子方程式): Fe 2+ + 2OH -→Fe (OH )24Fe (OH )2+O 2+2H 2O →4Fe (OH )↓19、氢氧化亚铁和氧气、水反应: 4Fe(OH)₂+O ₂+2H 2O →4Fe(OH)₃↓ 20、氢氧化铁(分解): 2Fe(OH)3−→−∆Fe 2O 3+3H 2O 21、硫酸亚铁呈酸性的原因(离子): Fe 2++2H 2O ⇌Fe(OH)2+2H +22、氯化铁水解(离子方程式): Fe 3++3H 2O →Fe(OH)3↓+3H +23、三价铁离子检验(三种方法):①加KSCN,离子方程式②使淀粉碘化钾试纸离子方程式 ③加氢氧化钠或氨水,离子方程式:① Fe 3+ +3SCN - →Fe(SCN)3 ②2Fe 3+ +2I - →2Fe 2+ +I 2③ Fe 3+ + 3NH 3·H 2O → Fe(OH)3↓+ 3NH 4+24、二价铁离子检验:加氢氧化钠或氨水,离子方程式: Fe 2+ + 2NH 3.H 2O →Fe(OH)2↓+ 2NH 4+25、氯化铜和硫化氢: H 2S+CuCl 2→CuS↓+2HCl26、工业炼铁: Fe 2O 3+3CO −−→−高温2Fe+3CO 2。
光照通电 氯及其化合物的有关化学反应方程式1、氢气在氯气中燃烧 Cl 2+H 22HCl (将H 2在Cl 2点燃;混合点燃、加热、光照发生爆炸)2、钠与氯气中燃烧 Cl 2+2Na2NaCl 2、铁在氯气中燃烧 3Cl 2+2Fe2FeCl 3 3、铜在氯气中燃烧 Cl 2+Cu CuCl 24、氯气通入水中 Cl 2+H 2O HCl+HClO(Cl 2+H 2O ==2H ++Cl –+HClO )5、氯气用氢氧化钠溶液尾气吸收 Cl 2+2NaOH==NaCl+NaClO+H 2O(Cl 2+2OH –=Cl –+ClO –+H 2O)6、工业上制取漂白粉 2Cl 2+2Ca(OH)2==CaCl 2+Ca(ClO)2+2H 2O7、 漂白粉在空气中失效 ①Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO ②2HClO ======2HCl+O2↑(见光易分解) 8、次氯酸见光分解 2HClO=========2HCl+O2↑(见光易分解)9、氯气通入氯化亚铁溶液中 Cl 2+2FeCl 2===2FeCl 3(在水溶液中:Cl 2+2Fe 2+===2Fe 3++3Cl -)10、氯气通入碘化钾溶液中 Cl 2+2KI===2KCl+I 2Cl 2+2I =2Cl +I 211、氯气通入亚硫酸钠溶液中 Cl 2+SO 32-+H2O=SO42-+2Cl -+2H +12、氯气通入溴化钠溶液中 Cl2+2NaBr===2NaCl+Br2Cl2+2Br =2Cl +Br213、氯气通入氢硫酸溶液中 Cl 2+H 2S===2HCl+S ↓(水溶液中:Cl 2+H 2S=2H ++2Cl –+S ↓14、二氧化硫通入氯水中 Cl 2+SO 2+2H 2O===H 2SO 4+2HClCl 2+SO 2+2H 2O=4H++SO 42–+2Cl –15、.实验室氯气的制法:: MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O 16、.工业制法氯气:2NaCl+2H2O ========== 2NaOH+H2↑+Cl2↑17、NaClO 溶液中通少量CO2: 2NaClO+CO2+H2O====Na2CO3+2HClO光照18、与SO2水溶液反应: Cl2+SO2+2H2O====H2SO4+2HCl19、与FeCl2溶液反应: Cl2+2Fe2+====2Fe3++2Cl-22氯化铝于水反应:AlCl3+3H2O====Al(OH)3+3HCl 。