第25章 芳环上的取代反应
- 格式:ppt
- 大小:1.04 MB
- 文档页数:53
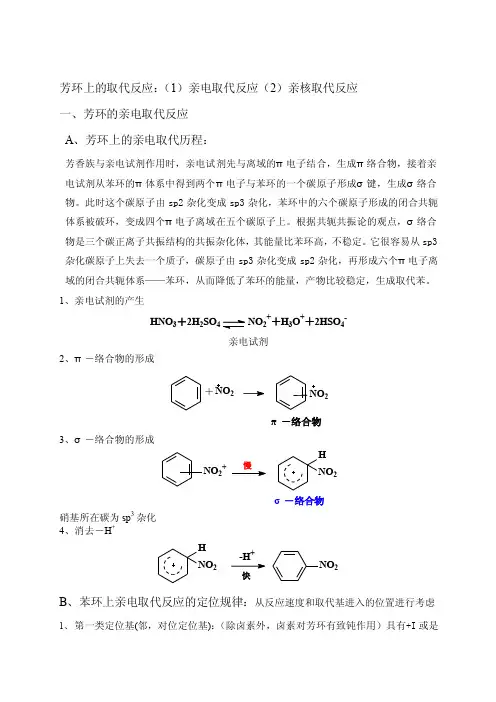
芳环上的取代反应:(1)亲电取代反应(2)亲核取代反应 一、芳环的亲电取代反应 A 、芳环上的亲电取代历程:芳香族与亲电试剂作用时,亲电试剂先与离域的π电子结合,生成π络合物,接着亲电试剂从苯环的π体系中得到两个π电子与苯环的一个碳原子形成σ键,生成σ络合物。
此时这个碳原子由sp2杂化变成sp3杂化,苯环中的六个碳原子形成的闭合共轭体系被破环,变成四个π电子离域在五个碳原子上。
根据共轭共振论的观点,σ络合物是三个碳正离子共振结构的共振杂化体,其能量比苯环高,不稳定。
它很容易从sp3杂化碳原子上失去一个质子,碳原子由sp3杂化变成sp2杂化,再形成六个π电子离域的闭合共轭体系——苯环,从而降低了苯环的能量,产物比较稳定,生成取代苯。
1、亲电试剂的产生HNO 3+2H 2SO4NO 2++H 3O ++2HSO 4-亲电试剂2、π-络合物的形成+NO 2π-络合物23、σ-络合物的形成NO 2+HNO2σ-络合物硝基所在碳为sp 3杂化 4、消去-H ++NO 2H NO 2快B 、苯环上亲电取代反应的定位规律:从反应速度和取代基进入的位置进行考虑1、 第一类定位基(邻,对位定位基):(除卤素外,卤素对芳环有致钝作用)具有+I 或是+C 效应,其作用是增大芳环的电子云密度。
致活基NH 2NHR2OHORNHCROPhR致钝基F Cl BrI2、 第二类定位基(间位定位基):具有-I 或-C 效应,使芳环上的电子云密度降低,均为致钝基NO 2NR 3COOHCOORSO 3HCNCHOCROCCl 3C 、影响亲电取代的因素:(1)芳环上取代基对于E +进入芳环位置的影响第一类定位基-邻对位定位基第二类定位基-间位定位基共振式越多, 正电荷分散程度越大,芳正离子越稳定。
(2) 动力学控制与热力学控制: α位取代-动力学控制产物; β位取代-热力学控制产物。
(3) 邻位和对位定向比:a 亲电试剂的活性越高,选择性越低。
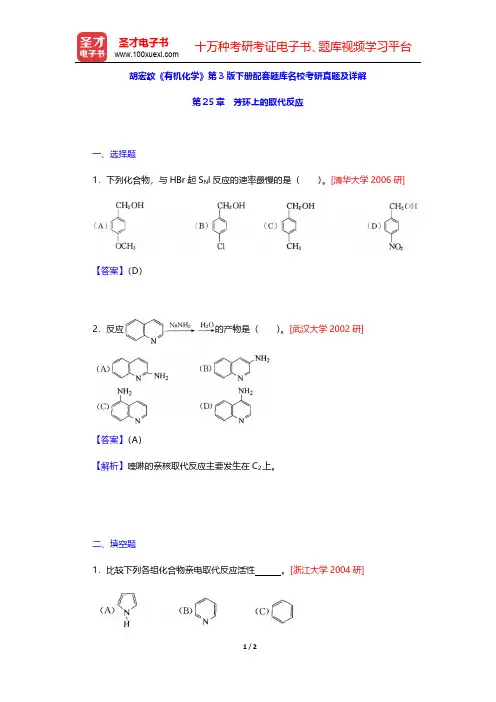
胡宏纹《有机化学》第3版下册配套题库名校考研真题及详解
第25章芳环上的取代反应
一、选择题
1.下列化合物,与HBr起S N l反应的速率最慢的是()。
[清华大学2006研]
【答案】(D)
2.反应的产物是()。
[武汉大学2002研]
【答案】(A)
【解析】喹啉的亲核取代反应主要发生在C2上。
二、填空题
1.比较下列各组化合物亲电取代反应活性。
[浙江大学2004研]
【答案】亲电取代反应活性:(A)>(C)>(B)
【解析】吡咯分子中环内每个碳原子提供1个p电子、氮原子提供2个p电子,组成大π键,氮原子的给电子共轭效应大于吸电子诱导效应,故吡咯中电子云密度比苯高;而吡啶分子中氮原子上的孤对电子没有参与大π键,氮原子的吸电子诱导效应大于给电子的共轭效应,故吡啶环内的电子云密度比苯低。
2.排出下列各化合物在亲电取代反应中的活性大小次序:。
[清华大学1999研、大连理工大学2003研]
【答案】亲电取代反应活性:(C)>(B)>(A)>D)
【解析】呋喃、噻吩电子云密度比苯高,相对而言,氧的给电子共轭效应比硫强,故呋喃的电子云密度比噻吩高,更易发生亲电取代反应,而吡啶中由于氮的电负性比碳强,故吡啶环上的电子云密度比苯低,其亲电取代反应活性不如苯。





技术资料精细有机单元反应习题集精细有机单元反应教材编写组2007,6第一章绪论一、填空题1、所谓“精细化率”是指。
2、精细化学品是经加工的,具有或最终使用性的,品种、产量小、附加高的一大类化工产品。
3、我国原化学工业部上个世纪八十年代颁布的《关于精细化工产品的分类的暂行规定和有关事项的通知》中明确规定,中国精细化工产品包括个产品类别。
4、有机精细化学品的合成是由若干个基本反应组成。
这些基本反应我们称之单元反应。
重要的单元反应有。
5、在新的合成路线设计和选择时,要优先考虑、污染环境不大且容易治理的工艺路线。
6、天然气的主要成分是。
根据甲烷含量的不同,天然气可分为两种。
7、煤通过方法提供化工原料。
8、催化重整是得到三种重要芳烃原料的方法。
二、判断题1、氧化锌类感光材料、铁酸盐类磁性材料、精细陶瓷产品、包括导电陶瓷、透光陶瓷等一般均属有机精细化学品。
2、在合成路线设计中,反应的排列方式也直接影响总收率。
一般来说,在反应步数相同的情况下,线性法的总收率高于收敛法,因此,尽可能采用线性法。
3、碳水化合物是由碳、氢、氧三种元素组成,它们的分子组成一般可表示为Cx(H2O)y, 如葡萄糖C6H12O6=C6(H2O)6,蔗糖C12H22O11=C12(H2O)11,所以说碳水化合物是由碳和水组成的化合物。
4、在进行合成路线设计和选择时,应尽量少用或不用易燃、易爆和有剧毒原料和试剂。
5、合成路线中反应步数和反应总收率是评价合成路线的最直接、最主要的标准。
三、简答题1、为什么说合成路线中反应步数和反应总收率是评价合成路线的最直接、最主要的标准。
2、简述精细化学品合成的原料来源。
3、在设计精细有机合成路线时,需要考虑哪些主要问题?4、写出以下基本化工原料主要来自哪种资源:(1)甲烷;(2)一氧化碳;(3)乙炔;(4)乙烯;(5)C18~C30直链烷烃;(6)C12~C18直链脂肪烃;(7)苯;(8)萘。
5、对精细化学品的定义进行释义。

芳环上的取代磺化一、磺化反应的历程及动力学磺化反应:一种向有机分子中引入磺酸基(—SO3H)或磺酰氯基(—SO3Cl)的反应过程,磺化是磺基(或磺酰卤基)中的硫原子与有机分子中的碳原子相连接形成C-S键的反应,生成的产物是磺酸(R—SO3H,R表示烃基)、磺酸盐(R—SO3M;M表示NH4或金属离子)或磺酰氯(R—SO2Cl)。
在这儿着重介绍芳环上的取代磺化。
磺化是亲电取代反应,因此芳环上有供电基使磺化反应速率变快,有吸电基使磺化反应速率变慢。
磺化也是连串反应,但是与氯化不同,磺酸基对芳环有较强的钝化作用,一磺酸比相应的被磺化物难于磺化,而二磺酸又比相应的一磺酸难于磺化。
因此,苯系和萘系化合物在磺化时,只要选择合适的反应条件,例如磺化剂的浓度和用量、反应的温度和时间,在一磺化时可以使被磺化物基本上完全一磺化,只副产很少量的二磺酸;在二磺化时只副产很少量的三磺酸。
例如,在苯的共沸去水一磺化时,磺化液中约含有88%~91%苯磺酸、小于 15%苯、小于0.5%苯二磺酸和2.0%~4%硫酸(均为质量分数,下同)。
芳香化合物进行磺化反应时,分两步进行。
首先,亲电质点向芳环进行亲电进攻,生成σ-配合物,后在碱作用下脱去质子得到芳环酸。
反应历程如下:研究证明,用浓硫酸磺化时,脱质子较慢,第二步是整个反应速率的控制步骤。
用稀酸磺化时,生成σ-配合物较慢,第一步限制了整个反应速率。
采用发烟硫酸或硫酸磺化芳烃时,其反应动力学可如下表示。
当磺化质点为SO3 时:v=kso3[ArH][SO3]=k′SO3[ArH][H2O]2-当磺化质点为H2S2O7时:v=kSA[ArH][H2S2O7]=k′H2S2O7[ArH][H2O]2-当磺化质点为H3SO4 +时:v=kH3SO4 +[ArH][H3SO4 +]=k′H3SO4 +[ArH][H2O]-由以上三式可以看出,磺化反应速率与磺化剂中的含水量有关。
当以浓硫酸为磺化剂,水很少时,磺化反应速率与水浓度的平方成反比,即生成的水量越多,反应速率下降越快。
芳环取代中的定位规律
芳环取代是有机化学中非常常见的反应之一,它指的是将芳环上的一个或多个氢原子替换为其他官能团。
在化学反应中,定位规律是非常重要的,因为它决定了反应产物的结构和性质。
在芳环取代中,定位规律有两种:电子效应和空间效应。
电子效应是指由于取代基对芳环的电子密度产生的影响。
对于电子给体取代基(如甲基、乙基等),它们会向芳环中心输送电子,增加芳环上的电子密度,因此更容易被亲电试剂攻击。
而电子受体取代基(如硝基、氰基等),则会吸引芳环上的电子,降低芳环上的电子密度,因此更容易被亲核试剂攻击。
空间效应是指由于取代基的体积和几何构型对反应的影响。
如果取代基体积较大,它可能会影响反应底物和试剂之间的空间排布,从而影响反应。
在某些情况下,取代基的几何构型也可能影响反应,例如在苯环的1,2位和1,3位上取代基的构型会影响它们对芳环上其他位置的反应活性。
总之,理解芳环取代反应中的定位规律是非常重要的,因为它可以帮助我们预测反应产物的结构和性质,并为有机化学合成和药物研究提供重要的指导。
- 1 -。
芳环上的取代氯化反应
芳环取代氯化反应是一种常见的有机化学反应,用于在芳环分子
的位置上引入氯原子。
该反应通常以氯化剂和芳环化合物为反应物,经过催化剂的作用,氯元素被取代到芳环化合物的碳原子上。
在常见的芳环取代氯化反应中,常用的氯化剂包括氯化亚铁(III)、氯化铁(III)、氯化亚锡(IV)等,催化剂常见的有氯化铜(II)、三氯化铝、五氯化钒等。
反应过程中,氯化剂首先被还原为氯离子,然后与芳环化合物发
生取代反应。
反应中,催化剂起到催化作用,降低了反应的活化能。
催化剂通常通过与氯离子形成络合物,加快了反应速率。
反
应的基本机理是亲电取代机理,即氯离子通过亲电攻击芳环化合物,将氯原子引入到芳环位置上。
芳环取代氯化反应的反应条件可以根据具体的反应物来确定。
通常,在适当的溶剂中进行反应,并控制反应温度和反应时间,以
获得较好的产率和选择性。
通过芳环取代氯化反应,可以在芳环化合物的分子结构上引入氯
原子,改变其物化性质以及反应性质。
此外,芳环取代氯化反应
还可用于合成具有特定结构的有机化合物,如取代基含有氯原子
的药物、杀虫剂等。
芳环取代氯化反应是一种常用的有机化学反应,能够在芳环化合
物的位置上引入氯原子。
该反应需要适当的氯化剂和催化剂,同
时在合适的条件下进行,以获得较好的反应产率和选择性。