芳环上的亲电和亲核取代反应
- 格式:ppt
- 大小:971.50 KB
- 文档页数:8

c-f键芳香亲核取代反应
C-F键芳香亲核取代反应是一种化学反应,其中芳香环(如苯环)中的碳-氟键在亲核试剂的作用下被取代。
这个反应通常需要一个具有足够
强亲核性的反应物(如醇、硫醇、酚或羧酸)和一个适当的芳香亲电
试剂(如卤代芳烃或硝基芳烃)。
这个反应的主要步骤包括:
1. 芳香亲电试剂进攻芳香环,使芳香环发生电子云密度分布的改变。
2. 氟原子从质子中释放出来,并从溶液中捕捉电子形成氟化物。
3. 亲核试剂(如醇)与氟原子进行交换,并在进攻邻近碳的同时提供
电子。
C-F键芳香亲核取代反应的主要应用是化学合成中的氟化物的引入。
这种反应的机理使得氟化物通常比其他卤素更容易发生亲核取代反应,
因为氟原子具有很高的电负性和共价键的稳定性。
需要注意的是,这个反应通常需要一定的条件,如酸催化剂或加热等,并且可能会产生副产物。
因此,在实际应用中,需要考虑到这些因素
并采取适当的措施。
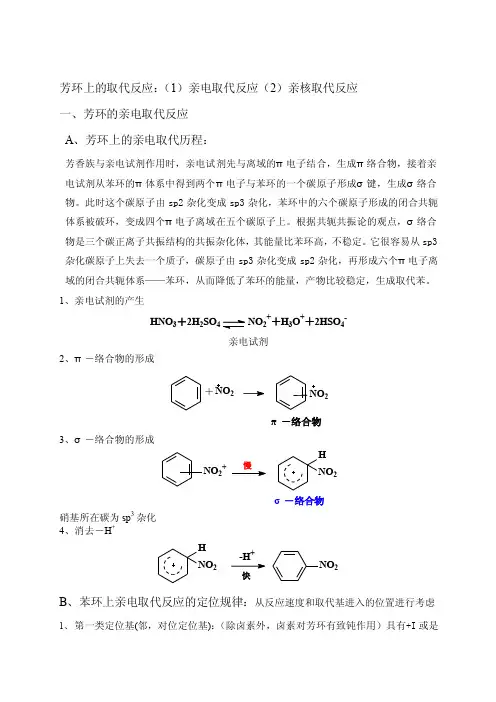
芳环上的取代反应:(1)亲电取代反应(2)亲核取代反应 一、芳环的亲电取代反应 A 、芳环上的亲电取代历程:芳香族与亲电试剂作用时,亲电试剂先与离域的π电子结合,生成π络合物,接着亲电试剂从苯环的π体系中得到两个π电子与苯环的一个碳原子形成σ键,生成σ络合物。
此时这个碳原子由sp2杂化变成sp3杂化,苯环中的六个碳原子形成的闭合共轭体系被破环,变成四个π电子离域在五个碳原子上。
根据共轭共振论的观点,σ络合物是三个碳正离子共振结构的共振杂化体,其能量比苯环高,不稳定。
它很容易从sp3杂化碳原子上失去一个质子,碳原子由sp3杂化变成sp2杂化,再形成六个π电子离域的闭合共轭体系——苯环,从而降低了苯环的能量,产物比较稳定,生成取代苯。
1、亲电试剂的产生HNO 3+2H 2SO4NO 2++H 3O ++2HSO 4-亲电试剂2、π-络合物的形成+NO 2π-络合物23、σ-络合物的形成NO 2+HNO2σ-络合物硝基所在碳为sp 3杂化 4、消去-H ++NO 2H NO 2快B 、苯环上亲电取代反应的定位规律:从反应速度和取代基进入的位置进行考虑1、 第一类定位基(邻,对位定位基):(除卤素外,卤素对芳环有致钝作用)具有+I 或是+C 效应,其作用是增大芳环的电子云密度。
致活基NH 2NHR2OHORNHCROPhR致钝基F Cl BrI2、 第二类定位基(间位定位基):具有-I 或-C 效应,使芳环上的电子云密度降低,均为致钝基NO 2NR 3COOHCOORSO 3HCNCHOCROCCl 3C 、影响亲电取代的因素:(1)芳环上取代基对于E +进入芳环位置的影响第一类定位基-邻对位定位基第二类定位基-间位定位基共振式越多, 正电荷分散程度越大,芳正离子越稳定。
(2) 动力学控制与热力学控制: α位取代-动力学控制产物; β位取代-热力学控制产物。
(3) 邻位和对位定向比:a 亲电试剂的活性越高,选择性越低。



有机化学中的芳香亲核取代与芳香亲电取代芳香亲核取代和芳香亲电取代是有机化学中的两个重要反应类型。
这两种反应是有机芳香化合物中的氢原子被置换为另一种原子或基团的过程。
本文将详细介绍芳香亲核取代和芳香亲电取代的原理、机理和应用。
一、芳香亲核取代芳香亲核取代反应是指芳香化合物中的氢原子被一个亲核试剂取代的过程。
亲核试剂可能是氢氧根离子、卤素离子、芳基负离子等。
这种反应一般需要在碱性条件下进行。
芳香亲核取代反应的机理是由共轭碳氢键的特殊性质决定的。
芳香环中的π电子可以共享给亲核试剂,而由于环上的π电子非常稳定,取代反应的活性较低,因此需要在碱性条件下进行。
常见的芳香亲核取代反应有苯酚的溴化反应、苯的硝化反应等。
苯酚的溴化反应以环境中的溴离子为亲核试剂,生成溴苯和溴化氢。
苯的硝化反应以硝酸为亲核试剂,生成硝基苯和水。
这些反应在有机合成中具有重要意义,可以用于合成药物、香料等化合物。
二、芳香亲电取代芳香亲电取代反应是指芳香化合物中的氢原子被一个亲电试剂取代的过程。
亲电试剂可能是正离子、电子不足的分子等。
这种反应一般需要在酸性条件下进行。
芳香亲电取代反应的原理是由共轭芳香体系的特殊稳定性决定的。
共轭芳香体系能够吸引亲电试剂的正电荷,使其参与反应。
芳香环上的π电子提供了稳定性和活性中心,使得亲电试剂能够与芳香化合物反应。
常见的芳香亲电取代反应有苯的硝化反应、苯的磺化反应等。
苯的硝化反应以浓硝酸为亲电试剂,在酸性条件下发生取代反应,生成硝基苯和水。
苯的磺化反应以浓硫酸为亲电试剂,生成苯磺酸和水。
这些反应在有机合成中也具有重要意义,可以用于合成各种化合物。
三、芳香亲核取代与芳香亲电取代的比较芳香亲核取代和芳香亲电取代在机理和反应条件上有明显的区别。
芳香亲核取代需要在碱性条件下进行,而芳香亲电取代需要在酸性条件下进行。
此外,芳香亲核取代的亲核试剂通常是负离子,而芳香亲电取代的亲电试剂通常是正离子或电子不足的分子。
两种反应类型在有机合成中有着不同的应用。



亲核取代和亲电取代机理亲核取代和亲电取代是有机化学中两种常见的取代反应机理。
它们分别指的是通过亲核试剂和亲电试剂进行的取代反应。
亲核取代是指以亲核试剂作为反应物,亲核试剂中的亲核原子攻击原有化合物的电子,将其替代出来的反应。
亲核试剂通常是带有孤对电子或具有亲电子云的化合物,如氢氧根离子(OH-)、氯离子(Cl-)等。
在亲核取代反应中,亲核试剂攻击原有化合物中具有较高反电子密度的原子,如卤素原子、烷基碳原子等。
亲核取代反应中,亲核试剂中的亲核原子与原有化合物中的原子形成新的化学键,使原有化合物中的原子被替代掉。
这种反应机理常见于醇的酯化反应、卤代烃的取代反应等。
亲电取代是指以亲电试剂作为反应物,亲电试剂中的亲电子云攻击原有化合物的电子,将其替代出来的反应。
亲电试剂通常是带有正电荷或具有亲电子云的化合物,如卤代烃、酸酐等。
在亲电取代反应中,亲电试剂中的亲电子云与原有化合物中的原子形成新的化学键,使原有化合物中的原子被替代掉。
亲电取代反应中,亲电试剂中的正电荷或亲电子云攻击原有化合物中的电子密度较高的原子,如孤对电子、芳环上的π电子等。
这种反应机理常见于卤代烃的取代反应、酯的水解反应等。
亲核取代和亲电取代机理之间存在一定的区别。
首先,在反应物的选择上,亲核取代需要选择具有亲核性的试剂,而亲电取代需要选择具有亲电性的试剂。
其次,在反应过程中,亲核取代是通过亲核试剂攻击原有化合物中的电子实现的,而亲电取代是通过亲电试剂攻击原有化合物中的电子实现的。
此外,在反应速率上,亲电取代的速率通常较快,而亲核取代的速率较慢。
另外,反应的产物也有所不同,亲核取代反应通常会产生亲核试剂中的原子或基团替代原有化合物中的原子或基团,而亲电取代反应通常会产生亲电试剂中的原子或基团替代原有化合物中的原子或基团。
总结起来,亲核取代和亲电取代是有机化学中常见的取代反应机理。
亲核取代通过亲核试剂攻击原有化合物中的电子,亲电取代通过亲电试剂攻击原有化合物中的电子。

亲电取代和亲核取代例子以亲电取代和亲核取代是有机化学中的两个重要概念,它们描述了在化学反应中发生的两种取代反应。
亲电取代是指一个亲电子试图取代一个离子或亲核物质中的一个原子或基团的反应。
亲核取代是指一个亲核试图取代一个分子中的一个原子或基团的反应。
下面将分别列举亲电取代和亲核取代的例子。
亲电取代的例子:1. 酸催化的醇酯化反应:酸催化下,醇和酸发生酯化反应,醇中的亲电子攻击酸中的羰基碳,形成酯。
2. 酮和醛的氧化还原反应:还原剂(如金属氢化物)提供亲电子,被酮或醛中的亲电子接受,形成醇。
3. 烯烃的电子亲加反应:亲电试剂(如卤素)攻击烯烃的π电子,形成加成产物。
4. 亲电芳香取代反应:亲电试剂(如卤素)攻击芳香化合物的芳环,取代芳环上的氢原子。
5. 酰氯酯化反应:酰氯作为亲电试剂,攻击醇中的亲电子,形成酯。
6. 羟基磺酸酯化反应:羟基磺酸作为亲电试剂,攻击醇中的亲电子,形成磺酸酯。
7. 酰基氯醇酯化反应:酰基氯作为亲电试剂,攻击醇中的亲电子,形成酯。
8. 亲电取代的氯化反应:亲电试剂(如氯化氢)攻击有机物中的亲电子,取代有机物中的原子或基团。
9. 亲电取代的溴化反应:亲电试剂(如溴化氢)攻击有机物中的亲电子,取代有机物中的原子或基团。
10. 亲电取代的碘化反应:亲电试剂(如碘化氢)攻击有机物中的亲电子,取代有机物中的原子或基团。
亲核取代的例子:1. 醇的亲核取代反应:亲核试剂(如卤代烃)攻击醇中的醇氧原子,形成醚。
2. 醛和酮的亲核取代反应:亲核试剂(如胺)攻击醛或酮中的羰基碳,形成亲核加合物。
3. 烯烃的亲核加成反应:亲核试剂(如水或醇)攻击烯烃的π电子,形成加成产物。
4. 亲核取代的碱性水解反应:碱催化下,亲核试剂(如水或醇)攻击酯或酰氯中的羰基碳,形成醇或酸。
5. 亲核取代的酸性水解反应:酸催化下,亲核试剂(如水或醇)攻击酯或酰氯中的羰基碳,形成醇或酸。
6. 亲核取代的酸性醇酯化反应:酸催化下,亲核试剂(如醇)攻击酯中的羰基碳,形成醚和酸。
