高二化学镁和铝及其化合物
- 格式:pdf
- 大小:924.43 KB
- 文档页数:8



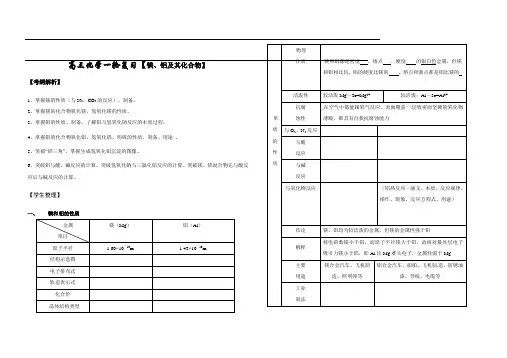
在空气中都能跟氧气反应,表面覆盖一层致密而坚硬的氧化物薄膜,都具有自我抗腐蚀能力铝合金汽车、船舶、飞机制造、防锈油漆、导线、电缆等易错点:(1)常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
(2)铝不但能与酸(H +)反应,还能够与碱溶液反应,表现为特殊性。
2Al +2OH -+2H 2O===2AlO -2+3H 2↑。
其反应机理应为:铝先与强碱溶液中的水反应生成H 2和Al(OH)3,然后Al(OH)3再与NaOH 反应生成H 2O 和NaAlO 2,反应中铝作还原剂,水作氧化剂,NaOH 无电子得失。
(3)铝热反应是在高温干态下进行的置换反应,铝只能与排在金属活动性顺序其后的金属氧化物反应。
铝不能与MgO 反应,铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
(4)Mg 在CO 2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
同时镁与氮气反应生成Mg 3N 2。
二、铝的重要化合物1.氧化铝(1)物理性质 色态: ;硬度: ;熔点: 。
(2)化学性质①属于两性氧化物,写出有关反应的离子方程式:,②电解 化学方程式为 2Al 2O 3(熔融)=====电解4Al +3O 2↑。
(3)用途熔点很高,是一种较好的耐火材料,天然产刚玉的成分是Al 2O 3,还可制作各种宝石。
2.氢氧化铝 (1)物理性质Al(OH)3是一种难溶于水的白色胶状物质,具有较强的吸附能力。
(2)化学性质 ①两性Al(OH)3的电离方程式为Al(OH)3既能溶于强酸又能溶于强碱,且都生成盐和水。
与强酸反应: , 与强碱溶液反应: 。
②不稳定性Al(OH)3受热分解: 。
(3)制备①向铝盐中加入氨水,离子方程式为 。
②NaAlO 2溶液中通入足量CO 2,离子方程式为 。
③NaAlO 2溶液与AlCl 3溶液混合:离子方程式为 。

镁及其化合物1.镁与氮气、氧气、氯气等非金属单质反应 2Mg+O 2点燃2MgO Mg +Cl 2点燃MgCl 2 3Mg+N 2点燃Mg 3N 22.镁与CO 2反应3. Mg 3N 2与水反应 2Mg+CO 2点燃2MgO+C Mg 3N 2+6H 2O=3Mg(OH)2↓+2NH 3↑4.镁与氯化铵反应5.镁的冶炼Mg+2NH 4Cl=MgCl 2 + 2NH 3↑+ H 2↑ MgCl 2(熔融)= Mg+Cl 2↑铝及其化合物1、铝在氧气、氯气中燃烧:4Al +3O 22Al 2O 32Al +3Cl 22AlCl 32、铝与稀硫酸反应:2Al +3H 2SO 4=Al 2(SO 4)3 +3H 2 ↑(2Al +6H +=2Al 3++3H 2 ↑) 3、铝和氢氧化钠溶液反应:2Al +2NaOH +2H 2O =2NaAlO 2+3H 2 ↑ (2Al +2OH -+2H 2O =2AlO 2-+3H 2 ↑) 4、铝和氧化铁高温下反应:2Al +Fe 2O 3=Al 2O 3+2Fe 5、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO 4=Al 2(SO 4)3 +3H 2O (Al 2O 3+6H +=2Al 3++3H 2O ) 6、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH =2NaAlO 2+H 2O (Al 2O 3+2OH -=2AlO 2-+H 2O )8、电解氧化铝的熔融液:2Al 2O 3(熔融)== 4Al +3O 2 ↑ 9、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4=Al 2(SO 4)3 +6H 2O (Al(OH)3 +3H +=Al 3++3H 2O ) 10、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH=NaAlO 2+2H 2O (Al(OH)3 +OH -=AlO 2-+2H 2O )11、加热氢氧化铝:2Al(OH)3 =Al 2O 3+3H 2O 12、向氯化铝溶液中加入氨水:AlCl 3 +3NH 3·H 2O=Al(OH)3 ↓+3NH 4Cl(Al 3++3NH 3·H 2O=Al(OH)3 ↓+3NH 4+)13、氯化铝溶液与氢氧化钠溶液:氢氧化钠不足时:AlCl 3+3NaOH=3NaCl +Al(OH)3 ↓ (Al 3++3OH -=Al(OH)3 ↓)氢氧化钠过量时:AlCl 3 +4NaOH=NaAlO 2+3NaCl +2H 2O (Al 3++4OH -=AlO 2-+2H 2O ) 14、向偏铝酸钠溶液通入二氧化碳气体:CO 2不足时:2NaAlO 2+CO 2+3H 2O =2Al(OH)3 ↓+Na 2CO 3(2AlO 2-+CO 2+3H 2O =2Al(OH)3 ↓+CO 32-)CO 2过量时:NaAlO 2+CO 2+2H 2O =Al(OH)3 +NaHCO 3(AlO 2-+CO 2+2H 2O=Al(OH)3 +HCO 3-)15、偏铝酸钠溶液与盐酸:盐酸不足时:NaAlO 2+HCl +H 2O =Al(OH)3 ↓+NaCl (AlO 2-+H ++H 2O=Al(OH)3 ↓)盐酸过量时:NaAlO 2+4HCl =NaCl +AlCl 3+2H 2O (AlO 2-+4H +=Al 3++2H 2O ) 16、偏铝酸钠溶液与氯化铝溶液:AlCl 3+3NaAlO 2+6H 2O =3NaCl +4Al(OH)3↓(Al 3++3 AlO 2-+6H 2O =4Al(OH)3 ↓)电解电解。

高考化学专项复习——镁、铝及其化合物金属镁的有关化学方程式1、镁在O 2中点燃: 2Mg + O 2== 2MgO2、与N 2反应: 3Mg + N 2== 3Mg 3N 23、与热水反应:Mg +2H 2O=== Mg(OH)2+H 2↑4、镁与酸反应: Mg +2HCl===MgCl 2+H 2↑5、与CO 2反应:2Mg +CO 2 === 2MgO +C6、海水提镁时,沉淀镁 :Mg 2++2OH -=== Mg(OH)2↓7、电解得Mg :MgCl 2(熔融)=== Mg+Cl 2↑8、MgO 与HCl 反应: MgO + 2HCl== MgCl 2 + H 2O9、Mg(OH)2与酸反应:Mg(OH)2 + 2H +==Mg 2++2H 2O金属铝的有关化学方程式Δ 点燃通电 点燃1.Al 与Cl 2反应:2Al+3Cl 2=== 2AlCl 32.Al 与O 2反应:4Al+3O 2=== 2Al 2O 33.铝热反应:2Al+Fe 2O 3===Al 2O 3+2Fe4.Al 与HCl 反应:2Al + 6H + == 2Al 3++ 3H2↑5.Al 与NaOH 反应:2Al+2OH --+2H 2O == 2AlO 2-- +3H 2↑6.Al 2O 3与HCl 反应:Al 2O 3+6H + === 2Al 3+ + 3H 2O7.Al 2O 3与NaOH 反应:Al 2O 3+2OH -===2AlO -2+H 2O8.Al 2O 3熔融电解:2Al 2O 3(熔融)=====通电冰晶石 4Al + 3O 2↑9.Al(OH)3与HCl 反应:Al(OH)3+3H + ===2Al 3+ + 3H 2O10. Al(OH)3与NaOH 反应:Al(OH)3+OH -===AlO -2+2H 2O11.Al(OH)3受热分解:2Al(OH)3===Al 2O 3+ 3H 2O12.Al(OH)3制备方法(1)Al 3+与碱(NH 3·H 2O )反应:Al 3++3NH 3·H 2O===Al(OH)3↓+3NH +4(2)AlO 2—与酸(CO 2+H 2O )反应:(CO 2少量):2NaAlO 2+CO 2+3H 2O ===CO 32- +2Al(OH)3↓(CO 2过量):AlO -2+CO 2+2H 2O===Al(OH)3↓+HCO -3(3)双水解反应(Al 3++AlO 2—):Al 3++ 3AlO -2+6H 2O=== 4Al(OH)3↓13.明矾净水原理:Al 3++ 3H 2O===Al(OH)3↓+3H +Δ高温14.AlCl3与NaOH反应:(1)向AlCl3中加NaOH:Al3++ 3OH-===Al(OH)3↓Al(OH)3+ OH-==AlO-2+2H2O(2)向NaOH中加AlCl3:Al3++4OH-===AlO-2+2H2O15.偏铝酸盐的水解:AlO-2+2H2O===Al(OH)3↓+OH --16.偏铝酸盐与HCl反应:(1)向NaAlO2加HCl:AlO-2+H++2H2O===Al(OH)3↓+H2OAl(OH)3↓+3H+===Al3++3H2O(2)向HCl加NaAlO2:AlO-2+4H+===Al3++2H2O镁、铝及其重要化合物一、镁及其重要化合物的性质及用途1、镁(1)物理性质银白色、有金属光泽、密度、硬度均较小、熔点低、有良好的导电、传热、延展性(2)化学性质①与O 2、Cl 2、N 2等非金属非金属反应与O 2反应: 2Mg + O 2 == 2MgO与Cl 2反应: Mg + Cl 2 == MgCl 2与N 2反应: 3Mg + N 2 == 3Mg 3N 2②与热水反应 Mg +2H 2O===Mg(OH)2+H 2↑③与酸反应:发生置换反应、放出H 2Mg +2HCl===MgCl 2+H 2↑④与CO 2反应2Mg +CO 2 === 2MgO +C(3)用途可用于生产合金、冶金工业上作还原剂和脱氧剂2、海水提镁沉淀Mg 2+ :Mg 2++2OH -=== Mg(OH)2↓制取MgCl 2 : Mg(OH)2 + 2HCl==MgCl 2+2H 2OΔ点燃电解得Mg :MgCl 2(熔融) === Mg+Cl 2↑3、镁的重要化合物(1)MgO :碱性氧化物与H 2O 反应: MgO + H 2O== Mg(OH)2与HCl 反应: MgO + 2HCl== MgCl 2 + H 2O(2)Mg(OH)2 :中强碱、难溶于水Mg(OH)2 + 2H +==Mg 2++2H 2O二、铝及其重要化合物的性质及用途1、铝(1)物理性质银白色固体、硬度较软、有良好的导电、传热性;(2)主要化学性质①与非金属单质反应 与Cl 2反应:2Al+3Cl 2===2AlCl 3 点燃 通电与O 2反应:4Al+3O 2===2Al 2O 3(常温下生成氧化膜)②与酸反应氧化性算:与冷的、浓的浓硫酸、浓硝酸-钝化非氧化性酸:2Al + 6HCl== 2AlCl 3+ 3H2↑2Al + 6H + ==2Al 3++3H2↑③与强碱反应:2Al+2NaOH+2H 2O == 2NaAlO 2+3H 2↑2Al+2OH --+2H 2O == 2AlO 2-- +3H 2↑④铝热反应:2Al+Fe 2O 3==Al 2O 3+2Fe(3)制备2Al 2O 3(熔融)=====通电冰晶石4Al + 3O 2↑镁、铝性质比较:判断正误,正确的划“√”,错误的划“×”(1)铝粉与氧化镁共热可制取金属镁( ×)(2)将镁条点燃后迅速伸入集满CO2的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生(√)(3)MgO的熔点很高,可用于制作耐高温材料(√)(4)铝在自然界中有游离态和化合态两种形式( ×)(5)一定条件下,镁能与一些非金属氧化物反应,铝能与一些金属氧化物反应(√)(6)足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气(×)2.氧化铝和氢氧化的性质(1)氧化铝的性质(2)氢氧化铝的性质Al2O3+2OH-===2AlO-2+H2O2Al2O3(熔融)=====电解4Al+3O2↑氢氧化铝的制备①向铝盐中加入氨水:Al 3++3NH 3·H 2O===Al(OH)3↓+3NH +4(不能用强碱)②NaAlO 2溶液中通入足量CO 2:AlO -2+CO 2+2H 2O===Al(OH)3↓+HCO -3(不能用强酸)③NaAlO 2溶液与AlCl 3溶液混合:Al 3++ 3AlO -2+6H 2O=== 4Al(OH)3↓ 注意1、氧化铝和氢氧化铝是两性化合物,但叙述时应强调是与强酸和强碱。

镁、铝及其重要化合物一、镁及其化合物镁合金强度高,机械性能好,制造汽车,飞机,火箭的重要材料,冶金时,镁常用作还原剂和脱氧剂.常温下氧化生成氧化物保护层,具有抗腐蚀的性质.镁与O2,N2,CO2等气体燃烧.2Mg+O22MgO CO2+2Mg2MgO+C 3Mg+N2Mg3N2镁与SiO2:2Mg+SiO2=2MgO+Si镁与冷水反应很慢,在加热时反应加快.Mg+2H2O=Mg(OH)2+H2↑镁与非氧化性酸.Mg+2HCl=MgCl2+H2↑镁与水解显酸性的盐溶液的反应. Mg+2NH4Cl =MgCl2+2NH3+H2↑镁盐与氨水,产生Mg(OH)2沉淀.Mg(OH)2又能溶解在NH4Cl溶液中.前者由Mg(OH)2的特殊溶解性决定.在常见的难溶性氢氧化物中,Mg(OH)2的溶解度最大.故产生Mg(OH)2的条件:浓的Mg2+ 盐溶液与浓氨水反应.后者是由Mg(OH)2的电离性质和的水解性质决定.通常认为Mg(OH)2完全电离,能溶解在饱和NH4Cl溶液中,MgCl2+2NH3·H2OMgOH2+2NH4Cl海水提镁:㈠海水加碱,得氢氧化镁沉淀,沉淀分离出来再加盐酸,变成氯化镁;后过滤,干燥,电解得镁.Mg2++2OH-==Mg(OH)2↓,Mg(OH)2+2HCl=MgCl2+2H2O,MgCl2Mg+Cl2↑㈡从海水提取出食盐、KCl、Br2以后留下的母液浓缩,得到卤块,主要成分是MgCl2·6H2O,然后脱水, MgCl2·6H2OMgCl2+6H2O,最后电解熔融的氯化镁得到镁.氧化镁(白色粉末,高熔点,碱性氧化物,)与水缓慢作用,与酸反应.MgO+2HCl=MgCl2+H2O MgO+H2OMg(OH)2氢氧化镁(白色粉末,难溶于水)与H+作用,与NH4Cl溶液作用,对热不稳定.Mg(OH)2+2HCl=MgCl2+2H2O Mg(OH)2MgO+H2O↑二、铝及其化合物铝(银白色金属,导电性仅次于银、铜和金。


课时11 镁、铝及其重要化合物知识点一 镁、铝的性质及应用【考必备·清单】 1.镁、铝的结构和存在名称 镁 铝 周期表中位置 第三周期ⅡA 族第三周期ⅡA 族原子结构示意图自然界存在形态 化合态化合态2.镁、铝的物理性质都是银白色、有金属光泽的固体,密度较小,硬度较低,均具有良好的延展性、导电性和导热性等。
3.铝的化学性质写出图中有关反应的化学方程式:②2Al +3Cl 2=====点燃2AlCl 3④2Al +2NaOH +2H 2O===2NaAlO 2+3H 2↑ ⑤2Al +Fe 2O 3=====高温Al 2O 3+2Fe(铝热反应)[名师点拨]①常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
②能与铝反应产生氢气的溶液可能呈强酸性也可能呈强碱性。
4.铝的用途纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。
5.与铝对比记忆镁的化学性质铝镁与非金属反应能被Cl2、O2、N2氧化2Mg+O2=====点燃2MgO(与O2反应)3Mg+N2=====点燃Mg3N2(与N2反应)与水反应反应很困难能与沸水反应:Mg+2H2O=====△Mg(OH)2+H2↑与碱反应能溶于强碱溶液不反应与某些氧化物反应能与Fe2O3、MnO2、Cr2O3等金属氧化物发生铝热反应能在CO2中燃烧:2Mg+CO2=====点燃2MgO+C[名师点拨]①Mg在CO2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
②镁也可在氮气中燃烧,生成氮化镁(Mg3N2),氮化镁能与水剧烈反应生成Mg(OH)2沉淀并放出氨气。
6.从海水中提取镁(1)工艺流程(2)基本步骤及主要反应[名师点拨]①由MgCl2·6H2O到无水MgCl2,必须在HCl气流中加热,以防MgCl2水解。
②因镁在高温下能与O2、N2、CO2等气体发生反应,故工业电解MgCl2得到的镁,应在H2氛围中冷却。

2023年高二化学教案镁、铝及其化合物(精选3篇)教案一:镁的性质及其化合物教学目标:1. 了解镁的性质和应用。
2. 掌握镁与氧、硫和氯的反应。
3. 熟悉镁的几种常见化合物的命名和性质。
教学过程:1. 引入:通过实验演示和图片展示介绍镁的性质和应用,如镁的轻便性、燃烧性、导电性和腐蚀性等。
2. 镁与氧的反应:- 展示镁与氧反应的实验现象,并解释反应过程。
- 写出反应方程式:2Mg + O2 → 2MgO。
- 引导学生分析反应类型、反应物和生成物。
3. 镁与硫的反应:- 展示镁与硫反应的实验现象,并解释反应过程。
- 写出反应方程式:Mg + S → MgS。
- 引导学生分析反应类型、反应物和生成物。
4. 镁与氯的反应:- 展示镁与氯反应的实验现象,并解释反应过程。
- 写出反应方程式:Mg + Cl2 → MgCl2。
- 引导学生分析反应类型、反应物和生成物。
5. 镁的常见化合物:- 介绍镁的几种常见化合物,如氯化镁、硫酸镁和碳酸镁等。
- 分析这些化合物的性质和应用。
- 让学生完成相关的实验操作或观察,加深对这些化合物的理解。
6. 总结:总结镁的性质和与氧、硫、氯反应的特点,以及常见化合物的命名和性质。
教案二:铝的性质及其化合物教学目标:1. 了解铝的性质和应用。
2. 掌握铝与氧、硫和氯的反应。
3. 熟悉铝的几种常见化合物的命名和性质。
教学过程:1. 引入:通过实验演示和图片展示介绍铝的性质和应用,如铝的轻便性、导电性和耐腐蚀性等。
2. 铝与氧的反应:- 展示铝与氧反应的实验现象,并解释反应过程。
- 写出反应方程式:4Al + 3O2 → 2Al2O3。
- 引导学生分析反应类型、反应物和生成物。
3. 铝与硫的反应:- 展示铝与硫反应的实验现象,并解释反应过程。
- 写出反应方程式:2Al + 3S → Al2S3。
- 引导学生分析反应类型、反应物和生成物。
4. 铝与氯的反应:- 展示铝与氯反应的实验现象,并解释反应过程。

高中化学-高二镁、铝及其化合物教案【课时要求】本课为化学高二必修三的第一课,建议学生预习前已学习完基础化学知识。
【教学目标】1.了解镁、铝的常见物理化学性质和制备方法;2.掌握镁和铝与非金属元素的反应特点;3.熟悉镁、铝及其化合物的性质、用途、反应和应用;4.培养学生的实验操作能力、观察能力和分析问题的能力。
【教学重点】1.镁和铝与非金属元素的反应特点;2.镁、铝及其化合物的性质和应用。
【教学难点】镁和铝的制备方法,以及镁铝合金在工业上的应用。
【教学方法】1.讲授-板书:通过讲授、板书及思维导图的形式传递知识,提高学生的理解能力。
2.实验演示:通过实验演示来引导学生理解理论,激发学生的学习兴趣和思考能力。
3.互动讲述:通过课堂展示和交流的形式,提高学生主动参与的积极性,增强学生的学习效果。
【教学内容】一、镁、铝的常见物理化学性质及制备(一)镁的物理化学性质和制备方法1.物理性质(1)颜色:银白色;(2)密度:1.74g/cm3;(3)熔点:651℃;(4)沸点:1090℃;(5)硬度:摩氏硬度为2.5。
2.制备方法(1)电解法制镁:镁是一种具有较强亲电性的金属,在水中不溶解,但在溶有Cl^-离子的水中具有显著的溶解度。
因此,可以采用电解的方法制备镁。
具体操作方法是,将适量的MgCl2用水溶解,然后电解2小时,电解液温度保持在650℃左右。
电解时,阳极反应为:2Cl-(溶解在熔融镁中)-2e^-→Cl2↑;阴极反应为:Mg2+(溶解在熔融镁中)+2e^-→Mg。
总反应式为:MgCl2→Cl2↑+Mg。
(图1. 电解法制镁实验操作流程图)(2)金属物理还原法制镁:在高温下,利用金属的物理还原性制备镁。
用Na、K等有亲氧性的金属还原MgO制得的镁比较纯。
在制备中一定要避免氧气的干扰,因为氧气会把MgO 转化为Mg2SiO4和Mg2Al4Si5O18等韧性物质,会影响金属还原制备镁的过程,从而增加生产成本。
金属及其化合物 镁、铝及其化合物(含答案)课标要求 核心考点五年考情核心素养对接1.结合真实情境中的应用实例或通过实验探究,了解镁、铝及其化合物的主要性质。
2.了解镁、铝及其化合物在生产、生活中的应用。
3.结合实例认识镁、铝及其化合物的多样性。
4.认识镁、铝及其化合物的转化在促进社会文明进步、自然资源综合利用和环境保护中的重要价值镁及其 化合物 2022广东,T12;2021年6月浙江,T15;2021重庆,T6;2021湖南,T6;2020山东,T9;2019全国Ⅰ,T26;2019天津,T2;2019年4月浙江,T31 1.宏观辨识与微观探析:能运用化学方程式、离子方程式描述镁、铝及其化合物的变化;能联系镁、铝的组成和结构解释宏观现象;能根据典型实验现象说明镁、铝及其化合物可能具有的性质,评估所作说明或预测的合理性。
2.证据推理与模型认知:能从镁、铝的提纯工艺流程中提取镁、铝及其化合物的性质,了解镁、铝的用途,建立物质性质与用途之间的联系。
3.科学态度与社会责任:主动关心与镁、铝制备有关的环境保护、资源开发等社会热点问题,形成与社会和谐共处、合理利用资源的观念铝及其 化合物 2023重庆,T2;2023年6月浙江,T4、T20;2023湖南,T7;2023年1月浙江,T7;2022全国甲,T9;2022湖南,T7;2022广东,T6;2022年6月浙江,T8;2021全国乙,T26;2021北京,T7;2021山东,T17;2021广东,T18;2020 北京,T6;2019江苏,T3命题分析预测高考常以选择题的形式考查镁、铝及其化合物的性质、应用、化学方程式的正误判断等;以工艺流程题的形式考查铝的化合物的制备等。
预计2025年高考仍会延续这种考查形式1.镁元素的价类二维图及转化关系2.铝元素的价类二维图及转化关系考点1镁及其化合物1.镁及其重要化合物的物理性质Mg:银白色固体,密度较小、质软、有延展性,是电和热的良导体。
第二讲 铝、镁及其重要化合物[2020备考·最新考纲]1.掌握铝的主要性质及其应用。
2.掌握铝的重要化合物的主要性质及其应用。
镁的性质Mg 是较活泼的金属,常温下能被空气中的O 2氧化,表面生成一层致密的氧化膜。
镁在纯氧中剧烈燃烧,发出耀眼的白光。
镁不易和冷水反应,但能与沸水迅速反应。
铝的物理性质注意:铝是地壳中元素含量最高的金属元素。
掌握铝的化学性质与用途(1)铝的化学性质图中标号反应的化学方程式或离子方程式:②2Al +3Cl 2=====△2AlCl 3④2Al +2OH -+2H 2O===2AlO -2+3H 2↑⑤2Al +Fe 2O 3=====高温2Fe +Al 2O 3(铝热反应)(2)铝的制备及用途氧化铝氢氧化铝(1)物理性质白色胶状固体,不溶于水,有较强的吸附性。
(2)化学性质①Al(OH)3的电离②两性氢氧化物注意:Al(OH)3不溶于弱酸(如H 2CO 3),也不溶于弱碱(如氨水)。
③受热分解:2Al(OH)3=====△Al 2O 3+3H 2O 。
(3)制备Al(OH)3的三种方法方法一:可溶性铝盐溶液与过量氨水反应离子方程式:Al 3++3NH 3·H 2O===Al(OH)3↓+3NH +4。
方法二:向可溶性偏铝酸盐溶液中通入过量CO 2离子方程式:AlO -2+2H 2O +CO 2===Al(OH)3↓+HCO -3。
方法三:相互促进水解法常见的铝盐(1)硫酸铝钾是由两种不同的金属离子和一种酸根离子组成的复盐。
(2)明矾的化学式为KAl(SO 4)2·12H 2O ,它是无色晶体,可溶于水,水溶液pH <7(填“<”“>”或“=”)。
明矾可以净水,其净水的原理是:Al 3++3H 2OAl(OH)3(胶体)+3H +,Al(OH)3胶体吸附水中杂质形成沉淀而净水。
(3)明矾溶液与Ba(OH)2溶液反应的离子方程式①Al3+恰好完全沉淀:2Al3++3SO2-4+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓。
系列二 主族金属专题8 镁铝及其化合物一、镁单质(1)镁在自然界没有单质存在,存在于各类硅酸盐和碳酸盐矿物里,如菱镁矿(MgCO 3)、白云石(CaCO 3·MgCO 3)、光卤石(KCl·MgCl 2·6H 2O)等。
海水中的镁是提取镁的主要来源,海水中的镁即使提取100万年也不会减少0.01%。
镁也是叶绿素的主要成分,在人体内镁以磷酸盐、碳酸盐的形式分布于骨头和肌肉中,缺乏会引起肌肉的颤动、脉象的混乱。
(2)强还原性:不论在固态或水溶液中都表现出强还原性,常用作还原剂。
高温下,镁夺取氧的能力特别强,甚至能在二氧化碳里燃烧,如2Mg+CO 2=====点燃2MgO+C ;也能够还原二氧化硅,2Mg+SiO 2=====点燃2MgO+Si ;常温下,由于镁表面的氧化膜导致镁不与水反应,但是加热下可以反应,Mg+2H 2O ====△Mg(OH)2+H 2↑。
(3)镁可以与大多数非金属和几乎所有的酸反应。
如2Mg+O 2=====点燃2MgO ,Mg+Cl 2=====点燃MgCl 2,Mg+S =====点燃MgS ,3Mg+N 2=====点燃Mg 3N 2(Mg 3N 2的特殊性质:Mg 3N 2+6H 2O =====3Mg (OH )2↓+2NH 3↑,导致其只能干态制取)。
镁不能和氢氟酸反应,因为MgF 2难溶会阻碍继续反应。
(4)格氏试剂:在醚的溶液中,镁能与卤代烃作用生成在有机化学中应用广泛的格氏试剂:Mg + RX =====醚RMgX(5)制取单质镁:一般是先从海水中得到氯化镁,然后电解熔融的氯化镁,MgCl 2(熔融) =====电解Mg+Cl 2↑。
二、镁的化合物(1)MgO 俗称菱苦土,是一种白色粉末。
MgO 对水呈一定惰性,特别是高温火烧后的MgO 难溶于水。
煆烧温度在923K 左右制成轻质MgO ,煆烧温度在1923K 以上制成重质MgO 。
“镁、铝及其化合物”知识点总结一、Mg、Al的化学性质(一)与非金属反应1.与O2反应。
常温下与空气中的O2反应生成一层致密的氧化物薄膜,所以镁、铝都有抗腐蚀的性能。
镁、铝都能在空气中燃烧:2.与卤素单质、硫等反应。
【特别提醒】(1)镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。
镁在空气中燃烧时有三个反应发生:(2)燃烧时都放出大量的热,发出耀眼的白光。
利用镁的这种性质来制造照明弹。
(3)集气瓶底部都要放一些细纱,以防集气瓶炸裂。
(二)与H2O反应Mg、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气(三)与酸反应置换出H2Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H2,其中铝在冷浓 H2SO4,冷浓硝酸中发生钝化现象。
所以可用铝制容器贮存冷的浓硫酸或浓硝酸。
(四)与某些氧化物反应1.镁与二氧化碳反应:[特别提醒]:“CO2不能助燃”的说法是不全面的,CO2对绝大多数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。
(2)铝热反应:2Al+ Fe2O32Fe+ Al2O3铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。
[特别提醒]:(1)铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe2O3、FeO、Fe3O4、Cr2O3、V2O5、Mn O2等。
(2)铝热反应的特点是反应放出大量的热,使生成的金属呈液态。
(3)要使用没有氧化的铝粉,氧化铁粉末要烘干。
(4)KClO3作为引燃剂,也可以用Na2O2代替。
实验时可以不用镁条点燃,而用在氯酸钾和白糖的混合物上滴加浓硫酸的方法来点燃。
(五)与碱反应镁不与碱反应,铝与碱液反应:二、氢氧化铝(一)物理性质:A l(O H)3是几乎不溶于水的白色胶状固体,具有吸附性。
(二)化学性质1.与酸反应:Al(OH)3 +3HCl=AlCl3+3H2O离子反应方程式:Al(OH)3+3H+=Al3++3H2O2.与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O离子反应方程式:Al(OH)3+OH =NaAlO2+2H2O3.Al(OH)3的制取(1)铝盐与碱反应:实验室制取氢氧化铝时采用过量的氨水,而不用强碱与可溶性铝盐溶液反应是因为氢氧化铝是两性氢氧化物,能溶于强碱溶液,不溶于弱碱溶液。