苯的分子轨道实验研究
- 格式:pptx
- 大小:1006.33 KB
- 文档页数:22

苯环的键能苯环是由六个碳原子组成的环状分子,在化学中非常常见。
苯环的化学性质与其分子结构密切相关,该分子中的键能是其碳-碳键及碳-氢键的总和。
下面将从不同角度探讨苯环化学中的键能问题。
首先,从分子轨道理论的角度,苯环6个碳原子上的电子可以形成三条π键和三条σ键,π键由三组平面的p轨道相互叠加形成,而σ键则由两个碳原子上的s轨道叠加形成。
在苯环中,π键的形成导致了电子密度不均匀的现象,即苯环中的每个碳原子上的π电子密度并不相等。
其中,π键面内侧的原子上的π电子密度最高,而π键面外侧的原子则电子密度较低。
这种电子密度不同带来的结果是苯环中某些地方的化学反应比其他地方更容易发生,这就解释了为什么苯环上存在独特的化学性质。
接下来,从电化学角度来看苯环的键能问题。
苯环具有良好的电化学性质,主要原因是苯环能够释放和接收电子,这种电子的迁移过程涉及到苯环中碳原子和氢原子上的键能。
苯环中碳原子之间的π键能是苯环分子分子中最强的键,其键能约为170 kcal/mol。
这种强的π键能使苯环分子比较稳定,难以发生化学反应。
但是,当苯环分子受到外界电磁场的影响时,就可能导致苯环分子上电子的迁移和加成反应。
这种现象在化学分析和电子传递领域有着广泛的应用。
最后,从化学反应角度来探讨苯环的键能问题。
苯环中的化学反应受到苯环的共振效应影响,所以苯环上发生化学反应时,往往涉及到苯环中的π键的断裂和形成。
例如,当苯环中的共轭双键被氢气加氢时,首先需要断裂双键,形成一个间隔较远的π电子贡献较弱的碳-碳单键,然后逐渐形成苯环上3个平面内部的π键。
这个过程需要克服苯环极强的π键能,在反应过程中产生大量的热能,并可能涉及到产生高能中间体。
因此,苯环化学反应的本质就是击穿强大的π键能,并利用中间体等化学方法完成目的。
综上所述,苯环化学中的键能问题对我们深入理解苯环分子的化学性质以及其化学反应规律至关重要。
虽然苯环上的化学反应需要克服苯环中巨大的π键能,但是利用苯环特殊的共振效应使得其在化学反应中具有非常广泛的应用前景,有助于我们在化学研究领域中更好地探索新的化学物质和反应过程。

西南大学化学化工学院物理化学实验报告实验名称苯分子轨道和电子结构级班姓名学号同组人指导老师实验日期年月日实验环境室温20 ℃大气压76 mmHg 仪器型号一体机实验目的( 1)掌握休克尔分子轨道法的基本内容( 2)学会用休克尔分子轨道法分析和计算苯分子Π轨道分布( 3)学会用计算的化学方法研究简单分子的电子结构实验原理基本理论离域Π键:形成Π键的电子不局限于两个原子的区域,而是在参加成键的多个原子形成的分子骨架中运动,这种由多个原子形成的Π型化学键称为离域Π键共轭效应:形成离域Π键,增加了Π电子的活动范围,使分子具有特殊的物理化学性质,这种效应称为共轭效应分子轨道法:原子组合成分子时,原来专属于某一原子的电子将在整个分子范围内运动,其轨道也不再是原来的原子轨道,而成为整个分子所共有的分子轨道休克尔分子轨道法:为了讨论共轭体系的分子轨道,1 931年休克尔应用LCAO-MO(分子轨道的原子线性组合)法,采用简化处理,解释了大量有机共轭分子性质,该方法称为休克尔分子轨道法,简称HMO法。
该方法针对平面共轭体系的主要特点,能给出离域Π键体系的基本性质休克尔分子轨道法主要运用了下列基本假设 :σ-Π分离体系:对于共轭分子,构成分子骨架的σ电子与构成共轭体系的π电子由于对称性不同,在讨论共轭分子的结构时,可以近似的看成互相独立的,把σ电子和π电子分开处理.独立π电子近似:分子中的电子由于存在相互作用,运动不是独立的,但若将其它电子对某电子的作用加以平均,近似地看成是在核和其它电子形成的固定力场上运动,则该电子的运动就与其它电子的位置无关,是独立的.LCAO-MO近似:对于π体系,可将每个π分子轨道看成是由各个碳原子提供的对称性匹配的p轨道φi 进行线性组合得的.ψ=C1φ1+ C2φ2 + …+ C NφNhuckel近似:认为每个电子在每个原子核附近运动时的能量相同休克尔分子轨道法基本内容在分子中把原子核、内层电子、非键电子连同σ电子一起冻结为“分子实”,构成了由σ键相连的分子骨架,π电子在分子骨架的势场中运动。

苯的离域大派键-概述说明以及解释1.引言概述离域大派键是有机化学中一个重要的概念,指的是分子中某些原子或基团之间的键对电子云不再局限于两个原子之间的共价键中,而是扩展到整个分子中的多个原子上。
苯的离域大派键是指苯分子中π电子云的形成机制,其具有特殊的稳定性和反应特性。
本篇文章将从离域大派键的概念、形成机制、化学反应中的应用以及未来研究方向等方面进行探讨,旨在深入了解和探索离域大派键在有机化学领域中的重要意义和应用价值。
写文章1.1 概述部分的内容1.2 文章结构文章结构本文共分为引言、正文和结论三个部分。
引言部分将介绍离域大派键的概念和重要性,并说明本文的目的和意义。
正文部分将分为三个小节,分别讨论离域大派键的概念、苯的离域大派键形成机制以及苯的离域大派键在化学反应中的应用。
结论部分将总结离域大派键的重要性,并探讨离域大派键研究的启示和未来发展方向,最后进行总结并提出展望。
通过这样的结构安排,读者能够清晰地了解本文的内容脉络,并对离域大派键有一个系统全面的认识。
文章的目的是探讨苯的离域大派键在有机化学中的重要性和应用价值,深入分析离域大派键形成的机制和特点,以及其在化学反应中的作用和影响。
通过对离域大派键的研究和探索,可以为有机化学领域的进展和发展提供新的思路和理论基础,同时也为未来离域大派键的应用和发展方向提供启示。
通过深入的分析和讨论,本文旨在全面了解离域大派键的性质和特点,为其在化学领域中的应用和发展做出贡献。
": {}}}}请编写文章1.3 目的部分的内容1.4 总结总结部分:通过本文的阐述,我们了解到离域大派键在有机化学中的重要性及其形成机制。
离域大派键不仅能够提供分子结构的稳定性,还可以广泛应用于有机合成反应中,为研究和实践提供了丰富的可能性。
同时,我们还展望了离域大派键研究在未来的发展方向,希望通过更深入的探索和实验,可以为离域大派键的应用和发展带来新的突破。
在未来的研究中,我们也将加强对离域大派键的理论和实验研究,以期能够更好地发挥其在有机化学领域的重要作用。

实验名称:分子轨道理论在有机化合物性质预测中的应用实验日期:2023年4月10日实验地点:化学实验室实验目的:1. 理解分子轨道理论的基本概念。
2. 学习如何使用计算化学软件进行分子轨道计算。
3. 应用分子轨道理论预测有机化合物的性质。
实验原理:分子轨道理论(Molecular Orbital Theory,MOT)是现代量子化学中的一个重要理论,它描述了分子中电子的运动状态。
通过分子轨道理论,可以计算分子的能量、键长、键角等性质,并预测分子的稳定性。
实验仪器与试剂:1. 仪器:计算机、计算化学软件(如 Gaussian、MOPAC等)、分子结构编辑软件(如 ChemDraw等)。
2. 试剂:无特殊试剂。
实验步骤:1. 分子结构构建:使用ChemDraw软件构建目标有机化合物的分子结构。
2. 分子轨道计算:- 打开计算化学软件,输入分子结构。
- 设置计算参数,包括基组、密度矩阵等。
- 运行计算,获取分子轨道能量、键长、键角等数据。
3. 结果分析:- 分析分子轨道能量,确定分子中电子的排布。
- 计算键长、键角,与实验值进行比较。
- 分析分子的稳定性,预测分子的反应活性。
实验结果:以甲烷(CH4)为例,进行分子轨道计算。
1. 分子结构构建:使用ChemDraw软件构建甲烷分子结构。
2. 分子轨道计算:- 使用 Gaussian 软件进行计算,选择 STO-3G 基组。
- 计算结果如下:- 最小能量轨道:σ1s(-4.598 eV)- 第二能量轨道:σ2s(-0.805 eV)- 第三能量轨道:σ2p(-0.073 eV)- 键长:C-H 键长为 1.09 Å。
- 键角:H-C-H 键角为109.5°。
3. 结果分析:- 甲烷分子中,电子主要填充在σ1s、σ2s 和σ2p 轨道中。
- C-H 键长与实验值基本吻合,说明计算结果可靠。
- H-C-H 键角与实验值相符,进一步验证了计算结果的准确性。


基于科学探究体验的“苯的发现与研究”的教学反思教学理念化学新课程标准明确指出化学课程的基本理念要“结合人类探索物质及其变化的历史与化学科学发展的趋势,引导学生进一步学习化学的基本原理和基本方法,形成科学的世界观”。
化学课堂教学中如何将化学知识的习得与科学研究的体验紧密结合,让学生感受化学的发展和了解化学家的工作,挖掘化学教学的人文内涵,启迪学生的科学精神与创造意识,借助化学史话不仅激起学生学习兴趣,更可以了解科学发展过程和科学探究的方法。
第一部分——教学设计思路反思一、教材分析1、教材的地位与作用本节选自人教版普通高中课程实验教科书化学必修2第三章第二节。
必修模块的有机化学内容,是以典型的有机物的学习为切入点,让学生在初中有机物常识的基础上,进一步从结构的角度,加深对有机物和有机化学的整体认识。
甲烷、乙烯、苯作为烃类有机化合物学习中的代表,这些物质都与生活密切相关,使学生感到熟悉、亲切,可以增加学习兴趣。
对于有机物苯的学习充分体现必修模块中有机化学的双重功能,一方面满足基本科学常识,提供有机化学最基本的核心知识,体会科学探究的基本方法;另一方面为进一步学习有机化学的学生,打好最基本的知识基础,激发他们深入学习的欲望。
2 、教材的内容选择与呈现根据课程标准和学时要求,本章化学知识的逻辑性和系统性有所弱化,联系社会的知识和知识的应用相对较强。
而为了提高学生的科学探究能力,对培养学生科学方法的要求则没有放松,为此“知识弱化了,怎样培养能力和方法”的问题摆在了我们面前。
在“苯”的教学中,以科学史料为依托,充分挖掘科学方法教育的因素,促进学生在运用科学方法探究苯的知识的过程中,进一步加深对有关科学方法的认识,提高科学探究的能力。
本节知道苯的主要物理性质,理解苯的结构,掌握苯的重要化学性质。
二、学情分析1、学生已有知识与起点能力分析已经学习了简单有机化合物甲烷和乙烯的性质,中的烃类有机化合物中碳、氢原子的成键特点,具备了进一步学习有机化合物的基础和素养。



一、实验目的1. 学习苯的制备方法及原理。
2. 掌握苯的性质,如溶解性、密度、沸点等。
3. 了解苯的物理、化学性质及其应用。
二、实验原理苯(C6H6)是一种无色、具有特殊芳香气味的液体,是重要的有机溶剂和化工原料。
苯的制备方法有多种,其中最常用的是甲苯催化氧化法。
本实验采用苯的蒸馏法制备,利用苯的沸点低于其他杂质的特性,通过蒸馏分离得到较纯的苯。
三、实验仪器与试剂1. 仪器:蒸馏装置(包括蒸馏烧瓶、冷凝管、接收瓶、温度计等)、酒精灯、铁架台、烧杯、玻璃棒等。
2. 试剂:苯、无水硫酸钠、氯化钠、活性炭、浓硫酸、氢氧化钠、蒸馏水等。
四、实验步骤1. 准备蒸馏装置,将蒸馏烧瓶放入铁架台上,连接冷凝管、接收瓶、温度计等。
2. 在蒸馏烧瓶中加入一定量的苯,加入适量的活性炭作为催化剂。
3. 加热蒸馏烧瓶,控制温度在70℃左右,使苯逐渐蒸发。
4. 观察冷凝管,当冷凝管中有液体滴下时,收集蒸馏液。
5. 将收集到的蒸馏液倒入烧杯中,加入适量的无水硫酸钠,充分振荡,使苯与水分离。
6. 用玻璃棒引流,将苯倒入接收瓶中,苯的密度小于水,苯将浮在水面上。
7. 将接收瓶中的苯倒入烧杯中,加入适量的氯化钠,充分振荡,使苯与水分离。
8. 再次用玻璃棒引流,将苯倒入接收瓶中,苯将浮在水面上。
9. 将接收瓶中的苯倒入烧杯中,加入适量的氢氧化钠,充分振荡,使苯与水分离。
10. 再次用玻璃棒引流,将苯倒入接收瓶中,苯将浮在水面上。
11. 将接收瓶中的苯倒入烧杯中,加入适量的蒸馏水,充分振荡,使苯与水分离。
12. 再次用玻璃棒引流,将苯倒入接收瓶中,苯将浮在水面上。
13. 将接收瓶中的苯倒入烧杯中,加入适量的无水硫酸钠,充分振荡,使苯与水分离。
14. 再次用玻璃棒引流,将苯倒入接收瓶中,苯将浮在水面上。
15. 将接收瓶中的苯倒入烧杯中,加入适量的氯化钠,充分振荡,使苯与水分离。
16. 再次用玻璃棒引流,将苯倒入接收瓶中,苯将浮在水面上。
实验五气相色谱-质谱(GC-MS)分离分析苯系物093858 张亚辉一、实验目的(1)了解气相色谱-质谱联用仪的基本构造,熟悉工作站软件的使用;(2)了解运用GC-MS仪分析简单样品的基本过程。
二、实验原理气相色谱法是利用不同物质在固定相和流动相中的分配系数不同,使不同化合物从色谱柱流出的时间不同,达到分离化合物的目的。
质谱法是利用带电粒子在磁场或电场中的运动规律,按其质荷比(m/z)实现分离分析,测定离子质量及强度分布。
它可以给出化合物的分子量、元素组成、分子式和分子结构信息,具有定性专属性、灵敏度高、检测快速等特点。
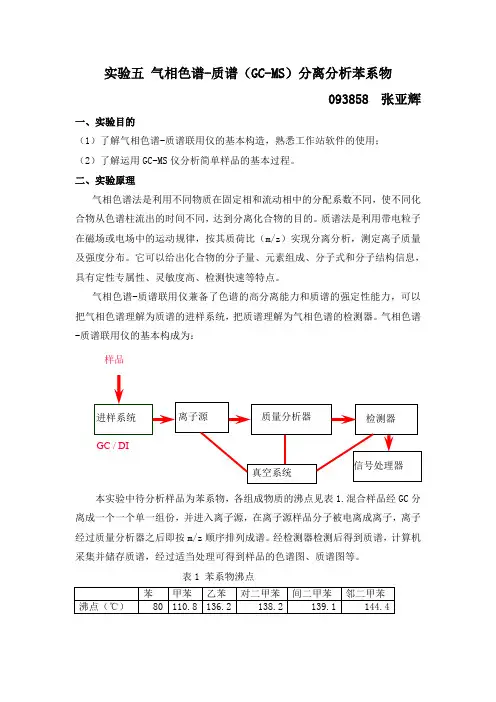
气相色谱-质谱联用仪兼备了色谱的高分离能力和质谱的强定性能力,可以把气相色谱理解为质谱的进样系统,把质谱理解为气相色谱的检测器。
气相色谱-质谱联用仪的基本构成为:样品本实验中待分析样品为苯系物,各组成物质的沸点见表1.混合样品经GC分离成一个一个单一组份,并进入离子源,在离子源样品分子被电离成离子,离子经过质量分析器之后即按m/z顺序排列成谱。
经检测器检测后得到质谱,计算机采集并储存质谱,经过适当处理可得到样品的色谱图、质谱图等。
表1 苯系物沸点三、仪器和试剂:(1)Agilent 6890-5973N GC-MS仪(安捷伦科技有限公司);(2)HP-5 MS 色谱柱;(3)0-5mL移液器 (Transferpette, 德国BRAND 公司);(4)0.45μm的有机相微孔膜过滤器;(5)苯、甲苯、二甲苯(分析纯),甲醇(色谱纯);(6)容量瓶四、实验内容与步骤:1)分别用移液器取1ml苯、甲苯、二甲苯混合后,用甲醇稀释1000倍后待用;2)用移液器取2ml稀释液,使用0.45μm的有机相微孔膜过滤器后,转移至标准样品瓶中待测;3)设定好GC-MS操作参数后,可进样分析:4)设置样品信息及数据文件保存路径后,按下“Start run”键,待“Pre-run”结束,系统提示可以进样时,使用10μl进样针准确吸取1μl样品溶液(不能有气泡)。
气相色谱-质谱(GC-MS )分离分析苯系物一、实验目的(1)了解气相色谱-质谱联用仪的基本构造,熟悉工作站软件的使用;(2)了解运用GC-MS 仪分析简单样品的基本过程。
二、实验原理气相色谱法是利用不同物质在固定相和流动相中的分配系数不同,使不同化合物从色谱柱流出的时间不同,达到分离化合物的目的。
质谱法是利用带电粒子在磁场或电场中的运动规律,按其质荷比(m/z )实现分离分析,测定离子质量及强度分布。
它可以给出化合物的分子量、元素组成、分子式和分子结构信息,具有定性专属性、灵敏度高、检测快速等特点。
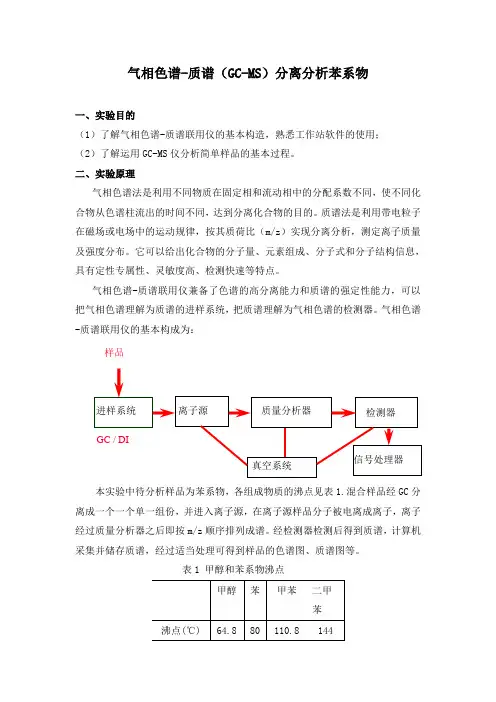
气相色谱-质谱联用仪兼备了色谱的高分离能力和质谱的强定性能力,可以把气相色谱理解为质谱的进样系统,把质谱理解为气相色谱的检测器。
气相色谱-质谱联用仪的基本构成为:本实验中待分析样品为苯系物,各组成物质的沸点见表1.混合样品经GC 分离成一个一个单一组份,并进入离子源,在离子源样品分子被电离成离子,离子经过质量分析器之后即按m/z 顺序排列成谱。
经检测器检测后得到质谱,计算机采集并储存质谱,经过适当处理可得到样品的色谱图、质谱图等。
表1 甲醇和苯系物沸点 甲醇 苯 甲苯 二甲苯沸点(℃) 64.8 80 110.8 144信号处理器进样系统离子源 真空系统 质量分析器 检测器GC / DI 样品三、仪器和试剂:(1)Agilent 6890-5973N GC-MS 仪(安捷伦科技有限公司);(2)HP-5 MS 色谱柱;(3)0-5mL 移液器 (Transferpette, 德国BRAND 公司);(4)0.45μm 的有机相微孔膜过滤器;(5)苯、甲苯、二甲苯(分析纯),甲醇(色谱纯);(6)容量瓶四、实验内容与步骤:1)分别用移液器取1ml 苯、甲苯、二甲苯混合后,用甲醇稀释1000倍后待用;2)用移液器取2ml 稀释液,使用0.45μm 的有机相微孔膜过滤器后,转移至标准样品瓶中待测;3)设定好GC-MS 操作参数后,可进样分析:4)设置样品信息及数据文件保存路径后,按下“Start run ”键,待“Pre-run ”结束,系统提示可以进样时,使用10μl 进样针准确吸取1μl 样品溶液(不能有气泡)。
苯的分子轨道苯是一种常见的有机化合物,化学式为C6H6。
它由六个碳原子和六个氢原子组成。
苯的分子轨道是苯分子中电子的可能运动轨迹。
苯分子轨道的研究对于理解苯分子的性质和反应机理具有重要意义。
苯分子的分子轨道可以分为σ轨道和π轨道。
σ轨道是通过原子间的头向叠加形成的,是较强的化学键;π轨道是通过原子间的侧向叠加形成的,是较弱的化学键。
苯分子中有三个σ轨道和三个π轨道。
这些分子轨道是通过分子对称性和量子力学计算得出的。
苯分子的σ轨道主要参与碳原子之间的共价键形成。
每个碳原子都有一个sp2杂化轨道和一个未杂化的p轨道参与形成σ轨道。
sp2杂化轨道和p轨道的叠加形成了σ轨道,其中sp2轨道与相邻碳原子的sp2轨道重叠,而p轨道与相邻碳原子的p轨道重叠。
这种头向叠加形成的σ轨道使得苯分子具有稳定的芳香性质。
苯分子的π轨道主要参与芳香性和反应机理。
苯分子中的π电子主要分布在苯环的平面上,形成了一个π电子云。
苯分子中的π轨道可以分为两种类型:分子轨道和反键轨道。
分子轨道是通过相邻碳原子的p轨道重叠形成的,而反键轨道是通过相邻碳原子的sp2轨道与未杂化的p轨道重叠形成的。
这些π轨道形成了一个共轭体系,使得苯分子具有很高的稳定性和芳香性。
苯分子的π电子云对于苯分子的性质和反应机理具有重要影响。
由于π电子云的存在,苯分子具有很高的稳定性和芳香性。
它可以与其他化合物进行共轭反应,参与电子的亲电和亲核反应。
苯分子的π电子云还可以与外界的电场相互作用,影响苯分子的电子结构和性质。
总结起来,苯分子的分子轨道是苯分子中电子的可能运动轨迹。
苯分子的分子轨道包括σ轨道和π轨道,它们分别参与碳原子之间的共价键形成和芳香性质。
苯分子的分子轨道对于理解苯分子的性质和反应机理具有重要意义。
通过研究苯分子的分子轨道,可以深入理解苯分子的结构和性质,为有机化学领域的研究和应用提供理论基础。
苯环的分子轨道苯环是有六个碳原子构成的环状分子结构,具有特殊的分子轨道。
本文将从分子轨道的角度来探讨苯环的性质和特点。
苯环的分子轨道可以分为两种类型:σ轨道和π轨道。
σ轨道是沿着分子轴向排列的成键电子轨道,而π轨道则是垂直于分子轴向的非成键电子轨道。
我们来探讨苯环的σ轨道。
苯环中的σ轨道包括6个碳原子的1s 轨道、2s轨道和2p轨道。
其中,1s轨道形成了6个碳原子之间的σ键,2s轨道和2p轨道则形成了碳原子与氢原子之间的σ键。
这些σ键使得苯环具有较高的稳定性和抗氧化性,使其成为许多有机化合物的重要结构单元。
接下来,我们来研究苯环的π轨道。
苯环中的π轨道是由6个碳原子的2p轨道构成的,这些轨道形成了苯环中的π键。
苯环中共有3个π键,分别是平面内的π键和垂直于平面的π键。
平面内的π键是由相邻的2个碳原子的2p轨道重叠形成的,而垂直于平面的π键是由相邻的2个碳原子的2p轨道与平面内的π键相互作用形成的。
这些π键使得苯环具有共轭体系的特性,使其具有较低的反应活性和较高的稳定性。
苯环的π电子具有很高的云度,即电子云分布在整个苯环上,而不是局限于某个特定的原子。
这种分布使得苯环具有共振稳定性,能够吸引外部的电子或电子云,从而发生亲电取代反应或电子亲和性反应。
苯环中的π电子还能够吸收紫外光和可见光,产生共振增强的吸收峰,使苯环具有良好的色素特性。
苯环的分子轨道还与其化学性质密切相关。
苯环具有芳香性,即具有稳定的π电子体系和不饱和键。
这种芳香性使得苯环具有较低的反应活性,往往需要较高的能量才能发生反应。
同时,苯环也具有较高的亲电性和亲核性,可以发生亲电取代反应和亲核加成反应。
苯环的分子轨道决定了其特殊的性质和特点。
苯环具有稳定性高、抗氧化性强、共振稳定性好等特点,成为有机化合物中重要的结构单元。
苯环的分子轨道还决定了其化学性质,使其具有芳香性、亲电性和亲核性等特性。
苯环的研究不仅对于有机化学领域具有重要意义,还对于材料科学、药物化学等领域有着广泛的应用前景。