晶型转变的影响因素
- 格式:doc
- 大小:1.99 MB
- 文档页数:10


影响晶型转变的因素众所周知,结构决定性质,而对于晶体来说,当外界条件变化时,晶体结构形式发生改变,碳、硅、金属的单质、硫化锌、氧化铁、二氧化硅以及其他很多物质都具有这一现象,所以本文通过查阅文献举例说明影响晶型的一些因素,主要有温度、压力、粒度和组成。
一、温度温度对晶型影响比较复杂,当温度升高时,晶体中的分子或某些离子团自由旋转,取得较高的对称性,而改变晶体的结构。
下面举例说明:(1) BaO·Al2O3·SiO2(BAS)系微晶玻璃的主晶相为钡长石。
钡长石主要的晶型有单斜钡长石(monoclinic celsian)、六方钡长石( hexa celsian)和正交钡长石(orthorhombic celsian),三者的关系如图1所示:Fig. 1 The phase transformation of celsian由图中我们可以看到:六方钡长石膨胀系数高,为8. 0×10-6/℃,而且在300℃左右会发生其向正交钡长石的可逆转变,转变过程中伴随着3-4%的体积变化。
(2)当预热温度小于400℃时,反应所得到的产物氧化铝为非晶态的A12O3。
非晶A12O3。
在热力学上是一种亚稳状态,所以它有向晶态转化的趋势。
当温度不够高时,非晶A12O3中的原子的运动幅度较小,同时晶化所必不可少的晶核的形成和生长都比较困难,因此非晶态向晶态的转化就不易。
为研究所制备的非晶A12O3。
向晶态Al2O3转变的规律,我们把在300℃时点火得到的非晶A12O3 进行了锻烧处理,结果见表2:Fig.1 XRD Patterns of Produets kept for 1.5h at 700一900℃Fig.2 XRD Pattems of produets kept for o.5h at l000一l200℃Fig.3 XRD Pattems of produets kept for o.5h at l000℃and l200℃Fig.4 XRD Pattems of produets kept for different time at l000℃Fig.5 XRD Pattems of produets kept for different time at 1100℃从图1中可以看到,非晶态的氧化铝经700、800、900℃锻烧1.5h后,氧化铝从非晶态转变为r-A12O3,并且随着温度的升高r- A12O3。
对晶型转变的综述化学组成相同的固体,在不同的热力学条件下,常会形成晶体结构不同的同质异构体(polymorph)[1, 2]或称为变体(modification),这种现象叫同质多晶或同质多相(polymorphism)[2]现象。
当温度和压力条件变化时,变体之间会发生相互转变,此称为晶型转变。
显然,晶型转变是相变的一种,也是最常见的一种固–固相变形式。
由于晶型转变,晶体材料的力学、电学、磁学等性能会发生巨大的变化。
例如,碳由石墨结构转变为金刚石结构后硬度超强,BaTiO3由立方结构转变为四方结构后具有铁电性。
可见,通过相变改变结构可达到控制固体材料性质的目的。
晶型转变有可逆转变与不可逆转变之分。
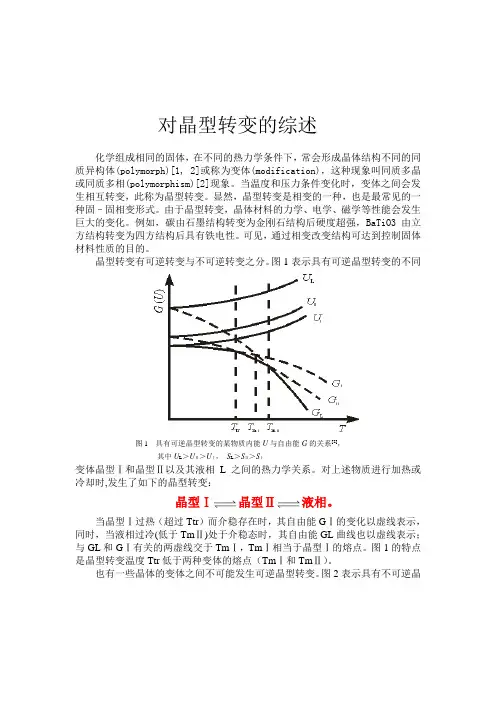
图1表示具有可逆晶型转变的不同图1 具有可逆晶型转变的某物质内能U与自由能G的关系[2],其中U L>UⅡ>UⅠ,S L>SⅡ>SⅠ变体晶型Ⅰ和晶型Ⅱ以及其液相L之间的热力学关系。
对上述物质进行加热或冷却时,发生了如下的晶型转变:晶型Ⅰ晶型Ⅱ液相。
当晶型Ⅰ过热(超过Ttr)而介稳存在时,其自由能GⅠ的变化以虚线表示,同时,当液相过冷(低于TmⅡ)处于介稳态时,其自由能GL曲线也以虚线表示;与GL和GⅠ有关的两虚线交于TmⅠ,TmⅠ相当于晶型Ⅰ的熔点。
图1的特点是晶型转变温度Ttr低于两种变体的熔点(TmⅠ和TmⅡ)。
也有一些晶体的变体之间不可能发生可逆晶型转变。
图2表示具有不可逆晶型转变的不同变体晶型Ⅰ、晶型Ⅱ及它们的液相L之间的热力学关系。
TmⅠ为晶型Ⅰ的熔点,TmⅡ相当于晶型Ⅱ的熔点。
虽然在温度轴上标出了晶型转变温度Ttr,但事实上是得不到的,因为晶体不可能在超过其熔点的温度下发生晶型转变。
此图的特点是,晶型转变温度Ttr高于两种变体的熔点(TmⅠ和TmⅡ)。
从图2可看出,三种晶型相互转变的过程可由下式表示.晶型Ⅰ熔体晶型Ⅱ先经过中间的另一个介稳相(如晶型Ⅱ),才能最终转变成该温度下的稳定态(晶型Ⅰ)的规律,称为阶段转变定律。

锐钛矿TiO2转变为金红石TiO2机制和性能摘要:TiO2 是多相光催化研究中使用较多的一种材料。
其在自然界存有3种不同的晶型:锐钛矿、金红石、板钛矿相。
锐钛矿相转变为金红石相的过程是扩散相变。
金红石是热力学稳定相, 锐钛矿是亚稳相, 并且从锐钛矿相到金红石相的相变是亚稳相到稳定相的不可逆相变。
而煅烧时间与煅烧温度会影响其晶型的转变。
在众多影响光催化性能的因素中,晶型是较为重要的一个因素。
关键字:锐钛矿、金红石、TiO2、相变、光催化光催化降解是一门新型的并正在迅速发展的科学技术。
研究表明,在适当的条件下,许多有机物污染物经光催化降解,可生成无毒无味的CO2、H2O及一些简单的无机物。
目前,在光催化降解领域所采用的光催化剂多为N型半导体材料, 如TiO2、ZnO、Fe2O3、SnO2、WO3和CdS 等, 其中TiO2以其无毒、价廉、稳定和特殊的光、电性能等优点倍受人们青睐,成为最受重视的一种光催化剂[1]。
1.二氧化钛的结构近年来, TiO2纳米材料制备、表征及改性一直是光催化研究领域的重点。
同一种半导体可能具有不同的晶型,晶型的不同实际上就是组成物质的原子不同的空间构型有序的排布。
二氧化钛是白色粉末状多晶型化合物, 自然界有锐钛矿型, 金红石型和板钛型三种晶型结构, 但板钛型二氧化钛极不稳定且无实用价值[2]。
所以目前的研究一般都主要为金红石相及锐钛矿相。
TiO2晶体基本结构是钛氧八面体( TiO6)。
钛氧八面体连接形式不同而构成锐钛矿相、金红石相和板钛矿相。
锐钛矿型和金红石型均属于四方晶系,二者均可用相互连接的Ti06八面体表示,但八面体的畸变程度和连接方式各不不同。
板钛矿型属正交晶系,一般难以制备,目前研究很少。
如图1所示,金红石型(a)的八面体不规则,微显斜方晶;锐钛矿(b)呈明显的斜方晶畸变,对称性低于前者。
从图2[3]中可以看出锐钛矿TiO2的Ti-Ti键长比金红石大,而Ti-O键比金红石小。

一、晶型现象固体物质可以由晶态物质与非晶态物质组成。
晶态物质是由于组成物质的分子、原子、离子在三维空间有序排列,具有周期性排列规律。
非晶态物质是指分子、原子、离子在三维空间无序堆积而成。
晶态物质又被称为晶体,当晶体结构测定发现样品分子中存在溶剂或水分子时,该样品晶体存在多晶型现象的可能性就会增大,因为样品分子容易与溶剂或水分子形成氢键,当被测样品的分子与不同的溶剂分子结合时,将会形成不同晶型的物质。
不含溶剂的晶体也可能由于分子的对称排列规律的不同而存在多晶型现象。
因此,晶型是化合物一个重要的理化性质,对于多晶型药物,因晶格结构不同,某些理化性质(如熔点、溶解度、稳定性)可能不同;且在不同条件下,各晶型之间可能会发生相互转化。
二、原料药晶型研究应注意的几个方面难溶性固体药物,在作为固体口服制剂开发时,应对原料药的晶型进行研究。
因为同一化合物可能因其制备工艺的差异(如重结晶使用不同的溶剂或不同的结晶方法),而产生不同的晶型。
化合物晶型的改变除由其本身性质决定外,还受其它一些因素的影响。
例如,在不同温度、光照、湿度的条件下,化合物的晶型会随着失水或吸收水分而变化;不同的溶剂对化合物的晶型也会产生不同的影响。
对于全新的药物,首先应研究其是否存在多晶型现象,考虑可能影响晶型的各种因素(温度、重结晶溶剂及重结晶条件),设计不同的重结晶方案。
选择重结晶溶剂时应考虑常用的溶剂,选择范围应考虑极性溶剂、中等极性溶剂、非极性溶剂等单一溶剂系统;在单一溶剂系统的基础上,还应使用混合溶剂和它们的不同配比来进行研究。
同时还应研究温度的变化对晶型的影响,通常根据样品的特性,可以将重结晶实验的温度设计在低温5℃和常温20℃左右为宜。
观察不同温度环境下样品晶体外形的变化情况,获得各种不同重结晶实验条件下的晶型样品。
确定化合物是否存在多晶现象后,应进一步对各晶型的理化性质的差异进行研究,固定目标晶型;规范制备工艺的操作,保证制备工艺中结晶条件稳定。

药物制剂开发中对晶型的考虑随着药物开发研究的深入,难溶性药物在新药中的比例不断的增大,晶型问题越来越被重视。
不同晶型会影响药物在体内的溶出、吸收,进而影响药物的临床疗效和安全性,特别是一些难溶性口服固体和半固体制剂。
因此,对于多晶型药物,在研制成固体和半固体口服制剂时,对晶型进行研究有利于开发一种在临床治疗上有意义且稳定可控的晶型。
目前,国内对晶型问题也愈来愈重视,2015版药典附录新增“9105 多晶型药品的质量控制技术与方法指导原则”指出: 固体药物及其制剂中存在多晶型现象时,应使用“优势药物晶型物质状态”作为药物原料及其制剂晶型,以保证药品临床有效性、安全性与质量可控性。
下面就药物审评工作中遇到的晶型问题,以及研究开发这类多晶型药物所需注意的问题谈一些看法。
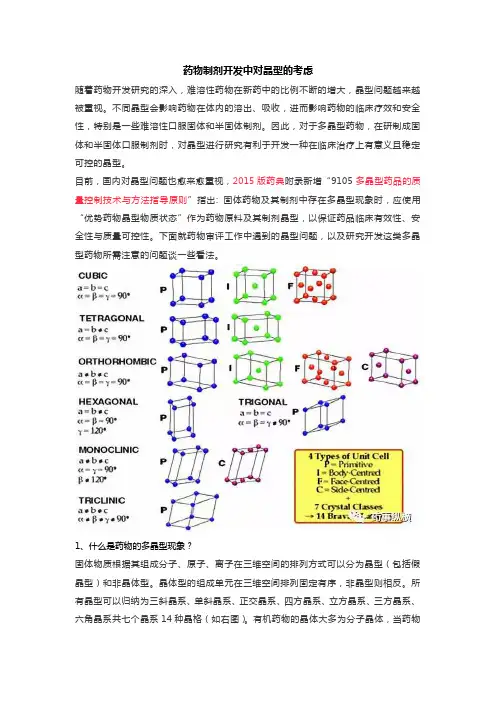
1、什么是药物的多晶型现象?固体物质根据其组成分子、原子、离子在三维空间的排列方式可以分为晶型(包括假晶型)和非晶体型。
晶体型的组成单元在三维空间排列固定有序,非晶型则相反。
所有晶型可以归纳为三斜晶系、单斜晶系、正交晶系、四方晶系、立方晶系、三方晶系、六角晶系共七个晶系14种晶格(如右图)。
有机药物的晶体大多为分子晶体,当药物分子中存在溶剂或分子时,因为药物分子易与溶剂或水分子形成氢键,药物分子与不同的溶剂分子结合,就会形成不同的晶型;不含溶剂的药物也可能由于分子的对称排列规律不同而存在的多晶现象,如药物结晶时的溶解、温度、湿度等,制剂过程中粉碎、混悬、压片等都会影响药物的晶型。
2、多晶现象会如何影响药物性质?众所周知,结构决定功能,同一药物的不同晶型在外观、溶解度、熔点、溶出度、生物有效性等方面都可能会有显著不同,从而影响了药物的稳定性、生物利用度及疗效,该种现象在口服固体制剂方面表现得尤为明显。
1)对药物理化性质及工业制剂的影响多晶型固体药物每个晶型有不同的表面自由能,而表面自由能大小是影响其溶出度的因素之一,像亚稳态的非极性表面自由能与稳态晶型基本相同,但极性表面自由能大于稳态的,因而总的表面自由能较大,更易被水润湿,在固体制剂崩解后形成的混悬液中,由于亚稳态粒子表面易水化,较厚的水化膜的反絮凝作用优于稳态晶型物,因而亚稳态的晶体粒子更易分散,顾有高的溶出度,如无味氯霉素共有A、B、C 3种晶型及无定型,我国1975年以前生产的无味氯霉素原料片剂、胶囊都为无效的A 型,后经改进生产工艺才生产出有生物活性的B型,并在质量标准中增加了非活性晶型的限度。

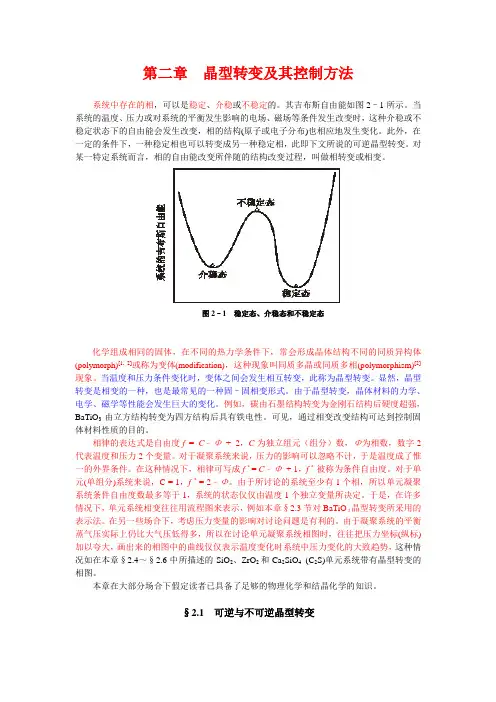
第二章晶型转变及其控制方法系统中存在的相,可以是稳定、介稳或不稳定的。
其吉布斯自由能如图2–1所示。
当系统的温度、压力或对系统的平衡发生影响的电场、磁场等条件发生改变时,这种介稳或不稳定状态下的自由能会发生改变,相的结构(原子或电子分布)也相应地发生变化。
此外,在一定的条件下,一种稳定相也可以转变成另一种稳定相,此即下文所说的可逆晶型转变。
对某一特定系统而言,相的自由能改变所伴随的结构改变过程,叫做相转变或相变。
图2–1 稳定态、介稳态和不稳定态化学组成相同的固体,在不同的热力学条件下,常会形成晶体结构不同的同质异构体(polymorph)[1, 2]或称为变体(modification),这种现象叫同质多晶或同质多相(polymorphism)[2]现象。
当温度和压力条件变化时,变体之间会发生相互转变,此称为晶型转变。
显然,晶型转变是相变的一种,也是最常见的一种固–固相变形式。
由于晶型转变,晶体材料的力学、电学、磁学等性能会发生巨大的变化。
例如,碳由石墨结构转变为金刚石结构后硬度超强,BaTiO3由立方结构转变为四方结构后具有铁电性。
可见,通过相变改变结构可达到控制固体材料性质的目的。
相律的表达式是自由度f= C–Φ+ 2,C为独立组元(组分)数,Φ为相数,数字2代表温度和压力2个变量。
对于凝聚系统来说,压力的影响可以忽略不计,于是温度成了惟一的外界条件。
在这种情况下,相律可写成f * = C–Φ+ 1,f * 被称为条件自由度。
对于单元(单组分)系统来说,C = 1,f * = 2–Φ。
由于所讨论的系统至少有1个相,所以单元凝聚系统条件自由度数最多等于1,系统的状态仅仅由温度1个独立变量所决定。
于是,在许多情况下,单元系统相变往往用流程图来表示,例如本章§2.3节对BaTiO3晶型转变所采用的表示法。
在另一些场合下,考虑压力变量的影响对讨论问题是有利的。
由于凝聚系统的平衡蒸气压实际上仍比大气压低得多,所以在讨论单元凝聚系统相图时,往往把压力坐标(纵标)加以夸大,画出来的相图中的曲线仅仅表示温度变化时系统中压力变化的大致趋势,这种情况如在本章§2.4~§2.6中所描述的SiO2、ZrO2和Ca2SiO4(C2S)单元系统带有晶型转变的相图。

CL-20重结晶过程中的晶型转变研究高能量密度化合物六硝基六氮杂异伍兹烷(CL-20)是现有综合性能最好的单质炸药之一,在推进剂、配方炸药、发射药领域有广阔的应用前景。
多晶型现象是炸药研究的重要方面,不同晶型晶体的存在会影响炸药的密度、感度、稳定性、爆轰性能等,需制备纯晶型晶体以满足使用要求。
CL-20属于多晶型炸药,常温常压下存在α-、β-、γ-及ε-四种晶型,其中ε-晶型的密度最大、稳定性最高、爆轰性能最好,最有使用价值。
结晶时CL-20易发生晶型转变,形成混合晶型晶体,影响炸药性能。
如何控制晶型转变行为,制备高晶型纯度、高品质ε-晶体是CL-20结晶技术中最关心的问题。
因此,通过研究不同结晶条件对CL-20晶型转变的影响,优化结晶技术,为高晶型纯度ε-CL-20的制备以及CL-20结晶机理的探索提供指导。
采用溶剂-非溶剂法重结晶CL-20,考察了非溶剂性质、溶剂滴加方式、溶剂/非溶剂比例、溶剂化物、结晶温度等因素对CL-20晶型转变的影响,采用PXRD及FTIR 确定了CL-20的晶型,获得了CL-20的晶型转变行为,初步掌握了CL-20的晶型转变规律及控制技术,并尝试解释了晶型转变机理。
主要结果如下:(1)非溶剂的偶极矩(或极性)对CL-20的结晶特性有重要影响,极性大的非溶剂倾向于先析出亚稳的β-晶体而后逐渐转变为稳定的ε-晶体,极性弱的非溶剂趋于直接得到ε-晶体。
(2)溶剂滴加速率越快,CL-20溶液过饱和度增大越快,越有利于β-晶体析出。
采用反倾方式结晶时,溶液过饱和度快速达到最大,均是首先析出β-晶体,此时非溶剂性质的影响变小。
(3)非溶剂所占比例越大,CL-20在溶液中的溶解度越小,亚稳晶型晶体转变为稳定晶型晶体所需的时间越多。
(4)发现了四种新的溶剂化物晶体:CL-20·丙酮、CL-20·乙腈、CL-20·碳酸二甲酯、CL-20·硫酸二乙酯。
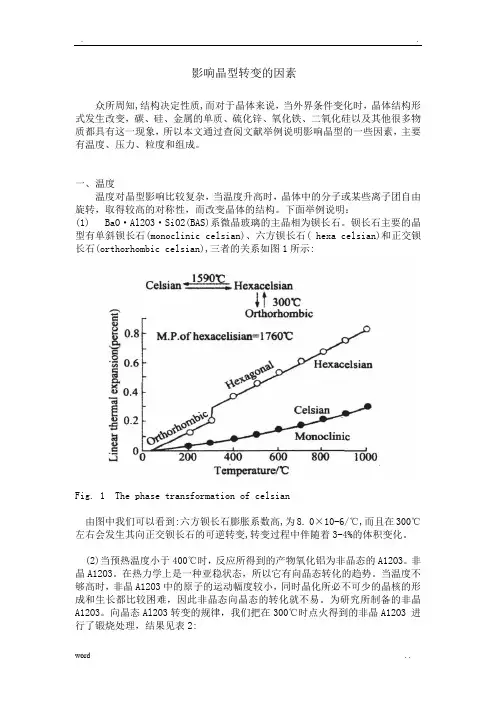
影响晶型转变的因素众所周知,结构决定性质,而对于晶体来说,当外界条件变化时,晶体结构形式发生改变,碳、硅、金属的单质、硫化锌、氧化铁、二氧化硅以及其他很多物质都具有这一现象,所以本文通过查阅文献举例说明影响晶型的一些因素,主要有温度、压力、粒度和组成。
一、温度温度对晶型影响比较复杂,当温度升高时,晶体中的分子或某些离子团自由旋转,取得较高的对称性,而改变晶体的结构。
下面举例说明:(1) BaO·Al2O3·SiO2(BAS)系微晶玻璃的主晶相为钡长石。
钡长石主要的晶型有单斜钡长石(monoclinic celsian)、六方钡长石( hexa celsian)和正交钡长石(orthorhombic celsian),三者的关系如图1所示:Fig. 1 The phase transformation of celsian由图中我们可以看到:六方钡长石膨胀系数高,为8. 0×10-6/℃,而且在300℃左右会发生其向正交钡长石的可逆转变,转变过程中伴随着3-4%的体积变化。
(2)当预热温度小于400℃时,反应所得到的产物氧化铝为非晶态的A12O3。
非晶A12O3。
在热力学上是一种亚稳状态,所以它有向晶态转化的趋势。
当温度不够高时,非晶A12O3中的原子的运动幅度较小,同时晶化所必不可少的晶核的形成和生长都比较困难,因此非晶态向晶态的转化就不易。
为研究所制备的非晶A12O3。
向晶态Al2O3转变的规律,我们把在300℃时点火得到的非晶A12O3 进行了锻烧处理,结果见表2:Fig.1 XRD Patterns of Produets kept for 1.5h at 700一900℃Fig.2 XRD Pattems of produets kept for o.5h at l000一l200℃Fig.3 XRD Pattems of produets kept for o.5h at l000℃ and l200℃Fig.4 XRD Pattems of produets kept for different time at l000℃Fig.5 XRD Pattems of produets kept for different time at 1100℃从图1中可以看到,非晶态的氧化铝经700、800、900℃锻烧1.5h后,氧化铝从非晶态转变为r-A12O3,并且随着温度的升高r- A12O3。
同种物质不同晶型的原因1.引言1.1 概述概述部分的内容应该对论文的主题进行简要介绍,并概括介绍同种物质不同晶型的原因。
以下是一个可能的概述部分的内容:概述同种物质在不同条件下可能会出现不同的晶型,这是化学、物理等领域中一个引人注目的现象。
晶体的结构对物质的性质和用途都起着关键性的作用,因此了解同种物质不同晶型的原因具有重要的科学和应用意义。
本文将对同种物质不同晶型的原因进行研究和分析,并探讨其背后的驱动力和机制。
首先,文章将介绍晶体的基本结构概念以及晶型的定义和分类方法,为后续的讨论奠定基础。
随后,文章将重点关注不同晶型的形成原因。
这包括外部条件因素(如温度、压力、湿度等)和内部因素(如晶体生长速率、晶体结构的稳定性等)对晶型选择的影响。
通过对已有研究成果的综述和分析,我们将探讨为什么同种物质在不同条件下会出现不同的晶型。
在了解这一现象背后的驱动力的基础上,本文将进一步探讨如何通过调控条件因素和晶体生长过程来控制晶型的选择。
这对于制备特定晶型的材料以及优化物质性能具有重要的实际应用价值。
最后,本文将总结相关研究的成果和发现,并对未来研究方向进行展望。
相信通过深入探究同种物质不同晶型的形成原因,我们可以更好地理解晶体的结构与性质之间的关系,为材料科学和化学领域的进一步发展提供有益的启示。
通过本文的研究和探讨,我们期望能够为同种物质不同晶型的原因提供全面而深入的了解,为相关领域的进一步研究和应用提供有益的参考。
让我们开始探索同种物质不同晶型的奥秘吧!1.2文章结构文章结构部分的内容可以包括以下内容:文章结构部分旨在介绍整篇文章的组织架构和内容安排,以便读者能够更好地理解文章的内容和逻辑发展。
通过清晰的结构安排,读者能够更好地把握文章的重点和主题,并能够更好地跟随文章的思路。
在本篇长文中,文章结构部分的主要内容包括以下几点:1. 介绍文章的章节安排和目录结构:首先,可以简要提及文章的大纲和目录结构,说明文章将会由几个主要部分组成,并且明确每个部分的主要内容和目的。
关于药物多晶型的专述关于药物多晶型的专述内容提要对于固体制剂、半固体制剂、混悬剂等剂型,应注意药物是否存在多晶型。
因为同一固体药物可因结晶条件、制备工艺不同而得到不同晶型的晶体。
由于药物晶型的不同,其物理化学性质也不同,直接影响药物的质量与药效,因此在新药申报生产过程中,需要进行实验研究。
为此,本章在介绍晶体基本概念与基本规律的基础上,重点阐述药物多晶型的产生与分类、多晶型的制备与鉴定方法、多晶型转变条件与控制、多晶型的理化性质变化、多晶型与药物制剂工艺、生物利用度的关系,为研究药物多晶型奠定理论与实验基础。
第一节药物晶体特性与点阵结构一、药物晶体特性(一)晶体与非晶体固体药物从内部结构质点排列状态可分为晶体与无定形体。
晶体(crystal)是固体药物内部结构中的质点(原子、离子、分子)在空间有规律的周期性排列。
质点排列有规律性反映在三个方面:质点间距离一定、质点在空间排列方式上一定、与某一质点最邻近的质点数(配位数)一定。
质点排列的周期性是指在一定方向上每隔一定距离就重复出现相同质点的排列。
固体药物内部结构中质点无规则排列的固态物质称无定形体(amorphism),或称非晶体。
如图2-1。
(a)晶体(b)非晶体图2-1 晶体与非晶体(二)晶体的特性1.晶体的自范性晶体具有自发地生长成为一个结晶多面体,即以平面作为与周围介质的分界面,称此性质为晶体的自范性。
因此晶体的外表具有整齐、规则的几何外形,无定形体则无此种特征。
2.晶体的各向异性与均匀性(1)各向异性由于晶体内部质点在各个方向上排列的距离不同,其性质也表现出差异。
例如晶体的光学性质如折射率、电学性质如导电系数、力学性质如弹性系数等在不同方向上具有不同的数值,称此为晶体的各向异性。
无定形体是各向同性。
(2)均匀性在宏观情况下,晶体中每一点上的物理性质与化学组成均是一致的。
例如各部分的密度,微观结构上的基本单位(晶胞)在空间排列的规律也是一致的。
新晶型的判断依据
新晶型的判断依据通常涉及到热力学稳定性、晶体结构预测、固态表征手段以及综合技术效果等方面。
具体如下:
1. 热力学稳定性:通过实验方法如差示扫描量热法(DSC)、热重分析法(TGA)等,评估不同晶型的热稳定性。
一般情况下,热力学稳定性最好的晶型往往是首选。
2. 晶体结构预测:利用计算模拟方法,基于分子的二维结构式预测所有可能的稳定晶型。
这一过程包含晶体搜索、能量排位和室温稳定性计算等关键阶段。
3. 固态表征手段:采用粉末X射线衍射(PXRD)、拉曼光谱仪等技术,鉴别并判断不同批次样品中原料药晶型的一致性和稳定性。
考察晶型转变的临界条件和转化关系,确保制剂工艺中晶型的稳定。
4. 综合技术效果:在审查药物晶型发明的创造性时,不仅要考虑新晶型本身技术方案是否非显而易见,还要考虑新晶型的综合技术效果是否预料不到。
这包括晶型的稳定性、生物利用度、制备工艺等多个方面的综合评估。
综上所述,新晶型的判断是一个综合考虑多个因素的过程,需要通过实验数据和理论分析相结合的方式来进行。
影响晶型转变的因素众所周知,结构决定性质,而对于晶体来说,当外界条件变化时,晶体结构形式发生改变,碳、硅、金属的单质、硫化锌、氧化铁、二氧化硅以及其他很多物质都具有这一现象,所以本文通过查阅文献举例说明影响晶型的一些因素,主要有温度、压力、粒度和组成。
一、温度温度对晶型影响比较复杂,当温度升高时,晶体中的分子或某些离子团自由旋转,取得较高的对称性,而改变晶体的结构。
下面举例说明:(1) BaO·Al2O3·SiO2(BAS)系微晶玻璃的主晶相为钡长石。
钡长石主要的晶型有单斜钡长石(monoclinic celsian)、六方钡长石( hexa celsian)和正交钡长石(orthorhombic celsian),三者的关系如图1所示:Fig. 1 The phase transformation of celsian由图中我们可以看到:六方钡长石膨胀系数高,为8. 0×10-6/℃,而且在300℃左右会发生其向正交钡长石的可逆转变,转变过程中伴随着3-4%的体积变化。
(2)当预热温度小于400℃时,反应所得到的产物氧化铝为非晶态的A12O3。
非晶A12O3。
在热力学上是一种亚稳状态,所以它有向晶态转化的趋势。
当温度不够高时,非晶A12O3中的原子的运动幅度较小,同时晶化所必不可少的晶核的形成和生长都比较困难,因此非晶态向晶态的转化就不易。
为研究所制备的非晶A12O3。
向晶态Al2O3转变的规律,我们把在300℃时点火得到的非晶A12O3 进行了锻烧处理,结果见表2:Fig.1 XRD Patterns of Produets kept for 1.5h at 700一900℃Fig.2 XRD Pattems of produets kept for o.5h at l000一l200℃Fig.3 XRD Pattems of produets kept for o.5h at l000℃ and l200℃Fig.4 XRD Pattems of produets kept for different time at l000℃Fig.5 XRD Pattems of produets kept for different time at 1100℃从图1中可以看到,非晶态的氧化铝经700、800、900℃锻烧1.5h后,氧化铝从非晶态转变为r-A12O3,并且随着温度的升高r- A12O3。
相的衍射峰有所增强;1000℃保温1.5h后有r- A12O3相产生,但仍有部分a- A12O3相存在;1100℃以上产物完全为a- A12O3,如图2所示。
所以在本试验条件下由低温燃烧合成法制备的非晶态的A12O3粉体向a相转变的温度>=1000℃。
图3为1000、1100℃保温0.5h的XRD图,从图中可见1000℃保温0.5h产物仍为,r- A12O3,而1100℃保温0.5h产物已完全转变为a- A12O3相。
可见r- A12O3向a- A12O3的转变与温度有很大关系。
随着温度的升高,r- A12O3向a- A12O3的转变就易于进行。
从图4中可以看出1000℃保温0.5h时没有a- A12O3相产生,保温1.5h时有a- A12O3相产生但没有转变完全,说明r- A12O3向a- A12O3转变与保温时间也有关系,随着保温时间的增加,r- A12O3向a- A12O3的转变逐渐完成。
图5为1100℃保温0.5、1.5h的XRD图,其衍射峰相似,说明影响r- A12O3向a- A12O3的转变最主要的因素是温度。
当温度足够高时,,r- A12O3向a-- A12O3的转变速度快,在较短时间内就可以完成r- A12O3向a相的转变。
二、压力压力的影响比较单纯,当压力增高时,促使晶体结构往高密度和高配位的方向转变。
下面看看具体例子:(1)相同温度下不同压力下的SiO2中硅氧键长、氧离子半径及阳离子硅的半径是不同的。
因此,不同压力范围内的SiO2的晶型也有很大差别。
如图一所示。
(2)前面已经说过温度对晶型转变有影响,所以温度与压力双重作用也会对晶型转变产生影响。
如图二所示。
(3)由图一我们看到,不同压力下SiO2有不同的晶型,那么只需要控制温度一定,改变压力,就可以得到新的晶型。
图三就是其中一个例子。
图1 高温下不同压力的SiO2多形中硅氧键长(顶部)、氧离子半径(中部)及阳离子硅的半径(底部)。
纵坐标,显示键长及离子半径,单位为 A ,横坐标,1:石英(常压),2:柯石英(4~8GPa,),3:斯石英(8~50GPa,),4:α-PbO2型SiO2(90~200GPa,),5:黄铁矿型SiO2(90~200GPa)图2二氧化硅(SiO2)物相在高温、高压条件下的相变情况图3 石英(左)和斯石英(右)的晶体结构图:实验表明,当压力增加到8GPa时阳离子硅会发生从硅氧四面体空隙向硅氧八面体空隙迁移的现象在上述各多形中晶体结构与常温常压力的石英比较起来最深刻的变化是配位多面体形态的改变。
众所周知,在地壳条件下石英如同其他硅酸盐及氧化物矿物一样,硅与氧的连接方式是硅氧四面体,四面体间均以共角顶方式连接(图4左)。
当压力高达8GPa以上时石英的。
晶体结构就开始发生相变形成斯石英晶体结构(图4右)。
变化发生时阳离子硅会从四面体空隙迁移至八面体空隙。
从而形成了与金红石(TiO2)相似的结构。
高压相变还导致氧离子半径不断缩小及氧-氧间距不断缩小,如当压力增至200~250GPa时形成黄铁矿型SiO2多形,在该结构中最短的氧-氧间距缩短至2.366 ,说明氧离子间的电子云已有严重交盖,共价键性质已十分明显了。
(2)再看看尼群地平的例子:Figure 6 X-ray diffraction pattern of nitrendipine polymorphs under high pressure a: NTDI under high pressure of 9.8×104N; b: NTDII under high pressure of9.8×104N; c: NTDIII under high pressure of 9.8×104N; d: NTDI; e: NTDII;f: NTDIII图6是将不同晶型尼群地平在 9.8×104N 压力下压片(直径=12 mm), 粉碎后测定 X 射线图谱, NTDI, NTDIII 未发生转型,而 NTDII 转化为 NTDI, 说明压力可以使晶体发生晶型转变。
又将 NTDII 分别在 4.9×104, 9.8×103, 4.9×103, 2.45×103N 压力下压片(直径=12 mm), 粉碎后测定 X 射线衍射图谱, 结果表明 NTDII在 2.45×103N 压力下晶型不发生相变, 在其它压力下 NTDII 都转化为 NTDI.结果见图7:Figure 7 X-ray diffraction pattern of NTDII under different pressurea: NTDII under high pressure of 4.9×104N; b: NTDII under high pressure of9.8×103N; c: NTDII under high pressure of 4.9×103N; d: NTDII under high pressure of 2.45×103N; e: NTDII; f: NTDI三、粒度颗粒大小也会影响晶型,下面举例说明:Fig. 1b δ-HMX a β-HMX粒度大小对HMX的晶型转变有着显著的影响。
Saw[22]采用XRD研究了升温过程中HMX的晶体结构变化,并用SHG和XRD结合研究了恒温下HMX的晶型转变,通过比较两种不同的测试方法,他认为SHG的强度受到晶粒表面积的影响较大, SHG方法容易得到错误的分析结果。
Saw利用原子力显微镜(AFM)观察单晶HMX,发现在180~184℃范围内的晶型转变完全后,HMX的表面积增大了103~105数量级。
粒度的影响和表面积的增加可以解释SHG和XRD数据不一致的矛盾。
在随后的研究工作中, Saw[8]研究了不同粒度HMX的β→δ晶型转变动力学。
结果表明:在同样的升温速率下,粒度大的HMX晶型转变温度低,粒度小的晶型转变温度高,即粒度大的HMX晶型转变活化能较低; Saw认为其原因是大颗粒HMX中存在较多的缺陷,降低了晶型转变的能量势垒,所以易于实现β→δ晶型转变。
但是,他未对不同粒度HMX的缺陷进行定性和定量表征,其结论还有待验证.四、组成组成会影响晶型,也就是结构因素能影响晶型。
(1)化学组成不同,晶型也不同PBT(聚对苯二甲酸丁二醋)和PET(聚对苯二甲酸乙二醋)是同族聚醋,其结晶均属三斜晶系。
但PET只有一种晶型,而PBT则有两种结晶变体—a型和b型。
由于PBT在低速(l000m/min以下)纺丝时有脱边现象,引起了人们对其结晶结构的兴趣。
近年来,许多文献报道了对PBT晶型的研究结果。
一致的观点是:在一定条件,卷缩形的a晶型与伸展形的b晶型能可逆转变。
金惠芬等人在600m /min 纺速下纺制了三种比例的共聚醋长丝。
纺丝过程中发现:乙二醇/丁二醇(EG/BD)为25/75(指摩尔比,下同)的共聚醋发生脱边,且随存放时间的延长,脱边越厉害,纤维松弛脱筒,卷装不良,而EG/BD为75/25和50/5的两种共聚醋不发生脱边。
用WAxS方法测试卷绕丝的结果说明,共聚醋的脱边现象不是晶型转变引起的,但共聚醋确实存在晶型的转变,所以说共聚醋的晶型与其组成密切相关(2)掺杂是组成变化的一种,会促使晶型改变。
下图为SN4+掺杂TiO2的相变。
图1A显示的纯TiO2样品退火后的XRD谱温度范围从300到700℃。
可以观察到,P-300,P-450和P-500样品表现出的锐钛矿结构。
19A弱峰在27.3°左右被发现在P-550除了锐钛矿峰,表明存在一个小的金红石结构的样品中的量。
与P-550相比,P-600增加的那些样本中金红石的衍射峰锐钛矿下降,这意味着相变锐钛矿型向金红石样品中发生。
一个纯金红石结构在P-700的样品观察到的,这意味着在锐钛矿结构完全转化为金红石型。
因此,最低温度从锐钛矿向金红石的相变是约550℃下纯二氧化钛。
XRD谱Sn4 +的掺杂TiO2样品退火温度范围从300至700℃的中演示,图1B。
D-300样品只显示了锐钛矿结构。