影响13C化学位移因素
- 格式:doc
- 大小:29.50 KB
- 文档页数:2







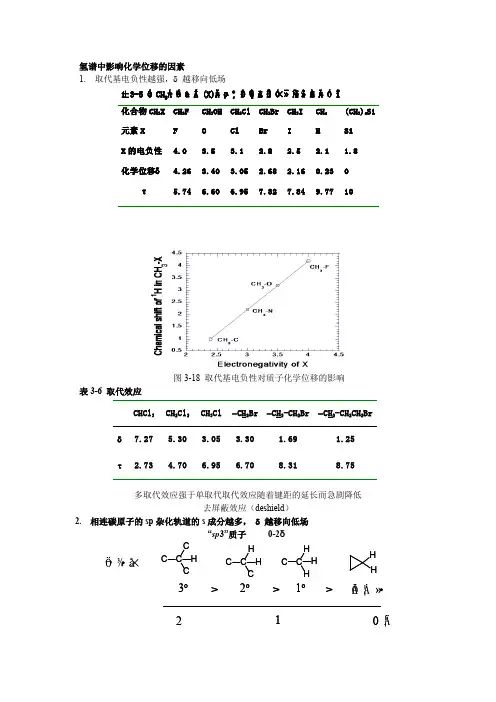
氢谱中影响化学位移的因素1. 取代基电负性越强,δ 越移向低场±í3-5 ÓëCH 3Á¬½Ó»ùÍÅ(X)µÄµç¸ºÐÔ¶ÔÆäÖÊ×Ó»¯Ñ§Î»ÒƵÄÓ°Ïì化合物CH 3X CH 3F CH 3OH CH 3Cl CH 3Br CH 3I CH 4 (CH 3)4Si 元素XFO Cl Br I H Si X 的电负性 4.0 3.53.12.82.52.11.8化学位移δ4.26 3.40 3.05 2.68 2.16 0.23 0 τ5.746.60 6.957.32 7.84 9.77 10图3-18 取代基电负性对质子化学位移的影响表3-6 取代效应CHCl 3CH 2Cl 2 CH 3Cl -CH 2Br -CH 2-CH 2Br -CH 2-CH 2CH 2Br δ 7.27 5.30 3.05 3.30 1.69 1.25 τ 2.734.706.956.708.318.75多取代效应强于单取代取代效应随着键距的延长而急剧降低去屏蔽效应(deshield )2. 相连碳原子的sp 杂化轨道的s 成分越多, δ 越移向低场“sp 3”质子 0-2δ 321C C C C H C C HCH C C H H H H H 0 ¦Ä12Ö¬·¾×åo ooÕÅÁ¦»·>>>“sp2”质子 4.5-7δ“sp”质子2-3δ3. 酸性质子10-12δRCOR OO作用和O电负性拉电子效应的双重影响氢键的影响和可交换质子能够形成氢键的质子(-OH,-NH2)化学位移可变±í3-7 ¿É±ä»¯Ñ§Î»ÒƵÄÖÊ×ÓAcids RCOOH 10.5-12.0δPhenols ArOH 4.0-7.0Alcohols ROH 0.5-5.0Amines RNH20.5-5.0Amides RCONH25.0-8.0Enols CH=CH-OH ≥15形成氢键的数目越多,质子的去屏蔽效应越强氢键数目通常是浓度和温度的函数R O OHδ游离羟基(稀溶液)0.5-1.0δ形成氢键(浓溶液)4-5δ可交换质子(活泼氢)HHR O H a+R'O H b R O H b+R'O H aR O+R O H+H SOLV SOLVR O+SOLV SOLVHR O+3. 共轭效应C H C 33.886.27C CC HCH 35.906.73CH7.81p-π共轭,邻位H 的电子密度增加(正屏蔽),δ值减少π-π共轭,邻位H 的电子密度减少(去屏蔽),δ值增加5. 相邻基团电偶极矩和范德华力的影响 当分子内有强极性基团时,它在分子内产生电场,影响分子内其余部分的电子云密度,从而影响其它核的屏蔽常数。

13c化学位移13C化学位移是指13C核磁共振(NMR)谱中化合物中13C原子的共振频率与参比化合物(通常为四氯化硅)的共振频率之间的差异。
13C化学位移可以提供有关化合物结构和化学环境的信息,因此在有机化学和生物化学研究中得到了广泛应用。
13C化学位移的数值通常以ppm(parts per million)为单位表示,即化学位移与参比化合物的共振频率之比乘以百万。
13C化学位移受到多种因素的影响,包括化合物的电子密度、杂化程度、相邻原子的影响等。
13C化学位移与化合物中原子的电子密度有关。
电子密度越高,13C 核周围的屏蔽效应越强,化学位移数值越高。
相反,电子密度越低,13C核周围的屏蔽效应越弱,化学位移数值越低。
这是因为电子云中的电子对13C核的磁场产生屏蔽效应,使13C核的共振频率降低。
13C化学位移还与化合物中原子的杂化程度有关。
杂化程度越高,13C核周围的屏蔽效应越强,化学位移数值越高。
相反,杂化程度越低,13C核周围的屏蔽效应越弱,化学位移数值越低。
这是因为杂化程度不同会导致13C核周围的电子云形状和分布不同,进而影响屏蔽效应的强弱。
13C化学位移还受到相邻原子的影响。
相邻原子中的电子云对13C 核的磁场也会产生一定的屏蔽效应或解屏蔽效应,从而影响13C化学位移。
例如,如果相邻原子中的电子云对13C核的磁场产生屏蔽效应,那么13C化学位移数值会增加;相反,如果相邻原子中的电子云对13C核的磁场产生解屏蔽效应,那么13C化学位移数值会减小。
13C化学位移是一种重要的结构表征工具,可以提供关于化合物结构和化学环境的信息。
通过对13C化学位移的研究,我们可以更好地理解和解释有机化合物的性质和反应机理,在药物研发、天然产物合成和材料科学等领域发挥重要作用。
希望本文能够帮助读者对13C化学位移有更深入的了解,并在相关研究中得到应用。
13c化学位移13C化学位移又称为碳-13核磁共振化学位移,是一种用于分析和鉴定有机化合物结构的重要技术。
本文将介绍13C化学位移的基本原理、应用领域以及相关实验方法。
一、基本原理13C化学位移是指13C核在磁场中吸收辐射的频率与参照物(通常为四氯化硅或甲基溴化锗)吸收辐射频率之间的差异。
13C原子的化学位移受到周围化学环境的影响,包括化学键的性质、取代基团的影响以及分子结构的排列方式等。
通过测定13C化学位移,可以推断化合物的结构和化学环境。
二、应用领域13C化学位移广泛应用于有机化学、药物研究、聚合物化学、天然产物研究等领域。
在有机化学中,13C化学位移可以用于鉴定和确认化合物的结构,尤其对于复杂分子或异构体的鉴定非常有帮助。
在药物研究中,通过测定药物分子中的13C化学位移,可以了解药物分子与生物体内其他分子的相互作用方式,从而优化药物的设计和性能。
在聚合物化学中,13C化学位移可以用于研究聚合物的结构和性质,指导聚合反应的优化和控制。
在天然产物研究中,通过测定天然产物中的13C化学位移,可以鉴定和分析复杂的天然产物结构,为天然产物的合成和开发提供依据。
三、实验方法测定13C化学位移通常采用核磁共振技术。
核磁共振仪是一种特殊的仪器,利用强大的磁场和射频辐射对样品中的核自旋进行激发和检测。
在13C核磁共振实验中,将待测样品放入核磁共振仪中,通过调整磁场强度和射频辐射的频率,可以使13C核发生共振吸收。
根据共振吸收的峰位和峰强,可以确定13C化学位移和化学环境。
四、注意事项在进行13C核磁共振实验时,需要注意以下几点。
首先,样品的纯度和浓度对实验结果有很大影响,因此需要保证样品的纯度和浓度。
其次,样品的制备需要遵循一定的规范和方法,以免影响实验结果。
此外,实验过程中还需要注意仪器的使用方法和参数设定,以确保实验的准确性和可重复性。
13C化学位移是一种重要的有机化学分析技术,可以用于鉴定和确认化合物的结构,应用领域广泛。
在早期的碳谱研究中,化学位移的表示方法各不相同。
有的用二硫化碳,也有的用苯作参比。
现在与。
H-NMR谱相同,均以TMS为标准。
13C-NMR的常规谱大都是质子噪声去偶(或宽带去偶),特征是所得各种核的共振峰表现为单峰,它们的位置取决于化学位移,所以化学位移δc是13C-NMR 最重要的参数。
δC有一点和δH不同,即δC受分子间影响较小,因为H一般处在分子的边缘,邻近分子对它的影响较大,如H键、缔合等,而碳处在分子的骨架上,所以分子间效应对C影响较小,但分子内部的相互作用就显得很重要。
(1)碳原子的杂化类型
δC受杂化影响很大,而次序基本与δH平行,一般情况是:
CH3-CH3 δC 5.7 sp3δC<50ppm
CH~CH δC 71.9 sp δC=70~l00ppm
CH2-CH2 δC 123.3 sp2δC=70~100ppm
CH2-O δC 123.3 sp2δC=70~100ppm
(2)诱导效应
电负性取代基使相邻碳化学位移δ增加,增加的大小随相隔键数的增多而减弱。
这是由于电负性基团的诱导效应,使碳原子2p轨道电子云密度减小所致。
诱导效应对直接相连碳的影响最大,即α效应。
由于碳原子的电负性比氢原子的大,所以,尽管烷基为给电子基团,但是,在烷烃化合物中,烷基取代越多的碳原子,其δC反而越向低场位移。
根据这一规律,可以有助于推断碳的种类,即:δ(伯碳)<δ(仲碳)<δ(叔碳)<δ(季碳) 不同取代基对β碳的影响差别不大,对1碳的影响都使其向高场位移。
这表明,除了取代基的诱导效应外,还有其它因素影响碳核的化学位移。
电负性取代基越多,化学位移越大。
(3)共轭效应
共轭效应对对π体系中电子云分布有很大影响,从而影响碳的化学位移。
取代苯环中,供电子基团取代能使其邻、对位碳的电子云密度增加,对应碳的化学位移δ值减小,而吸电子基团取代则使其邻、对位碳的电子云密度减小,对应碳的化学位移δ值增加。
取代基对其间位碳的电子云密度的影响不大,故间位碳化学位移δ值的蛮化较小。
根据测得13C核的化学位移值,可推知分子中π价键被共轭极化的程度。
共轭多烯中,由于共轭所致的π电子离域,使共轭链中间烯碳的屏蔽增加,δ值减小。
由于类似的效应,不饱和羰基化合物(醛、酮、酸等)与相应的饱和羰基化合物相比,羰基碳的化学位移减小约10ppm,且不饱和β烯碳一般比α烯碳在更低场共振。
这种共轭作用受立体环境的影响。
当由于立体障碍共轭体系不能达到共平面时,则羰基碳δ值的高场位移的作用减弱。
(4)取代基对其γ碳的空间效应
取代基和空间位置很靠近的碳原子上的氢之间存在Vander Waals力作用,使相关C-H键的Q价电子移向碳原子,从而使碳核所受的屏蔽增加,化学位移δ值减小,称为空间效应。
取代基对其R碳的空间效应,使R碳的共振峰向高场位移常称为R效应。
空间效应使与取代基处于邻位交叉位置碳的共振峰向高场位移,而处于反式位置碳的共振峰的移动很小。
在链烷中,α一甲基取代后γ一邻位交叉构象约占30%,由于构象间的快速变换,γ碳的化学位移平均减小约
2ppm。
卤素等杂原子基团取代的γ效应可达7ppm。
在构象同定的环状结构中,γ一邻位交叉效应常常十分明显。
顺式取代烯烃中也常有明显的空间效应。
(5)电场效应
与胺基相邻近的碳核在胺基成盐(质子化)后共振向高场位移,这个现象无法用诱导效应进行解释。
这种变化是由于胺基在质子化后可在一定的部位产生局部电场,并由此引起邻近C-HQ键的极化,使对应碳核外电子云密度增加致使化学位移减小。
带电基团的局部电场作用,称为电场效应。
a碳由于诱导效应向低场位移和电场效应向高场位移的作用相互抵销,因而化学位移变化不大。
β碳向高场位移显著。
一般情况下基团质子化后,其d和β碳约向高场位移0.15~4ppm,γ和δ碳的位移通常小于1ppm。
含酸或碱基团化合物,由pH改变所致的与酸或碱取代基相邻近碳的化学位移变化,亦是由于分子内的电场效应所致。
在硝基苯中,硝基为强的吸电子取代基,理应使其邻位碳的电子云密度减小而δ增加。
但是,实际测得邻位碳的化学位移比间位碳的还小,表明邻位碳受到更强的屏
蔽。
显然,这不是由于诱导及共轭效应所致,而是由于硝基在分子内部形成的电场作用所致。
硝基的电场使其邻位C-Hq键电子云向碳核靠近所致的屏蔽增加抵销了吸电
子共轭效应,对应碳核的共振峰向高场位移。
而硝基苯中邻位的质子却是由于这种电场的作用,质子共振显著地向低场位移。
影响13C化学位移的因素还有重原子效应,同位素效应,超共轭效应,分子内氢键作用,以及介质影响等。
综上所述,13C化学位移受多种因素的综合影响。
取代基影响13C化学位移的主要特点是取代基对化学位移的贡献具有加和性。
因此,在13C -NMR光谱解析及结构测定中,可利用一些经验规则对化合物中不同化学环境碳的化学位移进行计算预测。
尤其是脂肪族开链烷烃,取代基的存在分别对其α一、β一、γ一及δ一位碳的化学位移产生加和性影响。
一碳位移变动主要是由诱导效应产生,因此,取代基的电负性决定了a一位碳位移变动的大小。
β一碳位移变动不仅受诱导效应的作用,而且受取代基在分子内的电场效应等多种因素的影响。
与a一及β一碳所受影响不同,γ一碳的化学位移变动主要是由于取代基与其γ一碳原子上相连氢之间的Vander Waals力作用(γ一效应)的结果。
不饱和碳的13C化学位移较易解析、预测,这是因为它们主要取决于局部电子云密度。
当然,还受其它因素的影响。