质谱的相关知识
- 格式:doc
- 大小:383.50 KB
- 文档页数:34

质谱基础知识汇总质谱,物质的分子在高真空下,经物理作用或化学反应等途径形成带电粒子,某些带电粒子可进一步断裂,形成离子,每一离子的质量与所带电荷的比称为质荷比(m∕z, 曾用m∕e),不同质荷比的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对强度,由此得出的谱图称为质谱。
不同离子的概念1、分子离子分子被电子束轰击失去一个电子形成的离子称为分子离子。
分子离子用疗表示。
分子离子是一个游离基离子。
在质谱图中与分子离子相对应的峰为分子离子峰。
分子离子峰的质荷比就是化合物的相对分子质量,所以,用质谱法可测分子量。
2、同位素离子含有同位素的离子称为同位素离子。
在质谱图上,与同位素离子相对应的峰称为同位素离子峰。
3、碎片离子分子离子在电离室中进一步发生键断裂生成的离子称为碎片离子。
4、重排离子经重排裂解产生的离子称为重排离子。
其结构并非原来分子的结构单元。
在重排反应中,化学键的断裂和生成同时发生,并丢失中性分子或碎片。
5、奇电子离子与偶电子离子具有未配对电子的离子为奇电子离子。
这样的离子同时也是自由基,具有较高的反应活性。
无未配对电子的离子为偶电子离子。
6、多电荷离子分子中带有不止一个电荷的离子称为多电荷离子。
当离子带有多电荷离子时,其质核比下降,因此可以利用常规的四极质量分析器来检测大分子量化合物。
7、亚稳离子从离子源出口到检测器之间产生的离子。
即在飞行过程中发生裂解的母离子。
由于母离子中途已经裂解生成某种离子和中性碎片,记录器中只能记录这种离子,也称这种离子为亚稳离子,由它形成的质谱峰为亚稳峰。
8、准分子离子比分子量多或少1质量单位的离子称为准分子离子,如:(M+H) + , (M-H)+o其不含未配对电子,结构上比较稳定。
分子离子峰1、分子离子峰强度分子离子是质谱图中最有价值的信息,它不但是测定化合物分子量的依据,而且可以推测化合物的分子式,用高分辨质谱可以直接测定化合物的分子式。
一般来讲,从分子中失去的电子应该是分子中束缚最弱的电子,如双键或叁键的π电子,杂原子上的非键电子。



高二物理质谱仪知识点物理中的“质谱仪”指的是通过对物质的成分及结构进行分析和鉴定的一种科学仪器。
在高二物理学习中,我们需要掌握质谱仪的原理、结构和应用等方面的知识。
接下来,本文将介绍高二物理中与质谱仪相关的一些重要知识点。
1. 质谱仪的基本原理质谱仪的基本原理是将待测物质离子化,然后利用电磁场对离子进行加速、选择、分离和检测。
主要包括四个步骤:离子化、加速、分离和检测。
2. 质谱仪的结构质谱仪的结构主要包括离子源、质量分析器和检测器。
离子源用于将待测物质转化为带电离子,质量分析器用于对离子进行分离,检测器用于检测分离后的离子。
3. 离子化方法常见的离子化方法有电离、化学离子化和热离子化等。
其中,电离是最常用的方法,包括电子轰击电离、化学电离和电喷雾等。
4. 质量分析器的种类常见的质量分析器有磁扇形质谱仪、四极杆质谱仪和飞行时间质谱仪等。
磁扇形质谱仪通过磁场和电场对离子进行分析和选择;四极杆质谱仪通过四个电极对离子进行加速和分离;飞行时间质谱仪利用离子在电场中的飞行时间与质量之间的关系进行分析和检测。
5. 检测器的种类常见的检测器有离子倍增器、电子倍增管和荧光屏等。
离子倍增器通过离子的碰撞和电子的发射来放大离子信号;电子倍增管通过电子的倍增来放大离子信号;荧光屏通过荧光触发和增强来检测离子信号。
6. 质谱图的分析质谱仪测量得到的结果以质谱图的形式呈现。
根据质谱图,我们可以分析和判断样品的组成成分、相对丰度以及结构等信息。
7. 质谱仪的应用质谱仪在科学研究、环境监测、食品安全、医药研发等领域具有广泛的应用。
例如,它可以用于鉴定和分析化合物的结构和组成,检测食品中的农药残留等。
通过学习以上关于质谱仪的知识点,我们可以了解质谱仪的基本原理和结构,掌握离子化方法、质量分析器和检测器的种类,学会解读质谱图和应用质谱仪进行实际分析。
这些知识将为我们将来的学习和科研提供基础和指导。
同时,质谱仪作为一种重要的分析仪器,对推动科学技术的发展和社会进步起着不可忽视的作用。
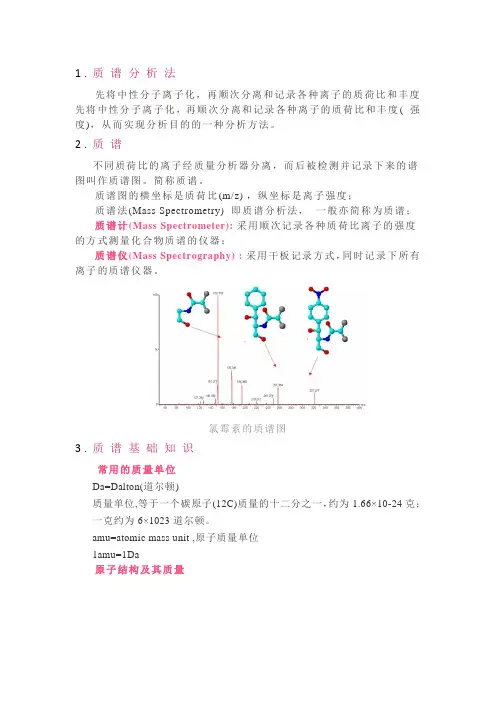
1.质谱分析法先将中性分子离子化,再顺次分离和记录各种离子的质荷比和丰度先将中性分子离子化,再顺次分离和记录各种离子的质荷比和丰度( 强度),从而实现分析目的的一种分析方法。
2.质谱不同质荷比的离子经质量分析器分离,而后被检测并记录下来的谱图叫作质谱图。
简称质谱。
质谱图的横坐标是质荷比(m/z) ,纵坐标是离子强度;质谱法(Mass Spectrometry) 即质谱分析法,一般亦简称为质谱;质谱计(Mass Spectrometer): 采用顺次记录各种质荷比离子的强度的方式测量化合物质谱的仪器;质谱仪(Mass Spectrography) :采用干板记录方式,同时记录下所有离子的质谱仪器。
氯霉素的质谱图3.质谱基础知识常用的质量单位Da=Dalton(道尔顿)质量单位,等于一个碳原子(12C)质量的十二分之一,约为1.66×10-24克;一克约为6×1023道尔顿。
amu=atomic mass unit ,原子质量单位1amu=1Da原子结构及其质量原子量* 国际协议赋予其确切的质量为12原子量(C) = 0.9889(12.0000) + 0.0111(13.0033)= 12.011一种元素的所有同位素的重量平均值叫作原子量同位素及同位素丰度同位素即具有相同的原子序数而又具有不同的质量数的原子叫作同位素。
同位素丰度即自然界中某同位素原子所占的百分数叫做该同位素的天然丰度。
同位素表示法质量数= 质子+ 中子具有相同的元素符号,在元素符号的左上角表明其质量数4.怎样计算质量数、分子量名义质量数采用元素质量数的整数进行计算,例如:C=12,H=1,O=16单同位素质量数或准确质量数用丰度最大的同位素准确质量数计算例如:12C=12,1H=1.0078,16O=15.9948平均质量数或化学质量数考虑到所有天然同位素丰度的该元素原子量来计算例如:C=12.001,H=1.00794,O=15.9994四极杆质谱获得的单电荷离子的m/z值,是单同位素质数,建议质谱峰标注到小数点后1位。

1、如何看质谱图(1)确定分子离子,即确定分子量:氮规则:含偶数个氮原子的分子,其质量数是偶数,含奇数个氮原子的分子,其质量数是奇数。
与高质量碎片离子有合理的质量差,凡质量差在3~8和10~13,21~25之间均不可能,则说明是碎片或杂质。
(2)确定元素组成,即确定分子式或碎片化学式:高分辨质谱可以由分子量直接计算出化合物的元素组成从而推出分子式,低分辨质谱利用元素的同位素丰度。
M-1,M-15,M-18,M-20,M-31......意味着失H,CH3,H2O,HF,OCH3......(3)峰强度与结构的关系,丰度大反映离子结构稳定:在元素周期表中自上而下,从右至左,杂原子外层未成键的电子越易被电离,容纳正电荷能力越强,含支链的地方易断。
2、离子源EI(Electron Impact Ionization):电子轰击电离—硬电离。
CI(Chemical Ionization):化学电离—核心是质子转移。
FD(Field Desorption):场解吸—目前基本被FAB取代。
FAB(Fast Atom Bombardment):快原子轰击—或者铯离子(LSIMS,液体二次离子质谱)。
ESI(Electrospray Ionization):电喷雾电离是最软的电离方式,采用离子蒸发,通常小分子得到[M+H]+]+,[M+Na]+或[M-H]-单电荷离子;化合物无需具有挥发性,离子在溶液中已生成;样品流速/min;适宜极性分子的分析,能分析小分子及大分子(如蛋白质分子多肽等),生物大分子产生多电荷离子,通常只产生分子离子峰,因此可直接测定混合物,并可测定热不稳定的极性化合物;通过调节离子源电压控制离子的碎裂(源内CID)测定化合物结构。
APCI(Atmospheric Pressure Chemical Ionization): 大气压化学电离也是软电离技术,高压放电发生了质子转移而生成[M+H]+或[M-H]-离子;化合物要具有挥发性且热稳定,离子在气态条件中生成;样品流速/min;只产生单电荷峰,适合测定质量数小于2000Da的弱极性的小分子化合物;适应高流量的梯度洗脱/高低水溶液变化的流动相;通过调节离子源电压控制离子的碎裂。


有机化学基础知识点质谱与有机化合物的分子结构鉴定质谱与有机化合物的分子结构鉴定有机化学是研究碳元素及其化合物的科学。
它以碳作为核心,研究有机物的结构、性质、合成以及反应机理等方面的知识。
而质谱则是有机化学中一种重要的分析手段,可以帮助科学家们揭示有机化合物的分子结构。
一、质谱的基本原理质谱法是利用物质离子在电场和磁场中做运动的性质来分析物质。
其基本原理可以分为以下几个步骤:1.样品的蒸发与电离首先,将待测样品进行蒸发,使其转变为气体态。
然后,在高能电子轰击下,样品分子中的原子或分子发生电离,形成正离子和电子。
2.正离子的分离与加速接下来,通过电场力和磁场力使正离子做加速和分离,使不同质荷比的离子被有效分离。
3.正离子的检测将正离子引入质谱仪器中,经过一系列的检测和测量,得到质谱图。
质谱图是以质荷比(m/z)为横坐标,离子相对丰度为纵坐标的图形。
二、质谱图的解读质谱图中的峰对应着不同质量荷比的离子,可以提供有机化合物的结构信息。
在解读质谱图时,需要注意以下几个重要的峰:1.基峰(base peak)质谱图上峰最高的峰被称为基峰,其离子相对丰度为100%。
其他峰的相对丰度则相对于基峰来表示。
2.分子离子峰(molecular ion peak)质谱图中,质荷比等于分子离子的离子峰被称为分子离子峰。
分子离子是在电子轰击下,原有物质分子中的一个电子被轰击后脱离的离子。
3.碎裂峰(fragmentation peak)质谱图中较低质荷比的峰被称为碎裂峰。
这些离子是由分子离子在质谱仪中的碰撞和解离过程中产生的。
三、质谱鉴定有机化合物的方法根据质谱图中的信息,可以进行有机化合物的分子结构鉴定。
一般来说,我们可以采取以下几个方面的方法:1.分子离子峰的鉴定根据分子离子峰的质荷比,可以初步确定分子式的质子数。
通过分子离子峰的丰度以及分子中不同原子的负质量,可以进一步推测分子式的组成。
2.碎裂峰的鉴定通过鉴定碎裂峰的质荷比和来源,可以推测有机分子中的键的裂解方式,从而推测有机化合物中各原子之间的连接方式。

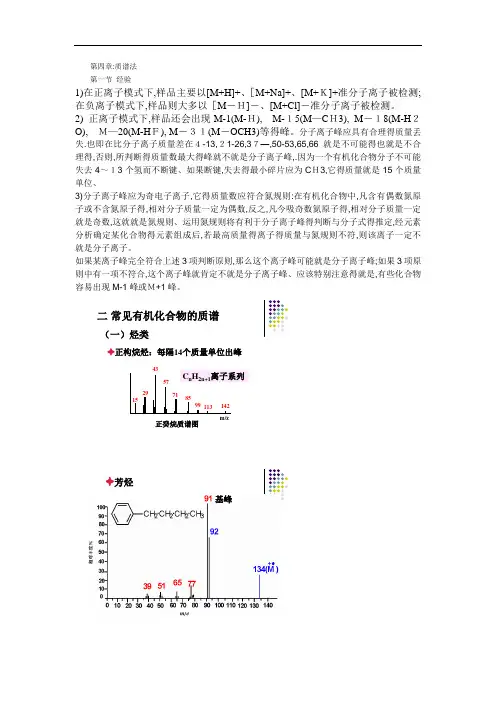
第四章:质谱法第一节经验1)在正离子模式下,样品主要以[M+H]+、[M+Na]+、[M+K]+准分子离子被检测;在负离子模式下,样品则大多以[M-H]-、[M+Cl]-准分子离子被检测。
2)正离子模式下,样品还会出现M-1(M-H), M-15(M-CH3), M-18(M-H2O), M-20(M-HF), M-31(M-OCH3)等的峰。
分子离子峰应具有合理的质量丢失.也即在比分子离子质量差在4-13,21-26,37-,50-53,65,66 是不可能的也是不合理的,否则,所判断的质量数最大的峰就不是分子离子峰,.因为一个有机化合物分子不可能失去4~13个氢而不断键.如果断键,失去的最小碎片应为CH3,它的质量是15个质量单位.3)分子离子峰应为奇电子离子,它的质量数应符合氮规则:在有机化合物中,凡含有偶数氮原子或不含氮原子的,相对分子质量一定为偶数,反之,凡今吸奇数氮原子的,相对分子质量一定是奇数,这就是氮规则。
运用氮规则将有利于分子离子峰的判断和分子式的推定,经元素分析确定某化合物的元素组成后,若最高质量的离子的质量与氮规则不符,则该离子一定不是分子离子。
如果某离子峰完全符合上述3项判断原则,那么这个离子峰可能是分子离子峰;如果3项原则中有一项不符合,这个离子峰就肯定不是分子离子峰.应该特别注意的是,有些化合物容易出现M-1峰或M+1峰。
基峰研究高质量端离子峰, 确定化合物中的取代基M-15(CH3); M-16(O, NH2M-17(OH, NH3); M-18(H2O);M-19(F); M-26(C2H2);M-27(HCN, C2H3); M-28(CO, C2HM-29(CHO, C2H5); M-30(NO);M-31(CH2OH, OCH3); M-32(S, CHM-35(Cl); M-42(CH2CO, CHM-43(CH3CO, C3H7); M-44(CO2, CS(.CH3) M-27(O) M-28第二节: 基本原理2.1基本原理质谱是唯一可以确定分子式的方法。

第四章:质谱法第一节经验1)在正离子模式下,样品主要以[M+H]+、[M+Na]+、[M+K]+准分子离子被检测;在负离子模式下,样品则大多以[M-H]-、[M+Cl]-准分子离子被检测。
2) 正离子模式下,样品还会出现M-1(M-H),M-15(M—CH3), M-18(M-H2O),M—20(M-HF), M-31(M-OCH3)等得峰。
分子离子峰应具有合理得质量丢失.也即在比分子离子质量差在4-13,21-26,37—,50-53,65,66 就是不可能得也就是不合理得,否则,所判断得质量数最大得峰就不就是分子离子峰,.因为一个有机化合物分子不可能失去4~13个氢而不断键、如果断键,失去得最小碎片应为CH3,它得质量就是15个质量单位、3)分子离子峰应为奇电子离子,它得质量数应符合氮规则:在有机化合物中,凡含有偶数氮原子或不含氮原子得,相对分子质量一定为偶数,反之,凡今吸奇数氮原子得,相对分子质量一定就是奇数,这就就是氮规则、运用氮规则将有利于分子离子峰得判断与分子式得推定,经元素分析确定某化合物得元素组成后,若最高质量得离子得质量与氮规则不符,则该离子一定不就是分子离子。
如果某离子峰完全符合上述3项判断原则,那么这个离子峰可能就是分子离子峰;如果3项原则中有一项不符合,这个离子峰就肯定不就是分子离子峰、应该特别注意得就是,有些化合物容易出现M-1峰或M+1峰。
基峰研究高质量端离子峰, 确定化合物中的取代基M-15(CH3); M-16(O, NH2M-17(OH, NH3); M-18(H2O);M-19(F); M-26(C2H2);M-27(HCN, C2H3); M-28(CO, C2HM-29(CHO, C2H5); M-30(NO);M-31(CH2OH, OCH3); M-32(S, CHM-35(Cl); M-42(CH2CO, CHM-43(CH3CO, C3H7); M-44(CO2, CS15 (。
第四章:质谱法第一节经验1)在正离子模式下,样品主要以[M+H]+、[M+Na]+、[M+K]+准分子离子被检测;在负离子模式下,样品则大多以[M-H]-、[M+Cl]-准分子离子被检测。
2)正离子模式下,样品还会出现M-1(M-H), M-15(M-CH3), M-18(M-H2O), M-20(M-HF), M-31(M-OCH3)等的峰。
分子离子峰应具有合理的质量丢失.也即在比分子离子质量差在4-13,21-26,37-,50-53,65,66 是不可能的也是不合理的,否则,所判断的质量数最大的峰就不是分子离子峰,.因为一个有机化合物分子不可能失去4~13个氢而不断键.如果断键,失去的最小碎片应为CH3,它的质量是15个质量单位.3)分子离子峰应为奇电子离子,它的质量数应符合氮规则:在有机化合物中,凡含有偶数氮原子或不含氮原子的,相对分子质量一定为偶数,反之,凡今吸奇数氮原子的,相对分子质量一定是奇数,这就是氮规则。
运用氮规则将有利于分子离子峰的判断和分子式的推定,经元素分析确定某化合物的元素组成后,若最高质量的离子的质量与氮规则不符,则该离子一定不是分子离子。
如果某离子峰完全符合上述3项判断原则,那么这个离子峰可能是分子离子峰;如果3项原则中有一项不符合,这个离子峰就肯定不是分子离子峰.应该特别注意的是,有些化合物容易出现M-1峰或M+1峰。
基峰研究高质量端离子峰, 确定化合物中的取代基M-15(CH3); M-16(O, NH2M-17(OH, NH3); M-18(H2O);M-19(F); M-26(C2H2);M-27(HCN, C2H3); M-28(CO, C2HM-29(CHO, C2H5); M-30(NO);M-31(CH2OH, OCH3); M-32(S, CHM-35(Cl); M-42(CH2CO, CHM-43(CH3CO, C3H7); M-44(CO2, CSM-15(.CH3)M-27第二节: 基本原理2.1基本原理质谱是唯一可以确定分子式的方法。
质谱基础知识汇总(精华版)质谱,即质量的谱图,物质的分子在高真空下,经物理作用或化学反应等途径形成带电粒子,某些带电粒子可进一步断裂,形成离子,质谱的离子可以质谱的核心内容,今天就和大家聊一聊质谱使用者都应该知道的离子。
质谱,物质的分子在高真空下,经物理作用或化学反应等途径形成带电粒子, 某些带电粒子可进一步断裂,形成离子,每一离子的质量与所带电荷的比称为质荷比(m/z,曾用m/e),不同质荷比的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对强度,由此得出的谱图称为质谱。
不同离子的概念1、分子离子分子被电子束轰击失去一个电子形成的离子称为分子离子。
分子离子用 M+表示。
分子离子是一个游离基离子。
在质谱图中与分子离子相对应的峰为分子离子峰。
分子离子峰的质荷比就是化合物的相对分子质量, 所以,用质谱法可测分子量。
2、同位素离子含有同位素的离子称为同位素离子。
在质谱图上,与同位素离子相对应的峰称为同位素离子峰。
3、碎片离子分子离子在电离室中进一步发生键断裂生成的离子称为碎片离子。
4、重排离子经重排裂解产生的离子称为重排离子。
其结构并非原来分子的结构单元。
在重排反应中,化学键的断裂和生成同时发生, 并丢失中性分子或碎片。
5、奇电子离子与偶电子离子具有未配对电子的离子为奇电子离子。
这样的离子同时也是自由基,具有较高的反应活性。
无未配对电子的离子为偶电子离子。
6、多电荷离子分子中带有不止一个电荷的离子称为多电荷离子。
当离子带有多电荷离子时,其质核比下降,因此可以利用常规的四极质量分析器来检测大分子量化合物。
7、亚稳离子从离子源出口到检测器之间产生的离子。
即在飞行过程中发生裂解的母离子。
由于母离子中途已经裂解生成某种离子和中性碎片,记录器中只能记录这种离子,也称这种离子为亚稳离子,由它形成的质谱峰为亚稳峰。
8、准分子离子比分子量多或少 1 质量单位的离子称为准分子离子,如:(M+H)+,(M-H)+。
质谱仪知识点质谱仪是根据物质原子中的电荷与其质量之比,而建立的一种分析技术。
用质谱仪来分析物质,称为质谱法。
质谱仪利用正负电荷相互吸引的特性使得各个原子上的电荷产生差异。
当带正电的质量增加时,则带负电荷也随之增加,而当电荷变化时,质量也随着改变,从而实现电荷的分离。
这样的分析方法叫做质谱法。
质谱仪主要由电子枪、分离器和离子源三部分组成。
电子枪产生的离子束轰击待测元素的原子核,形成带电粒子,并使之发生散射;电子经过质量分析器后,再将这些带电粒子进行收集。
经过电子的轰击,质量不同的原子被散射出来,按照不同的速度与方向,就可以分开带正电和带负电的两类不同的原子。
质谱仪分为二级质谱仪和四极质谱仪。
它们具有不同的能量和束流形式。
二级质谱仪是根据质量减小的原理工作的,只分离带正电的原子,因此所需的能量较低。
但是由于能量不足,会导致检测限低(约数十个分子)。
质谱仪用得最多的是二级质谱仪。
四极质谱仪利用样品中电子的不对称运动来实现电荷分离。
其检测限高,灵敏度高,分辨率好,重现性好,且不会造成分子干扰。
采用四极质谱仪分析样品的原理主要有三种:(1)电子从n电子空穴对(二级质谱仪)发射出来,如果电子携带一个正电荷,电子就被n电子中的一个电子捕获,这个电子会在质量分析器的一个电场作用下,围绕它自己的轴旋转一圈,并将这一事件记录下来。
如果电子携带的是负电荷,则会同样被一个电场吸引到质量分析器上,这个电场会将它周围的电子全部排斥掉,这样电子便落到质量分析器上。
(2)正离子从电子束发射出来,电子和正离子碰撞,在它们彼此达到平衡之前,电子不停地跟正离子碰撞,一旦碰撞结束,电子就沿着电场的反方向飞行。
质谱仪主要有六种检测器,它们分别是: (1)离子阱检测器, (2)正离子回旋扫描检测器,(3)电荷交换检测器,(4)光学离子检测器,(5)电子倍增器,(6)电子空穴对检测器。
质谱仪所用电子的能量大多在100--200eV,常用电压200v,可以进行痕量分析。
MS - 质谱入门了解质谱本入门指南覆盖了现代质谱实践相关的大部分主题,并解答了质谱使用和性能方面的一些常见问题。
文中还提供了便于深入学习相关文章的链接。
第一部门内容讨论谁使用质谱仪的问题,接着讲述化合物在离子源怎样被电离,以便于质谱仪分析。
然后通过对质量准确性和分辨率等重要主题的讨论,或我们怎样区分紧密相关化合物之间的差别,来讲述各种类型的质谱仪。
本指南涉及化学、样品制备和数据处理,以及当今最流行的MS应用中一些专业用语的定义。
谁要使用质谱?在考虑使用质谱仪(MS)之前,应当考虑您分析工作的类型、您预期获得的结果等:- 您分析的是像蛋白质、肽等大分子,还是获取水溶性小分子的数据?- 您在确定的水平寻找目标化合物,还是表征未知样品?- 针对复杂基质,您当前的分离技术抗干扰能力强吗,或者您必须开发新的方法?- 您要求单位质量精度(比如400 MW),或5 ppm的质量精度(比如,400.0125 MW或质量为400时准确度为2 mDa)?- 您必须每天处理几百个样品?上千个样品?上万个样品?Who Uses MS?图1:表征被测物特征的能力随质谱性能的增加而增强。
化学、生物化学和物理学领域的各学科和分支学科的研究人员和专业技术人员通常会用到质谱分析。
医药工业领域的工作人员在进行药物发现和药物开发时需要利用MS的特异性、动态范围及其灵敏度,区分复杂基质中紧密相关的代谢物,从而鉴定并量化代谢物。
尤其是在药物的开发过程中,药物需要进行鉴定、纯化,确定早期的药代动力学,MS已经证实是不可或缺的工具。
生物化学家扩展了MS的使用领域,将其应用到蛋白、肽和寡核苷酸的分析中。
使用质谱仪,生物化学家们能够监测酶的反应,确定氨基酸序列,并通过包含有蛋白裂解片段衍生物样品数据库鉴别大分子蛋白。
生物化学家通过氢-氘交换在生理条件下形成重要的蛋白-配体的复合物,监测蛋白质的折叠。
临床化学家在药物检测和新生儿筛查中也应用MS,取代结果不确定的免疫分析。
食品安全和环境研究人员也是这样。
他们跟行业中相关的企业工作人员一样,也使用MS,比如:PAH和PCB分析,水质量分析,及食品农药残留分析。
确定油组成是一项复杂且昂贵的工作,这刺激了早期质谱仪的发展,并不断推动该技术的继续创新。
现今,MS的专业人员可以在各种质谱仪、一系列完善可靠的电离技术中进行选择。
什么是质谱?质谱是怎样工作的?质谱仪可以比一枚硬币小,也可以装满非常大的房间。
虽然不同仪器类型有不同的应用,但是其工作原理相同。
测量单位为道尔顿(Da),代替其它单位,比如原子质量单位(amu)。
1 Da=单个碳12(12C)同位素原子质量的1/12。
以前认为质谱仪不具定量能力,仅能作为定性设备,辅助化合物的鉴定。
但现今,已经证实质谱兼具定性和定量功能。
只有分子转化为气相离子后,质谱仪才能测量其质量。
为了达到这一目的,质谱仪使分子带上电荷,然后将带电离子流转化为数据系统能够识别的成比例电流。
数据系统将这一电流转化为数字信息,得到质谱图。
图2:a)像色谱图形一样,当总离子电流随时间改变时,总离子电流(TIC)的丰度增加。
b)每个峰的数字部分表示此刻的离子,其构成了离子电流,离子电流通常被称为轮廓图或连续采集。
X或‘时间'轴为质荷比(m/z),在图谱中(比如同位素)能读出相邻离子的分辨率。
c)轮廓图谱通常缩减为‘棒状图,从每个峰的顶点降低质心,形成棒状图,从而减小存放文件的大小,有利于增加分辨信息。
对目标分析物,有很多适合的方式,使其电离成离子:1) 在平面上,激光激发溶解在基质中的化合物,比如基质辅助激光解吸离子化(MALDI)法。
2) 通过与带有能量的离子或电子的相互作用,比如电子轰击离子化(EI)。
3) 自身输送过程的一部分,像我们已熟知的电喷雾电离(ESI),在此种电离中,从液相色谱流出的洗脱液经高电压作用,从气溶胶中形成离子。
例子按照其质荷比(m/z),进行分离、检测而得到测量。
将相对离子流(信号)与m/z制图,得到质谱图。
小分子通常仅带单一电荷:因此m/z是质量与1的比值。
"1"表示在离子化过程中增加了一个质子(表示为M+H+,或如果丢失一个质子表示为M-H-),或如果丢失一个电子形成离子,被称为自由基正离子(M+)。
质谱仪的准确性,或质谱仪怎样测量实际真实的质量,可在本入门指南的后续章节中看到。
较大分子自身结构的多个位点可捕获电荷。
小肽通常能带2个电荷(M+2H+),而非常大的分子具有多个位点,可使用简单的算法,推断谱图中表示的离子质量。
图3:当准确校正后,低分辨率的质谱仪也可以得到非常准确的质量,但是因为较多的数据挤占了有限的分辨空间,因此不能提供更多的谱图信息。
常见的含有9个氨基酸的Brad ykinin多肽的代谢片段(BK1-5或Arg-Pro-Pro-Gly-Phe),ACE(血管紧缩素转化酶)用于扩张血管的抑制剂,可携带2个电荷(单个电荷或M+H的单同位素值为573.3149,而双电荷峰,或M+2H为287.1614)。
戴带双电荷的同位素峰,也会挤占有效的分辨空间。
能够分析的分子有多大?解吸电离(如在第22页所述)扩展了分析的能力,可分析分子量大、非挥发性、易碎的分子。
对分子量40,000Da的常规检测,其准确度可达0.01%,(即质量偏差在4Da)允许过程中发生较小变化的测定,比如蛋白质的翻译后修饰。
可带多个电荷扩展了质谱仪的测量范围,可以超越其设计的上限,可检测1000000Da或更大的质量。
同位素和元素的质谱仪天然同位素丰度已清楚的表征。
虽然通常认为丰度比较稳定,但是同位素丰度可能出现显著的特征性改变。
在代谢研究中,应用同位素比例测定(同位素丰富的元素作为示踪剂),在气候研究中,测量温度依赖性氧和碳的变化。
在实际中,使用高准确性的质谱仪,测量前,将复杂分子转化为简单分子化合物,这样转化后的化合物能通过扇形磁质谱仪检测。
元素分析通常针对无机材料,确定元素组成,而不是结构,在一些情况下,可分析固体金属样品。
常见于诱导偶合等离子体(ICP)源,放电器(或较低能量的发光放电)电离样品。
在万亿分之一(ppt)水平使用专用仪器检测较为常见。
常见的电离方法常见的电离方法电子离子化[EI]电子电离(EI)为很多人所熟知。
(在较早的时候称为"电子撞击",但是从技术上来说不准确。
) EI,通常将样品暴露在70eV的电子下,被称为"硬"技术。
电子与目标分子互作用的能量,通常要比分子的化学键要强的多,因此分子发生电离。
过量的能量按照特定方式打开化学键。
结果产生能够预见的、可鉴别的碎片,通过这些碎片,我们能够推测出分子结构。
这些能量可将单个电子激发,从分子外层逸出,形成正离子自由基,得到丰富的碎片波谱。
不同于"较软"的大气压电离技术,波谱响应会受到离子源设计特征的影响,EI技术完全独立于离子源的设计。
同一化合物在一台EI质谱仪产生的图谱与另一台EI质谱仪得到的图谱非常相似,基于这一原理,可建立图谱库,将未知化合物的谱图与参照谱图比较。
化学电离[CI]分子过度裂解的称为"软"技术。
化学电离(CI)通过一较温和的质子转移过程生成离子,有利于分子离子的生成。
将样品暴露到大量的溶剂气体,如甲烷形成质子化的分子离子(M+H)。
反向过程将形成负离子。
在一些情况下,质子被转移到气体分子上,形成负离子(M-H)。
采用EI分析时,碎片丰富的化合物,有时可采用CI分析,以增加分子离子的丰度。
类似于E I,样品必须具有热稳定性,因为在离子源里,被测物需要加热气化。
对起始电离步骤,CI 的电离机理依赖于EI,但是在离子源里是有高压化学反应气体,比如甲烷、异丁烷或氨。
比被测物(R)的浓度高很多反应气体通过电子电离作用,发生电离,起初产生R+t,溶剂离子。
R+离子与中性R分子发生碰撞,形成稳定的次级离子,其具有反应性,然后通过离子分子反应,使被分析物分子(A)离子化.负离子化学电离[NCI]对含捕获电子基团(例如,氟原子或硝基苄基)的被测物,能形成负离子化学电离(NCI)。
比EI的灵敏度提高了很多倍(据报道,在某种情况下可提高100到1000倍以上)。
NCI广泛应用于各种小分子,这些小分子通过或能够被化学修饰,促进电子捕获。
在负离子中,有两类主要的负离子形成机制:电子捕获和反应物离子化学离子化。
在CI条件下,电负分子能够捕获热电子,产生负离子。
实际上的负离子化学电离,通过被测化合物(AH)与带负电的反应离子(R-或R-)之间反应引起电离。
可能存在几类离子分子反应的类型,最常见的是脱质子反应。
气相色谱[GC]可能对很多人来说,第一次接触质谱是将其作为气相色谱的检测器。
GC/MS联用仪类型的范围已大大扩展,超越早期仪器设计的范围,在使用中满足日渐严格的法规要求,像环境分析、食品安全筛查、代谢组学,以及包括法医学、毒理学和药物筛查的临床应用。
在过去,两种类型的质谱主导着GC/MS分析:扇形磁场和单四极杆质谱仪。
对于前者,可提供高分辨率和准确的质量分析,用于有极高灵敏度要求的分析中。
后者适合目标化合物的常规分析。
[ 液相色谱]扇形磁场质谱仪,具有最具挑战的GC/MS分析能力:环境或工业样品中的二英,或竞技比赛中非法使用兴奋剂的筛查。
在扇形质谱仪上能够以飞克(fg)检测水平进行高分辨率或选择性的分析。
四极杆GC/MS系统推出不久,在目标分析应用中就已取得认可。
美国环境保护局(USEPA)要求对大量环境污染物样品采用四极杆GC/MS质谱仪分析。
因为这些分析应用的检测级别仅在皮克到纳克之间,相对于扇形磁场来说,四级杆磁场的灵敏度较低,但四极杆并没因此受到限制,相反,采用四级杆可大大降低成本,方便使用,并且便于携带。
液相色谱[LC]这是一项革命性的技术,为大约80%不能采用GC分析的化学物质提供了分析途径,在近几十年来促进了质谱技术的显著提高。
少数几个模型被挑出来(参见质谱‘简史'章节中的内容),开始实现MS与LC联用。
可以说LCMS联用开始于1970年代,在1990年代早期,我们今天所熟知的LCMS技术成熟起来。
很多现在我们使用的装置和技术都直接来自那个时候。
在1900年代早期,俄国植物学家Mikhail S.T swett定义了液相色谱技术。
他的研究工作主要是分离从植物萃取的叶色素,在他的研究中,他用溶剂冲洗装填微粒的柱子。
这是液相色谱最简单的形式,被测物溶解的溶液(流动相或浓缩相)与溶液流过的装填颗粒的床体(固定相)之间存在竞争作用,液相色谱就是依靠这种可预测、不断再现且具有很高精确性的相互作用实现分离。
近年来,在色谱柱中装填各种功能性组分,以及能够准确传送流动相的溶剂输送系统的发展,使得LC成为很多分析行业的支柱。