亲电加成
- 格式:ppt
- 大小:3.60 MB
- 文档页数:92

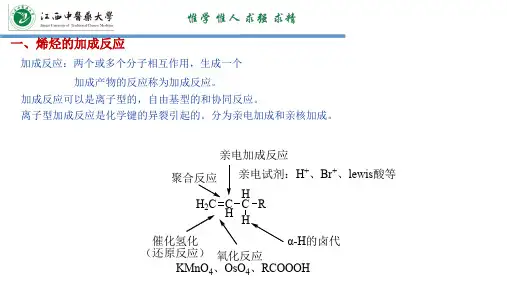



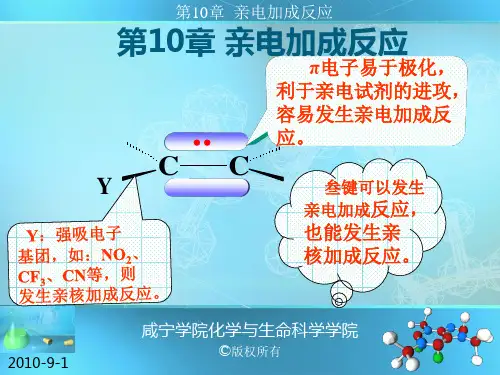





《有机化学反应类型》亲电加成实例有机化学反应类型——亲电加成实例在有机化学的广阔领域中,亲电加成反应是一类非常重要的反应类型。
亲电加成反应是指不饱和键(如双键或三键)的电子云密度较高,容易受到亲电试剂的进攻,从而发生加成反应。
接下来,让我们通过一些具体的实例来深入了解亲电加成反应。
首先,我们来看看乙烯与溴的加成反应。
乙烯分子中含有碳碳双键,双键上的电子云密度相对较高。
溴分子在接近乙烯时,会在一定条件下发生极化,形成溴正离子和溴负离子。
溴正离子作为亲电试剂进攻乙烯的双键,形成一个环状的溴鎓离子中间体。
随后,溴负离子进攻这个中间体,最终生成 1,2-二溴乙烷。
这个反应的化学方程式可以表示为:CH₂=CH₂+ Br₂ →CH₂BrCH₂Br从反应机理来看,亲电加成反应通常分为两步。
第一步是亲电试剂进攻不饱和键,形成一个不稳定的中间体;第二步是负离子或者其他亲核试剂进攻中间体,完成加成过程。
再比如,丙烯与氯化氢的加成反应。
丙烯分子中由于甲基的存在,双键上的电子云分布不均匀,导致双键的一端电子云密度相对较高,另一端相对较低。
当氯化氢接近丙烯时,氢离子(亲电试剂)会优先加到电子云密度较高的一端,形成 2-氯丙烷。
其反应式为:CH₃CH=CH₂+HCl → CH₃CHClCH₃这个例子展示了亲电加成反应的区域选择性,即亲电试剂在进攻不饱和键时,会倾向于加到电子云密度较高的位置。
另外,乙炔与水的加成反应也是一个典型的亲电加成实例。
在硫酸汞和稀硫酸的催化作用下,乙炔首先与水发生加成反应生成乙烯醇,但乙烯醇极不稳定,会迅速发生分子内重排,转化为乙醛。
反应过程可以表示为:CH≡CH + H₂O → CH₂=CHOH (不稳定)→ CH₃CHO这一反应不仅体现了亲电加成的特点,还涉及到了后续的分子内重排过程。
亲电加成反应在有机合成中具有广泛的应用。
例如,通过对烯烃的亲电加成,可以引入各种官能团,从而合成出具有特定结构和性质的有机化合物。
亲电加成反应的机理-回复亲电加成反应是有机化学中常用的一种反应类型,也是一种非常重要的反应。
它是指通过亲电试剂与底物发生加成反应,生成化合物中新的化学键。
在这篇文章中,我将详细介绍亲电加成反应的机理,从反应物的构型到产物的形成,一步一步回答。
首先,我们来讨论亲电试剂。
亲电试剂是一种具有正电荷或部分正电荷的化合物,通常有金属阳离子、卤素或含有电子亲和性较强的官能团等。
它们具有亲电子活性,可以与电子丰富的底物发生反应。
常见的亲电试剂有卤代烷、硫酸酐、酸酐、酢酸酐等。
接着,我们来看底物。
底物是指参与反应的有机化合物,其中有一个或多个具有电子富余的键。
这些键可以成为亲电试剂攻击的中心,从而形成新的化学键。
在亲电加成反应中,亲电试剂以“亲电子”的形式攻击底物中具有电子富余的键。
亲电试剂的正电荷会与底物中的负电荷形成电荷云重叠,从而产生共轭体系。
这种电荷云重叠有助于亲电试剂与底物之间的相互作用,并降低活化能,促进反应的进行。
然而,亲电加成反应并不是简单地将亲电试剂与底物中的电子富余键结合。
在反应中,还需要考虑到化学键的断裂和重组。
亲电试剂攻击底物中的电子富余键后,通常会导致一个中间产物的生成。
这个中间产物具有比反应物更高的能量,因为生成了一个新的化学键。
为了使反应更容易进行,并得到一个稳定的产物,通常会加入一个试剂作为辅助。
这个辅助试剂通常具有负电性,可以吸引亲电试剂上的正电荷。
这种吸引力可以促使亲电试剂更容易接近底物,并减少不利的电子间排斥作用。
例如,用碱金属盐类作为辅助试剂时,亲电试剂中正电荷将与负离子结合,形成一个离子对。
这个离子对可以提高亲电试剂的亲电性,并促进反应的进行。
在亲电加成反应中,中间产物通常是一个离子。
这个离子可以是正离子、负离子或离子对。
这取决于亲电试剂和底物的性质,以及辅助试剂的影响。
最后,我们来看产物的形成。
在亲电加成反应中,生成的产物是经过化学键的重新排列而得到的。
这种重新排列可以发生在中间产物中,也可以发生在反应结束后。