丙型肝炎病毒抗体诊断试剂盒
- 格式:doc
- 大小:30.00 KB
- 文档页数:1



丙肝抗体检测(胶体金法)原理丙肝抗体检测(胶体金法)原理一、背景知识丙型病毒性肝炎(HCV)是一种常见的慢性肝炎,也是世界范围内常见的肝病之一。
据统计,全球有约7000万人感染了丙型病毒,其中3万到5万人每年死于丙型肝炎相关疾病。
因此,对于丙型病毒的检测非常重要。
二、丙肝抗体检测(胶体金法)原理丙肝抗体检测是目前世界上常用的一种诊断丙型病毒感染的方法。
胶体金法(Colloidal gold assay)是一种免疫层析技术,也是一种常用的检测试剂盒。
该检测方法具有简单、快速、准确、可视、无需特殊设备等特点。
该方法利用金纳米颗粒在一定条件下可与形成抗原-抗体复合物沉淀形成聚集而呈现不同颜色的特性,对丙肝病毒感染有敏感性、特异性的检识能力。
三、具体步骤1.标本采集:采集病人的血清标本。
2.检测卡准备:将检测卡取出。
3.标本加样:用采集的血清标本滴在检测卡的标本孔内。
4.移液盒加入显色液:用移液器将显色液滴在检测卡的移液孔内。
5.结果判读:5-15分钟后可根据颜色反应标准,对试结果进行判读。
四、结果分析1.阴性:检测卡的检测线和对照线都呈现紫色。
2.弱阳性:检测卡的检测线和对照线都呈现紫色,但检测线有浅浅的黄色。
3.阳性:检测卡的检测线呈现浅浅的黄色,在检测线下方有一条紫色的线,同时对照线依旧有紫色。
五、结语丙肝抗体检测是一种特别重要的检测方法,也是诊断丙型病毒感染的一种主要方法。
而胶体金法,则是其中常用的一种检测方法,有效、简便、快速。
六、参考文献1. 王文生,刘志华. 胶体金技术及其在抗体检测中的应用[C]. 现代医学技术:中国医药科技出版社,1999,34-40。
2. 李永畅,徐妍. 胶体金法检测丙型病毒抗体的临床应用价值[J].中华医院感染学杂志,2009,5(12):1126-1128。

丙型肝炎病毒抗体的双抗原夹心检测方法的初步建
立的开题报告
1. 研究背景
丙型肝炎是由丙型肝炎病毒(HCV)引起的一种肝脏疾病,全球约
有7000万人患有慢性丙型肝炎。
早期发现和治疗至关重要,因为丙型肝炎会导致肝硬化、肝癌等严重后果。
目前,最常用的诊断方法是检测患
者血液中的丙型肝炎病毒抗体,但由于HCV存在多种亚型和变异株,部
分患者可能无法被准确诊断。
因此,建立一种敏感、特异和简便的检测
方法是非常必要的。
2. 研究目的
本研究旨在建立一种基于双抗原夹心法的丙型肝炎病毒抗体检测方法,以提高检测的准确性和灵敏度,同时简化检测流程。
3. 研究内容和方法
(1) 实验室制备丙型肝炎病毒抗体的检测试剂盒,包括对丙型肝炎病毒核心抗原的多克隆抗体和靶向丙型肝炎病毒E1/E2区的多克隆抗体。
(2) 收集正常人群和丙型肝炎患者的血液样本,进行单抗原夹心试验。
(3) 进行双抗原夹心试验,确定最佳的反应条件和检测灵敏度。
同时,检测多种丙型肝炎病毒亚型和变异株中的抗原。
(4) 与常规的单抗原夹心试验进行比较,评估该双抗原夹心试验的准确性和灵敏度。
4. 预期结果和意义
预计本研究能够成功建立一种双抗原夹心检测法用于丙型肝炎病毒
抗体的检测,该方法可提高检测的准确性和灵敏度,同时具有快速、简
便的优势。
本研究可为临床诊断和丙型肝炎的治疗提供有力支持。



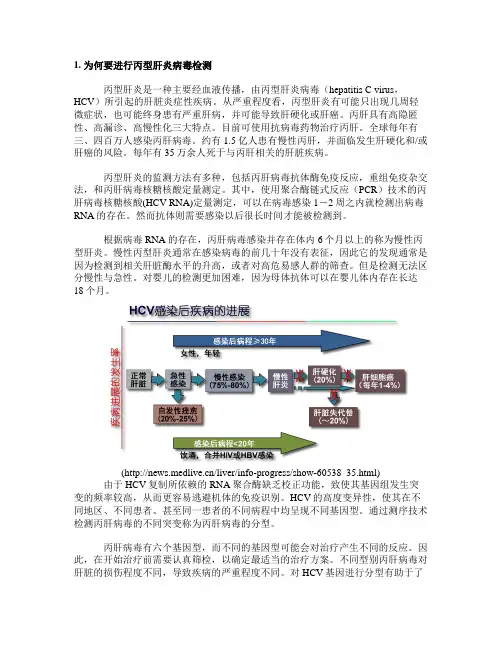
1. 为何要进行丙型肝炎病毒检测丙型肝炎是一种主要经血液传播,由丙型肝炎病毒(hepatitis C virus,HCV)所引起的肝脏炎症性疾病。
从严重程度看,丙型肝炎有可能只出现几周轻微症状,也可能终身患有严重肝病,并可能导致肝硬化或肝癌。
丙肝具有高隐匿性、高漏诊、高慢性化三大特点。
目前可使用抗病毒药物治疗丙肝。
全球每年有三、四百万人感染丙肝病毒。
约有1.5亿人患有慢性丙肝,并面临发生肝硬化和/或肝癌的风险。
每年有35万余人死于与丙肝相关的肝脏疾病。
丙型肝炎的监测方法有多种,包括丙肝病毒抗体酶免疫反应,重组免疫杂交法,和丙肝病毒核糖核酸定量测定。
其中,使用聚合酶链式反应(PCR)技术的丙肝病毒核糖核酸(HCV RNA)定量测定,可以在病毒感染1-2周之内就检测出病毒RNA的存在。
然而抗体则需要感染以后很长时间才能被检测到。
根据病毒RNA的存在,丙肝病毒感染并存在体内6个月以上的称为慢性丙型肝炎。
慢性丙型肝炎通常在感染病毒的前几十年没有表征,因此它的发现通常是因为检测到相关肝脏酶水平的升高,或者对高危易感人群的筛查。
但是检测无法区分慢性与急性。
对婴儿的检测更加困难,因为母体抗体可以在婴儿体内存在长达18个月。
(/liver/info-progress/show-60538_35.html) 由于HCV复制所依赖的RNA聚合酶缺乏校正功能,致使其基因组发生突变的频率较高,从而更容易逃避机体的免疫识别。
HCV的高度变异性,使其在不同地区、不同患者、甚至同一患者的不同病程中均呈现不同基因型。
通过测序技术检测丙肝病毒的不同突变称为丙肝病毒的分型。
丙肝病毒有六个基因型,而不同的基因型可能会对治疗产生不同的反应。
因此,在开始治疗前需要认真筛检,以确定最适当的治疗方案。
不同型别丙肝病毒对肝脏的损伤程度不同,导致疾病的严重程度不同。
对HCV基因进行分型有助于了解HCV感染的分布特征、变异及进化演变情况,有助于丙肝疫苗的研制。

论 著・ ・丙型肝炎患者的临床检验分析梁有娣1,梁玉金2(1.广州中医药大学附属中山中医院 检验科,广东 中山 528400;2.佛山市顺德区中医院检验科,广东 佛山 528333)摘要:目的 与临床经验相结合,探讨和研究丙型肝炎患者的有效检验方案。
方法 研究对象是1222例在2010年10月至2011年10月期间在我院检验丙型肝炎的患者,这些患者都采取常规抽取静脉血,将静脉血采取离心方式提取血清待用。
并且患者们要进行双向检验,两种检验分别是酶联免疫法检验和胶体金法,酶联免疫法即使用丙型肝炎病毒抗体诊断试剂盒检验,由中山生物有限公司生产;胶体金法检验即使用丙型肝炎病毒抗体诊断试剂盒检验,由英科新创科技有限公司生产。
检验结果出来后对以上两种方案的有效性进行判定。
结果 此次研究结论表明,通过这两种方案对丙型肝炎阳性率检验的χ2=1.03且P>0.05,由此判断两种方案的差异没有统计学意义,结论表明在临床检验上这两种方案都能使用,并且可以肯定其有效性。
结论 虽然两种方法的有效性都得到了肯定,但是胶体金法与酶联免疫法相比较,具有以下几个优良性质,即:便捷的操作、更短的时间、直观的观察、没有特殊设备作为辅助、价钱便宜有保障等等,并且能够测定单份丙型肝炎病毒,特别是在急诊和临床上的优势更加突出。
因此胶体金法是更加适合丙型肝炎病毒检验的方法,这种方法不但可以检验出早期的丙型肝炎,更可以对预防以及控制丙型肝炎有重要意义。
关键词:丙型肝炎;胶体金法;酶联免疫法;临床检验中图分类号:R 512.6 文献标识码:AClinical examination and analysis of patients with hepatitis CLIANG You-di1, LIANG Yu-jin2(1.Zhongshan Hospital of Traditional Chinese Medicine,Zhongshan,Guangdong 528400,P.R.China;2.Shunde District Hospital of Traditional Chinese Medicine,Foshan, Guangdong 528333,P.R.China) Abstract:【Objective】Combination of exploration and study of an effective inspection program for patients with hepatitis C and clinical experience. 【Methods】 Study of 1222 cases of patients with hepatitis C test in the hospital in the period from October 2010 to October 2011, these patients are taking conventional venous blood, venous blood by centrifugation to extract serum stand. And patients have to be bi-directional test, the two tests are the ELISA test and the colloidal gold method, Enzyme-linked immunosorbent assay, hepatitis C virus antibody test diagnostic kits, manufactured by Zhongshan Biotechnology Co., Ltd; Colloidal gold assay test that the use of the hepatitis C virus antibody test diagnostic kits, Science and Technology Co., Ltd. production InTec.【Resluts】The test results out to determine the validity of the above two programs. Results: The conclusions of this study show that both scenarios the positive rate of hepatitis C test χ 2 = 1.03 and P> 0.05 Judging from the two programs was not statistically significant, the conclusion that these two programs in clinical laboratorycan be used, and can be sure of its effectiveness. 【Conclusion】Although the effectiveness of the two methods have been affirmed, but the colloidal gold assay and enzyme-linked immunosorbent wears, with the following excellent properties, namely: the convenient operation, shorter period of time, visual observation, there is no special equipment as an auxiliarycheap security, etc., and be able to determine a single hepatitis C virus, in particular, is more prominent in the emergency department and clinical advantages. Colloidal gold method is more suitable for the hepatitis C virus testing methods, this method can not only test out early hepatitis C, but also of great significance for the prevention and control of hepatitis C.Key words:hepatitis C;colloidal gold method;elisa;clinical laboratory丙型肝炎或者丙肝(HC)是丙型病毒性肝炎的简称,丙型肝炎属于急性肝脏炎症,丙型肝炎病毒(HCV)通过血液传播是导致患上丙型肝炎的主要途径,也有个别患者是通过跟丙肝病人亲密接触后患病,丙型肝炎与乙型肝炎在临床上的表现有很多相同的地方。

雅培Real Time HCV 检测是一种应用体外聚合酶链反应(PCR)对丙型肝炎病毒(HCV)感染个体血浆或血细胞中HCV核酸DNA定量检测的方法,基于Abbott m2000 rt 实时荧光定量PCR平台,利用RT-PCR 原理定量检测人血清和血浆中HCV DNA。
独特的探针设计不但使检测具有极佳的检测性能,而且对各种亚型都有很好的检出率,对于病毒的突变也有很好的耐受性,雅培Real Time HCV 检测与感染者临床表现和其他实验室指标结合用于评估疾病预后,同时通过检测血浆或血清中HCV核酸水平的变化用于评估抗病毒治疗效果的辅助指标。
Abbott Real Time HCV临床分子诊断实验室对检测结果的可靠性提出很高的要求,尤其对于各种亚型的检出率,雅培Real Time HCV 能很好的满足临床分子诊断实验室的要求。
准确的定量依赖于独特的设计和创新引物设计:Real Time HCV 引物结合HCV 基因组5撇UTR区域探针设计探针设计:单直链探针循环条件:扩增延伸和荧光读取在不同的温度下进行,在较低的温度条件下结合探针读取荧光Real Time HCV探针设计单直链探针没有目标序列时探针两端随机缠绕,荧光基因结合萃灭基团,没有荧光目标序列存在时,探针优先结合目标序列,荧光基团远离萃灭基团发出荧光引物和探针设计:Real Time HCV探针设计HCV基因组5撇UTR区域临床分子诊断实验室对检测结果的可靠性提出很高的要求,尤其对于各种亚型的检出率。
Abbott Real Time HCV能很好的满足临床分子诊断实验室的要求。
Real Time HCV 引物结合于HCV基因组5撇UTR区域。
该区域是HCV特异性的高保守区域。
结合这个区域可以最大限度的减少各个亚型错配造成的漏检。
循环条件:扩增延伸和荧光读取在不同的温度下进行,在较低的温度条件下结合探针读取荧光低温条件下结合探针使得探针对错配具有耐受性,使检测具有更好的检出率雅培 Real Time HCV 性能灵敏度 12 IU/mL(0.5ml样本量); 30 IU/mL(0.2ml 样本量)线性范围 12 IU/ml 至10的8次幂 IU/mlSD值 SD小于0.1特异性大于等于99.5%适用亚型 1、2、3、4、5、6国际标准 WHO国际标准内部质控添加于裂解液中,质控整个实验操作流程Abbott Real Time HCV为HCV1-6亚型定量检测提供了高灵敏度、高特异性和宽线性范围的检测产品,满足您实验室的需要。
丙型肝炎抗体化学发光法丙型肝炎是由丙型肝炎病毒引起的肝炎,它是一种常见的肝病,主要通过血液传播。
丙型肝炎抗体化学发光法是目前临床上常用的检测方法之一,下面我们来详细介绍一下。
1.检测原理丙型肝炎抗体化学发光法是一种间接免疫荧光法,通过荧光信号检测样本中的丙型肝炎抗体。
检测时,将被检测的样本加入已经涂有丙型肝炎病毒(HCV)抗原的微孔板孔中,如果样本中存在丙型肝炎抗体,它将和孔中的抗原结合形成抗原-抗体复合物。
接着,将荧光标记的抗人类IgG抗体加入孔中,与抗原-抗体复合物发生结合,形成荧光信号。
最后,使用发光仪检测样本的荧光信号,根据荧光强度来判断是否存在丙型肝炎抗体,从而确定阳性或阴性结果。
2.适用范围丙型肝炎抗体化学发光法适用于检测人体血清和血浆中的丙型肝炎抗体,适用于肝炎病例的早期诊断、血液安全筛查及慢性丙型肝炎的治疗效果监测。
3.操作步骤①标本采集和处理:新鲜静脉全血或血浆样本进行分离和预处理。
②实验室仪器和试剂:普通实验室仪器,包括荧光孔板读板仪、自动化化学发光免疫分析仪等。
试剂包括微孔板、丙型肝炎抗体、荧光标记的抗人类IgG抗体等。
③操作流程:样本加入孔中→酶联免疫吸附反应→清洗→添加荧光标记的抗人类IgG抗体→显色检测→荧光检测。
4.结果判断丙型肝炎抗体化学发光法结果通过荧光测定来判断,荧光测定值越高,表明样本中丙型肝炎抗体的含量越高。
根据不同医疗机构或实验室的标准,阳性和阴性的荧光值解释也有所不同。
5.注意事项①标本应该及时送达实验室,存放时间不能过长。
②严格按照实验操作规范进行操作。
操作过程中,应保持实验区域清洁,避免污染。
③注意试剂的使用期限,过期试剂会影响结果准确性。
④操作过程中应注意眼、口、鼻的保护,避免直接接触检测物质。
丙肝抗体灰区报告一、引言丙肝抗体灰区的报告是指在丙肝抗体检测中,结果属于灰区范围的情况。
丙肝抗体是一种针对丙型肝炎病毒(HCV)感染的特异性抗体,可以帮助诊断和监测丙型肝炎的感染情况。
在丙肝抗体检测中,通常根据抗体阳性或阴性的结果来判断是否存在丙型肝炎感染,然而,当抗体检测结果处于灰区时,就需要进一步进行其他检测来确定感染状态。
本文将介绍丙肝抗体灰区报告的内容和解读方法,以帮助读者更好地理解和正确解读这类报告。
二、丙肝抗体灰区的定义丙肝抗体灰区是指在丙肝抗体检测中,结果介于阳性和阴性之间的范围。
通常,抗体检测的结果会根据某个特定的阈值来判断是否阳性或阴性,而灰区则表示检测结果未能明确地超出或低于这个阈值。
在这种情况下,就需要进一步的检测来确定是否存在丙型肝炎感染。
三、丙肝抗体灰区的解读方法1. 了解抗体灰区范围不同的丙肝抗体检测方法和试剂盒可能存在不同的抗体灰区范围,因此,在解读报告之前,首先应该了解所使用试剂盒的相关信息。
一般来说,试剂盒的说明书中会明确说明阳性和阴性的判断标准,同时也会提及灰区范围。
2. 考虑临床病史和相关检测结果对于抗体灰区的结果,建议综合考虑患者的临床病史和其他相关的检测结果,包括血清丙型肝炎病毒核心抗体(HCV-CoreAb)、病毒核酸检测(PCR法)等。
如果患者具有可能感染丙型肝炎的因素,如输血史、静脉注射史等,且其他检测结果提示可能存在感染,则有必要进一步确认感染状况。
3. 重复检测和动态监测如果初次检测结果处于丙肝抗体灰区范围内,建议进行重复检测。
有时候,灰区范围的结果可能是由于技术原因或其他干扰因素导致的假阳性或假阴性结果,重复检测可以排除这种可能性。
此外,对于已经明确感染丙型肝炎的患者,也需要进行动态监测,以及时评估感染的变化和疗效。
4. 咨询专业医生无论是初次报告还是重复检测后仍处于灰区的结果,如果对结果的解读存在疑问,建议及时咨询专业医生。
医生可以根据患者的具体情况提供专业的解释和建议,以确定是否需要进一步的检测和治疗措施。
丙型肝炎病毒(HCV)核酸定量检测标准操作规程(PCR-荧光探针法)1.目的:规范HCV-RNA(PCR)检测操作流程,保证检测结果的准确性。
2.应用范围:HCV-RNA荧光定量检测。
3.职责:3.1 文件编写:实验室技术员。
3.2 文件审核:实验室主管。
3.3 文件审批:实验室主任。
3.4 执行:PCR实验室所有工作人员。
4. 参考文献:4.1 中山大学达安基因股份有限公司丙型肝炎病毒核酸检测试剂盒(PCR-荧光探针法)说明书。
4.2 中山大学达安基因股份有限公司核酸扩增荧光检测系统DA7600型使用说明书。
5.内容:5.1 检测方法:PCR-荧光探针法5.2 实验原理:用一对丙型肝炎病毒特异性引物和一条丙型肝炎病毒特异性荧光探针,配以逆转录液、逆转录酶、PCR反应液、耐热DNA聚合酶(Taq 酶)、四种核苷酸单体(dNTPs)等成分,先将RNA逆转录成cDNA,再通过PCR体外扩增法,即高温变性、低温退火、适温延伸进行DNA扩增,并对PCR全过程进行实时监测,从而检测丙型肝炎病毒RNA。
主要用于HCV病毒感染的辅助诊断及其疗效监测的标准。
5.3 性能参数:5.3.1精密度:检测下限为1.0x103copies/ml。
5.3.2 线性范围:1.0x103~1.0x108copies/ml。
5.4 标本采集:5.4.1 使用标本类型:血清。
5.4.2 标本采集:由合作单位按照以下要求进行采集,采集后及时分离出血清在2~8℃条件下保存。
用一次性无菌注射器抽取受检者静脉血2ml,注入无菌的干燥玻璃管,室温(22~25℃)放置30~60 min,全血标本可自发完全凝集析出血清,或直接使用水平离心机,1500 rpm离心5min;吸取上层血清,转移至1.5ml灭菌离心管。
5.4.3 标本保存和运送:分离后的血清在2~8℃条件下保存应不超过72小时,-20℃可保存1个月,要长期保存的需分装后储存于-70℃。
不同ELISA试剂检测传染病四项弱反应性结果的比较目的对比进口和国产几种不同厂家品牌的试剂对HBsAg、抗-HCV、抗-HIV1/2、抗-TP传染病四项的检测结果,观察分析不同试剂对传染病四项检测弱反应性结果的差异。
方法2017年1—12月无偿献血者血液标本47 586份,应用不同全自动酶免分析仪进行ELISA 2次检测,并对除梅毒以外的167份弱反应性样本利用NAT检测技术进行确认。
结果47 586份样本中HBsAg弱反应性120份(伯乐71份;万泰49份);抗-HCV弱反应性20份(丽珠5份;万泰15份);抗-HIV1/2弱反应性27份(丽珠5;伯乐22);抗-TP弱反应性98份(丽珠41;万泰57),167份弱反应性样本NAT检测结果HBV DNA有反应性5份(其中伯乐3;万泰2);HCV RNA有反应性0份;HIV-1 RNA有反应性0份;梅毒螺旋体离体存活时间短不进行核酸检测。
结论不同试剂对传染病四项检测弱反应性结果存在差异,尽管存在假反应性结果的可能,但核酸检测发现仍有输血残余风险,单独使用都有可能存在漏检。
为了进一步提高临床输血安全水平,2次ELISA检测在血液筛查中仍有实际应用价值。
标签:ELISA;NAT;传染病四项;弱反应性;血液筛查酶联免疫吸附实验(ELISA)是将已知的抗原或抗体吸附在固相载体表面,使酶标记的抗原抗体反应在固相表面进行的技术[1-2]。
其方法简单,方便讯速,特异性强,目前仍广泛应用于医疗及采供血机构[3]。
国内绝大部分采供血机构对献血者筛查可经血传播感染的检测项目和方法的模式,仍主要以选择2个不同生产厂家的ELISA试剂检测为主,进行2次ELISA方法的血液筛查。
目前我国采供血机构已普遍开展NAT检测,血液筛查策略下一步可能有所改进。
为此,选取2017年1—12月无偿献血者血液标本47586份将不同ELISA试剂对传染病四项检测弱反应性结果进行了统计分析和比较,并利用NAT检测技术进行确认。
丙型肝炎病毒抗体诊断试剂盒(酶联免疫法)
说明书
96 人份试剂盒(可单分拆开)
国药准字 S10950041
本试剂盒采用EIA 法检测丙型肝炎抗体,适用于血清或血浆标本。所用抗原为合成多肽及基因工程抗原。具
有灵敏度高、特异性好、操作简便等优点。对肝炎的诊断、献血员的筛选等有重大意义。
【测定原理】
采用EIA 间接测定法,在预包被有丙肝抗原的反应孔内加入待测标本,若标本中有抗HCV,则可在微孔板
表面形成抗原-抗体复合体,再与酶标抗人IgG 结合,形成抗原-抗体-酶标抗体复合物,经显色系统显色后,根据
OD 值判定有无HCV 抗体的存在。
【使用方法】
1. 每次试验设阴性、阳性对照各两孔、分别加入阴、阳性对照血清100μl, 再设一孔空白对照, 加样品稀
释液100μ l。其余孔加入100μl 样品稀释液, 再加待测血清10μl。充分混匀后, 置37℃温育30 分钟。
弃去孔内样品,扣干。
2. 用洗涤液注满每孔(至少300μ l 洗涤液/孔),勿溢出,静置5 秒钟后扣干,重复5 次。
3. 每孔加酶结合物100μl( 空白对照孔除外),置37℃温育20 分钟,同上法洗反应板5 次。
4. 每孔加显色剂A 液、B 液各50μ l, 轻轻振荡后, 37℃避光静置10 分钟。
5. 每孔加入终止液50μ l 终止反应, 以空白调零, 在酶标仪中读取各孔OD450。
【结果判断】
1. 阳性对照平均值大于1.2,实验结果有效。
2. 实验设计要求阳性、阴性对照OD 值之差应大于1.2,否则本次实验无效。
3. 若阴性对照读数小于0.050 时,按0.050 计算。
4. 临界值(Cut off value)=阴性对照平均值+0.1。
5. 测试标本的计算值小于Cut off value 则为HCV 抗体阴性。
6. 测试标本的计算值等于或大于Cut off value 则为HCV 抗体阳性。
【注意事项】
1. 从冷藏环境中取出的试剂盒应置室温平衡20 分钟再进行测试。
2. 若洗涤液不够可自行配制。PH7.2 0.1MPBS-0.5%Tween20 。用前10 倍稀释成0.01M PBS-0.05%Tween20。
3. 本试剂盒中的样品稀释液采用变色技术,在加原始血清或血浆标本后由黄绿色变为篮紫色。非原始血清或
血浆(如稀释标本等)颜色变化不明显或变为其他颜色,为正常现象。
4. 不同批号试剂请勿通用。
5. 本试剂盒应视为有传染性物质,请按传染病实验室检查规程操作。