丙型肝炎病毒抗体诊断试剂盒(胶体金法)
- 格式:doc
- 大小:31.00 KB
- 文档页数:2

生猪的软脚不用愁入冬以来,不少农民朋友对我说,养的生猪先天还好,第二天在栏里就突然站不起来了,强迫起立,跛行严重,但食欲一般正常。
问这是什么原因?有什么办法治疗?生猪软脚,有多种情况,需根据病因对症治疗。
笔者根据临床观察总结,认为主要有如下3种疾病:生猪风湿症风湿症是生猪冬春季节的常见病。
饲养管理不良、猪舍潮湿、生猪长期受风寒侵袭或长期生活在潮湿环境中时,容易在受寒受潮、天气变冷之后突然发病。
肌肉风湿,触压患部肌肉疼痛,病猪表现痛苦尖叫。
四肢关节风湿,则患病关节肿胀、疼痛,起立行走困难,开始运步时,跛行明显;随着运动量增加,跛行症状减轻,跛行还可出现转移,有时在前肢,有时在后肢,或左右肢互相转移。
遇到这种情况,可采用如下方法治疗:①针刺百会、三台、七星、追风、寸子、大胯、涌泉、滴水等穴位。
②局部涂擦酒精、松节油或进行热敷;将酒糟炒热,装入布袋敷患部;或醋炒麦麸、糠壳,热敷患部。
③内服水杨酸钠与小苏打各2~3次,1日2次;或静脉注射水杨酸钠2克,1日1~2次。
④五加皮50克、银花藤120~180克煎水服,或鸡血藤150克煎水服,连用7~10天。
⑤当归15克,川芎10克,防风10克,荆芥10克,桂枝7克,独活10克,羌活10克,茴香10克,红花5克,乳香7克,没药7克,甘草5克,煎水后,候温加白酒30毫升内服,1日1刘,连服3~5剂。
以上剂量可根据病情及猪体大小适当增减。
母猪瘫痪母猪瘫痪常发生在产前及产后不久。
怀孕后期母猪对钙、磷等矿物质的需要量增加,后肢负担增大,母猪分娩后,大量血钙与血塘随乳汁排出。
这段时间,如果饲喂精料过多,而矿物质供应不足,容易发此病。
母猪年老体弱、缺乏运动、分娩过度紧张、产后大脑抑郁或受寒冷刺激,也可促进本病的发生。
母猪发病后,伏卧地上,后肢站立困难,强行起立,步态不稳,后躯摇摆,随着病情发展,最后完全不能起立。
病猪精神萎顿,反射减弱,食欲减少,体温略低,呼吸缓慢,甚至处于昏睡状态。



丙型肝炎病毒抗体(金标法)SOP【检验原理】本试剂使用包被HCV混合抗原和免疫HCV抗体包被在硝酸纤维素膜上作为检测线和质控线,另外用胶体金标记HCV混合抗原,应用免疫层析双抗原夹心法原理检测人血清中的HCV抗体。
当待检标本中含HCV 抗体时,该抗体与金标抗原形成”抗体-金标抗原复合物”,并在层析作用下向前移动,与包被抗原形成“抗原-抗体-金标抗原复合物”,出现一条肉眼可见的紫红色沉淀线(检测线,T),包被膜上还有一条控制反应过程的质控线(C),根据质控线是否出现判断检测是否有效:根据检测线是否出现,判断待测标本中是否含有HCV 抗体。
【主要组成成份】HCV混合抗原(固相金标物),包被HCV混合抗原(固相有检测线),免疫HCV抗体(质控线)。
【样本要求】取静脉血,静置使其自然收缩,离心得血清。
血清样本2-8°C冰箱存放最好不超过3天,若不能及时检测应-20°C冻存。
【检测方法】测试条把测试条和样本预先平衡至室温(20~30°C)。
在没有准备好之前,不可撕开铝箔袋,测试条打开包装后需在1小时内使用(湿度:20%~90%)。
1、打开铝箔袋,取出测试条,放在台面上。
2、用吸管加一滴(约25μL)样本于测试条指示箭头下端的加样处。
3、随即滴加2滴样本稀释液(约100μL)4、10~20分钟观察结果,20分钟后结果无效。
测试卡把测试卡和样本预先平衡至室温(20~30°C)。
在没有准备好之前,不可撕开铝箔袋,测试卡打开包装后需在1小时内使用(湿度:20%~90%)。
1、打开铝箔袋,取出测试卡,放在台面上。
2、用吸管加一滴(约25μL)样本于测试卡S孔内。
3、随即滴加2滴样本稀释液(约100μL)到测试卡上的D孔内。
4、10~20分钟观察结果,20分钟后结果无效。


医疗器械监督管理条例试卷一、填空题(每题2分,2分×10,共20分)1、(HCV)丙型肝炎病毒抗体检测试剂盒(胶体金法)国械注准20143401951 属于第类医疗器械.2、医用干式激光胶片(SD—S片)闽厦械备20150043属于第类医疗器械。
3、医疗器械产品应当符合医疗器械强制性标准;尚无强制性国家标准的,应当符合医疗器械强制性标准。
4、第一类医疗器械实行产品管理,第二类、第三类医疗器械实行产品管理。
5、医疗器械注册证有效期为年。
有效期届满需要延续注册的,应当在有效期届满前向原注册部门提出延续注册的申请。
6、具有高风险的医疗器械不得委托生产,具体目录由国务院食品药品监督管理部门制定、调整并公布。
7、提供虚假资料或者采取其他欺骗手段取得医疗器械注册证、医疗器械生产许可证、医疗器械经营许可证、广告批准文件等许可证件的,由原发证部门已经取得的许可证件,并处罚款,5年内不受理相关责任人及企业提出的医疗器械许可申请。
8、医疗器械经营许可证有效期为_______年.有效期届满需要延续的,依照有关行政许可的法律规定办理延续手续.9、从事医疗器械经营活动,应当有与经营规模和经营范围相适应的________和________,以及与经营的医疗器械相适应的质量管理制度和质量管理机构或者人员。
10、国家对医疗器械按照风险程度实行 .二、判断题(每题2分,2分×15,共30分 )1、第一类医疗器械产品备案,不需要进行临床试验( )2、任何单位以及个人不得伪造、变造、买卖、出租、出借《医疗器械经营许可证》和医疗器械经营备案凭证( )3、经营第一类医疗器械和第二类医疗器械都需要许可和备案()4、从事第三类医疗器械经营的,经营企业应当向省级食品药品监督管理部门提出申请许可证()5、医疗器械应当使用通用名称。
通用名称应当符合国务院食品药品监督管理部门制定的医疗器械命名规则()6、委托生产医疗器械,由委托方对所委托生产的医疗器械质量负责( )7、进口医疗器械没有中文说明书、中文标签或者说明书、标签不符合本条规定的,不得进口。


丙肝抗体检测(胶体金法)原理丙肝抗体检测(胶体金法)原理一、背景知识丙型病毒性肝炎(HCV)是一种常见的慢性肝炎,也是世界范围内常见的肝病之一。
据统计,全球有约7000万人感染了丙型病毒,其中3万到5万人每年死于丙型肝炎相关疾病。
因此,对于丙型病毒的检测非常重要。
二、丙肝抗体检测(胶体金法)原理丙肝抗体检测是目前世界上常用的一种诊断丙型病毒感染的方法。
胶体金法(Colloidal gold assay)是一种免疫层析技术,也是一种常用的检测试剂盒。
该检测方法具有简单、快速、准确、可视、无需特殊设备等特点。
该方法利用金纳米颗粒在一定条件下可与形成抗原-抗体复合物沉淀形成聚集而呈现不同颜色的特性,对丙肝病毒感染有敏感性、特异性的检识能力。
三、具体步骤1.标本采集:采集病人的血清标本。
2.检测卡准备:将检测卡取出。
3.标本加样:用采集的血清标本滴在检测卡的标本孔内。
4.移液盒加入显色液:用移液器将显色液滴在检测卡的移液孔内。
5.结果判读:5-15分钟后可根据颜色反应标准,对试结果进行判读。
四、结果分析1.阴性:检测卡的检测线和对照线都呈现紫色。
2.弱阳性:检测卡的检测线和对照线都呈现紫色,但检测线有浅浅的黄色。
3.阳性:检测卡的检测线呈现浅浅的黄色,在检测线下方有一条紫色的线,同时对照线依旧有紫色。
五、结语丙肝抗体检测是一种特别重要的检测方法,也是诊断丙型病毒感染的一种主要方法。
而胶体金法,则是其中常用的一种检测方法,有效、简便、快速。
六、参考文献1. 王文生,刘志华. 胶体金技术及其在抗体检测中的应用[C]. 现代医学技术:中国医药科技出版社,1999,34-40。
2. 李永畅,徐妍. 胶体金法检测丙型病毒抗体的临床应用价值[J].中华医院感染学杂志,2009,5(12):1126-1128。

传染病四项通常指的是乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)、人类免疫缺陷病毒(HIV)和梅毒螺旋体(Syphilis)的检测。
胶体金法是一种快速、简便的免疫层析检测方法,常用于临床实验室进行这些传染病的初筛检测。
以下是检验科进行传染病四项胶体金法标准操作程序的大致步骤:1. 准备阶段:确认胶体金试剂盒的有效期、批号,并按照说明书储存条件保存。
准备必要的器材,如移液器、测试板、计时器、记录表格等。
确保操作环境符合生物安全要求。
2. 样本采集:遵循相关的生物安全规程,采集患者的血液样本,通常为指尖血或静脉血。
确保采血器具的清洁和无菌。
3. 样本处理:根据胶体金试剂盒的说明书,将血液样本加入特定的试剂中,并按照规定的程序进行混合。
等待试剂反应规定的时长,通常为1520分钟。
4. 结果判读:在胶体金测试板上,根据对照线和测试线的出现情况判断结果。
通常,如果对照线和测试线同时出现,判定为阳性;只有对照线出现,判定为阴性;对照线不出,测试线出现,判定为无效,需要重新检测。
5. 结果记录和报告:记录检测结果,并填写检测报告。
如果检测结果为阳性,需要按照实验室规定进行复检,并采取相应的生物安全措施。
6. 废弃物处理:按照规定处理使用后的试剂、样本和废弃物,确保符合环保和生物安全要求。
7. 质量控制:定期进行质量控制检查,包括使用已知阴性和阳性的质控样本进行检测,确保检测系统的准确性。
请注意,以上步骤仅供参考,具体的操作程序应遵循实验室的标准操作规程和胶体金试剂盒的说明书。
操作过程中应严格遵守实验室安全规范,确保检测结果的准确性和安全性。
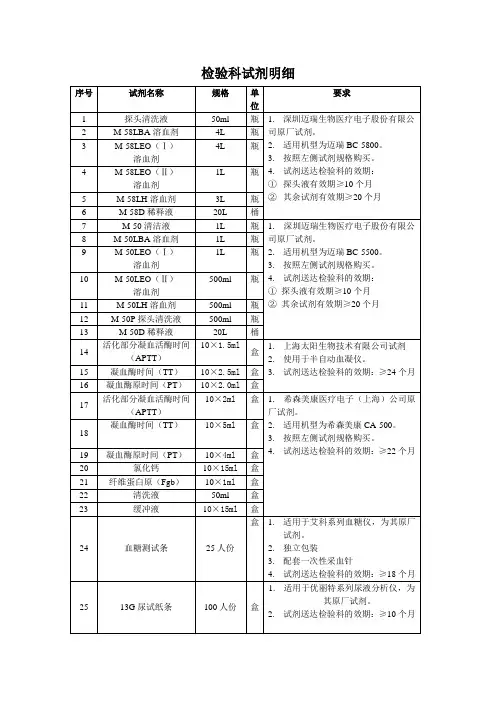
丙型肝炎病毒抗体检测试剂(胶体金法)说明书【产品名称】通用名称:丙型肝炎病毒抗体检测试剂(胶体金法)【包装规格】条型单人份:50人份/盒;板型单人份:40人份/盒。
【预期用途】本产品用于定性检测人血清.血浆样本中的丙型肝炎病毒(HCV)抗体。
丙型肝炎病毒是一种很小的.具有包膜的单股正链RNA病毒,是主要引起非肠道传播的非甲非乙型肝炎病毒,据文献报道,90%以上非肠道传播的非甲非乙型肝炎(NANBH)和25%以上急性散发性肝炎均为HCV感染所致,且35-50%的非甲非乙型肝炎发展为慢性肝炎,与肝癌的发生相关。
HCV主要传播通过血源传播,此外还可以其他方式如通过母婴垂直传播,家庭日常接触和性传播等。
【检验原理】本试剂采用高度特异性的抗体抗原反应原理及胶体金标记免疫层析分析技术,试剂含有被预先固定于膜上检测区(T)的包被用HCV重组抗原。
检测时,样本滴入试剂加样处于预包被的胶体金颗粒结合的标记用HCV重组抗原反应。
然后,混合物再毛细效应下向上层析。
如是阳性,标记用HCV重组抗原金标粒子在层析过程中先于样本中的HCV重组抗体结合,随后结合物会被固定在膜上的包被用HCV重组抗原结合,在检测区内(T)会出现一条紫红色条带。
这条带是包被用HCV重组抗原-HCV抗体-标记用HCV重组抗原金标粒子的复合物在膜上结合形成的。
如是阴性,则检测区内(T)将没有紫红色条带。
无论HCV抗体是否存在于样本血样中,一条紫红色条带都会出现在质控区内(C).质控区内(C)所显现的紫红色条带是判定是否有足够样本,层析过程是否正常的标准,同时也作为试剂内控标准。
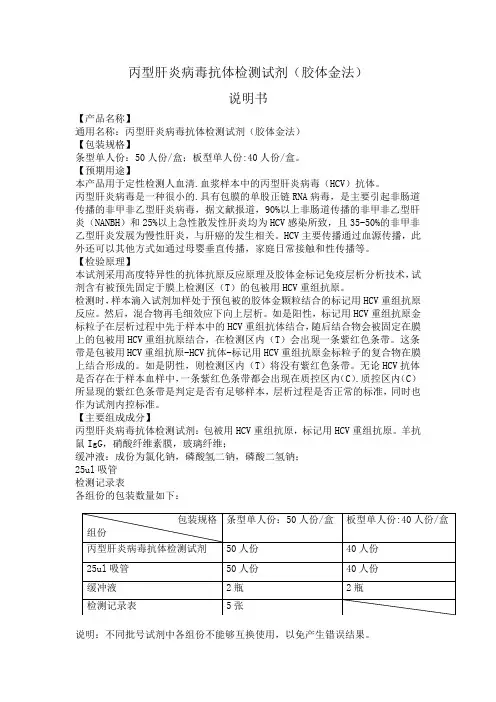
【主要组成成分】丙型肝炎病毒抗体检测试剂:包被用HCV重组抗原,标记用HCV重组抗原。
羊抗鼠IgG,硝酸纤维素膜,玻璃纤维;缓冲液:成份为氯化钠,磷酸氢二钠,磷酸二氢钠;25ul吸管检测记录表各组份的包装数量如下:说明:不同批号试剂中各组份不能够互换使用,以免产生错误结果。
检验时另需准备样本收集容器和计时器。
对比分析酶联免疫法和胶体金法检测病毒性丙型肝炎的效果丙型肝炎若不及时进行治疗,可逐渐发展为慢性疾病并向肝硬化发展,严重者可引起肝癌。
此类疾病可相互传染,因此,准确的检测尤为重要。
为了更加深入地研究酶联免疫法和胶体金法两种检测方法的临床效果,选择20xx年1月~20xx年3月进行丙型肝炎抗体检测的患者950例,现报告如下。
1 资料与方法1.1 一般资料:选择20xx年1月~20xx年3月在我院进行丙型肝炎抗体检测的患者950例,按其接受检测方法的不同分为对照组(470例)与试验组(480例)。
对照组男201例,女269例,年龄18~54岁,平均(35.717.1)岁。
试验组男204例,女276例,年龄19~55岁,平均(36.116.8)岁。
两组一般资料比较差异无统计学意义(P0.05),具有可比性。
1.2 方法:均在清晨抽取待检测者的空腹血液,进行离心分离出血清标本待检测。
给予对照组采用酶联免疫法进行检测:稀释酶复合物,加入血清孵育1 h,并进行洗板、加底物等操作,保持半小时的避光状态,使其充分反应后加入终止液停止反应。
给予试验组采用胶体金法进行检测:将病毒抗原和抗体分别固定在试剂条上的测试区和质控区,将血清加入试剂条中使其充分反应,15 min内判定结果,判定阴性阳性时注意不可混淆测试区和质控区。
1.3 判定标准:酶联免疫法阳性标准:标本A值大于等于Cut-off;阴性标准:标本A值小于Cut-off。
胶体金法阳性标准:测试区出现明显的紫红色条带;阴性标准:测试区没有明显的条带出现。
1.4 观察指标:观察比较两种检测方法的检测时间长短和检测成本情况。
1.5 统计学处理:使用SPSS 17.0对各项资料进行统计、分析,以P0.05为差异有统计学意义。
2 结果2.1 两种检测方法的准确性:对照组酶联免疫法检测出34例阳性,试验组胶体金法检测出50例阳性。
两组经过化学发光法确诊发现:试验组有55例为阳性,对照组有52例为阳性,试验组检测方法的准确率(90.91%)明显高于对照组检测方法的准确率(65.38%),差异有统计学意义(P0.05)。
检测项目:抗-HCV 温度(℃):25 湿度(%RH):43.3检测试剂:英科新创丙型肝炎病毒抗体诊断试剂盒(胶体金法)批号:20100741 有效期:20121003 地点:HIV实验室实验过程:1. 将待测标本从储存条件下取出,平衡至室温并编号,2. 将胶体金测试卡从包装盒中取出,打开铝箔包装袋,平置于台面上,3. 用塑料滴管加1滴样本血清或血浆,加到测试卡上的S孔,4.随即滴加2滴(约100ul)样本稀释液到测试卡上的D孔,5.加样后,阳性标本可在1至15分钟内检出,15分钟后再最终观察并记录实检测日期:检测项目:梅毒螺旋体抗体检测温度(℃):25 湿度(%RH):43.3 检测试剂:艾康生物梅毒螺旋体抗体检测试剂(胶体金法)批号:201008299/3 有效期:2012-07 地点:HIV实验室实验过程:1.使用前将试剂和标本恢复至室温(20℃-30℃),2.从原包装铝箔袋中取出试剂条,在1小时内尽快地使用,特别是温度高有于30℃或在高湿度条件下,3.将试剂置于干净平坦的台面上,用塑料吸管吸取全血/血清/血浆标本2滴,垂直滴加于加样区,然后再加入1滴缓冲液,4.等待紫红色带的出现,测试结果应在10至30分钟内读取,30分钟后判断检测日期:检测项目:HIV抗体温度(℃):25 湿度(%RH):50检验依据:《全国艾滋病检测技术规范(2009修订版)》检测试剂:丽珠人类免疫缺陷病毒(HIV)1+2型抗体诊断试剂盒批号:2010051312 有效期:20110518仪器设备:酶标仪/洗板机(1-001-2) 型号:MK3/MK2 地点:HIV实验室仪器状态:合格实验过程:1.取出样品血清和试剂盒,静置于操作台面30分钟,与室温充分平衡。
2.按照酶标仪设置的孔位,设置空白对照孔,其他孔内分别用移液器加入50μL阴性对照,阳性对照,外部对照血清和样品血清。
(加样前对血清进行各自均匀)3.封板,置于37±1℃培养箱内30分钟后,按试剂盒要求设置洗板程序,进行洗板。
丙型肝炎病毒抗体诊断试剂盒(胶体金法)
【临床意义】
定性测定人血清(浆)中的HCV抗体,用于无偿献血及临床术前的初筛查检测。
【实验原理】
丙型肝炎病毒抗体诊断试剂(胶体金法)采用胶体金免疫层析技术,在玻璃纤维素膜上预包被金标鼠抗人lgG抗体(anti-lgG Ab),在硝酸纤维素膜上检测线和对照线处分别包被丙肝混合抗原(Core、NS3、NS4、NS5)和人lgG抗体。
检测阳性样本时,血清样本中HCV-Ab 与胶体金标记鼠抗人lgG抗体结合形成复合物,由于层析作用复合物沿纸条向前移动,经过检测线时与预包被的抗原结合形成“Au-anti-lgG Ab-HCV Ab-HCV Ag”夹心物而凝聚显色,游离金标鼠抗人lgG抗体则在对照线处与人lgG抗体结合而富集显色。
阴性标本则仅在对照线处显色,15分钟内观察结果即可。
【主要组成成分】
1、HCV胶体金试纸条/试卡
2、说明书
3、样本稀释液
4、塑料滴管
【样本要求】
1、采集静脉血样本必须在无菌条件下操作,并避免样品溶血。
2、如果血清和血浆样品收集后7天内检测,样品须放在0-4℃保存;大于7天必须-20℃一下
冷冻保存。
3、常规抗凝剂不影响实验结果。
4、溶血、粘稠及高指标本不适于本试剂。
含特殊物质的标本可能会导致检测结果不稳定,
在检测前须清除。
5、在标本中加0.1%NaN3不影响实验结果。
【试验方法】
测试条:
1、将待测标本从储存条件下取出,平衡至室温并编号。
2、将胶体金试纸条从包装盒中取出,打开铝箔包装袋,平置于台面上。
3、用塑料滴管加1滴(10μl)样本血清或血浆,加到试纸条指示箭头下端的加样处。
4、随即滴加2滴样本稀释液(约100μl)。
5、加样后,阳性标本可在1~15分钟内检出,建议15分钟后在最终观察并记录实验结果。
测试卡:
1、将待测标本从储存条件下取出,平衡至室温并编号。
2、将胶体金测试卡从包装盒中取出,打开铝箔包装袋,平置于台面上。
3、用塑料滴管加1滴样本血清或血浆,加到测试卡上的S孔。
4、随即滴加2滴(约100μl)样本稀释液到测试卡上的D孔。
5、加样后,阳性标本可在1~15分钟内检出,建议15分钟后在最终观察并记录实验结果。
【结果判断】
阳性:试纸条/试卡在检测区和对照区位置出现两条紫红色条带。
阴性:试纸条/试卡只在对照线位置出现一条紫红色条带。
失效:对照区(C)未出现紫红色条带,表明不正确的操作过程或试剂盒已变质损坏。
在此情况下,应再次仔细阅读说明书,并用新的试纸条/试卡重新测试。
如果问题仍然存在,应立即停止使用此批号产品,并与当地供应商联系。
注意:测试区(T)内的紫红色条带可呈现颜色深浅的现象。
但是,在规定的观察时间内,不论该色带颜色深浅,即使只有非常弱的色带也应判定为阳性结果。
【该试验方法的局限性】
本法为初筛。
任何测定阳性结果都须用其他方法,例如EIA,进一步确认。
【产品性能指标】
符合《丙型肝炎病毒抗体诊断试剂(胶体金法)制造检定规程》要求。
【注意事项】
1、本试纸条/试卡仅用于体外诊断试验。
仅用于人血清或血浆,其他体液和样品可能得不到
准确的结果。
2、实验环境应保持一定湿度,避风。
避免在过高的温度下进行实验。
3、试剂从包装中取出后,应尽快进行实验,避免放置于空气中过长时间,导致受潮。
4、试剂可在室温下保存,谨防受潮。
低温下保存的试纸条应平衡至室温方可使用。
5、对于那些含有感染源和怀疑含有感染源的物质应有合适的生物安全保证程序,下列为有
关注意事项:
1)戴手套处理样品和试剂
2)不要用嘴吸样
3)不可再处理这些物品时吸烟、进食、喝饮料、美容和处理隐形眼镜
4)用消毒剂对溅出的样品或试剂进行消毒
5)按当地的有关条例来消毒和处理多有标本、试剂和现在的污染物
6)试剂各组份在正当处理和保存的情况下直至失效期都保持稳定,不能使用过效期的试剂盒
6、检测线颜色的深浅的程度与样品中的抗体的滴度没有一定的必然联系。
7、任何一种测试都不能绝对保证样品中没有低浓度的抗体存在,所以阴性结果任何时候不能排除含有HCV暴露和感染的可能。
8、本法为初筛。
任何测定阳性结果否须用其他方法,例如EIA,进一步确认。
9、实验证实,乙肝、HIV、甲肝、庚肝、戊肝、类风湿因子(RF)、红斑狼疮等各种类型的标本不会对测试产生干扰。
【包装、规格】
密封铝箔袋包装,每袋一人份。
【贮存】
2~30℃密封干燥处保存。
【医疗器械生产企业许可证编号】
闽食药管械生产许第20020068号
【医疗器械注册证书编号】
国食药监械(准)字2007第3401086号
【产品标准编号】
丙型肝炎病毒抗体诊断试剂(胶体金法)制造检定规程
【有效期】
24个月。
[医疗器械生产企业许可证编号]闽食药管械生产许第20050068号
[医疗器械注册证书编号]国食药监械(准)字2007第3401086号
[产品标准编号]丙型肝炎病毒抗体诊断试剂(胶体金法)制造检定规程。