人骨髓间充质干细胞的生物学特性分析
- 格式:pdf
- 大小:142.83 KB
- 文档页数:3



在复合成分培养基中骨髓间充质干细胞的诱导成骨徐丽丽;孙晓娟;郝秀仙;谢婷婷;杨乃龙【摘要】背景:研究显示骨质疏松多伴有成骨细胞的减少,成骨细胞替代疗法成为治疗骨质疏松症的新靶点。
目的:观察人骨髓间充质干细胞在含地塞米松、维生素C及β-甘油磷酸钠培养基中向成骨细胞分化的能力。
方法:采用人淋巴细胞分离液从成人骨髓血中分离纯化间充质干细胞,应用流式细胞仪检测其表面标志物的活性,透射电镜观察骨髓间充质干细胞的超微结构;将骨髓间充质干细胞在含有地塞米松、维生素 C 与β-甘油磷酸钠的成骨诱导培养基中诱导分化, RT-PCR检测骨髓间充质干细胞成骨诱导后骨形态发生蛋白2 mRNA的表达情况。
结果与结论:培养2周后可见细胞呈成纤维状生长,强表达 CD44,CD29,不表达 CD34,CD45,具有向成骨细胞诱导分化的潜能,茜素红及碱性磷酸酶染色阳性,骨形态发生蛋白2 mRNA表达阳性,说明人骨髓间充质干细胞在含地塞米松、维生素C及β-甘油磷酸钠培养基中可向成骨细胞诱导分化,具有治疗骨质疏松症的潜能。
%BACKGROUND:Studies have shown that the number of osteoblasts is often decreased after osteoporosis, and osteoblast replacement therapy becomes a new target for the treatment of osteoporosis. OBJECTIVE:To observe the osteogenic differentiation of human bone marrow mesenchymal stem cels cultured in dexamethasone, vitamin C and beta-glycerophosphate. METHODS:Mesenchymal stem cels were isolated and purified from adult bone marrow using human lymphocyte separation medium. The expression of cel surface markers was detected by flow cytometry. Cel ultrastructure was observed by transmission electron microscope. Then, the bone marrow mesenchymal stem cels were culturedin osteogenic induction medium containing dexamethasone, vitamin C andβ-glycerophosphate, and RT-PCR was used to detect the bone morphogenetic protein-2 mRNA expression after osteogenic induction. RESULTS AND CONCLUSION:A large number of adherent cels were visible as fibrous growth at 2 weeks after culture and strongly expressed CD44, CD29, but did not express CD34, CD45. These cels could be induced to differentiate into osteoblasts, and express bone morphogenetic protein-2 mRNA. Alizarin red staining and alkaline phosphatase staining were positive for the cels. These findings suggest that human bone marrow mesenchymal stem cels cultured in dexamethasone, vitamin C and beta-glycerophosphate can differentiate into osteoblasts, and has a potential for the treatment of osteoporosis.【期刊名称】《中国组织工程研究》【年(卷),期】2015(000)010【总页数】5页(P1501-1505)【关键词】干细胞;骨髓干细胞;人骨髓间充质干细胞;成骨细胞;诱导分化【作者】徐丽丽;孙晓娟;郝秀仙;谢婷婷;杨乃龙【作者单位】青岛大学医学院附属医院内分泌科,山东省青岛市 266003;青岛大学医学院附属医院内分泌科,山东省青岛市 266003;青岛大学医学院附属医院内分泌科,山东省青岛市 266003;青岛大学医学院附属医院内分泌科,山东省青岛市 266003;青岛大学医学院附属医院内分泌科,山东省青岛市 266003【正文语种】中文【中图分类】R394.2文章亮点:1 碱性磷酸酶是成骨细胞的标志性酶之一,也是成骨细胞活动的副产物,而且在体内的钙化中也起关键性作用,可以破坏钙化抑制剂,从而启动钙化。

骨髓间充质干细胞成骨分化的研究进展1. MSCs成骨分化途径的调控机制:多种信号通路参与了MSCs的成骨分化,特别是BMP (bone morphogenetic protein) 信号通路、Wnt/β-catenin 信号通路、TGF-β (transforming growth factor-beta) 信号通路等。
这些信号通路可以通过调控一系列关键性转录因子例如Runx2 (runt-related transcription factor 2)、Osx (osterix) 和Ocn (osteocalcin)等,来促进MSCs向成骨细胞分化。
2. MiRNA 调控MSCs成骨分化:近年来,研究发现MicroRNA (miRNA) 在调控MSCs成骨分化中起着重要作用。
例如,miR-2861 可以通过靶向抑制MEKK2 (mitogen-activated protein kinase kinase kinase 2) 来促进MSCs的成骨分化。
此外,miR-125b 可以通过调控Smurf1 (SMAD specific E3 ubiquitin protein ligase 1) 表达来抑制MSCs的成骨分化。
3.MSCs与激素调控成骨分化:激素对于MSCs的成骨分化也具有重要影响。
例如,雌激素通过与雌激素受体结合,可以促进MSCs向成骨细胞分化,并抑制骨吸收。
此外,研究还发现糖皮质激素会抑制MSCs成骨分化并诱导MSCs向脂肪分化。
4. MSCs与骨组织工程:越来越多的研究开始将MSCs应用于骨组织工程中,通过将MSCs和多种生物材料结合,可以制造出用于骨缺损修复的生物人工骨。
例如,Makino等人成功地利用MSCs和羟基磷灰石(HA)复合材料构建了能够促进骨骼再生的生物人工骨。
此外,MSCs与多肽纳米材料的结合也显示出了巨大的应用潜力。
5.MSCs与骨性疾病的治疗:由于MSCs具有分化为成骨细胞的潜能,并能产生一系列促进骨骼再生的细胞因子,因此MSCs也被广泛应用于骨性疾病的治疗。

DB32/T3544-2019临床级人体组织来源间充质干细胞质量控制管理规范1范围本标准规定了临床级人体组织来源间充质干细胞制备的基本要求、操作规范和质量控制。
本标准适用于临床级人体组织来源间充质干细胞的样本采集、制备、冻存、复苏与质量控制。
2规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB3095环境空气质量标准GB19489-2008实验室生物安全通用要求GB50073-2001洁净厂房设计规范GB50346实验室建筑技术规范GB50591洁净室施工及验收规范WHO实验室生物安全手册(第三版)药品生产质量管理规范(卫生部令第79号)中华人民共和国药典(2015年版)干细胞制剂质量控制及临床前研究指导原则(试行)(国卫办科教发﹝2015〕46号)T11/CSSCR001-2017干细胞通用要求(中国细胞生物学学会-干细胞生物学分会团体标准)3术语和定义下列术语和定义适用于本标准。
3.1临床级人间充质干细胞clinical grade human mesenchymal stem cells符合质量要求,可用于临床研究和应用的人多种组织来源(脐带血、脐带、胎盘、子宫内膜、脂肪、牙齿、骨髓等组织)间充质干细胞。
3.2伦理审查委员会ethical review committee负责对科学研究中涉及的伦理道德问题进行评估和审查的专门组织。
3.3科学审查委员会scientific review committeeDB32/T3544-2019负责对生物样本采集和使用的方案进行科学性审查的专门组织。
3.4生物安全委员会institutional biosafety committee负责制定生物安全政策和安全操作规范的专门组织。
3.5知情同意informed consent具有完全民事行为能力的自然人在重复获取信息并准确理解其内容后,作出接受或不接受样本采集的决定,此决定不受恐吓、利诱或其他不当行为的影响。

骨髓间充质干细胞在Matrigel凝胶支架上的生长与变化张斌斌;高全文;李冰;黄沙;姚斌【摘要】背景:研究表明,Matrigel 作为一种细胞外基质复合物加入到细胞培养体系中,对细胞的增殖、分化、胶原分泌具有促进作用.目的:建立Matrigel复合骨髓间充质干细胞的三维培养模型,观察Matrigel三维培养条件下骨髓间充质干细胞的形态、增殖及存活情况.方法:全骨髓贴壁法分离培养骨髓间充质干细胞,进行成骨、成脂诱导鉴定;CCK-8测定第3代骨髓间充质干细胞的生长曲线;选取生长状态良好的第2代骨髓间充质干细胞,与Matrigel混合形成细胞凝胶复合物,采用相差显微镜和苏木精-伊红染色观察骨髓间充质干细胞的形态及增殖情况,Live/Dead染色评价细胞活性.结果与结论:①全骨髓贴壁法分离培养的比格犬骨髓间充质干细胞具备向成骨、成脂细胞分化的能力;②骨髓间充质干细胞的生长曲线呈 S 形,符合正常细胞的生长特性;③相差显微镜下可见骨髓间充质干细胞在Matrigel中逐渐伸长相互交联,呈三维网状生长,增殖状态良好,随着时间延长(7 d后),基质胶逐渐变软塌陷, 14 d时仍可见少部分细胞网状交联生长;苏木精-伊红染色可见第4天时细胞胞质较大,第7天时细胞细长、相互交联;④三维培养第1,4,7天,骨髓间充质干细胞在Matrigel中活性百分比分别为92.57%,95.54%,97.37%,呈逐渐升高趋势;⑤结果表明,骨髓间充质干细胞在Matrigel中的增殖能力较强,活性较高.%BACKGROUND: Matrigel as an extracellular matrix complex can facilitate cell proliferation, differentiation and collagen secretion in a cell culture system. OBJECTIVE: To establish a three-dimensional culture model of Matrigel combined with bone marrow mesenchymal stem cells (BMSCs) and to observe the morphology, proliferation and survival of BMSCs in the Matrigel three-dimensional culture model. METHODS: BMSCs were isolated and culturedby the whole bone marrow adherent method, followed by osteogenic and adipogenic induction and identification. The growth curve of passage 3 BMSCs was determined through the CCK-8 experiment. Passage 2 BMSCs were combined with Matrigel, and the morphology and proliferation of BMSCs were observed by hematoxylin-eosin staining under a phase contrast microscope. The viability of the cells was evaluated by theLive/Dead staining. RESULTS AND CONCLUSION: (1) BMSCs cultured bythe whole bone marrow adherent method had the ability to differentiate into osteoblasts and adipocytes. (2) BMSCs exhibited an "S"-shaped growth curve, which was consistent with the growth characteristics of normal cells. (3) Under the phase contrast microscope, BMSCs cultured by the Matrigel model were extended and interconnected in a three-dimensional network growth state with good proliferation. The Matrigel gradually became soft and collapsed over time (7days) and a few cellswere still in a network growth after 14 days. Hematoxylin-eosin staining results showed that the cell cytoplasm was larger at 4 days and the cells became thinned and mutually cross-linked at 7 days. (4) The active percentage of BMSCs in the Matrigel model was 92.57%, 95.54% and 97.37% at 1, 4, 7 days of culture, respectively. To conclude, BMSCs cultured on the Matrigel has good proliferation and high viability.【期刊名称】《中国组织工程研究》【年(卷),期】2018(022)013【总页数】6页(P1993-1998)【关键词】干细胞;骨髓间充质干细胞;三维培养;Matrigel;细胞增殖;细胞活性;北京市自然科学基金【作者】张斌斌;高全文;李冰;黄沙;姚斌【作者单位】山西医科大学口腔医学系,山西省太原市 030001;解放军总医院第一附属医院烧伤整形科,北京市 100048;山西医科大学口腔医院,山西省太原市030001;解放军总医院基础医学研究所,北京市 100853;解放军总医院基础医学研究所,北京市 100853【正文语种】中文【中图分类】R394.20 引言 Introduction组织工程是应用细胞生物学和工程学的原理,培养出新的具有特定功能和形态的组织器官,达到修复组织器官和重建功能的目的[1-2]。

间充质干细胞成脂成骨分化实验方法学开发思路和流程干细胞是一种具有自我更新能力和多潜能分化的细胞,可以分化成为各种类型的细胞,包括脂肪细胞和骨细胞。
间充质干细胞(MSCs)是一种重要的干细胞类型,它们存在于各种组织中,如骨髓、脂肪组织和胎盘组织等。
间充质干细胞成脂成骨分化的实验方法学开发,是生物医学研究中一个重要的课题。
本文将从方法学开发的思路和流程入手,对间充质干细胞成脂成骨分化实验方法学进行探讨。
一、研究背景间充质干细胞成脂成骨分化是指间充质干细胞在一定的诱导条件下分化为脂肪细胞或骨细胞的过程,这一过程在细胞生物学和再生医学领域具有重要意义。
成脂成骨分化的研究有助于深入了解骨质疏松症、骨折愈合和脂肪代谢等疾病的发病机制,同时也为干细胞治疗提供了理论基础。
因此,开发一套可靠的实验方法学对于间充质干细胞成脂成骨分化研究至关重要。
1.确定分化诱导条件间充质干细胞在体外培养时,可通过添加不同的生长因子、细胞因子或药物来诱导其分化为脂肪细胞或骨细胞。
因此,确定最佳的分化诱导条件是方法学开发的第一步。
此过程需要考虑到诱导因子的种类、浓度、培养时间等因素,以及不同来源的间充质干细胞在分化过程中的差异性。
2.确定评价指标分化过程中,需要通过一系列的生物化学和分子生物学方法来评价间充质干细胞的脂肪细胞或骨细胞特征。
这些评价指标包括脂肪细胞的油红O染色、脂肪球形成实验,以及骨细胞的矿化实验、ALP染色等。
确定合适的评价指标对于评估分化效果至关重要。
3.确定实验方案在确定了分化诱导条件和评价指标后,需要制定详细的实验方案。
包括细胞的处理方法、诱导条件的优化、实验的时间节点等,以便后续实验的顺利进行。
1.间充质干细胞的提取和培养首先需要从适当的组织中分离和提取间充质干细胞,并进行细胞培养。
这一步需要注意细胞的纯度和活性,以保证后续实验的准确性。
2.分化诱导实验将培养好的间充质干细胞分别进行脂肪和骨分化诱导实验,根据预先确定的诱导条件进行处理。

骨髓间充质干细胞(BMSCs)的分离培养鉴定方法主要包括以下步骤:**一、分离方法**1. **差速贴壁法**:利用BMSCs与骨髓中其他细胞的贴壁性能差异及酶消化敏感性差异进行分离。
这种方法快速、简单、经济,但细胞纯度可能相对较低。
2. **密度梯度离心法**:基于骨髓中不同细胞的大小和密度差异进行分选。
通过流式细胞术检测,细胞表面抗原表达CD105,CD73和CD90必须≥95%,同时表达CD45、CD34、CD14或CD11b、CD79α,或CD19和HLA - DR必须≤2%。
**二、培养方法**培养BMSCs的难点在于保持细胞活性。
不同种属来源的BMSCs在体外培养扩增方法基本相似,但细微的营养条件、培养环境等差异都将会对细胞性能产生影响。
**三、鉴定方法**1. **细胞形态学观察**:利用组织块贴壁法、酶消化法或其结合来分离MSC,并通过传代培养进行形态学观察。
几乎所有的MSC都是贴壁生长,具有较强的贴壁能力。
MSC多数呈纤维细胞样生长,少量呈梭形或不规则三角形。
2. **表面标志物鉴定**:采用流式细胞仪对MSC的细胞表型进行鉴定。
MSC的表面抗原具有非专一性,可以同时表达间质细胞、内皮细胞和表皮细胞的表面标志,如粘附因子、生长因子和细胞因子受体以及整合素家族等。
MSC的细胞表面标志物鉴定标准为:CD105、CD73和CD90的阳性率≥90%;而CD45、CD34、CD14、CD19和HLA-DR 呈阴性,阳性率≤5%。
综上所述,骨髓间充质干细胞的分离、培养和鉴定是一个复杂的过程,涉及多个步骤和专业的技术操作。
在进行这些操作时,需要严格遵守实验规程,确保实验的准确性和安全性。
同时,对实验结果的解读也需要具备一定的专业知识和技能。

miRNAs对骨髓间充质干细胞分化的影响共3篇miRNAs对骨髓间充质干细胞分化的影响1miRNAs对骨髓间充质干细胞分化的影响随着生物技术和分子生物学技术的不断发展,科学家们开始深入研究微小RNA(miRNA)在生物体内的作用机制,尤其是在干细胞分化过程中的重要作用。
骨髓间充质干细胞(BMSCs)是一类广泛应用于细胞治疗和组织工程的干细胞类型,也是研究miRNAs作用机制的重要研究对象之一。
本文将从miRNAs在骨髓间充质干细胞分化中的作用入手,探讨其影响及机制。
miRNAs是一类长度为20-25个碱基的小分子RNA,在细胞内发挥着调控基因表达的重要作用。
miRNAs通过与靶基因的3'未翻译区相结合,并抑制靶基因的转录和翻译,从而调控基因表达。
在BMSCs的分化过程中,miRNAs发挥着调节器的作用,可以促进或抑制干细胞的分化过程。
近年来的研究表明,miRNAs在BMSCs分化过程中的作用是复杂的。
miR-125b和miR-146系列miRNAs在BMSCs的分化中起着正向调节作用,可以促进细胞向骨细胞和软骨细胞分化。
miR-21和miR-34系列miRNAs则起着负向调节作用,可以抑制BMSCs分化为成骨细胞。
miR-29系列miRNAs在细胞外基质(ECM)的形成和骨细胞成熟过程中发挥着重要作用。
除此之外,还有一些miRNAs被发现与多种信号途径相互作用,参与了BMSCs分化的调控。
例如,miR-10系列miRNAs通过调节HOXA1和WNT信号通路等基因的表达,既可以促进BMSCs向软骨细胞分化,也可以抑制BMSCs向骨细胞分化。
同时,miR-145和miR-221等miRNAs也通过作用于TGF-β和PI3K/Akt通路等因子的表达,参与了BMSCs的分化和增殖。
此外,miRNAs在BMSCs分化中还涉及到多种相互作用和调节机制。
比如,miRNAs和转录因子相互作用,共同调控干细胞分化。

人骨髓间充质干细胞提取方法
人骨髓间充质干细胞(BM-MSCs)的提取方法主要有以下几种:
1. 离心沉积法:通过采集骨髓样本后,使用离心机进行离心,将骨髓中的红白细胞分离,并将沉积在离心管底部的间充质干细胞收集。
2. 粘附法:将骨髓样本放入培养皿中,使细胞在培养皿内粘附并扩增,再通过培养基的更换来去除非粘附的细胞,最终收集纯化的间充质干细胞。
3. 感应细胞培养法:将骨髓样本中的间充质细胞进行体外培养,通过特定的培养基和生长因子的添加,促使间充质细胞分化为间充质干细胞。
4. 密度梯度离心法:通过将骨髓样本在密度梯度离心离心离心,将不同密度的细胞分离,并收集到含有骨髓间充质干细胞的层。
这些方法都可以用于提取人骨髓间充质干细胞,具体选择哪种方法取决于具体实验需求和实验室条件。
骨髓间充质干细胞对衰老模型大鼠肺损伤的修复作用王志红;陈为民;曲双;郭坤元【摘要】BACKGROUND:Studies have shown that exogenous bone marrow mesenchymal stem cells can settle down in lung tissue, participate in long regeneration, but few studies concerned the repair of aging lung injury. OBJECTIVE:To observe the effect of bone marrow mesenchymal stem cells on lung injury induced by D-galactose. METHODS:A total of 30 Sprague-Dawley rats were equal y divided into three groups at random:control group, aging model group and celltreatment group. To establish the aging rats, 10 rats each in the aging model group and celltreatment group were daily subcutaneously injected with D-galactose for 4 months. 3×106 bone marrow mesenchymal stem cells were transplanted via caudal vein in the celltreatment group, once a week, for 4 weeks. cellmedium of equal dose was added in the control and aging model groups. Bone marrow mesenchymal stem cells were transfected by lentiviral vectors expressing green fluorescent protein to determine the implantation of bone marrow mesenchymal stem cells in rat lung. Superoxide dismutase activity and malondialdehyde content in rat lung were measured in each group. The difference in rat lung structure was observed using hematoxylin-eosin staining in each group. RESULTS AND CONCLUSION:Bone marrow mesenchymal stem cells marked by green fluorescent protein were implanted in rats, migrated towards lung tissue and survived. Compared with aging model group, superoxide dismutase activity was apparentlyincreased, but malondialdehyde content was obviously diminished in the celltreatment group. In each group, histopathological sections revealed that normal pulmonary alveolus was damaged in the aging model group, showing enlarged air cavity and emphysema. Lung injury was evidently repaired inthe celltreatment group. Results suggested that bone marrow mesenchymal stem cells could repair lung injury in aging rats, and exert anti-aging effects.%背景:研究发现外源性骨髓间充质干细胞能够定居于肺脏组织,参与肺组织的再生,但其修复衰老肺损伤方面的报道较少。
脐带间充质干细胞概述医学实验班 70080103 王雪彤脐带是胎儿时期连接母体与胎儿的索状结构,其外被羊膜,内含2条脐动脉、1条脐静脉,在动静脉之间含有特殊的胚胎粘液样结缔组织———华尔通氏胶(Whartonps Jelly) ,从华尔通氏胶分离得到的基质细胞即为人脐带间充质干细胞(HUMSCs) 。
1人脐带间充质干细胞(HUMSCs) 的形貌分析:倒置显微镜下观察人脐带间充质干细胞贴壁生长, 为形态相对均一的梭形细胞,呈平行排列生长或旋涡状生长,低密度时较扁平, 密度增加趋于融合时细胞变细长。
扫描电镜下观察呈长条状纤维样, 细胞膜表面不光滑, 有小结节状物, 细胞无明显突起,细胞间无网络状连接。
透射电镜观察核大, 不规则, 核仁明显, 常染色质多, 异染色质少, 胞浆少。
胞质内细胞器较少, 以粗面内质网和线粒体为主, 内有大量游离核糖体, 部分细胞可见内质网肿胀。
——植块法培养获得的人脐带间充质干细胞(×200)例如三代细胞的形态学特征——人体脐带间充质干细胞离体培养后,培养至第三代。
第三代人脐带间充质干细胞以均一长梭形的细胞为主,细胞周边有较多的丝状伪足,见图1,2;并形成毗邻细胞之间的网状连接,见图3;细胞核较大,核膜清晰,含两三个核仁,核质比较小,见图4。
2人脐带间充质干细胞(HUMSCs) 的生物学特性:HUMSCs既非胚胎干细胞又非成体干细胞,是别于两者之间的一类新的多能间充质细胞,它们之间既有联系又有差异。
根据国际细胞疗法间充质与组织干细胞委员会( the Mesenchymal and Tissue Stem Cell Committee of the Internation2 al Society for Cellular The rapy)制定的最低标准, 脐带间充质干细胞(MSCs)需满足以下条件: 1)MSCs在标准培养条件下呈贴壁生长; 2 )MSCs表达CD105, CD73和CD90,不表达CD45, CD34, CD14或CD11b, CD79a 或CD19和HLA2DR; 3)MSCs在体外至少能向成骨细胞、脂肪细胞和软骨细胞分化。
间充质干细胞对T淋巴细胞的免疫调节作用间充质干细胞(MSCs)具有增殖能力强、分化范围广及低免疫原性等生物学特性,被广泛用于免疫性疾病的研究。
同时,越来越多的研究发现在免疫性疾病的发生发展中T淋巴细胞具有重要作用,并证实MSCs可通过直接接触、细胞因子作用等途径影响T淋巴细胞的激活、增殖及亚群比例,继而达到免疫调控、缓解病情的目的。
Abstract:Mesenchymal stem cells have the biological characteristics involving strong proliferation capability,widely distribution and low immunogenicity,which are used in the treatment of the immune diseases.A growing number of studies have found that T lymphocytes play a significant role in the development and progression of autoimmune disease.And MSCs can influence the activation,proliferation and the proportion of subsets of T lymphocytes through the cell-cell contact,cytokine,then achieve the goal of immune regulation,relieve illness.The review summarizes that the immune effect of MSCs on T lymphocytes.Key words:Mesenchymal stem cells;T lymphocytes;Immune regulation相关研究证明,T淋巴细胞的异常表达和缺失可导致自身免疫性疾病的发生,而间充质干细胞具有多项分化潜能及免疫调节功能,可通过细胞间的直接接触或(和)通过产生可溶性因子对调节性T细胞进行调控,从而控制自身免疫性疾病的发生和发展。
骨髓间充质干细胞治疗大鼠脑缺血的实验研究的开题报告一、研究背景随着人口老龄化程度的加剧,脑卒中发生率逐年增加。
其中,脑缺血是一种常见的脑卒中类型。
脑缺血可导致脑细胞缺氧、缺血,导致神经元死亡,从而导致严重的脑功能障碍。
传统的治疗方法主要为早期血管再通,但随着时间的推移,神经细胞死亡已经成为一条不可逆的路线。
因此,需要新的治疗方式来恢复缺血脑组织的功能。
骨髓间充质干细胞(MSCs)是来自骨髓的一种多功能细胞。
这些细胞具有自我更新的能力,可分化为多种细胞类型,包括肌肉细胞、软骨细胞和成骨细胞。
此外,MSCs还具有细胞因子和分泌物的作用,可抑制炎症反应,并促进组织修复。
在很多研究中,MSCs已被证明是有效的治疗方法,可用于治疗多种神经系统疾病,包括脑梗死和脑损伤。
通过转移MSCs来治疗脑缺血的前体细胞,可恢复缺血脑的功能。
二、研究目的本研究旨在探究骨髓间充质干细胞是否能够促进大鼠脑缺血后的康复,通过实验验证骨髓间充质干细胞对缺血脑组织的治疗作用,并对治疗机制进行探讨。
三、研究内容1.建立大鼠脑缺血模型。
2.通过尾静脉注射MSCs,评估其治疗效果。
3.对比治疗组和对照组在行为学和神经组织学方面的差异,并进一步探讨骨髓间充质干细胞的治疗机制。
四、研究方法大鼠脑缺血模型的制作:采用经颅供血不足法制作大鼠脑缺血模型。
将大鼠分为治疗组和对照组,治疗组在脑缺血后24小时内尾静脉注射MSCs。
对照组则接收相同的操作但未注射MSCs。
观察制备胶质纤维蛋白(GFAP)和神经元特异性脯氨酸酶(NSE)染色的神经元分布和神经组织损伤,并通过行为测试(如同仁圆盘试验和Morris水迷宫试验)评估大鼠神经学功能的恢复情况。
此外,还将通过ELISA分析细胞因子IL-6和TNF-α的表达以及其他分子的变化。
五、研究预期成果预计本研究将进一步确认骨髓间充质干细胞的神经保护作用,说明其治疗缺血后神经功能障碍的机制,并为开发人类脑缺血的治疗方法提供基础数据。
[基金项目]广东省科技计划项目资助(2002A3020206)。õ论著õ人骨髓间充质干细胞的生物学特性分析陈建锋1,高 毅2,潘明新2(1中国人民解放军第401医院,山东青岛266071;2南方医科大学珠江医院)
[摘要] 目的 对人骨髓间充质干细胞(HMSCs)的生物学特性进行初步分析,为其临床应用奠定基础。方法 抽取4例健康人髋骨内骨髓5~20ml,密度梯度离心法分离HMSCs。体外培养扩增后流式细胞仪检测HM-
SCs表面标记物;MMT法绘制生长曲线,计算细胞倍增时间;吉姆萨染色法检测细胞核型。结果 HMSCs表面标记物CD29、CD44、CD71、CD105、CD166、HLA-ABC、UEA-1阳性表达;CD34、CD45、HLA-DR阴性表达;生长曲线呈S形,细胞倍增时间随代次增加而延长;核型分析显示第3、6代HMSCs的染色体数目未发生改变。结论 密度梯度离心法可得到纯度较高的HMSCs,表可达人类间充质干细胞的表型特征。HMSCs可在体外较长时期培养。在第7代之前细胞增殖旺盛,之后细胞增殖能力逐渐下降;在第6代之前染色体数目未发生改变。[关键词] 人;骨髓;间充质干细胞;细胞培养[中图分类号] R329.2+7 [文献标识码] A [文章编号] 1002-266X(2006)29-0001-03
IsolationandcultivationofhumanbonemarrowmesenchymalstemcellsinvitroandanalysisoftheirbiologicalcharacterizationsCHENJian-feng,GAOYi,PANMing-xin(401HospitalofPLA,Qingdao266071,P.R.China)
Abstract:[Objective]Toestablishasimpleandfeasiblemethodtocultureandproliferatehumanbonemarrowderivedmesenchymalstemcells(HMSCs)invitroandanalyzetheirbiologicalcharacterizations.[Methods]HMSCswereisolatedbycombininggradientdensitycentrifugationwithplasticadherence.ThegrowthcurvesofHMSCsweredrawnbyMTTassay,cellphenotypesweredetectedbyflowcytometry,celldoublingtimewascaculated,andcellkaryotypesweremeasuredbyGiemsastaining.[Results]ThepositiveexpressionofcellphenotypeofHMSCsincludesCD29,CD44,CD71,CD105,CD166,HLA-ABC,UEA-1,whilethenegativeexpressionofcellphenotypein-cludesCD34,CD45,HLA-DR.ThegrowthcurveofHMSCswas“S”shaped.Thecelldoublingtimeprolongedwiththepassagesincreased.ThechromosomenumberofHMSCsofpassage3and6wereboth46,sameashumanbe-ings.[Conclusion]HMSCsofhigherpuritycanbeisolatedbycombininggradientdensitycentrifugationwithplasticadherence,andmaintaincellphenotypesashumanbeings.TheproliferationabilityofHMSCsisstrongbeforepas-sage7,butdecreasesrapidlylater.ThechromosomenumberofHMSCsremainsoriginalbeforepassage6.Keywords:human;bonemarrow;mesenchymalstemcell;cellculture
骨髓组织可分为造血和基质两大系统。骨髓基质细胞是来源于骨髓基质的一种间充质细胞,在空间上起支持作用,在造血方面起精细的调节作用。体外获得足够的基质细胞是进行各项研究的基础。2004~2005年,我们对人骨髓间充质干细胞(HMSCs)进行了体外培养扩增,并对其表型、生长曲线、核型等生物学特性进行了初步分析。现报告如下。1 材料与方法1.1 HMSCs的获取及培养 采集4例无血液疾病志愿者髂骨内骨髓5~20ml。5ml骨髓标本中加入5ml的PBS,900g离心10min2次,以PBS制成4×107细胞数的悬液,取5ml加到5mlPercoll分离液(1.073g/ml)上,900g离心30min,吸取富含有核细胞的中间细胞层。将获取的单个核细胞加2倍量的PBS,900g离心5min,弃上清,以1×106/ml的密度接种于50ml培养瓶中,加入HMSCs完全培养基10ml。待贴壁细胞达到80%~90%融合后,以1÷3的比例传代培养。1.2 HMSCs表型鉴定 取传至第3~6代HMSCs,1
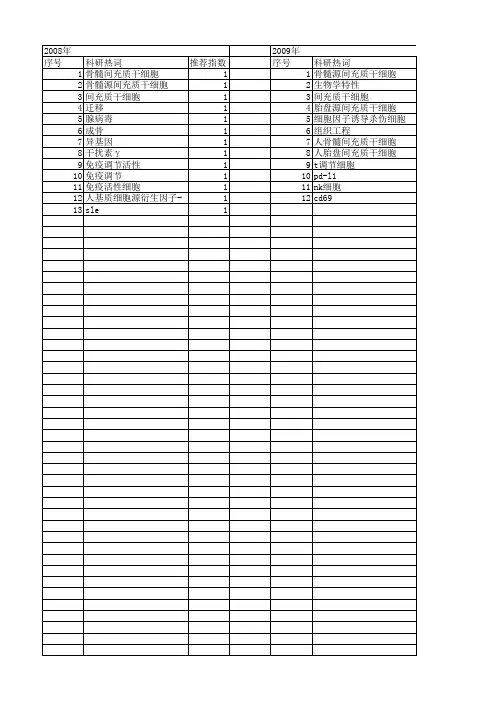
山东医药2006年第46卷第29期用0.25%胰酶室温下消化10min,1500r/min离心15min,收集细胞沉淀,PBS洗涤3次,制成1×105/ml细胞数的悬液。各取1×105个细胞悬液100Ll加入荧光标记的抗体10Ll,室温下反应孵育30min,PBS洗去未标记抗体,去上清后加300LlPBS;流式细胞仪检测细胞表型,Cell-Quest软件分析结果。1.3 HMSCs生长曲线绘制 取原代和第3、5、7、9代细胞悬液,以1×104个/孔接种于96孔培养板中,加200Ll细胞培养基,37℃恒温细胞培养箱中培养。培养第0、2、4、6、8、10、12天,各代次分别取5孔进行检测。每孔分别加入5mg/mlMTT溶液20Ll,置于恒温细胞培养箱培养4h。弃培养液,加入DMSO150Ll,振荡15min裂解细胞,使沉淀物充分溶解。用酶联免疫检测仪(波长570nm)检测光密度(OD)值。以天数为横轴,OD值为纵轴绘制细胞生长曲线。按公式计算倍增时间(DT)。DT=t[lg2/(lgODt-lgOD0)],OD0和ODt分别代表接种后和培养td的细胞OD值。1.4 HMSCs核型分析 取第3、6代的HMSCs,每瓶培养基内加入40Lg/ml秋水仙素1滴,37℃孵箱中孵育2.5h后吸去瓶内液体,0.25%胰蛋白酶消化,1500r/min离心8min。弃上清,加入0.075mMKCl低渗液1ml,混匀后置于37℃水浴中16min。加入1ml核型固定液,1500r/min离心8min,弃上清,加入8ml核型固定液混匀,1500r/min离心8min。弃上清,再加入8ml核型固定液混匀过夜。再次1500r/min离心8min,弃上清,加入新配制核型固定液0.5ml制成悬液,0.25%胰蛋白酶消化50s后滴片,70℃烘干4h。Giemsa染色液显带5min。应用人类染色体计算机辅助识别系统镜下随机观察细胞染色体,计数染色体条数。1.5 统计学方法 采用SPSS10.0软件。计量资料均采用x±s表示,组间差异采用完全随机设计资料的方差分析。检验水准A=0.05。2 结果2.1 细胞形态 HMSCs形态较为均一,呈大圆形,单核;培养24h后部分细胞开始贴壁生长,少量细胞呈现短梭形改变;培养48~72h贴壁细胞明显增多,以圆形和短梭形为主;传至第3代时细胞增殖迅速,几乎全部贴壁生长,以长梭形为主,体积小,核浆比大,呈明显同向性改变,漩涡状盘旋排列。2.2 表型鉴定 HMSCs中CD29阳性表达细胞比率为95.3%,CD34阳性细胞比率为1.8%,CD44阳性细胞比率为94.7%,CD45阳性细胞比率为0.8%,CD71阳性细胞比率为96.2%,CD105阳性细胞比率为96.6%,CD166阳性细胞比率为92.7%,HLA-ABC阳性细胞比率为96.3%,HLA-DR阳性细胞比率为1.1%,UEA-1阳性细胞比率为98.7%。2.3 生长情况 原代细胞接种后0~4d细胞贴壁增长,增生不活跃,为细胞潜伏期;4~10d细胞增长极为活跃,呈指数级递增,为对数增长期;此后细胞增长逐渐减缓,进入平台期,细胞生长曲线呈S形。传代后细胞潜伏期和对数生长期均相对缩短,平台期提前,细胞生长逐渐减慢。细胞传至7~9代后增生能力逐渐降低。DT随代次增加而逐渐延长。第1、3、5、7、9代HMSCs的DT值分别为3.19±0.44、4.57±0.51、5.93±1.84、6.71±1.59、6.91±2.52,细胞生长曲线见图1。2.4 核型分析 第3、6代HMSCs染色体条数均为46条,未见数目改变。
图1 不同代次HMSCs生长曲线 注:P1、P3、P5、P7、P9分别代表第1、3、5、7、9代HMSCs3 讨论Friendenstein等[1]发现在骨髓中存在能贴附塑料培养皿、呈长棱形成纤维细胞样的细胞,培养时呈克隆生长,能形成成纤维细胞样集落形成单位,这种细胞具有多向分化潜能,即BMSCs。BMSCs易与造血系细胞区分,但其缺乏特异性的表面或胞质内抗原,目前鉴别主要依赖其形态学及功能学表现[2]。骨髓基质细胞目前尚无明确的表型分类,BMSCs亦无高度特异的表面抗原。目前研究表明,BMSCs的表面表达SH2、SH3、CD29、CD44、CD71、CD9、CD106、CD120a、CD124等,而不表达CD14、CD31、CD34、CD45等细胞表面抗原[3]。本研究发现,其表面表达CD29、CD44、CD71、CD105、CD166、HLA-ABC和UEA-1,而不表达CD34、CD45和HLA-DR。从HMSCs生长曲线图上可以看出,传代早期(接种后前4d)细胞生长速度较为缓慢,第4~10天,生长速度显著加快,这种现象可能与其自分泌调节2
山东医药2006年第46卷第29期