差热分析法
- 格式:ppt
- 大小:671.00 KB
- 文档页数:48

差动热分析仪热分析是在程序控温条件下,测量物质物理化学性质随温度变化的函数关系的一种技术。
程序控温可采用线性、对数或倒数程序。
热分析法依照所测样品物理性质的不同有以下几种:差热分析法,差示扫描量热法,热重分析法,热膨胀分析及热——力分析法等。
图a. 差动热分析仪整机线路连接图1.电炉2.气氛控制单元3.数据站接口单元4.差动热补偿单元5.差热放大单元6.可控硅加热单元7.微机温控单元图b. 仪器各主要部件2图c. 加热炉组件图d. 电炉(一)差热分析差热分析(differential thermal analysis, DTA)法是在程序控温下,测量物质与参比物之间温度差随温度或时间变化的一种技术。
根据国际热分析协会(international confederation for thermal analysis, ICTA) 规定,DTA曲线放热峰向上,吸热峰向下,灵敏度单位为微伏(μV)。
如图1-1为苦味酸(三硝基苯酚)的DTA曲线。
图1-1 苦味酸在动态空气中的DTA曲线可见,体系在程序控温下,不断加热或冷却降温,物质将按照它固有的运动规律而发生量变或质变,从而产生吸热或放热,根据吸热或放热便可判定物质内在性质的变化。
如:晶型转变、熔化、升华、挥发、还原、分解、脱水或降解等。
差热分析测量原理如图1-2所示。
图1-2 差热分析原理示意图图1-3 仪器工作原理差热分析仪主要由温度控制系统和差热信号测量系统组成,辅之以气氛和冷却水通道,测量结果由记录仪或计算机数据处理系统处理。
1.温度控制系统该系统由程序温度控制单元、控温热电耦及加热炉组成。
程序温度控制单元可编程序模拟复杂的温度曲线,给出毫伏信号。
当控温热电耦的热电势与该毫伏值有偏差时,说明炉温偏离给定值,由偏差信号调整加热炉功率,使炉温很好地跟踪设定值,产生理想的温度曲线。
2.差热信号测量系统该系统由差热传感器、差热放大单元等组成。
差热传感器即样品支架,由一对差接的点状热电耦和四孔氧化铝杆等装配而成,测定时将试样与参比物(常用α-Al2O3)分别放在两只坩埚中,置于样品杆的托盘上,然后使加热炉按一定速度升温(如10℃〃min-1)。

差热分析的基本原理
差热分析的基本原理是利用样品与参比样品在相同温度下的热量差异来研究样
品的热性质。
在差热分析实验中,通常将样品和参比样品分别放置在两个独立的样品盒中,然后同时加热它们。
当样品和参比样品吸收或释放热量时,会导致它们的温度发生变化,而这种温度变化可以通过热敏电阻或热电偶等传感器来检测。
通过测量样品和参比样品在相同温度下的热量差异,就可以得到样品的热性质信息。
在差热分析实验中,通常会控制样品和参比样品在相同的升温速率下升温,以
保证它们受热的条件相同。
在升温过程中,如果样品吸收热量,则其温度会上升的比参比样品快,反之则慢。
通过测量样品和参比样品的温度差异,就可以得到样品的吸热或放热曲线。
根据吸热或放热曲线的特征,可以得到样品的热性质参数,如熔点、熔化热、玻璃化转变温度等。
差热分析广泛应用于材料科学、化学、生物学等领域。
在材料科学中,差热分
析可以用来研究材料的热稳定性、相变行为、玻璃化转变等;在化学领域,差热分析可以用来研究化学反应的热效应、化学物质的热分解等;在生物学领域,差热分析可以用来研究生物大分子的热性质、生物反应的热效应等。
总之,差热分析是一种重要的热分析方法,它通过测量样品与参比样品在相同
温度下的热量差异,来研究样品的热性质。
差热分析的基本原理是简单而有效的,广泛应用于材料科学、化学、生物学等领域,为科研工作者提供了重要的实验手段。
希望本文的介绍能够帮助读者更好地理解差热分析的基本原理,进一步应用于科研实践中。


差热分析法(DTA)简介(Differential Thermal Analysis)1.DTA的基本原理差热分析是在程序控制温度下,测量物质与参比物之间的温度差与温度关系的一种技术。
差热分析曲线是描述样品与参比物之间的温差(ΔT)随温度或时间的变化关系。
在DAT试验中,样品温度的变化是由于相转变或反应的吸热或放热效应引起的。
如:相转变,熔化,结晶结构的转变,沸腾,升华,蒸发,脱氢反应,断裂或分解反应,氧化或还原反应,晶格结构的破坏和其它化学反应。
一般说来,相转变、脱氢还原和一些分解反应产生吸热效应;而结晶、氧化和一些分解反应产生放热效应。
差热分析的原理如图Ⅱ-3-1所示。
将试样和参比物分别放入坩埚,置于炉中以一定速率进行程序升温,以表示各自的温度,设试样和参比物(包括容器、温差电偶等)的热容量Cs、Cr不随温度而变。
则它们的升温曲线如图Ⅱ-3-2所示。
若以对t作图,所得DTA曲线如图Ⅱ-3-3所示,在0-a区间,ΔT大体上是一致的,形成DTA曲线的基线。
随着温度的增加,试样产生了热效应(例如相转变),则与参比物间的温差变大,在DTA曲线中表现为峰。
显然,温差越大,峰也越大,试样发生变化的次数多,峰的数目也多,所以各种吸热和放热峰的个数、形状和位置与相应的温度可用来定性地鉴定所研究的物质,而峰面积与热量的变化有关。
图Ⅱ-3-1差热分析的原理图 II-3-1 差热分析的原理图图II-3-2试样和参比物的升温曲线1.参比物;2.试样;3.炉体;4.热电偶(包括吸热转变)图Ⅱ-3-3 DTA吸热转变曲线TA曲线所包围的面积S可用下式表示式中m是反应物的质量,ΔH是反应热,g是仪器的几何形态常数,C是样品的热传导率ΔT是温差,t1是DTA曲线的积分限。
这是一种最简单的表达式,它是通过运用比例或近似常数g和C来说明样品反应热与峰面积的关系。
这里忽略了微分项和样品的温度梯度,并假设峰面积与样品的比热无关,所以它是一个近似关系式。

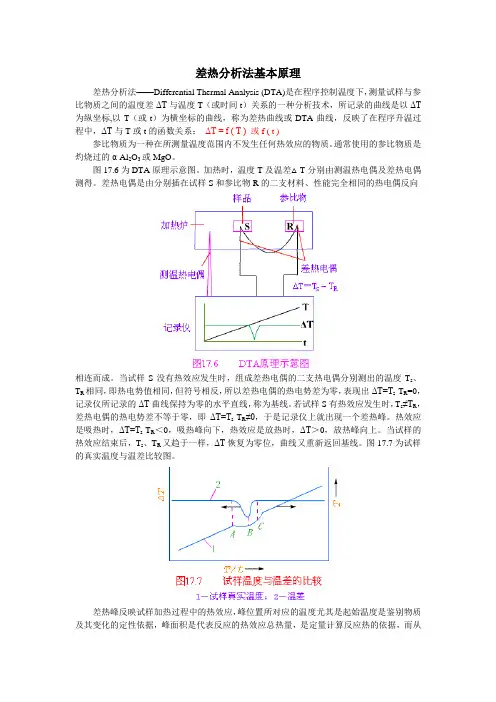
差热分析法基本原理差热分析法——Differential Thermal Analysis (DTA)是在程序控制温度下,测量试样与参比物质之间的温度差ΔT与温度T(或时间t)关系的一种分析技术,所记录的曲线是以ΔT 为纵坐标,以T(或t)为横坐标的曲线,称为差热曲线或DTA曲线,反映了在程序升温过程中,ΔT与T或t的函数关系:ΔT = f ( T ) 或f ( t )参比物质为一种在所测量温度范围内不发生任何热效应的物质。
通常使用的参比物质是灼烧过的α-Al2O3或MgO。
图17.6为DTA原理示意图。
加热时,温度T及温差△T分别由测温热电偶及差热电偶测得。
差热电偶是由分别插在试样S和参比物R的二支材料、性能完全相同的热电偶反向相连而成。
当试样S没有热效应发生时,组成差热电偶的二支热电偶分别测出的温度T s、T R相同,即热电势值相同,但符号相反,所以差热电偶的热电势差为零,表现出ΔT=T s-T R=0,记录仪所记录的ΔT曲线保持为零的水平直线,称为基线。
若试样S有热效应发生时,T s≠T R,差热电偶的热电势差不等于零,即ΔT=T s-T R≠0,于是记录仪上就出现一个差热峰。
热效应是吸热时,ΔT=T s-T R<0,吸热峰向下,热效应是放热时,ΔT>0,放热峰向上。
当试样的热效应结束后,T s、T R又趋于一样,ΔT恢复为零位,曲线又重新返回基线。
图17.7为试样的真实温度与温差比较图。
差热峰反映试样加热过程中的热效应,峰位置所对应的温度尤其是起始温度是鉴别物质及其变化的定性依据,峰面积是代表反应的热效应总热量,是定量计算反应热的依据,而从峰的形状(峰高、峰宽、对称性等)则可求得热反应的动力学参数。
表17.2列出了各种吸热和放热体系的类型,供判断差热峰产生机理时参考。
表17.2 差热分析中吸热和放热体系的主要类型现象(物理的原因)吸热放热现象(化学的原因)吸热放热结晶转变○○化学吸附○熔融○析出○气化○脱水○升华○分解○○吸附○氧化度降低○脱附○氧化(气体中)○吸收○还原(气体中)○氧化还原反应○○固相反应○○影响DTA的因素影响DTA的因素很多,下面讨论几种主要的因素:★升温速度的影响保持均匀的升温速度(ψ)是DTA的重要条件之一,即应:ψ = dT R / dt = 常数若升温速度不均匀(即ψ有波动),则DTA曲线的基线会漂移,影响多种参数测量。


差热分析法(DTA)简介(Differential Thermal Analysis)1.DTA的基本原理差热分析是在程序控制温度下,测量物质与参比物之间的温度差与温度关系的一种技术。
差热分析曲线是描述样品与参比物之间的温差(ΔT)随温度或时间的变化关系。
在DAT试验中,样品温度的变化是由于相转变或反应的吸热或放热效应引起的。
如:相转变,熔化,结晶结构的转变,沸腾,升华,蒸发,脱氢反应,断裂或分解反应,氧化或还原反应,晶格结构的破坏和其它化学反应。
一般说来,相转变、脱氢还原和一些分解反应产生吸热效应;而结晶、氧化和一些分解反应产生放热效应。
差热分析的原理如图Ⅱ-3-1所示。
将试样和参比物分别放入坩埚,置于炉中以一定速率进行程序升温,以表示各自的温度,设试样和参比物(包括容器、温差电偶等)的热容量Cs、Cr不随温度而变。
则它们的升温曲线如图Ⅱ-3-2所示。
若以对t作图,所得DTA曲线如图Ⅱ-3-3所示,在0-a区间,ΔT大体上是一致的,形成DTA曲线的基线。
随着温度的增加,试样产生了热效应(例如相转变),则与参比物间的温差变大,在DTA曲线中表现为峰。
显然,温差越大,峰也越大,试样发生变化的次数多,峰的数目也多,所以各种吸热和放热峰的个数、形状和位置与相应的温度可用来定性地鉴定所研究的物质,而峰面积与热量的变化有关。
图Ⅱ-3-1差热分析的原理图 II-3-1 差热分析的原理图图II-3-2试样和参比物的升温曲线1.参比物;2.试样;3.炉体;4.热电偶(包括吸热转变)图Ⅱ-3-3 DTA吸热转变曲线TA曲线所包围的面积S可用下式表示式中m是反应物的质量,ΔH是反应热,g是仪器的几何形态常数,C是样品的热传导率ΔT是温差,t1是DTA曲线的积分限。
这是一种最简单的表达式,它是通过运用比例或近似常数g和C来说明样品反应热与峰面积的关系。
这里忽略了微分项和样品的温度梯度,并假设峰面积与样品的比热无关,所以它是一个近似关系式。


差热分析实验报告思考题
实验名称:差热分析实验
实验目的:通过对不同物质进行差热分析实验,研究其热化学
性质。
实验原理:差热分析法是一种测量样品在非绝热条件下吸放热
量的方法,该方法可以用来研究化学反应、热化学稳定性、热分
解反应等问题。
在实验中,将样品与标准物质一起放置在加热炉
中加热,在整个过程中测量样品与标准物质所吸收或放出的热量,从而分析样品的物化性质。
实验步骤:
1.取一个净重约为1g的样品,放置在标准热物质中心,称量出
标准热物质的质量。
2.将装有样品和标准热物质的盘子放入试样盒中,在该温度下
预热30分钟。
3.设定升温速率,开启差热仪开始实验,对样品进行相应升温控制。
4.记录标准样品的热变化,计算出样品的热变化。
实验结果:通过实验,得到了不同物质在加热过程中的热变化曲线,并可以对其进行热化学性质的分析。
思考题:
1.为什么要进行差热分析实验?
2.使用差热分析法测定样品吸放热量的条件有哪些?
3.什么情况下样品的热变化为正值?什么情况下样品的热变化为负值?
4.如果样品为化合物,使用差热分析法需要注意哪些问题?
5.差热分析法的应用有哪些?。
