2差热分析法PPT课件
- 格式:ppt
- 大小:2.59 MB
- 文档页数:53

实验二热重-差热分析法一、实验目的1.掌握热重和差热分析的基本原理。
2.学习热重和差热分析仪的操作。
3.学会定性解释差热谱图。
4.用差热仪测定绘制CuSO4·5H2O的DTA曲线,分析其水分子的脱去顺序。
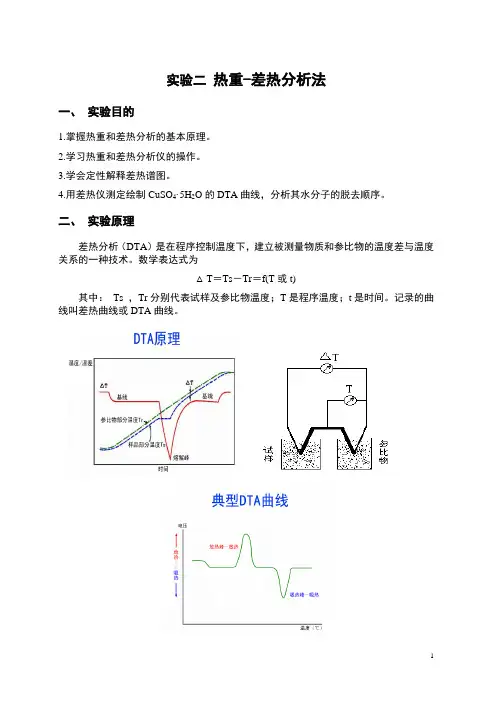
二、实验原理差热分析(DTA)是在程序控制温度下,建立被测量物质和参比物的温度差与温度关系的一种技术。
数学表达式为△T=Ts-Tr=f(T或t)其中:Ts ,Tr分别代表试样及参比物温度;T是程序温度;t是时间。
记录的曲线叫差热曲线或DTA曲线。
本实验以α – Al2O3作为参比物质,记录CuSO4·5H2O的DTA曲线,从而考察其失去五分子结晶水的情况。
物质受热时,发生化学变化,质量也就随之改变,测定物质质量的变化也就随之改变,测定物质质量的变化就可研究其变化过程,热重法(TG)是在程序控制温度下,测量物质质量与温度关系的一种技术,热重法实验得到的曲线称为热重曲线(TG曲线)。
三、实验仪器:差热分析仪由加热炉、试样容器、热电偶、温度控制系统及放大、记录系统等部分组成。
四、实验步骤:1.依次开启稳压电源、工作站、气体流量计、主机(开关均在后面)、电脑,打开氮气瓶,使之压力为0.5MP。
2.打开炉子,手动在左右两个陶瓷杆放入铝坩埚容器,关好炉子,在操作界面上调零,仪器自动扣除了空坩埚的重量。
3.打开炉子取出样品坩埚容器将约5-10mg的样品研成粉末放入铝坩埚容器。
4.打开软件TA-60WS Collection Monitor 点击measure,出现measure parameter,在这里我们可以设置所需要的程序温度,然后点击Start,要我们文件保存在哪里。
5.单击Start。
6.仪器测定结束。
四、结果处理1.仪器结束后,打开软件TA60,找到要保存的结果文件。
2.依次找到重量线,热线,程序升温线。
3.首先从热线中分析出样品的吸热峰和放热峰。
从重量线上分析出样品重量的损失(单击重量线,点击Analysis,出现Weigh loss,然后分析)。



差热曲线方程ΔH=KS差热曲线的峰面积S;反应热效应ΔH;传热系数K1975年,神户博太郎对差热曲线提出了一个理论解析的数学方程式,该方程能够十分简便的阐述差热曲线所反映的热力学过程和各种影响因素。
DTA存在的两个缺点:1)试样在产生热效应时,升温速率是非线性的,从而使校正系数K值变化,难以进行定量;2)试样产生热效应时,由于与参比物、环境的温度有较大差异,三者之间会发生热交换,降低了对热效应测量的灵敏度和精确度。
→使得差热技术难以进行定量分析,只能进行定性或半定量的分析工作。
为了克服差热缺点,发展了DSC。
该法对试样产生的热效应能及时得到应有的补偿,使得试样与参比物之间无温差、无热交换,试样升温速度始终跟随炉温线性升温,保证了校正系数K值恒定。
测量灵敏度和精度大有提高。
标准卡片有:萨特勒(Sadtler)研究室出版的卡片约2000张和麦肯齐(Mackenzie)制作的卡片1662张(分为矿物、无机物与有机物三部分)。
差热分析的应用凡是在加热(或冷却)过程中,因物理-化学变化而产生吸热或者放热效应的物质,均可以用差热分析法加以鉴定。
其主要应用范围如下:1)含水化合物对于含吸附水、结晶水或者结构水的物质,在加热过程中失水时,发生吸热作用,在差热曲线上形成吸热峰。
2)高温下有气体放出的物质一些化学物质,如碳酸盐、硫酸盐及硫化物等,在加热过程中由于CO2、SO2等气体的放出,而产生吸热效应,在差热曲线上表现为吸热峰。
不同类物质放出气体的温度不同,差热曲线的形态也不同,利用这种特征就可以对不同类物质进行区分鉴定。
3)矿物中含有变价元素矿物中含有变价元素,在高温下发生氧化,由低价元素变为高价元素而放出热量,在差热曲线上表现为放热峰。
变价元素不同,以及在晶格结构中的情况不同,则因氧化而产生放热效应的温度也不同。
4)非晶态物质的重结晶有些非晶态物质在加热过程中伴随有重结晶的现象发生,放出热量,在差热曲线上形成放热峰。
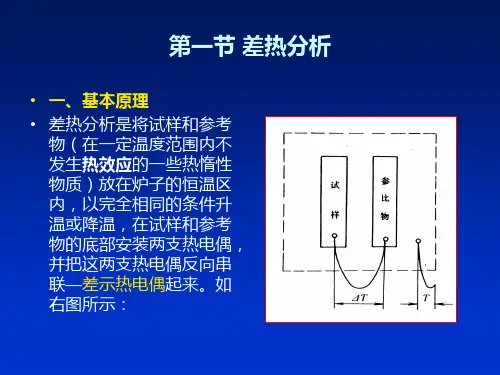
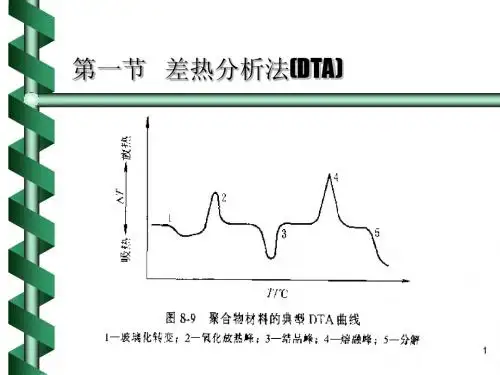

实验二差示扫描量热法(DSC)在等速升温(降温)的条件下,测量试样与参比物之间的温度差随温度变化的技术称为差热分析,简称DTA(Differential Thermal Analysis)。
试样在升(降)温过程中,发生吸热或放热,在差热曲线上就会出现吸热或放热峰。
试样发生力学状态变化时(如玻璃化转变),虽无吸热或放热,但比热有突变,在差热曲线上是基线的突然变动。
试样对热敏感的变化能反映在差热曲线上。
发生的热效大致可归纳为:(1)发生吸热反应。
结晶熔化、蒸发、升华、化学吸附、脱结晶水、二次相变(如高聚物的玻璃化转变)、气态还原等。
(2)发生放热反应。
气体吸附、氧化降解、气态氧化(燃烧)、爆炸、再结晶等。
(3)发生放热或吸热反应。
结晶形态转变、化学分解、氧化还原反应、固态反应等。
用DTA方法分析上述这些反应,不反映物质的重量是否变化,也不论是物理变化还是化学变化,它只能反映出在某个温度下物质发生了反应,具体确定反应的实质还得要用其他方法(如光谱、质谱和X光衍射等)。
由于DTA测量的是样品和基准物的温度差,试样在转变时热传导的变化是未知的,温差与热量变化比例也是未知的,其热量变化的定量性能不好。
在DTA基础上增加一个补偿加热器而成的另一种技术是差示扫描量热法。
简称DSC(Differential Scanning Calorimetry)。
因此DSC直接反映试样在转变时的热量变化,便于定量测定。
DTA、DSC广泛应用于:(1)研究聚合物相转变,测定结晶温度Tc 、熔点Tm、结晶度XD。
结晶动力学参数。
(2)测定玻璃化转变温度Tg。
(3)研究聚合、固化、交联、氧化、分解等反应,测定反应热、反应动力学参数。
一、目的要求:1.了解DTA、DSC的原理。
2.掌握用DSC测定聚合物的Tg 、Tc、Tm、XD。
二、基本原理:1.DTA图(11-1)是DTA的示意图。
通常由温度程序控制、气氛控制、变换放大、显示记录等部分所组成。


