苏教版有机化学基础脂肪烃
- 格式:ppt
- 大小:416.00 KB
- 文档页数:10

专题3 常见的烃领先一步,领跑一生:每一个成功者都有一个开始。
勇于开始,才能找到成功的路。
第一单元脂肪烃细品书中知识关键词:烷烃和烯烃、取代反应、加成反应1.烃的分类①烃的分类脂肪烃和芳香烃属于脂肪族化合物的烃是脂肪烃,属于芳香族化合物的烃是芳香烃。
脂肪烃中一定没有苯环,芳香烃中一定有苯环。
②脂肪烃的分类饱和烃和不饱和烃把含有双键或者叁键等不饱和键的脂肪烃叫做不饱和脂肪烃,简称不饱和烃;把不含有双键或者叁键等不饱和键的脂肪烃叫做饱和脂肪烃,简称饱和烃。
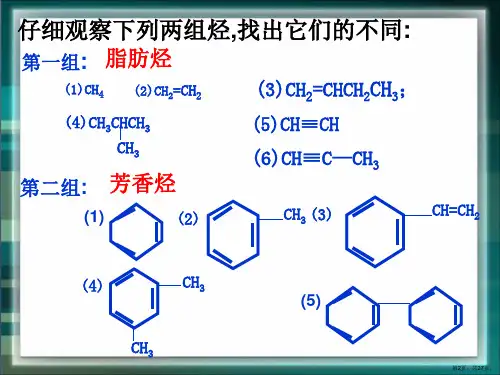
例1 下列物质属于芳香烃,但不是苯的同系物的是解析:含有苯环的化合物就属于芳香族化合物,含有苯环的烃属于芳香烃,而苯的同系物的定义是含有一个苯环且侧链为饱和烃基的芳香烃。
A、B属于苯的同系物,C不属于芳香烃,D属于芳香烃但侧链不饱和,不属于苯的同系物。
答案:D点拨:注意烃在不同角度分类时结果是不一样的,还要理解分类的范围,如饱和烃和不饱和烃都是脂肪烃。
2.脂肪烃的物性(1)甲烷的物理性质甲烷为无色无味的气体,密度比空气小,所以收集甲烷可以用向下排空气法,又因为甲烷不溶于水,所以甲烷也可用排水法收集,甲烷是有机物分子中相对分子质量最小的烃。
(2)乙烯的物理性质通常情况下,乙烯是一种无色稍有气味的气体,密度与空气相近,难溶于水。
(3)物理性质的递变规律①烷烃随着碳原子数的增加,相对分子质量增大,分子间作用力增大,熔沸点逐渐升高。
②分子式相同的不同烷烃,支链越多,熔沸点越低。
例如:CH3(CH2)3CH3> (CH3)2CHCH2CH3>C(CH3)4。
③烷烃都不溶于水,且比水的密度小。
例2 含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:* 燃烧热:1 mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量。
根据表中数据,下列判断错误的是( )A.正庚烷在常温常压下肯定不是气体B.烷烃燃烧热和其所含碳原子数成线性关系C.随碳原子数增加,烷烃沸点逐渐升高D.随碳原子数增加,烷烃沸点和燃烧热都成比例增加解析:从表中数据可知,烷烃随碳原子数目递增沸点依次升高,燃烧热依次升高,但这种增长只是一种趋势,不是成比例增长。

第一单元脂肪烃脂肪烃的性质一、教学目标【知识与技能】1. 了解烷烃、烯烃、炔烃的物理性质的变化与分子中碳原子数目的关系。
2. 掌握烷烃、烯烃、炔烃的主要化学性质。
【过程与方法】1.通过对比甲烷、乙烯的结构和性质的方法,进一步讨论烷烃和烯烃的结构和性质。
【情感、态度、价值观】1.培养学生自主观察得出结论,验证结论的能力。
2.培养学生严谨求实、勇于探索的科学态度。
二、学情分析学生在化学2中已经简单学习了烷烃和烯烃的典型代表物——甲烷和乙烯。
本节课在复习乙烷和乙烯结构与性质的基础上,重点引导学生掌握有机化学的基本方法——“结构决定性质,性质反映结构”;注重培养学生的演绎思维、迁移能力,从甲烷、乙烯的结构和性质迁移到烷烃、烯烃的结构和性质。
三、教学思路本节课教学过程中以任务驱动为线索,将烷烃与烯烃物理性质的递变规律,有机物结构(官能团)与化学性质的关系,从个别到一般的演绎思维能力与按类别学习有机化合物的学习方法隐藏在其中,教学过程中注重实施层层深入、演绎与归纳相结合的教学策略,并注重对学生分析问题的合理性及有序性等方面能力进行逐步培养,力图达到课堂教学的实效性。
四、教学重点烷烃、烯烃、炔烃的结构特点和主要化学性质五、教学难点烷烃、烯烃、炔烃的结构特点和主要化学性质六、教学过程【过渡】:那他们的化学性质又如何呢?【师】1、通常状况下,它们很稳定,跟酸、碱及氧化物都不发生反应,也难与其他物质化合。
【过渡】:但是烷烃能够在点燃的条件下被氧气氧化。
例如:甲烷可以在氧气中点燃。
请同学试着写出他们反应的化学方程式。
【师】:非常好。
其实烷烃除了能在氧气中点燃以外,还可以在光照的条件下与氯气发生取代反应。
【设问】:那什么又叫取代反应呢?【投影】:反应方程式并讲解。
【投影】:练习。
【学生】:CH4 + 2O2 CO2 + 2H2O【学生】:取代反应:有机物分子中某些原子或原子团被其它原子或原子团所代替的反应。
教师引导,并且启发学生学习烷烃的物理性质。

06脂肪烃的来源知识梳理1.几种典型烃的实验室制法 (1)甲烷的实验室制法原理:实验室里通常用 和混和加热而制得。
反应方程式: 反应装置:此实验成功与否的关键主要取决于药品是否无水(2)乙烯的实验室制法原理: 装置:注意事项:温度必须达到 ℃否则会有其它产物生成 温度计应插入浓H 2SO 4 的作用:(3)乙炔的实验室制法电石,主要成分是________,通常还含有CaS 、Ca 3P 2等杂质,电石中的这些成分遇水都可以发生水解,因此在制取的乙炔气体中通常会含有_________________等杂质气体,需用____________________加以除去。
原理: 装置:注意事项:一般用饱和食盐水与CaC 2反应,这样可以减缓反应速率 2.脂肪烃的工业来源(1)石油的成分——各种烃的混合物 (2)石油炼制方法A .分馏——根据石油中各物质的沸点不同,用加热的方法,使各成分分离,是石油炼制过程中最常用的方法B .裂化——为了提高轻质油(如汽油)的产量,用加热或催化剂使石油中碳链较长的有机物分解为碳链较短的物质,通常分为热裂化和催化裂化C .裂解——深度裂化,目的是为了获得小分子的烯烃(乙烯丙烯等)D .催化重整——获得芳香烃的主要途径E .催化加氢 〖例1〗某同学设计了如图装置进行石油蒸馏的实验,回答下列有关问题: (1) 指出实验装置中仪器A 、B 、C 、D 的名称。
A B C D (2)指出该同学所设计的实验装置中存在的错误,并给予改正。
〖例2〗某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H 2的13.5倍,则下列说法中正确的是 A .混合气体中一定有乙炔 B .混合气体中一定有乙烯C .混合气体可能由乙炔和丙烯组成D .混合气体一定由乙烯和乙炔组成随堂练习1.石油炼制过程中,既能提高汽油产量又能提高汽油质量的方法是A .蒸馏B .分馏C .裂解D .催化裂化 2.下列液体分别和溴水混合振荡,静置后分为两层,水层、油层均为无色的是 A .己烷 B .四氯化碳 C .NaOH 溶液 D .直馏汽油 3.下列物质的电子式正确的是4.下列物质属于纯净物的是A .甲烷与氯气在光照下取代的有机产物B .铝热剂C .明矾D .汽油5."辛烷值"用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,右图(图3—1—1)是异辛烷的球棍模型,则异辛烷的系统命名为A .1,1,3,3-四甲基丁烷B .2,2,4-三甲基-戊烷C .2,4,4-三甲基戊烷D .2,2,4-三甲基戊烷6.氢核磁共振谱是根据不同化学环境的氢原子在谱中给出的信号不同来确定有机物分子中氢原子种类的。







05脂肪烃知识梳理一、烷烃1.定义2.分子通式3.物理性质(1)烷烃的熔、沸点随碳原子数变化规律(a)随着分子里含碳原子数的增加,熔点、沸点逐渐,相对密度逐渐;(b)分子里碳原子数等于或小于4的烷烃。
在常温常压下都是,其他烷烃在常温常压下都是或;(c)烷烃的相对密度于水的密度。
(2)水溶性——烷烃分子均为分子,故一般溶于水,而溶于有机溶剂,液态烷烃本身就是良好的有机溶剂。
4.化学性质(特征反应)甲烷与纯卤素单质(Cl2)发生反应5.烃的燃烧:随着碳原子数的增加,往往燃烧越来越不充分,火焰明亮,并伴有。
烷烃燃烧的化学方程通式:____________________________烃燃烧的化学方程通式:____________________________二、烯烃和炔烃1.定义(1)烯烃:单烯烃:多烯烃:炔烃:2.单烯烃的通式:3.烯炔的加成反应乙烯与HCl的反应:乙烯与H2O的反应:乙烯与氯气的反应:乙烯与H2的反应:乙炔(“能”或“不能”)使溴水褪色。
乙炔与少量溴水反应:乙炔与过量溴水反应:乙炔与足量H2反应:乙炔制备氯乙烯:4.烯烃的不对称加成马氏规则——当不对称烯烃与卤化氢发生加成反应时,通常H加到含H多的不饱和碳原子一侧。
2.二烯烃中的加成反应1,3—丁二烯(结构简式):二烯烃发生加成反应,低温时发生1,2-加成;高温时发生1,4-加成。
请写出2-甲基-1,3-丁二烯与Br2 1:1发生加成反应的方程式3.加聚反应(1)乙烯型加聚反应(1)聚乙烯的合成:nCH2= CH2乙烯聚乙烯注意:a 单体——用以形成高分子化合物的小分子物质b 链节——高分子化合物中不断重复的基本结构单元c 聚合度——链节的数目n叫做。
由于n不同因此高聚物都是混合物。
(2)聚苯乙烯的合成(3)聚氯乙烯的合成(4)聚丙烯的合成这一类加聚反应都可以理解为以乙烯为母体,其它原子或原子团,去取代乙烯上的H原子。
(2)1,3-丁二烯型加聚反应天然橡胶是异戊二烯(CH2=C-CH=CH2通过加聚反应形成的一类高分子物质。
专题3 常见的烃第一单元脂肪烃课前预习情景导入在初中我们已了解到天然气的主要成分为CH4,甲烷俗称沼气。
也初步了解了有机物有易燃烧的通性。
在必修Ⅱ的学习中我们知道,天然气和沼气的主要成分——甲烷为最简单的有机物,与一氧化碳或氢气相比,相同条件下等体积的甲烷燃烧时,释放的热量较多,是高效、较洁净的燃料。
在石油的炼制过程中,也会得到一系列和甲烷相似的化合物,如乙烷、丙烷、丁烷等,这些化合物都是碳氢化合物,统称为烃。
在石油的炼制过程中,除了获得一系列的低分子烷烃外,还能得到许多有机化合物,在石油的分馏过程中得到的产物都是混合物,它们分子中的碳氢原子个数均不同,但经过石油的催化裂化反应能得到相对分子质量较小,沸点较低的烃。
石油的裂解使石油分馏产物中的长链烃断裂成乙烯、丙烯等气态短链烃。
通过本节课我们将会学习到乙烯、乙炔等脂肪烃的性质,脂肪烃的主要来源以及石油的化学工业。
在必修Ⅱ的基础上进行知识的系统化,对石油的化学工业进行更专业化的学习。
知识预览一、脂肪烃的性质1.烃是一类十分重要的有机化合物,烃可以分为__________和__________。
属于脂肪族的化合物的烃为__________,其分子中一定不含__________;属于芳香族的化合物的烃为__________,其分子中一定含__________。
2.根据脂肪烃的结构,人们把含双键和叁键等不饱和键的脂肪烃称为__________,简称不饱和烃;把不含不饱和键的脂肪烃称为__________,简称饱和烃。
3.脂肪烃包括__________、__________、__________等。
__________是饱和烃,__________是不饱和烃。
4.用甲烷在光照条件下与氯气或溴蒸气能发生__________,其他的烷烃在一定条件下也能发生此反应。
烷烃发生此类反应时,其分子中的__________被__________代替。
像烷烃的卤代反应那样,有机化合物分子中的__________被__________代替的反应称为取代反应。
脂肪烃的性质[复习回顾]1、在前面学习的有关物质的分类中,我们已经对烃从不同角度进行了分类。
有人说:脂肪烃和芳香烃的区别在于有机物中是否含有碳环结构,你认为这话对吗?为什么?2、请举例说明符合下列类别的烃,写出结构简式或键线式:(1)环状饱和脂肪烃;环状不饱和脂肪烃;链状饱和烃;(2)最简单的二烯烃;最简单的芳香烃;最简单的稠环芳香烃。
[新识体系]一、脂肪烃的物理性质脂肪烃(烷烃、烯烃、炔烃)的物理性质随呈变化。
2.烃的状态一般呈气态到液态,再到固态的变化趋势。
在常温常压下,脂肪烃分子中碳原子数小于4的烃一般为气态,C5—C15之间的烃一般为液态,C16以上的烃一般是固体。
3.烃的密度随着相对分子质量的增大而增大,但都于水。
4.烃一般难溶于水而易溶于有机溶剂。
[课前预复习]脂肪烃包括烷烃、环烷烃、烯烃(单烯烃、多烯烃和环烯烃等)、炔烃,还有一些结构特殊的烃,如立方烷等。
不同类别的烃具有不同的结构和组成,当然化学性质也不相同。
完成课本P41[整理与归纳][知识体系]二、脂肪烃的化学性质1.烷烃的主要化学性质(1)与卤素的反应。
烷烃与卤素的反应机理是反应。
此类反应比较慢,反应难以控制停留在哪一步,产物不纯。
例如,要获得较纯净的CH3—CH2Cl,一般不用CH3—CH3与Cl2的反应,常用(只要写出一种反应)反应。
(2)烷烃还能发生燃烧反应和分解。
请写出烷烃C n H2n+2完全燃烧的化学方程式:。
利用烷烃高温(加催化剂时温度可低一些)分解的性质,常常用石油加工过程中的重油来制得汽油(裂化),或制备短链不饱和烃用作化学化工原料。
写出①C16H34催化裂化制得8碳分子烃的化学方程式;②写出C4H10制备乙烯、丙烯的化学方程式;③甲烷在一定温度下分解生成乙炔和氢气。
1、烯烃和炔烃的加成反应①定义:②原理:③举例:一般可以与X2、HX、H2、H2O、HCN等发生加成反应。
写出乙烯与H2O反应的化学方程式。
[试一试] 丙烯和溴化氢如何加成呢?烯烃的不对称加成:遵循规则。
化学:3.1《脂肪烃》教案(苏教版选修5)要点:一、饱和烃与不饱和烃的概念二、脂肪烃的分类及特性1 物理性质(1)烷烃的熔沸点(2)烷烃的水溶性2 化学性质(1)知识回顾(2)特征反应:a烷烃的取代反应b烯烃、炔烃的加成反应(不对称加成、二烯烃的加成) c加聚反应:乙烯型加聚反应1,3-丁二烯型加聚反应三脂肪烃的来源1工业制法2实验室制法(第一课时)【问】你知道什么是烃?烃是一类只含有C、H元素的有机物。
一烃的分类1 结构中有无苯环不含双键、叁键等不饱和键——饱和烃——烷烃不含苯环————脂肪烃含双键、叁键等不饱和键——不饱和烃——烯烃、炔烃烃含有苯环————芳香烃二脂肪烃的性质1 物理性质【交流与讨论】(1)烷烃的熔、沸点(见课本P40)【问】烷烃的沸点与其分子中所含有的碳原子数之间有什么关系?(a)随着分子里含碳原子数的增加,熔点、沸点逐渐升高,相对密度逐渐增大;(b)分子里碳原子数等于或小于4的烷烃。
在常温常压下都是气体,其他烷烃在常温常压下都是液体或固体;(c)烷烃的相对密度小于水的密度。
注意:表中所列烷烃均为无支链的烷烃,常温常压下是气体的烷烃除了上述碳原子数小于或等于4的几种分子之外,还有一种碳原子数为5的分子,但分子中含有支链的戊烷,【问】烷烃分子的熔沸点为什么会随着碳原子数的增大即相对分子质量的提高而升高呢?由于随着相对分子质量的增大,分子之间的范德华力逐渐增大,从而导致烷烃分子的熔沸点逐渐升高。
补充:烷烃的熔点在开始时随着碳原子数的增加而呈折线上升,这是由于其熔点不仅与分子间作用力有关,还与结构的对称性有关。
(2)水溶性——烷烃分子均为非极性分子,故一般不溶于水,而易溶于有机溶剂,液态烷烃本身就是良好的有机溶剂。
二化学性质1 【知识回顾】完成下表2 特成反应【学生回答】——完成下列填空(1)甲烷与纯卤素单质(Cl2)发生取代反应这类反应中,有机物分子中的某些原子或原子团被其它原子或原子团所代替的反应称为取代反应(2)不饱和键的加成反应——构成有机物不饱和键的两个原子与其它原子或原子团直接结合生成新物质的反应A 单烯烃中的加成反应乙烯与HCl的反应乙烯与H2O的反应乙烯与氯气的反应乙烯与H2的反应乙炔(“能”或“不能”)使溴水褪色。